INTRODUCCIÓN
El maíz (Zea mays L.) es de gran importancia económica a nivel mundial; toda la planta puede ser aprovechada y las aplicaciones posibles de este cereal incluyen alimento, forraje o materia prima para diferentes industrias [1].
Como alimento, se puede utilizar todo el grano, maduro o no, o se pueden emplear técnicas de molienda en seco para obtener productos intermedios. También a partir de él puede producirse almidón, aceite, proteínas, bebidas alcohólicas y combustible [2]. Globalmente el maíz se cultiva en más de 140 millones de hectáreas con una producción anual de más de 580 millones de toneladas métricas, lo que lo convierte en el segundo cultivo más importante del mundo después del trigo [1]. A nivel experimental el maíz es de gran importancia dado sus cortos tiempos de germinación y a que puede ser utilizado como indicador en los procesos germinativos de la semilla. La germinación del maíz implica indispensablemente la presencia del ácido giberélico (GA3), debido a que esta hormona induce la producción de enzimas hidrolíticas como las α-amilasas, las cuales desencadenan procesos metabólicos en la planta generando su crecimiento y desarrollo [3]. El GA3 es una fitohormona que hace parte de la familia de los diterpenos tetracíclicos de naturaleza ácida [4], la cual es esencial para el desarrollo de las plantas; está encargada de controlar aspectos relacionados con su desarrollo y crecimiento, especialmente la germinación. El GA3 ha sido evaluado en diferentes especies vegetales tales como Arabidopsis thaliana [ 5], fresno blanco (Fraxinus americana) [ 6], arroz (Oryza sativa) [ 7] y flores de melocotón (Prunus persica L.) [ 8], y se ha utilizado de diferentes maneras para acelerar procesos de germinación [9]. Sin embargo, los trabajos reportados sobre esta fitohormona en el maíz se centran en el papel fisiológico en los procesos de germinación. Soló el trabajo realizado por Rivera et al., 2017[10] reporta cuantificación de ácido giberélico en semillas de maíz con el fin determinar el mejor método de extracción de esta fitohormona.
Los bioensayos han sido utilizados como una técnica para detectar el ácido giberélico en extractos parcialmente purificados. Sin embargo, el uso de estos protocolos se ha dejado de lado a medida que se han desarrollado técnicas físicas de medida que permiten la identificación y la cuantificación precisa de giberelinas específicas a partir de pequeñas cantidades de tejido vegetal (del orden de mg a g) [11]. En la actualidad se emplea con más frecuencia la cromatografía líquida de alta eficiencia con detector de arreglo de diodos (HPLC-DAD) [12]-[14] y la cromatografía líquida de alta eficiencia acoplada a espectrometría de masas (HPLC-MS) [5], [7], [15], Estas técnicas tienen como ventajas mayor eficiencia en la separación y alta especificidad en la detección del analito de estudio [16]. Otro método menos utilizado es la electroforesis capilar acoplada a espectrometría de masas (CE-MS) [17] y la cromatografía de gases acoplada a espectrometría de masas (GC-MS) [18]-[20], sin embargo, en esta última técnica cromatográfica la muestra a analizar debe ser derivatizada previamente lo cual alarga el proceso de análisis y no asegura la modificación de la muestra [21].
Partiendo de lo anterior, el objetivo de este trabajo fue estandarizar un método cromatográfico para la identificación del ácido giberélico a partir de semillas germinadas de maíz (Zea mays L.), el cual permitirá hacer evaluaciones de este analito en diferentes matrices vegetales, en menor tiempo y costo.
MATERIALES Y MÉTODOS
Reactivos químicos
El estándar del ácido giberélico empleado fue Sigma Aldrich (Sigma, USA), el acetonitrilo y el metanol fueron grado cromatográfico (Fisher Scientific, USA), el acetato de etilo y el ácido fórmico fueron grado analítico (Scharlau, España). El agua fue purificada empleando un sistema Direct-Q (Millipore, USA).
Muestra de estudio
Se usaron semillas de maíz (Zea mays L.) variedad ICA-V305 tipo comercial producidas por la empresa Semillas del Pacífico (Cartago, Colombia). Se seleccionaron semillas sin daños visibles y con forma uniforme, las cuales tuvieron una masa promedio de 0.3878 ± 0.0002 g. y un volumen promedio de 0.356 ± 0.008 cm3.
Preparación de la muestra
Las semillas de maíz previamente seleccionadas se colocaron en cajas Petri (100 x 15) mm., con papel absorbente como soporte. A cada caja se le adicionaron 12.0 mL de agua destilada y se colocaron en una incubadora Incucell de 222 L sin luz, a una temperatura de 30.1 ± 0.1 °C. La humedad del sistema fue de 59.00 ± 3.39%. Después de 48 horas, las semillas se sacaron de la incubadora y fueron trituradas en un molino eléctrico, hasta obtener un polvo muy fino que se guardó en bolsa de sello hermético y en un congelador (Thermo Scientific) a -20 °C para su posterior extracción [22].
Extracción del ácido giberélico
La obtención del GA3 se realizó empleando la técnica de extracción dinámica con disolvente asistida por sonicación (DSASE), según el método descrito por [10], en el cual se utilizó como solvente acetonitrilo - ácido fórmico 5% (80:20). La celda de extracción de acero inoxidable de 3.0 mL. se llenó con 0,8000 g. de muestra y se colocó en el interior de un baño ultrasonido (Branson 5210) al cual se le controló la temperatura del agua para que no fuera superior a 35.0 °C. Posteriormente el sistema se conectó a una bomba peristáltica para controlar el flujo del solvente a través de la celda, siendo este de 0.4 mL min-1.; la extracción se realizó por un tiempo 25.0 min., al final del cual se obtuvo un volumen de 10.0 mL del extracto.
Dopaje de muestras
A los extractos obtenidos, se les determinó la concentración del GA3 empleando las mejores condiciones cromatográficas determinadas. Posteriormente, y con base en esta concentración, se realizaron dopajes de las muestras. Esto se logró al adicionar 20 mL. del estándar de GA3 a una concentración de 20 mg/kg., de tal forma que la señal del analito aumentara el doble de la señal original [23].
Condiciones cromatográficas
El análisis del ácido giberélico se realizó en un cromatógrafo líquido de alta eficiencia (HPLC) Shimadzu, equipado con un desgasificador prominence DGU-205, un detector de ultravioleta visible (UV-Vis) con arreglo de diodos (DAD) prominence SPD-M20A, un horno Shimadzu CTO-10AS VP y un automuestreador Shimadzu SIL-10AF. El software empleado para el análisis de los datos fue LC-Solution Shimadzu. Se empleó una columna Supelcosil LC-18-DB (150 x 4.6 mm. de diámetro) con un tamaño de partícula de 5.0 μιη.
Para obtener las condiciones óptimas de separación en fase reversa, se inyectaron alternadamente el estándar del GA3, muestra dopada y sin dopar, en las diferentes fases móviles y flujos empleados por HPLC-DAD. Posterior a la elección de las mejores condiciones para el eluyente, se varió la longitud de onda para seleccionar la de mejor absorción. El flujo óptimo se determinó a partir de la curva de Van Deemter, la cual se obtuvo empleando los datos de tiempo de retención y ancho del pico del estándar del ácido giberélico a flujos desde 0.2 mL min-1. hasta 0.8 mL min-1. Para determinar la fase móvil óptima, se realizaron pruebas basadas en los trabajos de Bhalla et al., [13], Xie et al., [ 21] y Stinemetz y Roberts [6], los cuales realizaron corridas cromatográficas en modo isocrático, empleando mezclas de acetonitrilo-ácido fórmico 0.01% y metanol-ácido fórmico 0.01%, a flujos de 0.5 mL min-1. y 0.6 mL min-1. respectivamente. Finalmente, se realizaron corridas en gradiente empleando los mismos solventes y flujos.
Para identificar la presencia del ácido giberélico en las muestras se realizaron comparaciones entre el tiempo de retención de la muestra y del estándar, se hicieron dopajes de la muestra, se determinó la pureza espectral de pico y se realizaron análisis por cromatografía líquida de alta eficiencia acoplada a espectrometría de masas (HPLC-MS). Estos análisis se realizaron en un equipo de cromatografía líquida de alta eficiencia Elite LaChrom (VWR - HITACHI) con detector de arreglo de diodos y acoplado a un espectrómetro de masas Amazon X (BrukerDaltonis) con ionización por electrospray (ESI) y analizador de trampa iónica (IT). El detector espectrométrico de masas se operó en modo Full scan negativo.
RESULTADOS
Optimización de las condiciones cromatográficas
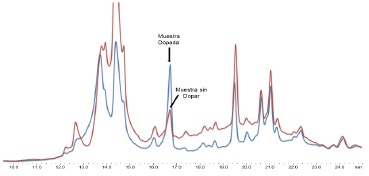
Se ensayaron varios tipos de fases móviles isocráticas, en las que se mezclaron metanol, acetonitrilo y agua para conseguir una separación adecuada del ácido giberélico. Bhalla et al., [13] y Xie et al., [ 21], ya habían estudiado un tipo similar de fases móviles para separar el GA3 en muestras vegetales, logrando buena separación y obteniendo el analíto en estudio con tiempo de retención de 3.651 min. Sin embargo, en este estudio no se logró una apropiada separación del GA3 bajo estas condiciones, esto tal vez debido a la complejidad de la matriz de estudio; evidenciada en el amplio intervalo de compuestos con diferente polaridad (Figura 1); por lo que fue necesario evaluar fases móviles en gradiente.
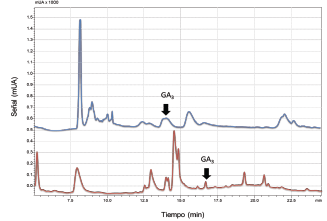
Figura 1 Cromatogramas de muestra de semillas de maíz: elución isocrática (azul), elución en gradiente (rojo)
Los mejores resultados en la separación del analito se obtuvieron trabajando con una fase móvil compuesta por una solución de acetonitrilo-ácido fórmico 0.01% en elución en gradiente con aumento lineal en el tiempo, iniciando con 10% de acetonitrilo por 5 min., incrementándolo hasta 70% en 25.0 min. y manteniéndolo durante 15.0 min (Figura 1). Por último, se disminuyó la proporción del acetonitrilo hasta 10% durante 5.0 min. obteniéndose una corrida de 45.0 min. Wu et al., [ 7] y Xie et al., [ 21] en una separación de giberelinas extraídas de vegetales y frutas, evaluaron diferentes solventes y eligieron agua y acetonitrilo como fases móviles por la buena resolución y separación obtenida. Al igual que los resultados obtenidos en este trabajo, Wu et al., [ 7] iniciaron con alto porcentaje de agua, aumentando el porcentaje total de acetonitrilo a lo largo de la separación cromatográfica. Bajo estas condiciones se encontró al patrón de ácido giberélico (GA3) a una longitud de onda máxima de absorción de 195 nm.; por debajo de lo reportado por Macías et al., [14], Bhalla et al., [13] y Schneider et al., [ 24], quienes obtuvieron la mejor señal a 205 nm., 206 nm. y 210 nm. respectivamente.
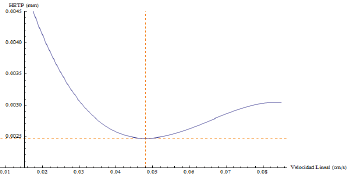
La curva de Van Deemter (Figura 2) muestra la relación entre la velocidad lineal (u) de la fase móvil y la altura equivalente de plato teórico (HETP). En esta se observa que la menor altura de equivalente de plato teórico (0.0025 mm.) se obtuvo cuando la velocidad del flujo fue de 0.048 cm s-1., por lo tanto, a esta velocidad se logró la mejor eficiencia de la columna, lo cual es ideal en procesos cromatográficos [25]. La velocidad lineal de 0.048 cm s-1. corresponde a un flujo de 0.5 mL min-1., por consiguiente, este flujo fue el óptimo y se empleó para el análisis del ácido giberélico en este estudio.
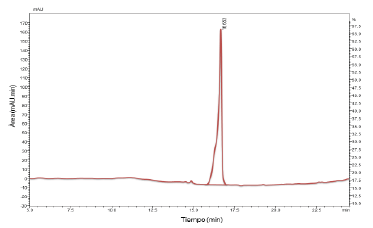
Por tanto, las condiciones óptimas para el análisis del ácido giberélico por HPLC son: fase móvil en elución en gradiente con aumento lineal en el tiempo de acetonitrilo-ácido fórmico 0.01%, flujo de 0.5 mL min-1. y longitud de onda de 195 nm. Además, la temperatura implementada fue de 30 °C. Bajo estas condiciones cromatográficas el ácido giberélico eluyó a un tiempo de retención (tR) de 16.670 ± 0.050 min. (Figura 3). Estas condiciones cromatográficas son semejante a las trabajadas por Urbanova et al., 2013 en plantas de Arabìdopsis thaliana y por Wu et al. , 2012 en plantas de arroz (oryza sativa) quienes reportaron análisis en fase reversa con tiempos de corrida 30.0 min. y tR para el GA3 de 6.8 min. y 9.7 min. respectivamente.
Identificación del ácido giberélico en muestras
En la Figura 4 se pueden observar los cromatogramas superpuestos de un estándar del ácido giberélico y de una muestra específica eluídos bajo las condiciones cromatográficas seleccionadas como ideales. Se puede observar que el estándar (azul) presentó un tiempo de retención de 16.680 min., mientras que en la muestra (rojo) se observó un pico a 16.653 min., estos tiempos tan cercanos fueron el primer indicativo de que la muestra contenía ácido giberélico. Al verificar la pureza espectral del pico en la muestra, se encontró un valor del 99.18%, lo cual indica que es un pico puro, en el cual los excipientes de la matriz no generaron señales que pudieran interferir con la señal del analito. La pureza de pico debe ser mínimo del 99.00% para considerar que no hay presencia de impurezas [24]. Además, también se compararon los espectros de absorción tomados en la porción ascendente, máxima y descendente del pico correspondiente al estándar de GA3 y al de esta fitohormona en la muestra, siendo estos iguales y demostrando la especificidad del método para la molécula en estudio. Gómez et al., [ 25], en un trabajo con HPLC, realizaron la comparación entre el espectro del pico del estándar de ibuprofeno y el espectro de la solución muestra, y determinaron la pureza de pico para la identificación de la molécula en estudio, demostrando que había una correlación espectral del 99.5%.
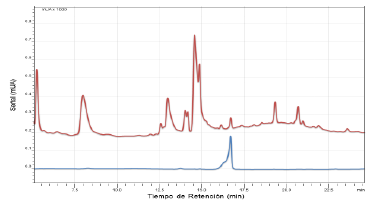
En la Figura 5 se pueden observar los cromatogramas de los extractos de semillas de maíz germinadas sin dopaje (rojo) y los extractos de la muestra dopada (azul). Encontrando a un tiempo de retención de 16.668 min. un aumento en la muestra dopada, lo que permitió inferir que esta señal efectivamente corresponde a la del analito de interés (GA3), además la pureza de pico de la muestra dopada no varía con respecto a la muestra sin dopar.
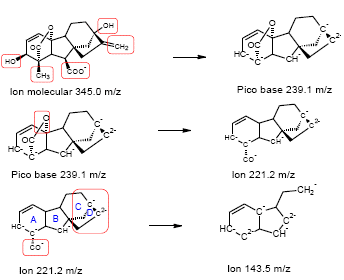
Cromatografía líquida de alta eficiencia acoplada a espectrometría de masas (HPLC-MS) Mediante HPLC-MS se pudo determinar el patrón de fragmentación característica del GA3 (Figura 6) al detectar el ion molecular a 345.0 m /z, el pico base a 239.1 m /z correspondiente a rupturas heterolíticas del grupo carboxilo en el carbono 6, de grupos hidroxilos en el carbono 3 y 13 y del grupo metilo del carbono 4.Además se evidencian los iones característicos a Cromatografía líquida de alta eficiencia acoplada a espectrometría de masas (HPLC-MS) Mediante HPLC-MS se pudo determinar el patrón de fragmentación característica del GA3 (Figura 6) al detectar el ion molecular a 345.0 m /z, el pico base a 239.1 m /z correspondiente a rupturas heterolíticas del grupo carboxilo en el carbono 6, de grupos hidroxilos en el carbono 3 y 13 y del grupo metilo del carbono 4. Además se evidencian los iones característicos a 143.5 m /z y 221.2 m /z correspondientes a la ruptura heterolítica del anillo de lactona y de los anillos C y D respectivamente (Figura 7). Estos datos concuerdan con lo reportado por Xie et al., [ 21] y Ge et al. , [17], lo cual permite inferir que se está obteniendo exclusivamente GA3
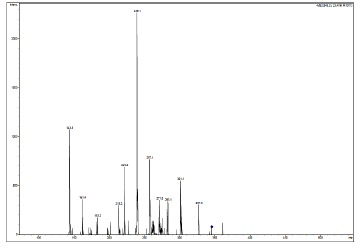
Figura 6 Espectro de masas del pico del ácido giberélico en una muestra con sus respectivos iones característicos.
Estos resultados permitieron concluir que la metodología es óptima para separar y detectar de manera inequívoca el ácido giberélico en semillas germinadas maíz. Lo anterior facilitará que al estudiar semillas de diferente tipo y procedencia, se pueda determinar la calidad de las mismas mediante la realización de un tamizaje inicial en el que se cuantificará esta fitohormona y de esta manera se puedan emplear metodologías como los campos magnéticos que estimularán el nivel de GA3 lo que daría como resultado una germinación en más corto tiempo.
CONCLUSIONES
A pesar de trabajar una matriz compleja, el método cromatográfico propuesto en este artículo permite distinguir, de manera simple, rápida y reproducible, entre el ácido giberélico y otros compuestos no identificados. Por tanto, es seguro utilizarlo en estudios posteriores, e incluso podría adaptarse para la determinación de esta molécula en otras matrices. Lo cual lo hace potencial para su implementación en laboratorios interesados en análisis de fitohormonas.