Introducción
En pacientes con leucemia mieloide aguda (LMA) el trasplante de progenitores hematopoyético (TPH) es el único tratamiento curativo. Históricamente, los mejores resultados del trasplante alogénico se han obtenido cuando el donante de células madre es un hermano HLA idéntico, es decir que comparte con el receptor los dos haplotipos o los diez antígenos del sistema HLA. Sin embargo, solo el 25% de los posibles receptores tienen hermanos HLA-idénticos, es por esto que se usan fuentes alternativas de células madre como donantes HLA idénticos no vinculados, que se buscan en los registros internacionales de donación; donantes haploidénticos y el trasplante de sangre de cordón umbilical1.
Los trasplantes haploidénticos son una oportunidad para pacientes sin donante idéntico dado que, casi todos los pacientes tendrán un donante haploidéntico disponible, padres, hermanos, hijos u otros parientes. Se ha estimado que más del 95% de los pacientes pueden encontrar al menos un donante haploidéntico en su familia2.
La búsqueda del donante es más rápida comparado con las otras fuentes ayudando así a los pacientes que necesitan un trasplante con urgencia, además el costo de adquirir el injerto es mucho menor que obtener células madre de cordón umbilical o HLA idénticos no vinculados en los países donde no existan registros de donantes voluntarios2.
El trasplante haploidéntico ha mostrado desenlaces en supervivencia comparable con trasplantes de hermanos HLA idénticos3,4 No obstante, se presenta una aloactividad bidireccional intensa que se relaciona con la alta carga de células T del donante reactivas a los antígenos HLA del receptor, aumentando la incidencia de falla del injerto y enfermedad injerto contra huésped (EICH) aguda y crónica5.
Existen poca evidencia científica en Latinoamérica sobre los desenlaces del trasplante haploidéntico en pacientes con LMA. El objetivo de este estudio es presentar la experiencia y resultados del trasplante haploidéntico en pacientes adultos con LMA en la Fundación Valle del Lili, Cali (Colombia).
Materiales y métodos
Se realizó estudio de cohorte retrospectiva. Los criterios de inclusión fueron pacientes adultos (> 18 años), con LMA no promielocítica de novo o secundaria en primera (CR1) o segunda (CR2) remisión completa, que no tuvieran donante idéntico relacionado (HLA compatible> 9/10), llevados a trasplante con donante haploidéntico (HLA compatible 5-8/10, usando tipificación para HLA con técnicas de mediana resolución de ADN) entre enero del 2013 y diciembre del 2017, en la Fundación Valle del Lili. Se excluyeron del estudio pacientes con diagnósticos de síndrome mielodisplásico y sarcoma mieloide.
Los pacientes fueron seguidos hasta la fecha de muerte o último seguimiento registrado en la historia clínica. La recolección de datos se realizó posterior a la aprobación del comité de ética de la institución.
Todos los pacientes recibieron protocolo de condicionamiento mieloablativo basado en: fludarabina (30 mg/m2 los días -5 a -2), busulfán (110mg/m2 día -5 a -2), más irradiación corporal total (TBI) fraccionado entre 400- 1300cGy. Profilaxis de EICH con ciclosporina (2mg/kg) y ciclofosfamida (50 mg/kg día +3 y +5). Se aplicó factor estimulante de colonias granulocíticas G-CSF a partir del día +7 hasta obtener injerto mieloide. Todos los pacientes recibieron profilaxis antiinfecciosa según protocolo institucional.
El protocolo de movilización y recolección de progenitores hematopoyéticos de sangre periférica se llevó a cabo con filgrastim (10 ug/kg/día) por 5 días, posterior crio preservación con dimetilsulfóxido y congelación de células a una temperatura de -84 °C.
Análisis estadístico
Se realizó un análisis estadístico descriptivo para las variables consideradas en el análisis. Las variables categóricas se resumen como proporciones y las variables continuas como mediana con su rango intercuartil (RIC).
Los resultados medidos fueron: supervivencia libre de evento (SLE); incidencia de recaída; mortalidad relacionada al trasplante; supervivencia global (SG); enfermedad de injerto contra huésped aguda (EICHa), y enfermedad de injerto contra huésped crónico (EICHc).
La recaída se definió como la presencia de 5% de blastos en médula ósea y/o reaparición de la enfermedad subyacente. Mortalidad asociada al trasplante se definió como muerte sin evidencia de recaída o progresión. SG se definió como el tiempo desde el trasplante hasta la muerte, independientemente de la causa. SLE fue definido como supervivencia libre de muerte o recaída. La enfermedad injerto contra huésped fue diagnosticada y graduada según los criterios clínicos y paraclínicos de la escala de Glucksberg6.
El injerto de neutrófilos se definió como el primer día cuando el conteo de neutrófilos fue >500 cel/uL durante tres días consecutivos. El injerto de plaquetas se definió como el primer día en que el recuento de plaquetas fue >20x 10A3/uL durante tres días consecutivos sin soporte transfusional. La falla primaria del injerto mieloide se definió como la ausencia de injerto después del TCMH hasta el día+28.
Las incidencias acumuladas se utilizaron para estimar los puntos finales de mortalidad asociada al trasplante, incidencia de recaída, injerto y EICH. Las probabilidades de SG y SLE se calcularon utilizando el método de Kaplan-Meier. Se hizo un análisis comparativo para SG y SLE según el puntaje de riesgo del grupo europeo para el trasplante de sangre y médula ósea (EBMT, por sus siglas en inglés) utilizando log-rank test. Los datos se analizaron en el software estadístico STATA 12®.
Resultados
En el periodo de estudio se realizaron 47 trasplantes en pacientes con leucemia mieloide aguda, de los cuales 21 fueron de donante haploidéntico. Las características basales se muestran en la tabla 1. La proporción de pacientes trasplantados en primera remisión completa fue del 67% (n=14). La mediana de edad de los pacientes al trasplante fue de 33 años (±11,8) y de los donantes de 31 años (±13). El 81% (n=17) eran hermanos. El 81% (n=17), tenían serología positiva para CMV tanto el donante como el receptor. La mediana de seguimiento fue de 38 meses. La fuente de célula madre fue de sangre periférica en el 100% de los receptores.
De los 21 pacientes incluidos 18 tuvieron injerto mieloide y plaquetar. Tres pacientes murieron antes del tiempo esperado de injerto. La mediana de injerto mieloide fue de 17 días (rango de 13 a 26 días) y la mediana de injerto plaquetar 19 días (rango 7 a 32 días).
De los 21 pacientes, solo 11 permanecen vivos hasta la fecha de censura, sin evidencia clínica, ni paraclínica de progresión de la enfermedad. La tasa de mortalidad de la cohorte fue de 47,6% (10/21 pacientes). La etiología de la muerte fue: 6 casos por infecciones severas (4 bacteriemias, 1 caso de enfermedad por citomegalovirus y 1 caso de fascitis necrotizante); 4 casos fueron muertes relacionadas a recaída. Siete pacientes fallecieron antes del día +100 postrasplante.
La incidencia de EICHa grado II-IV fue del 19% (4/21 pacientes), de los cuales el 5% tenían EICH grave (grado III-IV). La incidencia acumulada de EICHc moderada-severa fue del 19% con compromiso hepático, neurológico, gastrointestinal y cutáneo. En todos los pacientes con EICH se administró manejo de primera línea con esteroides. En este estudio no se registraron muertes por enfermedad injerto versus huésped.
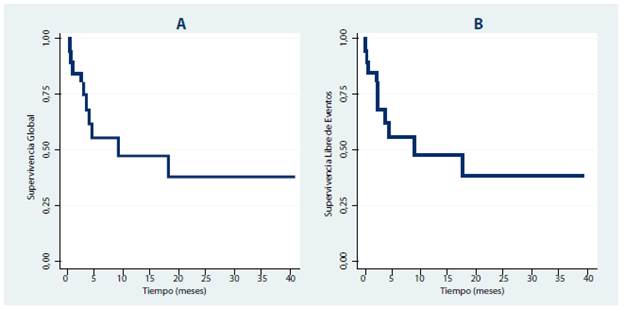
A 38 meses de seguimiento la incidencia acumulada de recaída fue del 37,6% y la mortalidad relacionada al trasplante fue del 38,3%. A los 3 años de seguimiento la SG y SLE fue del 38% (fig. 1). Al estratificar la supervivencia según score de riesgo pretrasplante EBMT, la supervivencia global a 3 años de pacientes con puntaje EBMT >3 es de 20% (fig. 2).
Discusión
El TPH es el tratamiento de elección para pacientes con leucemia mieloide aguda: estándar, de alto riesgo o quimiorrefractaria. Con el tiempo los avances en los protocolos de condicionamiento, la manipulación de las células, la profilaxis de EICH y los cuidados de apoyo han permitido que el trasplante haploidéntico sea una opción para estos pacientes3,7.
En nuestro país la tasa de trasplantes haploidénticos ha aumentado: en 2015, el Instituto Nacional de Salud y la Coordinación nacional de la red de donación y trasplantes informó que las 15 instituciones con servicio de trasplante de precursores hematopoyéticos realizaron un total de: 632 trasplantes, con un aumento del 8% con respecto al 2014, el 16% era de donante haploidénticos. Presentando un incremento del 24% con respecto al año anterior. El mayor número de los trasplantes haploidénticos para ese año (29/102) fueron realizados en nuestro centro Fundación Valle de Lili8.
El TPH alogénico es una terapia potencialmente curativa para la LMA con tasas de SG a 3 y 5 años que van desde 23% a 88% en función del perfil de riesgo y la respuesta a la terapia de inducción8. En nuestro estudio la SG fue del 38% a 3 años, al compararnos con estudios que incluyeron población y regímenes de acondicionamiento similares a la nuestra (tabla 2)3,9-12, la supervivencia en nuestro centro fue inferior, creemos que esto está relacionado con la curva de aprendizaje derivado de la reciente implementación del trasplante alogénico haploidéntico en nuestro centro, que inició en 2013 mientras que los otros centros iniciaron entre 2005 y 20087,10-12. Otro factor que impactó la supervivencia de nuestros pacientes fue la alta tasa de infecciones por gérmenes multirresistentes, esto se explica por el estado profundo y prolongado de la inmunosupresión asociada al trasplante lo cual incrementa el riesgo de infecciones oportunistas letales, a pesar de la profilaxis antiinfecciosa y las medidas generales13,15.
La supervivencia libre de enfermedad (SLE) para esta cohorte fue del 38%, lo cual es comparable con los demás centros de trasplante haploidéntico en LMA donde las tasas oscilan entre 22-61% (tabla 2)3,9-12. Se debe tener en cuenta que nuestra población incluye pacientes con diagnóstico de LMA, la mayoría en primera remisión completa y pueden encontrarse variaciones al compararnos con otros estudios, pues los resultados se modifican dependiendo del subtipo de LMA, el riesgo citogenético y las estrategias de condicionamiento usadas en el trasplante.
La mortalidad relacionada al trasplante en nuestro estudio fue del 26% a 100 días y de 38,3% a 38 meses de seguimiento, similares e incluso inferiores a otras series con menor tiempo de seguimiento como la de Sestili et al. con una mortalidad del 48%15, sin embargo, es importante referir que en los últimos 10 años la mortalidad relacionada al trasplante ha venido en descenso asociado a la mejoría en las estrategias de soporte, los protocolos de condicionamiento y la mejor tipificación de los HLA10,16.
Otra preocupación relacionada a los trasplantes haploidénticos es el tiempo entre el trasplante y el injerto. La mediana de injerto para neutrófilos y plaquetas en nuestro estudio fue de 17 y 19 días respectivamente. Resultados similares a los reportes de Di Stasi, Ciurea y Rashidi3,11,16.
Los resultados iniciales de los trasplantes con donante haploidéntico no fueron satisfactorios dado la alta incidencia de ElCHa17. Se han planteado diversas estrategias para disminuir la incidencia de EClHa, estas se basan en injertos con depleción de células T ex vivo y las técnicas con células T repletas en las cuales se encuentran los protocolos basados en ciclofosfamida postrasplante18. En este estudio se encontró una incidencia acumulada de EICHa grado II-IV y grado III-IV, del 19% y 5% respectivamente. Esta cifra es comparable con los estudios en los que se usó similar estrategia de profilaxis basada en ciclofosfamida postrasplante (tabla 2). Es un resultado satisfactorio dado que el EICHa es una complicación postrasplante que se asocia con una disminución significativa en la supervivencia, por otro lado, la incidencia de ECIH crónico también es similar a lo reportado en las otras series mencionadas.
Nuestro estudio tuvo como limitaciones ser un diseño retrospectivo con un número reducido de pacientes, creemos que hay algunas variables no medidas que podrían impactar la supervivencia global como la evaluación de riesgo citogenético y molecular que no estaba disponible para los pacientes trasplantados antes de 2016. Otro factor es el tiempo prolongado que tienen la mayoría de los pacientes entre la indicación del trasplante y su autorización por parte de la entidad de salud responsable3, lo cual los expone a un periodo mayor de susceptibilidad a infecciones y recaída de la enfermedad de base. Sin embargo, los resultados son comparables con los reportes de las grandes series internacionales en pacientes con LMA.
Los resultados de esta serie permiten establecer la base de un perfil demográfico y los resultados del trasplante alogénico haploidéntico con ciclofosfamida postrasplante para nuestro país y región, además de identificar variaciones en relación a desenlaces y complicaciones en un país latinoamericano.
Los resultados de este estudio sugieren que el trasplante haploidéntico es una alternativa factible como tratamiento para pacientes con diagnóstico de LMA en nuestro medio.