Introducción
El propóleo es un producto natural de consistencia cauchosa y pegajosa. Es elaborado por las abejas a partir de resinas, gomas y exudaciones de las plantas que han sido modificadas tras la adición de enzimas y secreciones. Presenta tonalidades de color castaño, marrón, pardo, rojizo y verde, y, en algunos casos, negros, según sea el origen botánico y geográfico (Salamanca, 2017). El producto contiene una amplia variedad de metabolitos, principalmente compuestos de estructura fenólica, a los que se les atribuyen diversas propiedades biológicas. Este material ha alcanzado una posición destacada en el mercado de los productos naturales a nivel mundial (Kuropatnicki, et al., 2013; Fabris, et al., 2013; Wagh, 2013; Banskota, et al., 2001).
Los propóleos de diferentes entornos biogeográficos del mundo han llamado la atención de muchos investigadores por sus reconocidas propiedades biológicas benéficas que lo proyectan como un producto de interés general debido a su amplio espectro antimicrobiano y antiinflamatorio, sus efectos cicatrizantes, anestésicos y anticariogénicos, su acción estimulante del sistema inmunológico, de protección del hígado, contra el cáncer, antiviral, antifúngica, antiprotozoaria, antirradicalaria, antioxidante y como agente recuperador de tejidos (Salamanca, 2017; Freires, et al, 2016; Silva-Carvalho, et al., 2015; Fabris, et al., 2013; Olivieri, et al., 2013; Sulaiman, et al., 2012; Urushisaki, et al., 2011; Valente, et al, 2011; Li, et al., 2009; Banskota, et al., 2001). El origen botánico de muchos propóleos se ha determinado mediante el análisis polínico y por comparación de fracciones epidérmicas de plantas de referencia con secciones aisladas de propóleos. Con el advenimiento de los métodos instrumentales de análisis se han podido determinar más de 300 principios activos según su origen biogeográfico en zonas templadas y tropicales del mundo (Urushisaki, et al., 2011).
Las propiedades del propóleo dependen de la composición de las plantas visitadas, de las resinas o exudados que las abejas hayan usado para formar el producto, de la forma de recolección, de las condiciones climáticas y del periodo en el cual haya sido beneficiado (Salamanca, 2017; Urushisaki, et al., 2011; Valente, et al., 2011; Silva-Carvalho, et al., 2015; Li, et al., 2009). En general, los propóleos tienen forma diversas: de aspecto duro o quebradizo, de textura suave, flexible o pegajosa, semidura o blanda, según la presencia de bálsamos, cera, gomas, resinas y restos de plantas (Sulaiman, et al., 2012; Freires, et al., 2016; Olivieri, et al., 2013; Salatino, et al., 2011).
A diferencia de las zonas templadas, en ambientes tropicales las abejas acuden a otras fuentes para suplir las necesidades de sostenimiento de las colonias y buscar resinas y exudados de las plantas para la elaboración de sus propóleos (Silva-Carvalho, et al., 2015; Miguel, et al., 2014; Bankova, et al., 2014; Rodríguez, et al., 2012). En consecuencia, se presentan importantes diferencias en su composición química, la cual depende de la flora local (Fabris, et al., 2013).
El análisis polínico, técnica de identificación del origen botánico de los propóleos, ha demostrado gran potencial como herramienta de diagnóstico. Los primeros trabajos de identificación del origen botánico conforme al origen geográfico de los propóleos, se remontan al final de la década de 1970 (D'Albore, 1979; Theobald, et al., 1979; Barth, 1998). Habitualmente, los componentes de las masas mecánicas del propóleo suelen ser filamentos de las hojas de las plantas, fragmentos de tricomas y fracciones de hojas y tallos, que pueden ser orientativos (Theobald, et al., 1979). Con esta técnica se ha identificado la presencia de polen de Eucalyptus sp., Populus sp., Pinus alba, P. nigra y P. trémula, (Freires, et al., 2016), de Dalbergia ecastophyllum, Macaranga tanarius y Cupressus sempervirens, entre otros (Bankova, et al., 2014; Daugsch, et al., 2008; Melliou, et al., 2007).
Entre los trabajos de identificación de fuentes florales propias de los propóleos tropicales de América, se destacan los de Brasil, en donde se ha identificado el espectro polínico de bosques secos de Bahia, Estado de Brasil, y se han descrito algunos tipos polínicos como Cupania, Eucalyptus, Schinus, que son propios de zonas costeras (Oliveira & Riveiro, 2018; Matos & Santos, 2016; Matos, et al., 2014); no obstante, en el polen de Río de Janeiro, Rio Grande do Sul y Minas Gerais se han relacionado especies de Eucalyptus, Eupatorium, Cecropia y Mimosa caesalpiniaefolia (Barth, 1998). En este último estado se identificaron granos de polen de Vellozia sp., Baccharis dracunculifolia, Eucalyptus sp., Hyptis sp. y Vernonia polyanthes, (Barth, et al., 1999). Asimismo, se han relacionado diferentes entornos biogeográficos del propóleo rojo. En Cuba estos corresponden a la localidad de Pinar del Río, en México, a Champotón, en el nordeste de Brasil, la zona de manglares, y a la isla de San Andrés en Colombia (Salamanca & Osorio, 2018; Omar, et al., 2016; Piccinelli, et al., 2011; Lotti, et al., 2010).
Los propóleos de tonalidades rojizas de Cuba y México se han relacionado con especies del género Clusia (C. grandiflora, C. lanceolata, C. paralicola, C. parviflora y C. espi-sanctensis) (Corbellini, et al., 2017). Los de Brasil han revelado la presencia de granos de polen de Schinus, Protium, Rhizophora, Laguncularia, Avicennia y D. ecastophyllum (Barth & Luz, 2009), en tanto que en el polen verde o marrón de Río de Janeiro, Rio Grande do Sul y Minas Gerais se han relacionado especies de Eucalyptus, Eupatorium, Mimosa caesalpiniaefolia y Cecropia (Barth, 1998). En esta última región se identificaron granos de polen de Vellozia sp., B. dracunculifolia, Eucalyptus sp., Hyptis sp. y V. polyanthes (Barth, et al., 1999) ; en Sao Paulo, se han identificado hasta 28 tipos polínicos, principalmente de las familias Leguminosae, Mimosoideae y Myrtaceae, (Silva, et al., 2013), y en geopropóleos los componentes mayoritarios se relacionan con el sílice, la arcilla y la ausencia de tricomas (Barth, 2006; Barth & Luz, 2003; Absy, et al., 1984; Absy & Kerr, 1977).
La flora apícola de mayor interés involucra una serie de plantas propias que se pueden clasificar según las zonas de vida y los pisos térmicos, como lo indican varios trabajos de identificación taxonómica y palinológica de plantas visitadas por las abejas en áreas andinas y páramos, en el Caribe, o consociaciones geográficas de ultramar, como en el caso de la isla de San Andrés (García, et al., 2011; Velandia, et al., 2012; Velásquez & Rangel, 1995). Asimismo, en el sureste de Brasil se han analizado sedimentos de propóleos y geopropóleos y se ha determinado que en los verdes, rojos y marrones sobresalen las especies de asteraceas y eucaliptos, mientras que entre los geopropóleos predominan las de Cecropia y Melastomataceae (Barth & Freitas, 2015). Cabe destacar que en estudios de la Universidad Nacional de Colombia se ha identificado la flora vascular terrestre de San Andrés (Lowy-Cerón, 2000), pero no hay reporte alguno sobre la identificación palinológica en el Archipiélago. Los trabajos polínicos revisten importancia taxonómica y contribuyen a dilucidar la relación entre plantas e insectos en los ecosistemas, cuyo estudio es determinante para identificar el origen botánico de la miel y los propóleos. Dichos estudios, sin embargo, son limitados y las publicaciones sobre el tema no son abundantes. Entre estas se destacan las investigaciones en muestras de propóleo de Turquia, Portugal y Brasil.
El polen es un componente habitual en muestras de propóleo; este proviene de las anteras de las flores visitadas por las abejas y es un indicador del origen botánico. En Colombia la cosecha y el beneficio de propóleos han permitido identificar los tipos de las muestras en función de las zonas de vida (Salamanca, 2017). Las determinaciones polínicas en esta matriz aún no se han relacionado ni se han considerado los aspectos polínicos como parámetro de autenticidad del producto. El análisis polínico en muestras de propóleo colombiano no se ha hecho y los reportes de los datos obtenidos en otros países (Corbellini, et al., 2017; Barth & Luz, 2009) solo proporcionan una referencia para iniciar los estudios en Colombia. En este contexto el presente trabajo se propuso estudiar los sedimentos polínicos de muestras de propóleo rojo de la isla de San Andrés después de una fase de extracción de grasas y resinas para enriquecer la naturaleza del sedimento.
Materiales y métodos
Zona de estudio. El entorno biogeográfico donde se recolectaron las muestras correspondió a la isla de San Andrés (12° 35' 37" y 14° 42' N y 81° 40' 49" y 81° 43' 13" O). La Isla posee una altitud de 85 m s.n.m. y la temperatura media es de 27,4 °C (Figura 1); predomina un sistema de precipitación bimodal: 121 a 307 mm/mes en el periodo lluvioso y 23 a 94 en el periodo seco. La humedad relativa multianual es del 82 %. Los ecosistemas de manglares son típicos y poseen reductos de flora endémica, propia de sistemas insulares caribeños. La flora predominante se caracteriza por elementos de bosque seco (bs-T), principalmente, con algunas especies presentes en la consociacion de bosque húmedo tropical (bh-T), (Valle, et al., 2011; Uribe & Urrego, 2009). El relieve de la isla está formado por una cadena de colinas que se extiende a lo largo de ella en su parte central, bordeada por una morfología plana de plataforma arrecifal emergida. Estas colinas constituyen un sistema montañoso longitudinal que se inicia al NE y se prolonga hacia el sur, alcanzando alturas máximas de 109 m.
Material biológico. Se recolectaron cinco muestras de propóleo rojo de colmenas Langstroth establecidas en cuatro apiarios cercanos a la zona de manglar de Bahia Hooker (BH: 12°56 ' 58 ' 'N y 81°70 '62 ' O) y El Cove (EC: 12°54 ' 35 ' N y 81°72 '62 ' 'O) y Flowers Hill (FH: 12°19 '7.2 ' 'N y 81°42 46 O), entre febrero y junio de 2016, mediante operaciones de raspado de los cuadros de las colmenas de abejas Apis mellifera L. (Hymenoptera: Apidae) de linaje europeo tipo M (Salamanca, et al., 2014). El material recolectado se dispuso en recipientes de vidrio de color ámbar con tapa de desenroscar y se refrigeraron a 4 °C, para posteriormente trasladarlos a la Universidad del Tolima, donde se congelaron a -20 °C, y completar las evaluaciones.
Caracterizaciones polínicas. Las muestras se procesaron usando una nueva metodología basada en una limpieza total, incluida la eliminación de ceras y resinas contenidas en los propóleos mediante la extracción Soxleth. En este caso, 1 g de propóleo crudo fue lixiviado con éter de petróleo para eliminar ceras y grasas con etanol al 96 % para remover gomas y resinas. Una vez hecha la limpieza total, el sedimento obtenido se sometió a acetólisis usando la técnica de Erdtman (1969). Una vez se cumplió con el protocolo, los sedimientos procesados se dispusieron en glicerina en tubos Eppendorf. Para su reconocimiento e identificación, las muestras se colocaron en un portaobjetos y se les agregó gelatina glicerinada para fijarlas y observarlas en el microscopio binocular (AmScopeTM).
Los registros polínicos se tomaron en una cámara digital (Moticam™), con el programa Motic Image PlusTM 2.0 ML acoplado al microscopio. En las evaluaciones del sedimento se hicieron barridos sobre las preparaciones acetolizadas que condujeron a la captura de imágenes a 10X, 40X y 100X. Más de 350 granos de polen de cada muestra se contaron directamente bajo el microscopio, además, se determinaron las frecuencias absolutas totales y la frecuencia relativa en el grupo de muestras estudiado. La identificación polínica se hizo haciendo uso de atlas polínicos de referencia de la costa caribe colombiana (García, et al., 2011; Willard, et al., 2004), y de manglares del noreste brasilero (Oliveira & Ribeiro, 2018; Matos & dos Santos, 2016; Freitas, et al., 2013; Magalhães & Ribeiro, 2009) que se compararon con otros trabajos de palinología en propóleos (Barth & Freitas, 2015).
Estadística. Se determinaron los conteos superiores a 400 granos de polen en cada uno de los sedimentos de las cinco muestras de propóleo rojo recolectadas, con los cuales se estimó la riqueza polínica por muestra y la frecuencia relativa con respecto a los granos. Además, se proyectó el análisis de conglomerados en un gráfico de constelación en función de los tipos polínicos dominantes. Estas evaluaciones se hicieron con el paquete estadístico JMP® Pro 14.0.0.
Resultados
En general, los tipos polínicos hallados en las muestras de los sedimentos de propóleo rojo correspondieron a 46 especies botánicas de interés apícola en las cinco zonas estudiadas (FH, ECi, ECii, BHi y BHii), entre las cuales predominaron C. nucífera, A. germinans, L. racemosa, C. erectus, R. mangle y S. mombin, que representaron el 13 % de los tipos polínicos identificados. La mayor frecuencia relativa en el total de tipos polínicos contados (2.616) de este grupo se presentó en C. nucifera (10,4 %), seguida de la de especies de manglar tales como A. germinans (8,4 %), y L. racemosa y R. mangle, cada una con 7,8 %. Por su parte, S. portulacastrum, especie de interés apícola, se halló recurrentemente en los sedimientos de todas las muestras, con una frecuencia relativa de 5,3 %; otras especies encontradas fueron C. haematodes (3,7 %), Artocarpus altilis y Psidium guajava (2,9 % cada una), M. citrifolia (2,8 %) y Crotalaria retusa (0,5 %). Las familias con mayor número de polen fueron Combretaceae (16,8 %), Acanthaceae y Arecaceae (10,4 %) y Rhizophoraceae (7,8 %). Después de la extracción Soxtleh persistieron pequeños fragmentos redondeados de tonos marrón oscuro y rojizo que se observaron incluso después, y que son atribuibles a la elevada fracción de células resinosas. Los tricomas no son abundantes y no se identificaron hifas o esporas fúngicas. El análisis de conglomerados proyectado como gráfico de constelación, reveló cinco grupos específicos (Figura 2) que representan la riqueza polínica de las muestras estudiadas. En total, 29 familias botánicas se han relacionado a partir de la identificación polínica en los sedimentos de las muestras. El 2,5 % de los granos polínicos no fueron asignados a ningún grupo, ya que no se logró su identificación. La Tabla 1 recoge los tipos de polen clasificados según la riqueza polínica y la frecuencia relativa, los cuales se relacionan con la representación del análisis de conglomerados de la Figura 2.
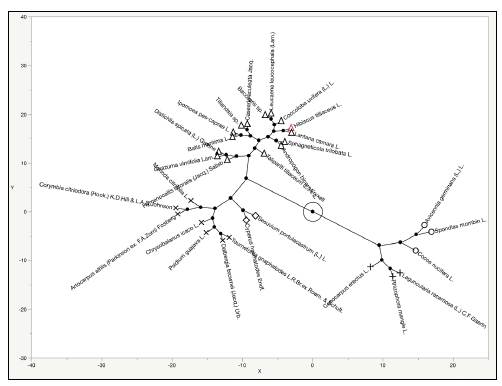
Figura 2 Análisis de conglomerados presentado como estructura de constelación de los tipos polínicos identificados en los sedimentos de propóleo rojo de la isla de San Andrés, Colombia
Tabla 1 Conteo de tipos polínicos identificados en las muestras de propóleo rojo recolectadas en la isla de San Andrés, Colombia
| Familia | Tipos polínicos | BHi | FH | BHii | ECi | ECii | FR |
|---|---|---|---|---|---|---|---|
| Amaranthaceae: | Amaranthus sp. | 9 | 3 | 7 | 0 | 0,7 | |
| Acanthaceae: | Avicennia germinans (L.) L. | 47 | 48 | 52 | 38 | 67 | 9,6 |
| Ruellia tuberosa L. | 3 | 3 | 7 | 7 | 0,8 | ||
| Aizoaceae: | Sesuvium portulacastrum (L.) L. | 16 | 30 | 34 | 33 | 26 | 5,3 |
| Amaryllidaceae: | Hymenocallis littoralis (Jacq.) Salisb. | 3 | 7 | 3 | 12 | 11 | 1,4 |
| Anacardiaceae: | Schinus terebinthifolia Raddi. | 0 | 2 | 0 | 1 | 0,1 | |
| Spondias mombin L. | 41 | 48 | 38 | 36 | 39 | 7,7 | |
| Tapirira sp. | 1 | 6 | 7 | 4 | 0,7 | ||
| Annonaceae: | Annona glabra L. | 3 | 0 | 8 | 3 | 0,5 | |
| Apiaceae: | Coriandrum sativum L. | 6 | 5 | 3 | 1 | 0,6 | |
| Arecaceae: | Cocos nucifera L. | 47 | 39 | 82 | 50 | 55 | 10,4 |
| Bataceae: | Batis maritima L. | 6 | 7 | 3 | 4 | 2 | 0,8 |
| Boraginaceae: | Tournefortia gnaphalodes L.R.Br.ex Roem. & Schult. | 14 | 7 | 19 | 14 | 11 | 2,5 |
| Bromeliaceae: | Tillandsia sp. | 6 | 4 | 3 | 2 | 1 | 0,6 |
| Combretaceae: | Terminalia catappa L. | 5 | 2 | 4 | 5 | 0,6 | |
| Laguncularia racemosa (L.) C.F Gaertn | 30 | 37 | 45 | 50 | 58 | 8,4 | |
| Conocarpus erectus L. | 22 | 29 | 52 | 39 | 61 | 7,8 | |
| Asteraceae: | Acmella darwinii (D.M.Porter) R.K.Jansen | 2 | 1 | 1 | 3 | 0,3 | |
| Baccharis sp. | 4 | 2 | 3 | 4 | 4 | 0,6 | |
| Bidens pilosa L. | 5 | 1 | 7 | 4 | 0,6 | ||
| Sphagneticola trilobata L. | 7 | 2 | 1 | 1 | 6 | 0,6 | |
| Convovulaceae: | Ipomoea pes-caprae L. | 5 | 6 | 3 | 2 | 6 | 0,8 |
| Cyperaceae: | Cyperus haematodes Endl. | 11 | 23 | 31 | 12 | 21 | 3,7 |
| Chrysobalanaceae: | Chrysobalanus icaco L. | 4 | 11 | 21 | 9 | 8 | 2,0 |
| Euphorbiaceae: | Hippomane mancinella L. | 9 | 0 | 3 | 0 | 0,5 | |
| Leguminosae: | Crotalaria retusa L. | 0 | 7 | 2 | 3 | 0,5 | |
| Dalbergia brownei (Jacq.) Urb. | 16 | 12 | 13 | 11 | 8 | 2,3 | |
| Leucaena leucocephala (Lam.) | 5 | 0 | 3 | 3 | 4 | 0,6 | |
| Mimosa tenuiflora (Willd.) Poir | 2 | 0 | 7 | 2 | 0,4 | ||
| Malvaceae: | Guazuma ulmifolia Lam. | 4 | 5 | 6 | 7 | 7 | 1,1 |
| Hibiscus tilliaceus L. | 2 | 3 | 2 | 5 | 3 | 0,6 | |
| Talipariti tiliaceum (L.) Fryxell | 8 | 12 | 4 | 2 | 0 | 1,0 | |
| Triumfetta lappula L. | 1 | 2 | 1 | 2 | 0,2 | ||
| Moraceae: | Artocarpus altilis (Parkinson ex. F.A.Zorn) Fosberg | 17 | 3 | 21 | 13 | 22 | 2,9 |
| Myrtaceae: | Psidium guajava L. | 11 | 14 | 17 | 21 | 13 | 2,9 |
| Corymbia citriodora (Hook.) | 13 | 7 | 6 | 11 | 21 | 2,2 | |
| Poaceae: | Andropogon bicornis L. | 7 | 3 | 4 | 4 | 7 | 1,0 |
| Distichlis spicata (L.) Greene | 3 | 4 | 7 | 3 | 9 | 1,0 | |
| Polygonaceae: | Coccoloba uvifera L. | 3 | 0 | 3 | 2 | 7 | 0,6 |
| Rhizophoraceae: | Rhizophora mangle L. | 33 | 33 | 41 | 52 | 44 | 7,8 |
| Rosaceae: | Rubus urticifolius Poir. | 1 | 0 | 3 | 0 | 0,2 | |
| Rubiaceae: | Morinda citrifolia L. | 23 | 16 | 12 | 8 | 14 | 2,8 |
| Salicaceae: | Casearia aculeata Jacq. | 5 | 3 | 6 | 3 | 0 | 0,6 |
| Sapindaceae: | Cupania glabra Sw. | 2 | 5 | 1 | 3 | 0,4 | |
| Verbenaceae: | Lantana camara L. | 5 | 3 | 0 | 5 | 3 | 0,6 |
| No identificados | No identificados | 11 | 21 | 15 | 19 | 2,5 | |
| Total de granos polínicos contados | 418 | 478 | 593 | 532 | 595 | 2616 | |
| Total de tipos de polen identificados | 30 | 46 | 46 | 46 | 46 |
BH: Bahia Hooker. EC: El Cove. FH: Flowers Hill. FR: Frecuencia relativa total
El análisis de la distribución de frecuencias predominantes de los tipos polínicos (Figura 3) permitió identificar dos grupos característicos preponderantes: A. germinans, C. nucifera y S. mombin fueron las especies más predominantes en los sedimentos según los porcentajes de frecuencia (entre 8,0 y 16,0 %); el segundo grupo mayoritario incluyó dos subgrupos en los que las especies C. erectus, C. haematodes, L. racemosa y R. mangle predominaron. En la Figura 4, se presentan algunas microfotografías de tipos polínicos observados en el microsopio de luz, característicos del sedimento de los propóleos rojos de la zona de la isla de San Andrés (Colombia).

Figura 3 Diagramas característicos de las frecuencias y los tipos polínicos presentes en las muestras de sedimentos de propóleo rojo de las zonas estudiadas en la isla de San Andrés, Colombia. FH, BH y EC: zonas de muestreo.

Figura 4 Algunos granos de polen identificados en las muestras de propóleo rojo de la isla de San Andrés, Colombia. A-C. Corymbia citriodora. D-F. Laguncularia racemosa. G. Tapirira sp. H. Cupania glabra L Spondias mombin. J. Morinda citrifolia. K. Rubus urticifolius. L. Schinus terebinthifolia. M. Triumfetta lappula. N. Mimosa tenuiflora. O. Rhizophora mangle. P. Baccharis sp. Q. Coriandrum sativum. R. Acmella darwinii. S. Bidens pilosa. T. Avicennia germinans. Escala: 10 µm
Discusión
En términos generales, la estructura boscosa de la isla de San Andrés en la Bahía Hooker y El Cove tienen un alto grado de desarrollo y se ubican detrás de la barrera arenosa, lo cual se debe a que permanecen inundados gran parte del año, bien sea por el sistema de lluvias o por el aporte de los drenajes que se depositan sobre los manglares. La unidad El Cove se extiende en un espacio de 1,2 ha y tiene una barrera monoespecífica de R. mangle, en tanto que en la Bahía Hooker, que se extiende a lo largo de 34 ha, hay 15,1 ha de R. mangle, 0,97 ha de A. germinans y 18,4 ha de bosques mixtos de R. mangle, L. racemosa, A. germinans y C. erectus. Los árboles de porte medio alcanzan hasta 5,6 m, con densidades de hasta 119 árboles por hectárea. En este entorno, la biomasa estimada de R. mangle es de 14,8 tn/ ha/año, la de A. germinans es ligeramente mayor, con 13,5 tn/ha/año, y la de L. racemosa es de 8,32. Los manglares de San Andrés son altamente productivos, en comparación con otros sistemas de manglar en el Caribe. La diversidad polínica observada en las muestras de propóleo rojo podría explicarse en función de la diversidad de la flora asociada con la zona de manglares (García-Hansen & Gaviría-Chiquazuque, 1996).
Dado que se han detectado solamente seis zonas geográficas en que se producen los propóleos rojos en el mundo, entre ellas las de Colombia (Salamanca & Osorio, 2018), solo se conocen los trabajos de caracterización palinológica del nordeste de Brasil (Barth & Luz, 2009; Avelino & Ribeiro, 2018). Allí hay una amplia biodiver-sidad florística que permite un mayor espectro polínico y reduce la posibilidad de hacer comparaciones directas con la isla de San Andrés. La flora insular del Caribe presenta algunas diferencias con respecto a las especies del nordeste brasileño, pero en las dos localidades predominan condiciones de manglar y tipos de flora similares, lo que explica la presencia de tipos polínicos de Arecaceae (C. nucifera), Anacardiaceae (Tapirira sp. junto a S. mombin), Aizoaceae (S. portulacastrum), Cyperaceae (C. haematodes), Moraceae (A. altilis) y Myrtaceae (C. citriodora), considerados como dominantes, con una frecuencia relativa total de 23,1 %, comparable con los conteos de polen de algunas de las muestras recolectadas en el nordeste de Brasil.
El origen de los propóleos rojos del nordeste de Brasil reside principalmente en las resinas de especies de Anacardiaceae y de los géneros Schinus (Barth & Luz, 2009) y Spondias y Tapiaria (Avelino & Ribeiro, 2018). En San Andrés, las fuentes de propóleo rojo pueden atribuirse a las exudaciones y resinas de las especies de manglar. En este sentido, es importante resaltar que las fuentes potenciales de propóleo rojo se distribuyen a lo largo del costado oriental de la isla, donde las condiciones hidrológicas, de sedimentación, geomorfológicas y de intensidad del oleaje son favorables para su distribución y predomina la vegetación costera y de manglar (R. mangle, asociada con otras especies también presentes: A. germinans, C. erectus y L. racemosa). Además, entre los sectores (Orange Hill y Little Hill), se observan zonas mixtas de R. mangle, L. racemosa, y parches de C. erectus en Smith Channel, Tom Hooker y Savanna, donde se mantiene la unidad del bosque de manglar más desarrollado de la isla.
Los estudios de flora juegan un papel singular cuando se trata del establecimiento de las relaciones entre plantas e insectos. En las muestras de propóleos rojos de Cuba, México, Nigeria y Shandong en China (Corbellini, et al., 2017), no se han hecho evaluaciones polínicas para identificar el origen botánico. Solo en Brasil se han identificado los tipos polínicos que se relacionan con especies de los géneros Avicennia, Baccharis, Clusia, Dalbergia, Protium, Rhizophora y Schinus (Barth & Luz, 2009). En el presente estudio, los tipos polínicos se relacionaron estrechamente con los descritos por Barth & Luz (2009), con excepción de B. dracunculifolia y Protium, principalmente.
Los tipos polínicos observados correspondieron a plantas de la zona de manglar presentes en el núcleo de la reserva de biosfera "Seaflower" en el archipiélago de San Andrés. El área de estudio no presentaba reductos de vegetación primaria, por el contrario, se evidenciaron formaciones de bosque secundario, con afectación permanente en términos de presión antrópica. En los recorridos realizados por las zonas de manglar siguiendo protocolos de evaluación rápida, se observaron abejas recolectando resinas de los fustes de los árboles e intenso pecoreo sobre las flores y glándulas secretoras de las plantas. En los sedimentos de propóleo rojo observados bajo el microscopio después de la extracción Soxleth y la acetólisis, se evidenciaron fragmentos de tejido vegetal, gomas, ceras, tricomas y abundantes piezas leñosas con residuos de hojas y cortezas, por ejemplo, secciones de neumatóforos.
La asociación vegetal característica que representa el espectro polínico en cada una de las cinco muestras de propóleo rojo estudiadas correspondió a los tipos de mangle identificados como blanco (L. racemosa), negro (A. germinans), botón (C. erectus) y rojo (R. mangle). Se sabe que la especie S. portulacastrum es una hierba suculenta que se expande en las zonas costeras y marítimas y que es representativa de la isla de San Andrés, al igual que C. nucifera, la más abundante en todos los sedimentos de propóleo rojo analizados. S. mombin, especie que también se destacó en las muestras estudiadas, es característica del Trópico y se extiende a lo largo de las zonas cálidas del país.
Los espectros polínicos caracterizados en este estudio pueden usarse para futuros análisis palinológicos de propóleos rojos, no solo de la isla de San Andrés, sino de otras regiones insulares del mundo aún no consideradas. Por las comparaciones visuales de los diferentes tipos polínicos encontrados en el estudio, así como la remoción de ceras y grasas mediante extracción Soxleth para visualizar mejor los granos, y la acetólisis, el presente documento sirve como punto de partida para posteriores investigaciones. Las especies de mangle registradas son tipos polínicos que dan cuenta de la versatilidad de A. mellifera en la isla a la hora de buscar materiales para la protección y sustento de las colonias. El estudio, asimismo, aporta una ruta apropiada para la identificación de polen a partir de matrices complejas, como es el caso de los propóleos.
Conclusiones
Se evaluaron sedimentos polínicos de muestras de propóleo rojo colombiano de la zona insular de San Andrés, Colombia. El espectro polínico de las muestras presentó algunas diferencias importantes con el del nordeste brasileño. En los sedimentos predominaron tipos polínicos propios de zonas de manglar, además de taxones de las familias Aizoaceae, Arecaceae, Anacardiaceae, Cyperaceae y Myrtaceae, que son representativas de plantas apícolas de las zonas donde se generó el muestreo. Las frecuencias polínicas revelaron grupos predominantes de especies de mangle: L. racemos, A. germinans, C. erectus y R. mangle, así como de S. portulacastrum, C. nucifera y S. mombin. Además, se observaron tipos polínicos acompañantes y accesorios con bajas frecuencias, que revelan la actividad de A. mellifera en la búsqueda de recursos poliníferos para su sustento. El estudio permitió implementar una metodología de tipos polínicos de referencia para establecer el origen botánico de los propóleos.















