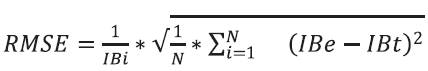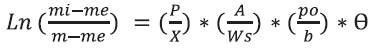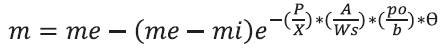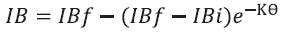Introducción
La eflorescencia grasa o ‘fat bloom’ es un fenómeno caracterizado por la aparición de una película blanca en la superficie del chocolate, lo que disminuye su calidad (Beckett, 2008; James y Smith, 2009). Dicho fenómeno es debido, en gran parte, a la formación de estructuras cristalinas inestables que pueden ser generadas por un deficiente atemperado o malas condiciones de almacenamiento. En manteca de cacao estas formas se clasifican en los tipos I a VI siendo las deseables los tipos V y VI por ser más densas, lo que evita que el chocolate se contraiga (Chire y Hartel, 2011). Beckett (2008) utilizando difracción de rayos X, clasificó el polimorfismo de la manteca de cacao en tres tipos de cristales, identificados como a, p y P'. En el estado líquido la migración de grasa a la superficie del chocolate es originada por una acción de bombeo debido a la diferencia de densidad de la manteca de cacao entre las fases sólida y líquida ocasionada por las fluctuaciones de temperaturas (Pastor-Navarro, 2010).
El desarrollo de la eflorescencia grasa en chocolate durante el almacenamiento puede ser explicado por la separación de fases y la transformación polimórfica, lo que produce una reducción en la calidad sensorial del producto y una separación debido a triglicéridos de bajo y alto punto de fusión, siendo los primeros los causantes de la eflorescencia, lo que se explica por la transformación debida a la transición de cristales de la manteca de cacao de la forma PV a la forma PVI (Bricknell y Hartel, 1998; Ali et al., 2001; Bui y Coad, 2014). Masuchi-Buscato et al. (2018) encontraron que, en almacenamiento a temperaturas oscilantes, la adición de 6% de estearina de manteca de cacao retarda la eflorescencia grasa hasta 45 días, debido a su efecto en la trasformación polimórfica de los cristales de este componente. La adición de otras grasas similares puede retardar la formación de la eflorescencia grasa, de acuerdo con el punto de fusión de las mantecas utilizadas (Bahari y Ako, 2018; Biswas et al, 2017; Halim et al., 2019; Jin et al., 2018).
La manteca de cacao está compuesta por una cantidad alta de ácidos grasos saturados como esteárico (21%) y palmítico (20%), y ácidos grasos no saturados como oleico (23%) (Mexis et al., 2010); en dos varietales de cacao peruano se ha encontrado cierta composición de ácidos grasos, respectivamente: 32.8 y 33.9% de esteárico; 32.3 y 32.6% de oleico; 29.3 y 28% de palmítico; 1.1% de araquidónico, 2.9 y 3.1% de linoleico y 0.2 % de linolénico (Chire et al., 2020). Este trabajo tuvo como objetivo determinar la cinética de eflorescencia grasa en la superficie de muestras comerciales de chocolate peruano evaluando el Índice de Blancura (IB) en muestras con 45% y 70% de cacao.
Materiales y métodos
Tratamientos y diseño experimental
Para el estudio se utilizaron tabletas de chocolate comercial sin envoltura, con 45% y 70% de cacao en su formulación y dimensiones de 2.93 ± 0.12 cm de largo, 2.29 ± 0.09 cm de ancho y 0.9 ± 0.03 cm de espesor, con un peso de 6.07 ± 0.59 g, que fueron almacenadas en cámaras climáticas a 30%, 50% y 70% de humedad relativa, obtenida con soluciones de cloruro de magnesio, bicromato de sodio y cloruro de sodio. El programa de temperaturas cíclicas para simular un almacenamiento acelerado (Zarringhalami et al., 2010) incluyó dos ciclos continuos de temperaturas entre 30 ± 1°C durante 8 h y 20 ± 1°C durante 16 h, para un total de 672 horas con mediciones cada 48 horas del Índice de Blancura (IB). En la cámara climática el cambio de temperatura ocurrió de 3.2 °C/ min hasta alcanzar una reducción a -1°C/min (Climacell®).
Para el análisis de los cambios en el IB se utilizó un diseño experimental de bloques completo al azar con tres repeticiones. Los IB se midieron en muestras almacenadas a 30% (M1), 50% (M2) y 70% (M3) de humedad relativa (hr). Los contenidos de cacao en las muestras fueron de 45% (A) y 70% (B) dispuestos en los bloques del diseño. La cinética de eflorescencia grasa se midió a 0, 48, 144, 192, 288, 336, 504, 552, 624 y 672 horas.
Análisis proximal
En las muestras se midió la humedad (AOAC 931.04, 2016), proteína cruda (AOAC 970.22, 2016), grasa cruda (AOAC 963.15, 2016), ceniza (AOAC 972.15, 2016), fibra cruda (AOAC 985.29, 2016) y carbohidratos totales por diferencia (Álvarez et al., 2007).
Los valores de IB fueron calculados a partir de los valores L*, a* y b* obtenidos de cuatro diferentes posiciones de lectura en la superficie de la tableta de chocolate con el colorímetro Minolta® CR-400, con ángulos variables de 0°, 90°, 180° y 270°. Las mediciones fueron realizadas a 20 °C (Pastor-Navarro, 2010). Con los datos obtenidos se calculó el IB, utilizando la ecuación de Lohman y Hartel (1994) (Ecuación 1)
donde, IB es el Índice de Blancura, L* la luminosidad en rango de 0 a 100, a* la coordenada CieLab en el rango de +60 a -60 que corresponde al intervalo entre rojo y verde, respectivamente, y b* es la coordenada CieLab en el rango de +60 a -60 que corresponde de amarillo a azul, respectivamente (Pastor-Navarro, 2010).
Análisis y procesamiento de datos
Para las comparaciones entre tratamientos de humedad relativa se utilizó el análisis de varianza; para el análisis proximal y de IB se utilizó la desviación estándar; la diferencia entre los resultados del análisis proximal; y para las coordenadas CieLab se utilizó la prueba ‘t’ de Student.
Modelamiento matemático
Según la ecuación de ganancia de humedad (Labuza, 1982) (Ecuación 2), se tiene:
donde; IB es el Índice de Blancura esperado, IBf es el máximo Índice de Blancura esperado, IBi es el índice de blancura inicial, 0 es el tiempo en horas, y K es la constante de reacción de la eflorescencia grasa en unidades/hora.
Escalamiento
El ajuste por escalamiento consiste en una serie de cambios sucesivos del valor K por iteración hasta obtener el valor K esperado (K2). Para ello se utilizó el programa Excel® 2007 con el fin de determinar el valor de la constante de reacción en cinética K calculada que explica mejor la cinética de eflorescencia grasa para cada tratamiento. Se utilizó la opción ‘ridge regression’ del paquete estadístico Statgraphics Centurion 16.1® para relacionar los valores de IB esperado con el IB teórico y determinar de esta forma, el grado de ajuste por el coeficiente de determinación (r2).
Validación del modelo
La validación se realizó utilizando el valor RMSE o raíz del cuadrado medio del error (Seid y Hensel, 2012) (Ecuación 3).
donde; RMSE es el cuadrado medio del error, IBi es el Índice de Blancura inicial, IBe es el Índice de Blancura experimental, IBt es el Índice de Blancura teórico, N es el número de repeticiones.
Variación no significativa en cinética (VNSC)
Consiste en un procedimiento estadístico que aplica en una primera etapa análisis de varianza y posteriormente, la prueba de comparación de medias de Tukey, teniendo como tratamientos el tiempo y sus valores de rango (Rubio, 2004), considerando los 10 tiempos de almacenamiento como tratamientos y como variable de respuesta los valores de IB. Con el VNSC se determinó el tiempo a partir del cual la cinética de variación del IB no presenta variación significativa (P > 0.05), lo que significa un valor de IB constante en el tiempo a partir del cual comienza el final del proceso de eflorescencia.
Resultados y discusión
Análisis proximal
Los valores del promedio del tenor graso de muestras de chocolate con 45% y 70% de cacao, respectivamente, fueron de 32 ± 1.14 y 40.80 ± 0.09% de la grasa total (Tabla 1).
Efecto de la humedad relativa en el alma cenamiento
Los valores promedio de IB presentaron un incremento acelerado en las primeras horas de almacenamiento para luego disminuir gradualmente hasta alcanzar un valor constante. Esto se explica considerando la formación de una fase líquida de la materia grasa en la matriz de las muestras, lo que acelera la migración a la superficie durante el cambio de temperatura en el tiempo de almacenamiento (Tabla 2). Altimira et al. (2007) encontraron valores y comportamientos similares a los hallados en el presente estudio; por otra parte, Clercq et al. (2014) encontraron que la migración de grasa no puede ser descrita como una difusión constante o difusión de Fick.
Tabla 2 Índice de Blancura (IB) promedio a través del tiempo para muestras de chocolate peruano con 45% y 70% de cacao, almacenados en tres niveles de humedad relativa.
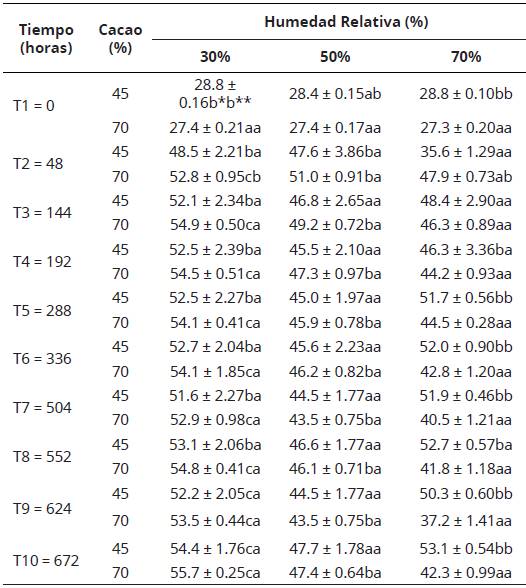
* Letras diferentes en cada línea indican significancia (P < 0.05) entre valores de humedad relativa. **Letras diferentes en cada columna indican diferencia (P < 0.05) entre tiempos de evaluación.
Los datos muestran que, los chocolates comerciales analizados no presentan diferencia de IB por efecto del contenido de cacao (P > 0.05), no obstante, el efecto de la humedad relativa mostró diferencias entre algunas muestras (P < 0.05). Skrabal et al. (2019) encontraron cambios significativos en la eflorescencia grasa de la superficie de muestras de chocolate elaborados con diferentes contenidos de grasa (manteca de cacao, grasa de leche, grasa vegetal) sometidas a cambios de temperatura (20 y 29 °C); así, las muestras almacenadas con una humedad relativa entre 50 y 75% presentaron cambios significativos en la composición de la superficie del producto, igualmente, encontraron que la mezcla de ácidos grasos provenientes de grasas vegetales sustitutas de avellana y manteca de cacao contribuyen a la aparición más rápida de la eflorescencia en comparación con chocolates elaborados sólo con este último producto.
Zarringhalami et al. (2010) y Chire y Hartel (2011) trabajando con ciclos de temperatura similares a los del estudio de Skrabal et al. (2019) obtuvieron un IB máximo de 32, un valor similar al encontrado en el presente estudio. Por el contrario, Flores, Chire y Lescano (2017); Ali et al (2001) encontraron eflorescencia atrasada después de 24 h de observación. Esto último puede ser debido a la composición de la formulación del chocolate, la adición de grasas sustitutas y emulsificantes que retardan la eflorescencia grasa. En estas evaluaciones es necesario tener en cuenta el tamaño de las partículas de chocolate ya que estas forman poros que facilitan la migración de grasa a la superficie (Afoakwa et al., 2009). Dahlenborg et al. (2015) encontraron que a menor tamaño de partícula la migración de grasa es acelerada. Utilizando microscopia de barrido laser 3D-LSCM se puede determinar la eflorescencia grasa desde sus etapas iniciales (pre-eflorescencia grasa) y determinar las partículas de grasa que empiezan a migrar a la superficie (Ashida et al., 2020).
Las temperaturas cíclicas de almacenamiento generan la aparición de la eflorescencia grasa de forma acelerada, debido a que el incremento de temperatura favorece una mayor fase líquida de la manteca de cacao que tiende a subir a la superficie. Se ha demostrado que los chocolates almacenados a temperaturas cíclicas de 20-32 °C muestran mayor eflorescencia grasa respecto a temperaturas cíclicas de 20-29 °C (Huanhuan y Bryoni, 2018).
Altos contenidos de azúcar en la superficie del chocolate pueden generar un fenómeno conocido como eflorescencia de azúcar o ‘sugar bloom’, que se manifiesta como una capa blanquecina en la superficie parecida a la eflorescencia grasa y se desarrolla por la reacción de la humedad del ambiente con los azúcares (Bricknell y Hartel (1998); Ghosh et al. (2005). Este fenómeno puede ocasionar un error en la lectura para determinar la eflorescencia grasa.
Modelamiento matemático de la cinética de eflorescencia grasa
La cinética de eflorescencia es explicada por una migración de grasa desde la matriz del chocolate hacia la superficie hasta conseguir un equilibrio (Dahlenborg, 2014; Galdámez et al, 2009). Comportamiento similar al observado en la migración de agua durante un proceso de deshidratación y que es definido por una ecuación exponencial invertida (Labuza, 1982). Con base en esa similitud en el comportamiento de migración de la materia, se ajustó la ecuación de Labuza (1982) para describir el fenómeno de eflorescencia grasa con base en una ecuación exponencial invertida (Ecuación 4).
que puede ser expresada como (Ecuación 5)
donde, me es la humedad de equilibrio (g H2O/g sólido), mi es la humedad inicial (g H2O/g sólido), m es la humedad esperada (g H2O/g sólido), po es la presión parcial del vapor del agua (cm de Hg), A es el área de contacto con el medio ambiente (m2), Ws es el peso seco del producto (g), P es la constante de permeabilidad (g/m2 por día), X es el espesor del empaque, b es la pendiente, 0 es el tiempo (horas).
Para adaptar la ecuación 5 de la curva de migración de agua a partir de la ecuación de Labuza (Ecuación 4) a la cinética de eflorescencia grasa, se reemplazaron en la ecuación los valores de ganancia de humedad (m) por los de índice de blancura (IB). Los valores (P/X)*(A/Ws)*(po/b) fueron considerados como el factor K en unidades/h, denominado para este estudio como constante de reacción de eflorescencia grasa.
Los valores K fueron obtenidos mediante la tabulación de los resultados reales utilizando el software Microsoft® Excel® y la ecuación 7, a continuación, se determinó el promedio de los valores de K teórica/calculada (K1) que aparecen en la Tabla 3, donde se asumió que el IBf o Índice de Blancura final corresponde a la manteca de cacao (IB = 60.9), punto en el cual las muestras alcanzaron el equilibrio. El IBi es el Índice de Blancura inicial que se obtuvo del promedio de los valores de IB tomados al comienzo de la prueba.
Tabla 3 Elementos de la curva de cinética de eflorescencia grasa, coeficiente de determinación y probabilidad antes del escalamiento y ajuste por iteración en muestras comerciales de chocolates de Perú (n = 2).

* Las características de las muestras y los tratamientos se presentan en la Tabla 1 y Tabla 2.
Para elaborar el gráfico de la cinética de eflorescencia grasa teórica (Figura 1) se utilizaron los valores de K teórica/K calculada. Para determinar el IB en la cinética de eflorescencia grasa, los resultados de Índice de Blancura teóricos fueron modelados con la Ecuación 6 adaptada de Labuza (1982), de la forma siguiente

Figura 1 Cinética de la eflorescencia grasa experimental, K teórica calculada (K1) y K ajustada por iteración (K2) para los tratamientos M1A (a), M1B (b), M2A (c), M2B (d), M3A (e) y M3B (f).
Despejando la constante K a partir de la ecuación 7, se tiene:
Escalamiento
El ajuste por escalamiento consiste en una serie de cambios sucesivos del valor K por iteración hasta alcanzar el valor K esperado (K2) o constante de reacción de eflorescencia grasa ajustada por escalamiento, el cual se expresa como coeficiente de determinación (r2 > 0.85), valor que indica una buena correlación entre los datos (Prieto et al., 2012). En la presente investigación se hizo un escalamiento gráfico con distintos valores del factor K utilizando el software Excel® 2007 y la opción ‘ridge regression’ del programa Statgraphic Centurion 16.1®, para relacionar los valores IB reales e IB esperados y obtener así, el valor de K calculado que mejor modela la cinética de eflorescencia grasa para cada tratamiento (Briones y Aguilera, 2005). Los valores K después del escalamiento (K2) con los cuales se alcanzaron y los valores más altos de r2 se incluyen en las Tablas 4 y 5. Se observa que solo en el tratamiento M3B ocurre un valor < 0.85. Los niveles de significancia para cada uno de los modelos fueron > 0.05, lo que indica baja correlación de la variación de IB con respecto al tiempo, por tanto, se sugiere agregar una variable independiente más de estudio a los modelos, como el contenido de sacarosa en el chocolate.
Tabla 4 Valores de la constante de reacción de eflorescencia grasa (K/h): teórica calculada (K1) y teórica calculada ajustada por escalamiento (K2).

Tabla 5 Elementos de la curva de cinética de eflorescencia grasa, coeficiente de determinación y significancia después del escalamiento y ajuste por iteración en muestras de chocolate peruano.

*K2 expresado como valor K constante de reacción de la eflorescencia grasa.
En la Tabla 6 se observan las ecuaciones de ajuste de la cinética de eflorescencia grasa para los tratamientos con r2 > 0.85, y en la Figura 1 las correlaciones para la cinética de la eflorescencia grasa experimental, K teórica calculada (K1), y K ajustada por iteración (K2) para los tratamientos M1A (a), M1B (b), M2A (c), M2B (d), M3A (e) y M3B (f).
Validación de resultados
El valor de la raíz cuadrada del error (RMSE) indica el ajuste de los datos experimentales a los modelados en relación con la cantidad de puntos que tiene la gráfica (Seid y Hensel, 2012). Para la validación de la cinética de eflorescencia grasa para el tratamiento M3B, que fue la de menor valor de r2, se utilizó la ecuación 3, de raíz cuadrada del error. El valor (10.7%) de RMSE obtenido para el tratamiento M3B (Figura 2) es similar al límite del rango superior encontrado por Sánchez-Silva et al. (2007).
VNSC
Una vez fueron obtenidas las significancias (P < 0.05) entre los valores de IB correspondientes a los distintos tratamientos (10 tiempos, entre T1 = 0 y T10 = 672 h)) (Tabla 2), se utilizó la prueba de Tukey para la comparación entre los pares de valores de IB correspondientes a tiempos contiguos (Tabla 7), encontrando que a partir de la comparación T4 vs. T3, no se observaron diferencias significativas (P > 0.05) (Figura 1). Lo anterior permite deducir que en el caso de los tratamientos M1A y M2A a partir de 144 horas (T3), los valores de IB se conservan en un valor promedio de 52.64 ± 0.78 y 54.31 ± 0.86 para las muestras con 45% de cacao sometidas a 30% y 50% de humedad relativa, respectivamente. Un comportamiento similar se observó en los tratamientos M1B (70% de cacao, 30% de HR), M2B (70% de cacao, 50% de HR), M3A (45% de cacao, 70% de HR) y M3B (70% de cacao, 70% de HR), que no presentaron diferencias (P > 0.05) entre valores de IB, cuando se compararon por pares (T4 vs. T3, T6 vs. T5, T6 vs. T5 y T5 vs. T4), correspondiendo a cada uno de estos tratamientos los valores promedio de IB: 45.78 ± 1.08; 45.43 ± 1.45; 51.95 ± 0.88 y 41.9 ± 2.3, respectivamente.
Tabla 7 Significancia por la prueba VNSC de las comparaciones pareadas de los tratamientos contiguos.

*S=diferencia significativa /NS=diferencia no significativa.
Con los promedios de los valores IB finales (Tabla 5), es posible decir que los valores más altos corresponden a muestras de chocolates con mayor cantidad de cacao (70%), en una atmósfera de menor humedad relativa (30%); ya que, con mayor cantidad de grasa presente en la composición, mayor es la celeridad de formación de la eflorescencia grasa, favorecida por la menor humedad de almacenamiento. Esto último debido a una menor presencia de moléculas de agua en la superficie que repelen la presencia de grasa. Esta observación fue corroborada parcialmente con los valores de eflorescencia alcanzados por los demás tratamientos de menor IB, que mostraron alta dispersión de sus valores alcanzando, en algunos tiempos, reducciones e incrementos en los valores de IB después de llegar a un IB alto, pero sin exceder el valor máximo de este índice. Estas variaciones se explican por los cambios en los valores de los componentes L*, a* y b* de la ecuación del IB.
Conclusión
Las muestras de chocolate con 70% de cacao presentaron mayor contenido graso (40.80 ± 0.09%) que con 45% de este componente. La humedad relativa y el contenido de cacao no tuvieron influencia significativa (P > 0.05) en la eflorescencia grasa dentro de las 48 h de almacenamiento, luego ésta presentó un comportamiento asintótico en el tiempo, llegando a un valor IB constante, cuyo promedio fue mayor en muestras de chocolates con mayor cantidad de cacao (70%) y menor humedad relativa de almacenamiento (30%).
La cinética de eflorescencia grasa se ajustó al modelo exponencial: IB = IBf - (IBf - IBi) e- Ke con un coeficiente de determinación esperado de r2 > 0.85 (P < 0.05) por lo que se recomienda incorporar una variable más de estudio al modelo para mejorar el grado de predicción, como puede ser considerar la cantidad de sacarosa adicionada a las formulaciones de chocolates.