Introducción
El síndrome de Fanconi (SF) es un desorden metabólico, inicialmente descrito por Lignac en 1924 y posteriormente definido por Fanconi en 1936 (1). Este se describe como las alteraciones de transporte en la región proximal del túbulo renal donde se presenta una pérdida anormalmente elevada de glucosa, aminoácidos, algunos electrolitos, ácido úrico y bicarbonato. El SF usualmente no es reportado y muchas veces no se realiza el diagnóstico. Dentro de las etiologías, se describen múltiples agentes quimioterapéuticos comúnmente usados que pueden causar formas completas o parciales, como la ifosfamida, los platinos, el metotrexato y la doxorrubicina.
La ifosfamida (IFA) es un derivado de la ciclofosfamida que se ha usado ampliamente en el tratamiento de lesiones tumorales malignas en niños (2), usualmente se utiliza junto con ácido 2-mercaptoetanosulfónico (Mesna) con el fin de disminuir el riesgo de cistitis hemorrágica, sin embargo, es uno de los agentes quimioterapéuticos que es responsable de toxicidad renal proximal; esta se presenta mediante la mayor captación de IFA por los transportadores de cationes orgánicos en las células proximales tubulares y la metabolización a cloro acetaldehído (3). La IFA junto con otros agentes quimioterapéuticos, como los platinos (principalmente cisplatino y en menor medida carboplatino), pueden incrementar el riesgo de nefrotoxicidad.
Existe literatura con menor fuerza de la evidencia sobre otros quimioterapéuticos que se encuentran asociados a SF, entre estos se destacan el metotrexato y la doxorrubicina que, a través de modelos animales, sustentan su plausibilidad biológica. Lo anterior, principalmente, bajo fenómenos de estrés oxidativo que derivan en peroxidación lipídica, liberación excesiva de óxido nítrico, aumento de la permeabilidad en los capilares glomerulares y degeneración tubular en zonas de alta susceptibilidad a este fenómeno como el túbulo contorneado proximal (4, 5).
A continuación se presenta una serie de casos de pacientes pediátricos oncológicos con función renal preservada, donde se produjeron diferentes manifestaciones de nefrotoxicidad tubular proximal secundarios al uso de agentes quimioterapéuticos, conformando SF parciales o completos.
Presentación de los casos clínicos
Caso 1
Se trata de una paciente femenina de 6 años con antecedente de prematuridad a las 32 semanas sin otros antecedentes médicos que ingresa a nuestra institución con un cuadro clínico de un mes de evolución de fiebre y pérdida de peso asociados a cefalea, disartria, ptosis palpebral y dolor mandibular. Se realizó un hemograma que evidenció monocitosis, anemia y trombocitopenia con hallazgo en extendido de sangre periférica de 71 % de blastos, por lo que se realizó una biopsia de médula ósea con hallazgos compatibles con linfoma de Burkitt asociado a compromiso en sistema nervioso central por infiltración meníngea.
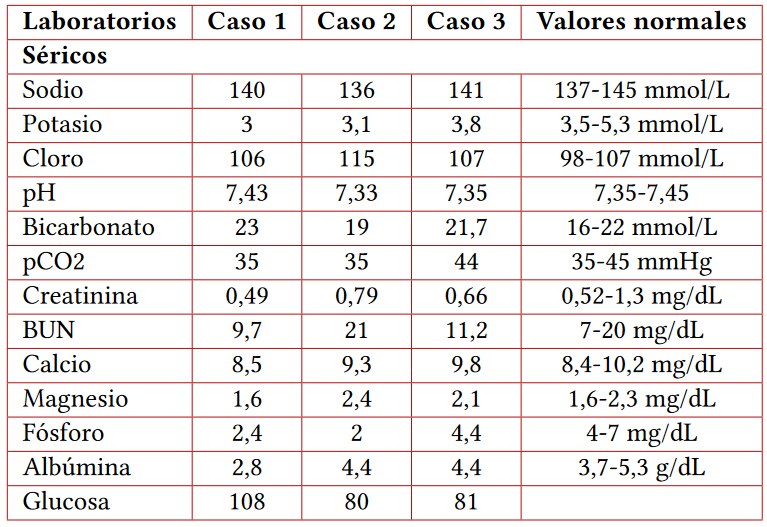
Al ingreso, la paciente tenía una elevación significativa de azoados, hiperpotasemia, hiperuricemia e hiperfosfatemia, configurando síndrome de lisis tumoral que no se resolvió con rasburicasa, alopurinol y líquidos endovenosos, por lo que se requirió de terapia de reemplazo renal. Posteriormente, la paciente recibe cinco días de prefase citorreductora con ciclofosfamida en dosis acumulada de 400 mg y quimioterapia intratecal con metotrexato de 12 mg y citarabina de 30 mg y finalmente un curso de cinco días de quimioterapia de ciclofosfamida de 3,82 g/m2, posterior a lo cual, la paciente presenta glucosuria sin hiperglucemia asociada a alteraciones electrolíticas dadas por hipomagnesemia, hipopotasemia e hipocalcemia, las cuales fueron corregidas con tratamiento endovenoso de reposición, persistiendo con hipofosfatemia (tablas 1 y 2).
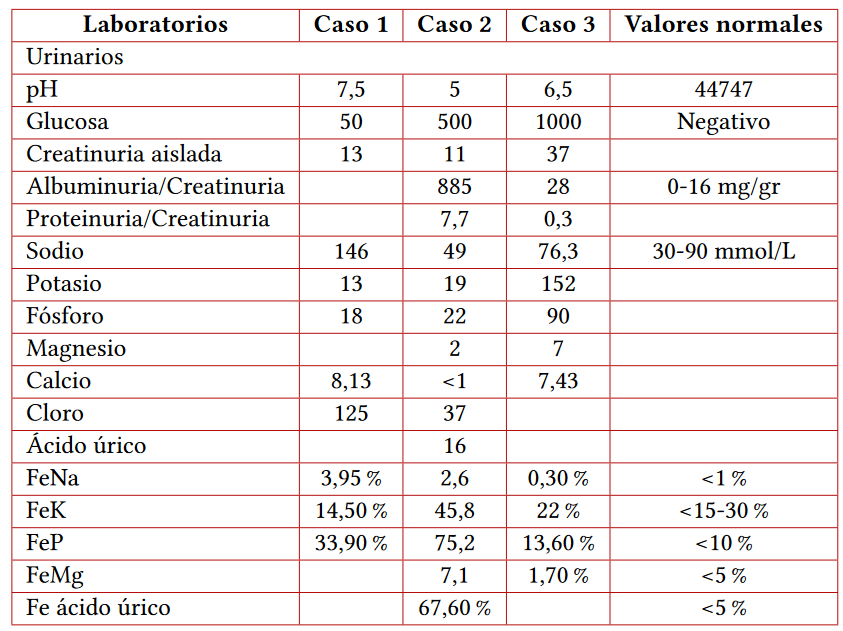
Es de aclarar que la hipocalcemia es una anormalidad poco frecuente y se asocia generalmente a niveles disminuidos de vitamina D más que a una tubulopatía específica de calcio. Ante sospecha de SF adquirido se solicitaron pruebas complementarias, entre las que se destacan: la relación calciuria/creatininurias elevadas, la vitamina D disminuida, las fracciones excretadas de sodio y potasio elevadas y la reabsorción tubular de fósforo disminuida (66 %), dado que la excreción de bicarbonato en la orina provoca un efecto anión no reabsorbible, lo cual genera pérdida de estos electrolitos. Se inició tratamiento con suplementos de sodio, fosfato monosódico, potasio y vitamina D con adecuada respuesta.
Caso 2
Paciente masculino de 21 meses de nacido con antecedente de prematurez a las 34,5 semanas y diagnóstico de miofibrosarcoma de alto grado, de órbita izquierda con extensión a fosa temporal y media que requirió siete ciclos de quimioterapia neoadyuvante, con ifosfamida y doxorrubicina con posterior resección quirúrgica. Al examen físico llegó con hipertensión arterial y en estudios previos al nuevo ciclo de quimioterapia adyuvante se evidenciaron paraclínicos con creatinina normal, hipofosfatemia, hipopotasemia leve, hipercloremia y uroanálisis con glucosuria sin hiperglucemia (tablas 1 y 2). Se sospechó de SF adquirido secundario a quimioterapéuticos, se solicitaron fracciones excretadas de magnesio, ácido úrico, sodio y potasio, las cuales estaban elevadas, proteinuria y albuminuria severas, así como acidosis metabólica hiperclorémica con anión gap sérico normal y acidosis urinaria.
Lo anterior se explica por el mecanismo de acidificación urinaria del túbulo colector que se encuentra conservando la acidosis tubular tipo II o proximal. Se descartaron otras causas de SF como cistinosis y se inició manejo con reposición oral de electrolitos, enalapril como antihipertensivo y antiproteinúrico, citrato de potasio e hidroclorotiazida, el último de los cuales fue utilizado dado el efecto paradójico de este diurético al aumentar la reabsorción proximal del bicarbonato. Se evidenció una mejoría de los parámetros de proteinuria, albuminuria y la tasa de filtración glomerular, así como de alteraciones electrolíticas y ácido base.
Caso 3
Paciente femenina de 17 años con antecedente de sarcoma pleomórfico indiferenciado de alto grado intracraneal, quien completó seis ciclos de quimioterapia en esquema ICE (ifosfamida, carboplatino y etopósido) y posterior al cuarto ciclo se documentó en paraclínicos de extensión: hipofosfatemia, hipomagnesemia y glucosuria sin hiperglucemia, por lo que se sospechó tubulopatía proximal. Se complementan estudios con fracción excretada de potasio elevado e índice calciuria/creatinuria elevado, así como aumento de aminoácidos en orina (cistina, glicina y serina) y proteinuria significativa (tablas 1 y 2), los resultados son compatibles con SF incompleto dado por gases venosos sin alteraciones.
Con el fin de disminuir la nefrotoxicidad, se cambió la ifosfamida a ciclofosfamida y se redujo un 25 % la dosis de etopósido y carboplatino. Además, la paciente recibió manejo con n-acetilcisteína y citrato de magnesio oral con adecuada respuesta clínica; dada la evidencia de proteinuria y albuminuria elevada en 24 horas, se inició antiproteinúrico (IECA) con mejoría de esta.
Se aportan únicamente las fracciones excretadas de los electrolitos dado que el valor absoluto de estos dependen de su valor sérico. Los valores que se omiten es porque no fueron realizados.
Discusión
El síndrome de Fanconi (SF) es una disfunción generalizada del túbulo proximal renal, caracterizado por un defecto en la reabsorción de bicarbonato y solutos como la glucosa, el fosfato ácido úrico y los aminoácidos. Los pacientes se pueden presentar con hipofosfatemia, glucosuria renal, hipouricemia o aminoaciduria.
Hay una capacidad reducida para recuperar el bicarbonato filtrado al túbulo renal, por lo cual hay una pérdida del bicarbonato que se presenta cuando la concentración sérica se eleva por encima del umbral de reabsorción del bicarbonato disminuido, es decir, acidosis metabólica con anión gap normal. Los pacientes no tratados tienen una concentración de bicarbonato entre 12 y 20 mEq/l, cuando el bicarbonato sérico es bajo, la mayoría del bicarbonato filtrado se puede reabsorber y entonces la acidificación distal procede normalmente. El pH urinario se encuentra dentro de parámetros normales y, después de una carga ácida, el pH urinario puede ser reducido a 5,3 o menos (6). Los casos mencionados presentaron el SF total o parcial, con síntomas secundarios a diferentes agentes quimioterapéuticos, por lo cual es indispensable prestar atención a este posible efecto adverso y sus complicaciones a largo plazo.
El espectro de la disfunción tubular en el SF varía en los diferentes pacientes, puede ir desde una tubulopatía proximal generalizada o completa hasta alteraciones parciales en la reabsorción de electrolitos como sodio, potasio, glucosa, aminoácidos, bicarbonato y fósforo. Los medicamentos quimioterapéuticos son causas importantes de SF adquirido.
La combinación de IFA, carboplatino y etopósido ha demostrado ser eficaz en la remisión a largo plazo de sarcomas de tejidos blandos que son resistentes a otros manejos (3). Algunas complicaciones renales asociadas como cistitis hemorrágica o daño tubular renal se pueden presentar, por lo que existen en la actualidad protocolos para minimizar el riesgo de complicaciones renales como disminución de dosis y uso de Mesna (3).
El SF adquirido secundario a IFA se describió por primera vez en 1972 por van Dyk et al (3) y se sabe que el tiempo para el inicio de la disfunción tubular es variable. Por su parte, la IFA es un agente alquilante derivado de la ciclofosfamida que se ha usado ampliamente en el tratamiento de sarcomas, linfomas y lesiones tumorales sólidas en niños (2). La ciclofosfamida y la IFA se metabolizan y se convierten en productos activos por el mismo sistema de citocromo p450, donde la excreción urinaria ocurre predominantemente como metabolitos inactivos y acroleína, que es el principal metabolito tóxico que causa cistitis hemorrágica, sin embargo, se ha demostrado que otro metabolito, cloro acetaldehído (CAA), es capaz de producir nefrotoxicidad (7). La IFA, en comparación con la ciclofosfamida, causa mayor N-decloroetilación, produciendo más CAA y mayor nefrotoxicidad. Se han reportado casos del 1,4 % al 30 % y, de estos, aproximadamente el 5 % desarrolla SF (3, 6). Uno de los casos recibió inicialmente IFA, sin embargo, ante los hallazgos descritos se decidió cambiar por ciclofosfamida, disminuyendo el riesgo de progresión de nefrotoxicidad debido a este agente quimioterapéutico.
La toxicidad se presenta debido a una mayor captación y selectividad de IFA por los transportadores de cationes orgánicos (OCT2) en la región basolateral de las células tubulares proximales y su metabolización a CAA produciendo injuria tubular (2, 8). Los factores de riesgo para nefrotoxicidad por ifosfamida son: dosis acumuladas (mayores de 100 g/m2), tener menos de cinco años y haber usado previamente o de forma concomitante con cisplatino o carboplatino, también tener antecedente de nefrectomía, presuntamente como consecuencia de una capacidad renal excretora disminuida (3, 9). En estos casos se recomienda monitorizar más frecuentemente los niveles de calcio, fósforo, bicarbonato séricos y uroanálisis, además de vigilar la presencia de proteinuria, antes y durante el tratamiento, con el fin de identificar tempranamente toxicidad, lo cual nos ayuda a prevenir un mayor daño y complicaciones más serias (3, 7, 8, 9).
El carboplatino, análogo del cisplatino, ha demostrado ser menos nefrotóxico, este es un agente antineoplásico a base de platinos que se une covalentemente al ADN, inhibiendo la reparación y la síntesis del ADN, el reemplazo de los ligandos de cloruro de cisplatino por el ligando de bis-carboxilato del carboplatino lo hace más estable, disminuyendo su toxicidad en comparación con el cisplatino (10, 11). La mayoría del carboplatino se une a proteínas y sólo la parte libre causa toxicidad; el 70 % de la dosis administrada se elimina por vía renal (7, 12) y la nefrotoxicidad es dosis dependiente; se ha reportado la alteración en la excreción de magnesio urinario, por lo que el seguimiento de magnesio sérico también es importante (10).
Los pacientes tratados con platinos generalmente no reciben una dosis fija para el cálculo de la dosis de carboplatino, por lo que se recomienda el uso de la fórmula de Calvert modificada, teniendo en cuenta la tasa de filtración glomerular (10). Así, se deben monitorizar los niveles del medicamento e incluir la medición de la tasa de filtración glomerular para ajustar las dosis en caso de ser necesario (11).
Para reducir el riesgo de nefrotoxicidad es necesario evitar la hipovolemia, el uso de antieméticos y el consumo de magnesio, ajustar la dosis del medicamento según la función renal y revisar la alcalinización de la orina (13).
El metotrexato es un fármaco del grupo de los antimetabolitos que, posterior a su entrada a la célula, presenta una reacción de poliglutamación y un enlace subsecuente a la enzima dihidrofolato reductasa con una afinidad mil veces mayor que el ácido fólico, inhibiendo su conversión de dihidrofolato a tetrahidrofolato (14). Es de esperar la presencia de varios efectos adversos, entre estos, compromiso a la función hepática, hematológica, gastrointestinal y neurológica, así como a la función renal. Este último fenómeno es relativamente infrecuente (con presentación entre el 2-12 % de los ciclos de tratamiento) y asociado a altas dosis de metotrexato, entendidas como mayores a 500 mg/m2 en niños o mayores a 1000 mg/m2 en adultos (15).
La principal teoría de daño renal en relación con este medicamento y sus metabolitos está dada por la precipitación de microcristales a nivel de los túbulos renales con su respectivo fenómeno obstructivo, así como algún componente de toxicidad a nivel tubular (16) que se puede confirmar por hallazgos a nivel de la microscopia electrónica, dados por células epiteliales tubulares, cilindros granulosos y, mucho menos frecuente, por la presencia de cristales del medicamento si la orina está ácida (13).
La doxorrubicina es un medicamento que pertenece al grupo de los antibióticos antitumorales del tipo antraciclinas, ampliamente utilizados en la actualidad para tratar varios tipos de cánceres tales como linfomas, mama y vesicales (17). Este grupo farmacológico condiciona importantes efectos nocivos a nivel de las funciones cardiaca, hepática y renal (18).
Con respecto a la función renal, este medicamento produce una alteración en la homeostasis renal, además de una acumulación directa de radicales libres en las células renales que condicionan los fenómenos de peroxidación lipídica, la liberación excesiva de óxido nítrico (generando un aumento de la permeabilidad de los capilares) y la degeneración glomerular (4).
Existe evidencia indirecta del compromiso tubular proximal, como la encontrada en el estudio de Hosseinzadeh et al. (5), en el que se usó gemfibrozil con el fin de atenuar el daño renal inducido por estrés oxidativo e inflamación en ratas sometidas al uso de doxorrubicina. Así pues, se evidenció una disminución del 9 % en el daño tubular proximal con respecto a los animales que se expusieron al quimioterapéutico exclusivamente. Es de destacar que no se encontró un efecto benéfico con el uso del gemfibrozil de manera aislada.
Por último, en estudios experimentales de metabolómica urinaria del grupo de Aiping et al. (19), a través de los cuales se determinaron cambios a nivel renal dependientes del tiempo, se describió en microscopia de luz con hematoxilina eosina anormalidades como infiltrado intersticial inflamatorio, hipertrofia tubular, degeneración hidrópica y picnosis en las células epiteliales tubulares, y algunos cristales y cilindros celulares en la médula, así como un número reducido de células glomerulares en relación con atrofia.
Las antraciclinas entonces poseen el sustrato fisiopatológico para potenciar (o producir) cambios bioquímicos en relación con el SF, sin embargo, es necesario sospechar de forma sistemática de medicamentos con una mayor evidencia de compromiso a este nivel.
Conclusiones
La nefrotoxicidad debido a agentes quimioterapéuticos en población pediátrica es más frecuente que en población adulta, donde es importante reconocer que, aunque se presenta poco, el SF parcial o completo se puede presentar, por lo cual es necesario sospecharlo, prevenirlo y tratarlo en caso de que se presente de forma temprana, con el fin de evitar complicaciones a largo plazo o evaluar diversas opciones terapéuticas que sigan siendo efectivas para el paciente oncológico, sin interferir en el pronóstico global del paciente.