Introducción
La estructura y dinámica de una población es el resultado de las interacciones entre los rasgos de la historia de vida de las especies y las características ambientales de sus hábitats (Clark et al., 1978); razón por la cual las mariposas son excelentes modelos para hacer estudios poblacionales, dada su sensibilidad a pequeños cambios ambientales en el espacio y el tiempo (Schaeffer et al., 2019).
Dentro de estos insectos, los Satyrinae son un grupo dominante en la mayoría de las comunidades de mariposas, debido a sus características biológicas, diversidad y distribución (Brown & Freitas, 2000; Ribeiro et al., 2008; Vu, 2009). Esta subfamilia contiene especies que exhiben especial afinidad por ciertos tipos de formaciones vegetales como bosques primarios, secundarios o áreas abiertas (Devries et al., 1997); razón por la cual se consideran buenos indicadores de las características del ecosistema (Kremen, 1994; Uehara-Prado et al., 2007) y son empleadas en estudios poblacionales (Besold et al., 2008). Una de las especies de este grupo de mariposas es Morpho helenor peleides Kollar 1850, la cual está presente al norte de Colombia, en los valles bajos del río Cauca, alto y medio Magdalena, Sierra Nevada de Santa Marta (SNSM) y serranía de Perijá. Habita en zonas de bosque seco tropical (BST), así como en bosques húmedos entre los 1000-1800 m de altitud (García et al., 2002). Los adultos suelen libar en suelo húmedo, excrementos de animales y sobre todo en fruta descompuesta (Andrade-C et al., 2007).
En la Costa Caribe se han registrado poblaciones de M. helenor peleides en el departamento del Cesar, en el Santuario de Vida Silvestre Los Besotes (Rodríguez et al., 2008), en Córdoba en los alrededores del complejo de humedales del valle inundable del río San Jorge (Campos-Salazar et al., 2011), en el Magdalena en la Reserva Natural Las Delicias (Vargas et al., 2011) y en Sucre en la Reserva Campo Aventura Roca Madre (Sampedro et al., 2013). En el caso de Bolívar, se ha registrado en el Santuario de Fauna y Flora los Colorados (SFFC) y la Reserva la Flecha (RLF) (datos sin publicar). Sin embargo, la dinámica y el tamaño poblacional de los insectos tropicales a nivel de paisajes es un tema que no ha recibido la atención por parte de algunos investigadores en las zonas bajas del Caribe colombiano; sobre todo en el departamento de Bolívar, el cual presenta la mayor extensión de BST natural (61,165ha) (Pizano & García, 2014). El BST es un ecosistema de vital importancia por tener poca representación en el sistema de áreas protegidas; razón por la cual ha sido explotado de manera indiscriminada (Martínez et al., 2010) y representa un 2,3% de lo que existía originalmente. La cobertura natural presenta remanentes debido a las modificaciones del paisaje natural por los procesos antrópicos, como la extracción de maderas y la expansión de áreas ganaderas y áreas agrícolas (Pizano & García, 2014). Teniendo en cuenta que la pérdida de hábitats es actualmente la amenaza más grande para las mariposas (Basset et al., 2012) del género Morpho y siendo el departamento de Bolívar una región donde los problemas ambientales asociados a la perdida de hábitat crecen a un ritmo muy acelerado; se hace urgente llevar a cabo estudios que permitan comprender las causas de la variación temporal y espacial en el número de individuos en una población y dilucidar los mecanismos que la estructuran. Lo anterior toma relevancia si se tiene en cuenta que la información disponible sobre la ecología poblacional de las mariposas del género Morpho en paisajes de bosque seco es aún escasa (Ochoa et al., 2018; Prieto et al., 2005).
Con el fin de contribuir a esta discusión, se analizó la variación de la estructura poblacional de M. helenor peleides, en un paisaje de BST en el departamento de Bolívar, a través del estudio de varios parámetros demográficos.
Metodología
Área de estudio
La presente investigación se llevó a cabo en un paisaje de bosque seco tropical (BST) en la Vereda La Flecha (VLF), municipio de San Jacinto, departamento de Bolívar, Colombia. La zona se encuentra localizada a 09º 51' 09-74" N, 75º 10' 32-32" O, con una altitud que oscila entre 324 y 451m y una extensión de 149ha. Se encuentra enmarcada en la subunidad climática D2 (Rangel & Carvajal, 2012) con un promedio anual de temperatura de 25°C (Castaño Uribe, 1999), y un promedio mensual de precipitación de 166mm respectivamente. El régimen de lluvias es bimodal tetraestacional, caracterizado por un periodo de sequía intenso correspondiente al periodo comprendido entre diciembre y marzo, y un periodo de sequía menos marcado, entre junio y julio (Rangel & Carvajal, 2012). La vegetación climática regional es de tipo higrotropofítica, lo que quiere decir que las plantas predominantes en la vegetación son de tipo caducifolio; sin embargo, en algunos sitios dentro de las estribaciones es de tipo subhigrofítica, donde cobran mayor importancia los elementos perennifolios o siempre verdes (Díaz et al., 1986). En la VLF se encuentran fragmentos de bosque en buen estado de conservación, bosques en regeneración y riparios inmersos en matrices de potreros y cultivos, destacándose la palma amarga (Sabal mauritiiformis), maíz (Zea mays L), aguacate (Persea americana), ñame (Dioscorea esculenta) y ají (Capsicum annuum L).
Diseño de muestreo
En un paisaje de BST en la zona se delimitó una ventana de 3,0 x 3,0 Km y se marcaron siete estaciones con un promedio de distancia de 384,1±91 m (mínimo 300m - máximo 622m), en diferentes unidades composicionales (cultivos, potreros, borde de bosque, bosque en sucesión, fragmentos de bosque) (Figura 1). Las estaciones seleccionadas se describen en el material suplementario (SP. 1). En cada estación se instalaron cinco trampas Van Someren-Rydon (VSR) (Devries, 1987) distanciadas entre sí con un promedio de 61,8±9 m (50m-70m), a una altura entre 1 y 1,2 m del suelo, para un total de 35 trampas. Se realizaron siete muestreos cada 15 días, entre marzo y julio de 2018. Las VSR fueron cebadas y revisadas durante tres días consecutivos y los cebos fueron reemplazados cada 24 horas. El cebo consistió en una mezcla de frutas (Musa paradisiaca, Carica papaya, Ananas comosus, Mangifera indica) y panela fermentada durante 48 horas (Devries et al., 1997; Ribeiro & Freitas, 2011).

Figura 1 Localización del paisaje de BST en la Vereda la Flecha, San Jacinto, Caribe colombiano (a) y las estaciones (E) de muestreo en el área de estudio (b).
Para realizar el marcaje de los ejemplares se removieron las escamas en la parte ventral de la celda discal del ala anterior izquierda con ayuda de un hisopo de algodón y se colocó un código alfanumérico con marcadores indelebles (Figura 2) (Heyer et al., 1994; Ramos & Freitas, 1999). Las mariposas fueron sexadas mediante la inspección visual de las estructuras genitales, con ayuda de pinzas entomológicas planas y se clasificaron por edad (young, middle-aged, old) según el grado de perdida de las escamas y el estado general de las alas (Ehrlich & Gilbert, 1973; Freitas & Ramos, 2001; Prieto et al., 2005; Schaeffer et al., 2019).

Figura 2 Captura y marcaje de Morpho helenor peleides. Marcaje de los individuos (A), marca en la parte ventral de M. helenor peleides (B), vista ventral de M. helenor peleides (C) y vista dorsal de M. helenor peleides (D).
Por otro lado, en cada punto/estación, se registró la temperatura ambiente y la humedad relativa con un termohigrómetro (Extech-IR), y la intensidad de luz con un luxómetro (Extech-DT-1308). La cobertura de dosel se determinó con un densitómetro, siguiendo la metodología propuesta por Strickler (1959) y con un pluviómetro se registró la cantidad de lluvia (mm) para cada muestreo.
Análisis de datos
La abundancia observada se expresó de dos formas: (I) abundancia total (Ntotal) como el número de individuos marcados y (II) abundancia neta (Nneta) como el número de individuos marcados y recapturados. Por otro lado, se realizó un modelo lineal generalizado (MLG) para determinar el efecto tanto de las estaciones como de los muestreos (variables explicativas) sobre la abundancia total (variable respuesta) de M. helenor peleides en el área de estudio. Este análisis se realizó con el programa InfoStat, versión 2019 (Di Rienzo et al. 2019). Usando el método de Jolly (1965) y Seber (1965), se estimaron tres parámetros poblacionales por muestreo: tamaño de la población, tasa de supervivencia y número de individuos nuevos o tasa de reclutamiento. Este método además de proporcionar el mejor ajuste a nuestro conjunto de datos (bondad de ajuste; X2 = 43,055; p<0,001), es apropiado para estimar parámetros demográficos en poblaciones abiertas y no sobreestima la amplitud de los intervalos de confianza (Allen & Thompson, 2014). Los parámetros de la población se estimaron con el programa Ecological Methodology versión 5,1 (Krebs & Kenney, 1998).
La proporción de sexos se calculó de acuerdo a la siguiente formula: machos/machos + hembras; el valor resultante de la proporción sexual es 0,5 si el número de machos y hembras es igual (Wilson & Hardy, 2002). Este método es el más recomendado para estimar las proporciones sexuales en la naturaleza debido a que considera a los individuos como unidades discretas y por lo tanto refleja la abundancia relativa de cada sexo en una población (Ancona et al., 2017). Se realizó la prueba de Chi-cuadrado para determinar diferencias significativas entre las proporciones observadas y esperadas, utilizando el programa PAST 3.17 (Hammer, 2013). La estructura de edad se estimó para cada muestreo a partir de la proporción de cada una de las tres categorías de edad registradas en campo. Para evaluar diferencias en el número de individuos por categoría entre muestreos se realizó un test de homogeneidad con Chi-cuadrado. El tiempo de residencia se calculó como una medida indirecta de la longevidad, considerando el número de días entre la primera y la última captura (Brussard et al., 1974; Schaeffer et al., 2019). Posteriormente los datos se compararon mediante una prueba U de Mann-Whitney, para evaluar si el tiempo de residencia difería entre sexos. El movimiento de los individuos marcados se calculó como la distancia entre la trampa donde fueron marcados y las trampas donde fueron recapturados. Se utilizó el software QGIS “Las Palmas” (Versión 2.18.0) para graficar las distancias recorridas. Se usó la prueba U de Mann-Whitney para evaluar si las distancias recorridas diferían entre sexos. Para determinar el grado de correlación entre la abundancia de individuos de M. helenor peleides y las variables abióticas registradas en campo (temperatura, humedad relativa, intensidad lumínica, cobertura de dosel), se realizó el índice de correlación de Spearman (programa PAST 3.17) (Hammer, 2013).
Resultados
Tamaño poblacional
Se capturaron y marcaron 287 (Ntotal) individuos de M. helenor peleides (217 machos; 70 hembras). La abundancia neta (Nneta) fue de 346 individuos (Tabla 1). El mayor número de capturas se presentó en junio-julio (M7) y mediados de abril (M3) con 92 y 83 individuos respectivamente; mientras que el menor número se registró en marzo (M1), mayo (M5) y principios de junio (M6) (Tabla 1).
Se recapturaron 59 mariposas (20,5%), 46 machos (21,1%) y 13 hembras (18,5%); de las cuales 40 fueron recapturadas una vez, 8 fueron recapturadas dos veces y sólo un individuo fue recapturado tres veces. Hay que destacar que los machos presentaron el mayor porcentaje de recaptura con 21,1%, mientras que para las hembras fue de 18,5%. Por otro lado, el mayor valor de recapturas se presentó a finales mayo (M4) con 21 mariposas (16 machos; 5 hembras) y los menores valores a principios de abril (M2) y julio (M7) con 3 y 2 individuos respectivamente (Tabla 1).
Tabla 1 Variación de la abundancia de M. helenor peleides durante los periodos de muestreo y por estaciones, en un paisaje de BST en la Vereda la Flecha, San Jacinto, Bolívar.

Abreviaturas: Capturas (C), Recapturas (R), Macho (♂), Hembra (♀)
Teniendo en cuenta las estaciones, la E4 presentó el mayor número de capturas con 111 mariposas (88 machos; 23 hembras) y la E5 presentó el mayor número de recapturas con 31 individuos (27 machos; 4 hembras), mientras que la E1 y E7 presentaron los menores valores de captura (6 y 2 respectivamente) y recaptura (0) (Tabla 1). Con el Modelo lineal generalizado (MLG) se demostró que la abundancia de M. helenor peleides varía de forma significativa (p<0.05) entre muestreos y entre estaciones. Además, se determinó que en la variación de la abundancia de esta mariposa en el área de estudio hay un efecto tanto de los muestreos y de las estaciones.
El tamaño de la población teniendo en cuenta el estimador de Jolly-Seber varió de 8 a 338 individuos durante los siete eventos de captura y recaptura en el área de estudio (Figura 3). Las probabilidades de supervivencia más altas se observaron en abril, donde también se registró la población más alta de individuos según el método utilizado (Tabla 2). Se registraron números poblacionales bajos en la época seca (marzo) y durante las lluvias fuertes (mayo), con picos en la abundancia poblacional luego de las primeras lluvias (abril) (Figura 3).
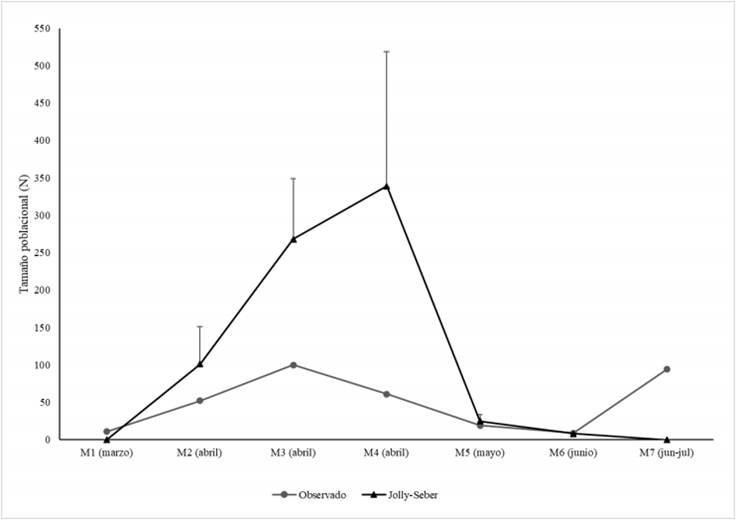
Figura 3 Tamaño poblacional estimado de Morpho helenor peleides durante el período de estudio (de marzo a julio de 2018) según el método Jolly-Seber en un paisaje de BST en la Vereda la Flecha, San Jacinto, Bolívar.
Tabla 2 Fluctuación del tamaño poblacional observado y estimado (Nt) de Morpho helenor peleides con el método de Jolly-Seber en un paisaje de BST en la Vereda la Flecha, San Jacinto, Bolívar.
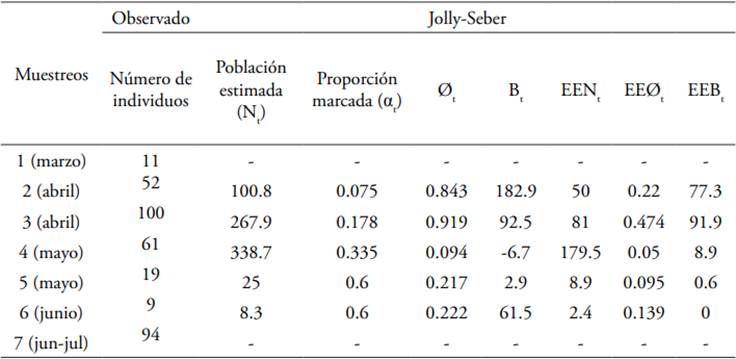
Abreviaturas: Øt: Probabilidad de supervivencia; Bt: Número de ganancias; EEJ: Error estándar Jolly-Seber; EEØt: Error estándar supervivencia; EEBt: Error estándar número de las ganancias.
Proporción Sexual
La proporción sexual (macho-hembra) fue 3:1, donde el número de machos generalmente fue mayor con respecto al número de hembras (Tabla 1). Se encontraron diferencias significativas (X2 = 45,734; p<0,001) entre las proporciones observadas y esperadas para los sexos. La máxima proporción de macho-hembra (14:1) se presentó en el muestreo siete, y la mínima (1:1) se presentó en el muestreo cuatro (Tabla 1). En el muestreo cinco la proporción sexual observada se invierte, siendo mayor el número de hembras (Tabla 1).
Estructura de edades
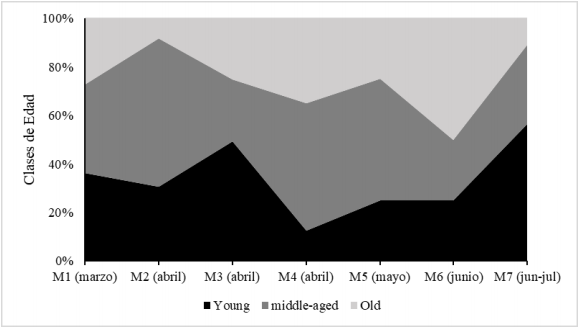
La estructura de edades de la población no fue constante durante el periodo de estudio; se encontraron diferencias significativas en el número de individuos por categoría de edad (X2 = 45,55; p<0,001). La mayor parte del tiempo, se capturaron mariposas nuevas (41,8%) e intermedias (38,6%) y pocos individuos viejos (19,5%) (Figura 4). En el mes de abril y principios de julio (M7) se registró el mayor porcentaje de individuos nuevos (M3) e intermedios (M2); mientras que el mayor porcentaje de individuos viejos se registró en junio (M6) (Figura 4). Por sexos, se encontró que el mayor porcentaje de machos (44,7%) se obtuvo en la categoría nuevo, mientras que el mayor porcentaje de hembras (45,7%) se obtuvo en la categoría intermedia. Para ambos sexos se obtuvo un menor porcentaje en la categoría viejos (18,8% machos y 21,4% hembras).
Tiempo de Residencia
No se encontraron diferencias significativas entre el tiempo de residencia de machos (17,02±7,3 días; N= 46) y hembras (18,6±6,8 días; N= 13) (U= 273; p>0,05). La mayoría de las recapturas ocurrieron en los intervalos de 11 a 20 días y de 21 a 30 días (Figura 5). La mariposa con el tiempo de residencia más largo fue un macho capturado y marcado por primera vez en los primeros días de abril y recapturado por última vez a mediados de mayo, con 38 días después de su primera captura.
Desplazamiento
Se calcularon distancias totales de vuelo (Dt) entre los 149m hasta los 1,231m. La distancia máxima recorrida por una hembra fue de 669m, mientras que la distancia máxima recorrida por un macho fue de 1231m. Se encontró un mayor promedio de distancia recorrida en las hembras (303.7±189.4m), mientras que en los machos fue menor (276.8±209.9m) (Figura 6). No se encontraron diferencias significativas entre las distancias recorridas por los machos y las hembras (U= 265,5; p>0,05); (mediana hembras= 220, N=13; mediana machos= 200, N=46). Se registraron desplazamientos entre las estaciones dos, cuatro, cinco y seis (E2, E4, E5 y E6). El mayor número de individuos recapturados se desplazó entre la E4 y E5 (Figura 7).

Figura 6 Distancias recorridas por M. helenor peleides durante el período de estudio (de marzo a julio de 2018) en un paisaje de BST en el área de estudio.
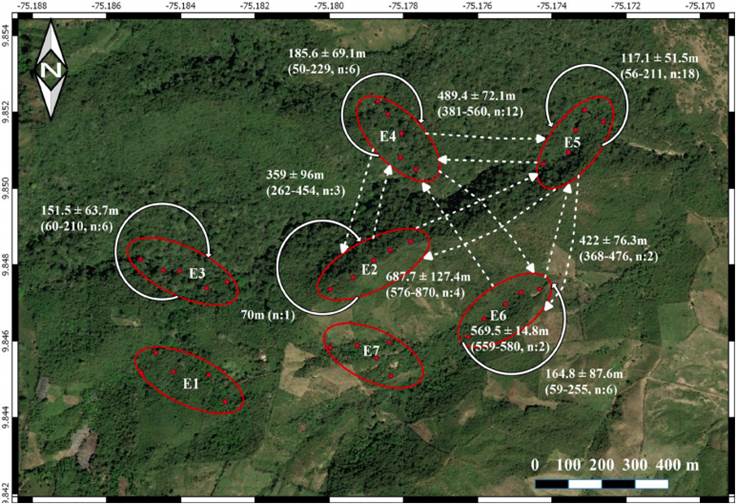
Figura 7 Desplazamiento de M. helenor peleides entre las estaciones (E) de muestreo en un paisaje de BST en la Vereda La Flecha, San jacinto, Bolívar, Colombia. Se indica el promedio y la desviación estándar; en paréntesis se indican los valores mínimos-máximos y el número de individuos. Las flechas continuas y curvas indican desplazamiento dentro de las estaciones. Las fechas punteadas y rectas indican desplazamiento entre las estaciones.
Correlación entre la abundancia de Morpho helenor peleides y las variables abióticas analizadas
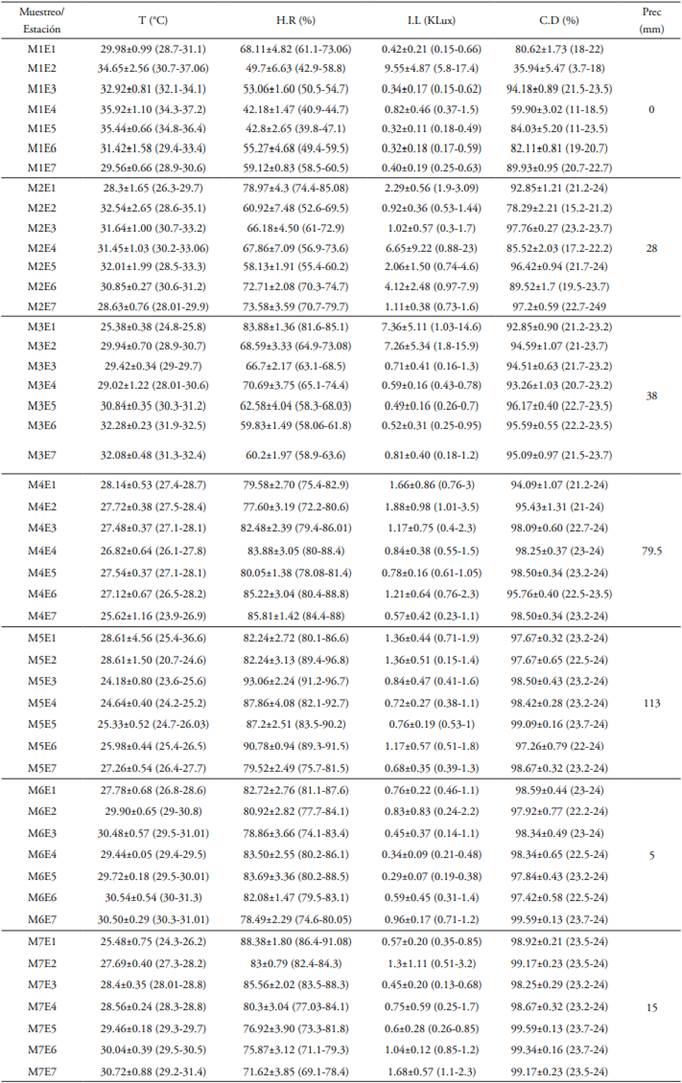
Teniendo en cuenta las variables ambientales, la temperatura (T) presentó el mayor valor (35,92±1,10°C) en marzo en E4 y el menor (24,18±0,80°C) en mayo en E3; mientras que la humedad relativa (H.R) fue inversamente proporcional a la temperatura, ya que el mayor valor (93,06±2,24%) se registró en mayo en E3 y el menor valor (42,18 ±1,47%) en marzo en E4. Por otro lado, el mayor valor (9,55±4,87 Klux) de intensidad lumínica (I.L) se registró en marzo en E2 cuando la cobertura de dosel (C.D) fue menor (35,94±5,47%) y el menor valor (0,29±0,075 Klux) se registró en junio en E5 cuando la cobertura de dosel fue mayor (97,84±0,43%). En el caso de la precipitación, los mayores valores (79,5; 113mm) se presentaron en abril (M4) y mayo respectivamente y los menores (0 y 5mm) en marzo y junio (tabla de variables, material suplementario 2).
Los análisis de correlación entre las variables abióticas (cobertura de dosel, temperatura, intensidad de luz, humedad relativa) mostraron que existe una correlación significativa entre la cobertura de dosel y el resto de las variables analizadas. Se observó una correlación inversa entre la cobertura de dosel con la temperatura (r= -0,58; p<0,001) y la intensidad de luz (r= -0,49; p<0,001), es decir que en puntos con alta cobertura de dosel se registraron bajas temperaturas y valores bajos de intensidad lumínica. En el caso de la humedad relativa, se observó una correlación positiva (r= 0,64; p<0,001), es decir que en puntos con alta cobertura de dosel se registraron valores altos de humedad relativa. Teniendo en cuenta lo anterior se realizaron análisis de correlación entre la abundancia de M. helenor peleides y la cobertura de dosel, por muestreos y estaciones. Los análisis de correlación por muestreos fueron bajos y no significativos. En los análisis de correlación por estaciones se observaron correlaciones altas y significativas entre la abundancia de esta mariposa y la cobertura de dosel, en las estaciones cuatro (E4) (r= 0,75; p<0,001) y cinco (E5) (r= 0,62; p<0,001).
Discusión
La abundancia de M. helenor peleides registrada a mediados de abril, puede deberse a que su ciclo reproductivo este sincronizado con las primeras precipitaciones; las cuales inciden en la productividad primaria del BST proporcionando un beneficio indirecto para este grupo de mariposas, debido a la alta disponibilidad de recursos alimenticios y sustratos para la ovoposición (Fagua & Ruiz, 1996; Pollard, 1988; Vargas et al., 2012; Wolda, 1978). Lo anterior refuerza lo obtenido por Freire, Nascimento, Konstantino y Diniz (2014); García, Galluser, Lachaume y Blandin (2014); quienes expresan que la transición entre la época seca y de lluvias es el periodo asociado con la mayor abundancia de mariposas Morpho. El incremento en el número de individuos a finales de junio y principios de julio, sugiere un nuevo pico de emergencia de imagos, ya que hasta esa fecha transcurrieron 73 días después de las primeras lluvias y del registro del mayor número de hembras. Lo anterior coincide con el tiempo de desarrollo desde huevo hasta adulto (entre 69 y 75 días) que se ha reportado para esta especie por Constantino y Corredor (2004), y Ruiz, Vásquez, Zarate y Pinedo (2015).
El método de JS funciona mejor cuando se tiene una gran cantidad de capturas y buen porcentaje de recapturas (Lemos et al., 2005), razón por la cual las estimaciones del tamaño poblacional en abril (M3 y M4) deben ser las más cercanas al tamaño de la población estimado para el paisaje estudiado. Así mismo, la población estimada para este mes concuerda con largos periodos de sol, lluvias moderadas y un aumento en la tasa de emergencia de imagos, lo que conllevó a un alto número de capturas y recapturas.
Comúnmente en las poblaciones de especies del género Morpho la cantidad de machos detectables es mayor que la de hembras; sin embargo, esto no se debe a una proporción diferencial en los nacimientos (Young, 1973; Young & Thomason, 1974), sino como resultado de los diferentes patrones de comportamiento y/o mortalidad entre los sexos que afectan las probabilidades de captura (Ochoa et al., 2018; Schaeffer et al., 2019; Young, 1982). Los machos de esta especie vuelan con mayor frecuencia a través de quebradas y senderos en el bosque, exhibiendo un comportamiento de patrullaje; mientras que las hembras vuelan a mayor altura cerca de la vegetación, probablemente en busca de plantas hospederas. De esta manera, este tipo de comportamiento influye en la probabilidad de captura de esta mariposa; por lo tanto, el sexo más activo es comúnmente el más recolectado u observado (Schaeffer et al., 2019). Estas observaciones son similares a las de Young (1973), García, Constantino, Heredia y Kattan (2002); Chazot, Panaras y Zilbermann (2016), quienes reportan que los machos de estas mariposas patrullan un área estableciendo rutas de vuelo. Por otro lado, la mejor estrategia para aumentar el número de hembras capturadas, sería instalar algunas trampas VSR a mayor altura y de forma alterna, de tal manera que se cubran varios estratos verticales de la vegetación. Esto no fue posible debido a la complejidad topográfica de algunas áreas del paisaje en las que el acceso y la instalación de las trampas eran complicados.
La estructura de edades con respecto al porcentaje de individuos nuevos y viejos, fue similar a lo reportado por Ochoa, Escorcia, Duran y Prieto (2018) para M. rhodopteron en la Sierra Nevada de Santa Marta y contrario a lo descrito por Prieto, Takegami y Rivera (2005) para Morpho sulkowskyi en la cordillera occidental colombiana. La distribución bimodal de la abundancia (dos picos marcados, en abril y julio), sugiere que probablemente esta es una especie bivoltina, sin embargo, es posible que se den más de dos generaciones anuales debido a los ciclos de vida cortos (menos de tres meses) reportados para M. helenor y todas sus subespecies (excepto M. helenor carillensis) (Constantino & Corredor, 2004; García et al., 2014; Ruiz et al., 2015); por lo que es necesario analizar el número de generaciones durante un ciclo anual completo. El menor porcentaje de individuos viejos en la población puede indicar alta mortalidad en esta categoría de edad por el aumento de la tasa de depredación por parte de aves, puesto que el deterioro de las alas afecta la capacidad de vuelo y la habilidad para escapar de los depredadores (Young & Thomason, 1974). Lo anterior se evidenció en que muchos individuos viejos, carecían de porciones muy simétricas de ambas alas posteriores; además en varias ocasiones se encontraron restos de alas debajo de algunos árboles en senderos y quebradas.
El individuo más longevo en este estudio fue capturado y registrado por primera vez en la categoría de edad nuevo, posteriormente al ser recapturado por última vez presentaba las alas deterioradas y muy descamadas, lo que ratifica las observaciones realizadas por Young y Thomason (1974) para M. peleides limpida en Costa Rica. Para las mariposas frugívoras los beneficios nutricionales de consumir frutas y materia orgánica en descomposición pueden ser uno de los factores responsables de prolongar la vida y pueden estar relacionados con la inclusión de aminoácidos en la dieta (Molleman et al., 2008).
Entre los diversos componentes del paisaje estudiado, se dan variaciones microclimáticas locales que condicionan la distribución de M. helenor peleides. El desplazamiento a través del borde (E2) indica que estas mariposas utilizan esta zona como corredor para moverse entre el interior del bosque (E3, E4, E5) y remanentes de vegetación en sucesión (E6), probablemente en busca de recursos alimenticios. En lugares con alto porcentaje de cobertura de dosel natural (84,03-99,59%) en los que el estrato arbóreo se encuentra bien representando (E4, E5), se mantienen niveles altos de humedad (77,5±9,8%) que son detectados por estas mariposas a través de receptores higroscópicos cuticulares (Palanca, 1975; Freire et al., 2014). Esto favorece la permanencia de la mariposa en lugares con alto porcentaje de cobertura vegetal natural, lo que se evidenció en la gran abundancia registrada en estas estaciones. Otro factor que podría explicar la abundancia de esta mariposa en estas estaciones (E4, E5) es la disponibilidad de la planta hospedera (Machaerium sp); en la cual se observaron hembras ovopositando. Por otro lado, en las áreas de cultivos y potreros (E1, E7), los cambios en la abundancia, composición y diversidad vegetal, ocasionados por los distintos usos del suelo, hacen que los parámetros microclimáticos sean más cambiantes (Collinge et al., 2003). Esto dificulta la estancia de esta mariposa en estos hábitats, por lo que la mayoría de los individuos se concentran en el interior del bosque (E3, E4, E5); donde las condiciones ambiéntales son más favorables para llevar a cabo muchas de sus funciones vitales.
Estos resultados sugieren que la cobertura de dosel natural y la presencia de las plantas hospederas, es un factor fundamental en la variación espacial de la estructura poblacional de M. helenor peleides en la VLF. Los registros de recaptura indican que esta mariposa se desplaza entre áreas de bosque y vegetación secundaria en la VLF, lo que sugiere que el movimiento de los individuos está influenciado por la variación de los parámetros ambientales en pequeñas escalas espaciales y la distribución de recursos alimenticios para larvas y adultos. De esta manera, la heterogeneidad del paisaje en la zona juega un papel importante en la variación de la abundancia de esta mariposa, demostrándose que este lepidóptero tiene una marcada preferencia por el interior de bosque. Esto representa mayor vulnerabilidad de extinción local (Vargas et al., 2011), razón por la cual se hace necesario gestionar la inclusión de esta “reserva” dentro del marco legal de áreas protegidas.