Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Ciencias Químico - Farmacéuticas
Print version ISSN 0034-7418On-line version ISSN 1909-6356
Rev. colomb. cienc. quim. farm. vol.37 no.1 Bogotá Jan./June 2008
Artículo de Revisión
Elementos conceptuales para estudiar el comportamiento bioadhesivo en polímeros
Conceptual elements to study the bioadhesive behavior in polymers
Bibiana M. Vallejo Díaz1, Jairo E. Perilla2
1 Universidad Nacional de Colombia, Departamento de Farmacia. Correo electrónico: bmvallejod@unal.edu.co
2 Universidad Nacional de Colombia, Departamento de Ingeniería Química. Correo electrónico: jeperillap@unal.edu.co
Recibido para evaluación: agosto 15 de 2007 Aceptado para publicación: marzo 17 de 2008
RESUMEN
La bioadhesión es un fenómeno interfacial que ocurre entre un material polimérico y una superficie biológica. Las interacciones entre las fases son el resultado tanto de las propiedades del polímero como de la naturaleza del sustrato.
En este documento se estudian los aspectos teóricos fundamentales que permiten entender los mecanismos que se proponen para la interpretación del fenómeno desde cada una de las teorías existentes, considerando los factores que determinan el comportamiento bioadhesivo de un polímero y las características del sustrato. Finalmente se analizan las técnicas experimentales existentes para determinar la bioadhesividad en materiales poliméricos y las aplicaciones en el diseño de algunos sistemas terapéuticos farmacéuticos.
Palabras clave: Bioadhesión, interfase adhesiva, tensión interfacial, mucoadhesión, superficies.
SUMMARY
The bioadhesion is an interfacial phenomenon ocurring between a polymer and a biological surface. Due to the complex nature of polymers and molecules present in the biological surfaces, many factors determine the strength and duration of the adhesion. However, the specific interactions in the polymer/biological substrate interface are governed by both, the properties of the polymer and the nature of the substrate.
In this document the theoretical fundamentals of the current mechanisms that have been proposed to explain bioadhesion are reviewed. Also, the main factors determining the bioadhesive behavior of a polymer and the properties of the substrate are discussed. Finally, the experimental techniques to evaluate the bioadhesion in polymers are analyzed, and the applications in some therapeutic pharmaceutical systems presented.
Key words: Bioadhesion, adhesive interface, interfacial tension, mucoadhesion, surfaces.
INTRODUCCIÓN
El término bioadhesión se ha utilizado para describir el fenómeno relacionado con la capacidad que tienen algunas macromoléculas de origen natural y de síntesis para adherirse a tejidos biológicos, se fundamenta en los mecanismos conocidos de la adhesión convencional, con la particularidad que representan las propiedades y características de los tejidos naturales (1).
Los sistemas bioadhesivos han sido empleados en el campo de la salud, especialmente para aplicaciones odontológicas y ortopédicas, como también para uso oftálmico y quirúrgico y actualmente en el estudio sobre reemplazo de tejidos y la liberación controlada y localizada de principios activos sobre mucosas (2).
Las aplicaciones potenciales de este fenómeno exigen un estudio minucioso sobre los fundamentos que rigen el comportamiento de los materiales poliméricos que se utilizan para estos desarrollos cuando se encuentran en contacto con superficies de tipo biológico y cómo, a partir del entendimiento de estos principios, es posible desarrollar materiales con mejores propiedades de desempeño y proponer formulaciones optimizadas para utilizar como sistemas bioadhesivos.
CONCEPTOS GENERALES
Se denomina "adhesiva" la sustancia que al estar en contacto entre dos superficies permite una unión resistente a la separación. Los sustratos o adherentes corresponden a los materiales que se unen por medio del adhesivo, y al conjunto de interacciones físicas y químicas que se presentan en la interfase adhesivo-adherente se le conoce como "adhesión"; la "cohesión" corresponde a la fuerza de atracción que mantiene unidas las moléculas de un material (Figura 1) (3).

El fenómeno adhesivo es complejo (4), al no poderse predecir completamente a partir de las propiedades superficiales del adhesivo y del sustrato (adhesión intrínseca) y la adhesión medida mediante un ensayo mecánico (adhesión experimental).
En el estudio de la adhesión se encuentra que la interfase puede ser dividida en diferentes regiones, que se diferencian en función de la distancia con respecto a la superficie del sustrato; su caracterización contribuye en la interpretación del comportamiento adhesivo en los materiales.
-
Región comprendida entre la superficie del adherente hasta 1 nm: en ésta se producen interacciones químicas entre átomos del adhesivo y del adherente. Cuando la ruptura se produce en esta zona, se encuentra relación entre la adhesión intrínseca y la experimental.
-
Región comprendida entre 1 y 103 nm: corresponde a los cambios morfológicos en la estructura de las cadenas poliméricas (interacciones moleculares entre cadenas de polímero). La ruptura en esta zona se asocia a las propiedades superficiales del adherente y del sustrato.
-
Región situada por encima de 103 nm: es la zona donde se transmiten los esfuerzos mecánicos realizados durante un ensayo de adhesión. En esta zona no es fácil diferenciar entre adhesión intrínseca y experimental.
INTERACCIONES FISICAS Y QUIMICAS
La adhesión en materiales poliméricos está determinada por uniones físicas, uniones químicas secundarias y uniones químicas primarias como enlaces iónicos o covalentes. Las uniones químicas primarias se obtienen a partir de la reacción química de grupos funcionales del material adhesivo con el sustrato. Su uso principal es en adhesivos empleados en ortopedia y odontología, cuando se requieren tiempos de uso prolongados (5).
En el caso de las uniones químicas secundarias que corresponden a enlaces químicos de menor energía, se presentan características más apropiadas para la bioadhesión por su transitoriedad. La interacción entre dos de estas moléculas es el resultado de fuerzas de atracción y repulsión; la cuantía de estos dos fenómenos determina si interaccionan o no. Para que ocurra la bioadhesión, la interacción atractiva debe ser mayor que la repulsión no específica (5, 6). Este tipo de fuerzas contribuye principalmente sobre las propiedades bioadhesivas de los polímeros, específicamente las fuerzas de Van der Waals y la formación de puentes de hidrógeno, y se relacionan con la estructura química del material adhesivo; los polímeros que presentan grupos carboxilos e hidroxilos en su composición presentan los mejores comportamientos bioadhesivos (7, 8).
Los puentes de hidrógeno tienen un papel importante en la unión adhesiva al generarse puntos de contacto entre las cadenas del polímero y la superficie del sustrato. Las energías de enlace correspondientes en cada uno de los tipos de unión pueden ser comparadas (Tabla 1).

Por lo que hace relación a los mecanismos físicos, el comportamiento adhesivo de los polímeros se estudia cuando se establece un contacto íntimo entre el polímero bioadhesivo y la superficie irregular del tejido. En la interfase de contacto se origina una interpenetración de las moléculas del polímero en el gel del tejido de la mucosa y viceversa, que da lugar a uniones semipermanentes que promueven la posterior interacción química propiamente bioadhesiva. Como factores que contribuyen al fenómeno de configuración de este entrabado se encuentran la fluidez y flexibilidad molecular del polímero, la viscosidad del bioadhesivo y la rugosidad del sustrato. El fenómeno también depende del tiempo; se requiere la difusión de las moléculas del polímero y la formación de entramados entre las cadenas (6, 10).
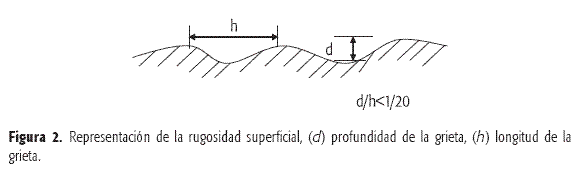
De los factores señalados, la colocación e inclusión del material adhesivo entre las cavidades o grietas del sustrato son importantes, razón por la cual la rugosidad superficial del sustrato contribuye en la manifestación del fenómeno (1).
A partir de un análisis microscópico de la superficie del sustrato, la rugosidad se define como la relación que existe entre la profundidad máxima (d) y la longitud de la grieta (h), (Figura 2). En este caso, la viscosidad del material es determinante para alcanzar a penetrar las cavidades y contribuir en la estabilidad de la unión adhesiva. Para considerar la contribución de la rugosidad en la unión, se requieren valores superiores de 1/20 de la relación d/h (7).
ANALISIS DE LA INTERFASE
En el estudio termodinámico de la interfase se define la tensión interfacial como el aumento en la energía libre de Gibbs de todo el sistema, resultado del incremento en el área interfacial, cuando el proceso se realiza en condiciones de temperatura y presión constantes (11), según la ecuación 1.

Cuando se considera la interfase formada entre dos fases A y B como una región de espesor infinito t donde la composición cambia por compresión de A sobre B, el potencial químico de cualquiera de las especies debe ser igual en las dos fases y en la interfase: (E 2)

Para cada una de las fases, la expresión general de la energía libre de Gibbs tiene la forma: (E 3)
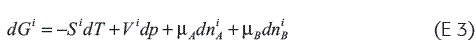
Al llevarse a cabo en condiciones de temperatura y presión constantes, el comportamiento en la interfase i se puede expresar: (E 4)

En la Ecuación 4, cualquier transferencia de A o de B o desde la región interfacial necesariamente involucra un cambio de área interfacial, por lo cual esta contribución debe ser incluida: (E 5)
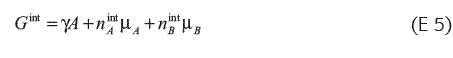
Cuando se expresa la concentración interfacial de especies como i, la ecuación anterior puede ordenarse en términos de la tensión interfacial y obtener la expresión: (E 6)
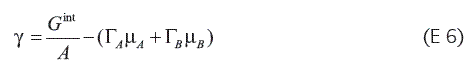
Entre tanto, la entropía de formación de interfase ΔSintA por unidad de área está dada por: (E 7)

La entalpía de formación de la interfase por unidad de área se define como: (E 8)

En síntesis, puede considerarse que el estudio termodinámico de la interfase formada implica la cuantificación de la energía en exceso y de la entropía asociada con la interfase.
TEORIAS QUE EXPLICAN EL COMPORTAMIENTO BIOADHESIVO
Para entender los mecanismos que explican la bioadhesión a partir del comportamiento de los materiales en la interfase, la comunidad científica ha interpretado las teorías aceptadas para adhesión, asimiladas al comportamiento de las interfases polímero-sustrato biológico (12); así, para estudiarlo pueden clasificarse de acuerdo con el mecanismo químico o físico de la interacción.
1. Teoría electrónica
Ha sido estudiada por Derjaguin, fundamentado en que el sistema adhesivo-sustrato se comporta como un condensador, que se carga por contacto entre los dos materiales. La separación de las partes, como una interfase de ruptura, da lugar a una separación de carga y a una diferencia de potencial que aumenta hasta que ocurre la descarga (3, 4).
En la formación de la doble capa, la energía Ac necesaria para separar la interfase está dada por: (E 9)

En la que Vc, es el potencial de descarga, en la distancia hc y ed, es la constante dieléctrica.
La interpretación en el comportamiento bioadhesivo establece que tanto el polímero como el tejido sustrato presentan diferente estructura electrónica, la cual da lugar a una doble capa con carga eléctrica localizada en la interfase entre el bioadhesivo y el tejido. Las fuerzas de atracción electrostática se deben a la transferencia de electrones, entre las glicoproteínas de la mucina del tejido biológico y el material bioadhesivo, lo cual induce atracciones electrostáticas entre las dos superficies (13).
2. Teoría de adsorción
También conocida como teoría de adsorción termodinámica, explica la bioadhesión en términos del desarrollo de fuerzas superficiales que generan uniones químicas entre el polímero y el sustrato-como enlaces covalentes y enlaces iónicos- o fuerzas débiles como puentes de hidrógeno y del tipo Van der Waals (3, 6).
De acuerdo con este modelo, la adhesión se produce cuando el adhesivo moja al sustrato. Para cuantificar esta capacidad se miden los ángulos de contacto (q) de diversos líquidos patrón sobre la superficie del sustrato. A partir de los valores de ángulo de contacto se puede calcular la energía de superficie (WA) del sustrato: (E 10)

Yl es la tensión superficial del líquido, la capacidad óptima para mojar, que se consigue cuando el ángulo de contacto es bajo. Además se produce una adhesión intrínseca adecuada cuando WA del sustrato es mayor que la energía superficial del adhesivo (14).
El trabajo de bioadhesión puede explicarse termodinámicamente como la suma de las tensiones superficiales del material bioadhesivo () y el tejido () menos la tensión interfacial (), de acuerdo con la ecuación de Dupre (1). (E 11)

3. Teoría mecánica
Es una de las primeras teorías planteadas para explicar el comportamiento adhesivo de materiales. En ella se establece que el fenómeno se debe al anclaje del adhesivo en los poros y oquedades superficiales del sustrato, que proveen un aumento de área superficial y al endurecerse se fijan a múltiples sitios de anclaje (9).
4. Teoría de fractura
En ésta se relacionan las fuerzas de adhesión con la fuerza necesaria para separar las dos superficies adheridas. Se utiliza para explicar el comportamiento bioadhesivo de polímeros rígidos; también se conoce como modelo de capas débiles de rotura preferente (Figura 3).

El esfuerzo de fractura asociado con la falla, σ, que es equivalente a la fuerza de la unión bioadhesiva, se puede calcular mediante la Ecuación 12, en la que E corresponde al módulo de elasticidad de Young, ε es la energía de fractura y L la longitud crítica de fractura durante la separación de las dos superficies (3, 15).

El estudio se realiza sobre la propagación de la falla en la unión adhesiva, la cual no se produce en la zona interfacial, sino que se manifiesta hacia zonas débiles de la superficie del sustrato o del adhesivo y se denomina falla cohesiva (6, 9).
5. Teoría de la humectación
Ha sido la teoría más aceptada para explicar el comportamiento de bioadhesivos líquidos y para analizar la bioadhesión en términos de la capacidad de un material para distribuirse sobre una superficie biológica. La capacidad bioadhesiva de un polímero es función de su coeficiente de dispersión, para desarrollar contacto con el sustrato biológico (14).
Mediante la ecuación de Young se relacionan las tensiones en las tres fases de contacto y el ángulo formado por el líquido bioadhesivo, (subíndice b)con el tejido que actúa como sustrato (subíndice t), en un ambiente fisiológico (subíndice f). Las tensiones en las tres fases de contacto se denotan bf, en el punto líquido / vapor, bt, en el punto sólido / líquido y tf, en el punto sólido / vapor (Figura 4). La ecuación de Young (13) tiene la forma:
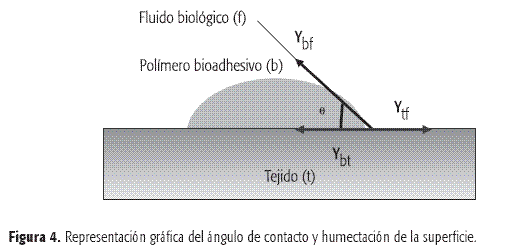

Cuando el ángulo θ es mayor que 0°, el líquido no se distribuye sobre la superficie, pero cuando es igual a 0°, el líquido humecta al sólido completamente y de manera espontánea se esparce sobre la superficie a una velocidad que depende de factores como la viscosidad del líquido y la rugosidad de la superficie sólida (1, 7).
La humectación del sistema se puede expresar mediante el parámetro denominado coeficiente de dispersión en equilibrio, S, que se relaciona con la diferencia entre el trabajo de bioadhesión y el trabajo de cohesión, de la forma: (E 14)

Cuando el valor de S es igual a cero o mayor, el adhesivo se dispersa espontáneamente sobre la superficie del tejido. Esto es posible también aun cuando θ>0°, pero requiere aplicar una presión o forzar al adhesivo a distribuirse sobre la superficie sólida (16).
Los parámetros que caracterizan la humectación son el ángulo de contacto θ, la tensión superficial γ y la energía libre interfacial líquido-sustrato W, que se relacionan con la ley de Young-Dupré:

La rugosidad superficial también tiene efectos sobre el ángulo de contacto cuando se estudia una superficie lisa, en cuyo caso se encuentra la expresión: (E 16)

En la cual rf es el factor de rugosidad, y los subíndices en cada caso corresponden a los ángulos de contacto que se observan sobre las superficies rugosa y lisa, respectivamente. Al aumentar la energía libre superficial del sólido, también aumenta la capacidad de humectación (7).
Como modelo para estudiar que puede ser aproximado al comportamiento de los materiales bioadhesivos, se encuentra la propuesta de Good y Girrfalco (3) para determinar la energía superficial de cada material que participa en la bioadhesión. La tensión interfacial entre dos fases se puede representar como: (E 17)
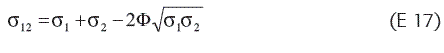
En la que σ1, σ2 son las tensiones superficiales de las fases simples, y σ12, la tensión interfacial entre las fases; corresponde a un parámetro de interacción, definido en términos de geometrías moleculares y fuerzas de interacción de las fases. Su cálculo se hace experimentalmente, (17). Esta expresión en la notación que se ha venido empleando en el texto da lugar a la ecuación: (E 18)
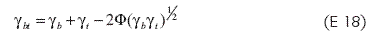
Para un mejor análisis del fenómeno, Fowkes introdujo las contribuciones de las fuerzas de dispersión debidas a la carga asimétrica alrededor de los átomos o con respecto al centro de gravedad de las moléculas (3, 4). Por consiguiente, la tensión interfacial se puede expresar como: (E 19)

En la cual las fuerzas de dispersión existen en todas las moléculas, y las fuerzas polares, sólo en moléculas especiales; estas fuerzas surgen de la diferencia de electronegatividad entre los diferentes átomos en la misma molécula. Owens, Wendt, Rabel y Kaeble estudiaron la existencia de la componente polar, para lo cual σd es la componente de dispersión y σp es la componente polar de la tensión interfacial: (E 20)

De acuerdo con estos planteamientos, la contribución de las fuerzas polares y de dispersión a la energía libre superficial de materiales bioadhesivos puede ser expresada mediante la ecuación: (E 21)

Ecuación en la cual i puede ser el material bioadhesivo o el tejido, y los superíndices d y p hacen referencia a los componentes de dispersión y polares del polímero bioadhesivo y de la red de la glicoproteína. En estos términos, la tensión interfacial γbt, puede ser expresada como: (E 22)
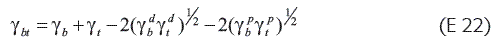
Así, mediante la determinación de la tensión superficial del polímero y del sustrato biológico, se pueden predecir fenómenos adhesivos de interés y proponer asociaciones entre materiales para obtener mejores resultados en una unión bioadhesiva.
6. Teoría de difusión
Es también conocida como teoría de la interpenetración. Se utilizó inicialmente en el estudio del comportamiento adhesivo de polímeros gomosos y es actualmente una de las más importantes para describir el fenómeno bioadhesivo, mediante la difusión (8).
La bioadhesión es el resultado de un gradiente de concentración entre las moléculas del sustrato biológico, como la mucina, y las cadenas flexibles del polímero hasta desarrollar el enredamiento físico entre los dos tipos de moléculas (Figura 5).
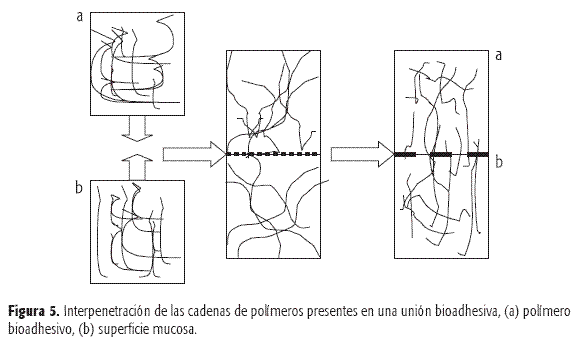
Los valores encontrados para el coeficiente de difusión de polímeros a través de redes de glicoproteínas de mucus se encuentran entre 10-10-10-16 cm2/seg; la profundidad exacta de interpenetración necesaria para que tenga lugar la unión adhesiva se estima que sea del orden de 0,2 -0,5 µm (10). De esta hipótesis es posible calcular el tiempo para la bioadhesión, según la Ecuación 23, en la cual l es la profundidad de interpenetración y Db corresponde al coeficiente de difusión del polímero bioadhesivo a través del mucus.

En la teoría desarrollada por Vasenin (3, 18, 19), se parte de la ley de Fick, que relaciona una cantidad de material w, que se difunde en la dirección x a través de un plano de área unitaria, normal al gradiente de concentración dc/dx y el tiempo t, en la cual Df es el coeficiente de difusión. (E 24)

El fenómeno no se presenta en estado estacionario. Se supone, por tanto, que las especies que difunden están interdifundiendo dentro de las regiones de la superficie, durante el tiempo de contacto tc. En la Ecuación 25, Dd corresponde a una constante que caracteriza la movilidad de las macromoléculas y β es una constante que determina la rapidez de cambio del coeficiente de difusión Df. El valor calculado para el coeficiente fue de 0,5; a partir de éste se obtuvo la profundidad de penetración lp, según la Ecuación 26, en la que k3 es una constante que caracteriza la rigidez y longitud de unión de las moléculas del polímero.


También se dedujo el número Nc de cadenas moleculares que cruzan las fronteras de la fase entre el adhesivo y el sustrato, expresado como: (E 27)

Ecuación en la cual N es el número de Avogadro, p corresponde a la densidad y M es el peso molecular del polímero.
FACTORES ASOCIADOS CON EL POLIMERO QUE DETERMINAN SU COMPORTAMIENTO BIOADHESIVO
1. Peso molecular
La fuerza bioadhesiva de un polímero aumenta con el peso molecular (20); sin embargo, pesos moleculares muy altos dificultan la hidratación de aquel y se impide la liberación de los grupos que interactuarán con el sustrato; entre tanto, pesos muy bajos dan lugar a geles débiles que se disuelven fácilmente (6, 21).
En algunos estudios se ha encontrado que la fuerza adhesiva aumenta con polímeros de peso molecular hasta 100.000. Este comportamiento se asocia con la longitud crítica molecular, necesaria para producir la capa de interpenetración y enredamiento (8, 22). Se recomienda hacer la comparación entre tamaño molecular más que entre pesos moleculares, si se tienen cadenas largas que puedan enredarse; en una longitud crítica, es posible que puedan formar puentes mientras se anclan en sus terminaciones, aumentando notablemente la bioadhesión a la interfase (23).
La ecuación de Pragger y Tirrell que se deriva del modelo de reptación de Gennes se utiliza para explicar la relajación configuracional en las uniones entre polímeros, considerando el movimiento aleatorio de una cadena polimérica confinada en un tubo (24). Los cálculos de Pragger y Tirrell consideraron la probabilidad de los desplazamientos de la cadena en el tiempo, estableciendo la posibilidad de generar uniones por unidad de área, como una función del tiempo de contacto y del peso molecular del polímero.
2. Flexibilidad
Por tratarse de un proceso difusivo de las cadenas del polímero en la región interfacial se requiere un alto grado de flexibilidad para lograr enredamientos con el mucus; a mayor densidad de enlaces, la longitud efectiva de la cadena que puede penetrar en el mucus disminuye, reduciéndose la fuerza mucoadhesiva (13).
Las propiedades de una solución de polímeros pueden ser simuladas por el modelo de cadena reptante (Kratky-Porod Worm-Like Chain Model) y se puede expresar en términos de rigidez o resistencia al doblado en términos de una longitud persistente, p (25, 26).
Este modelo fue desarrollado sin considerar la libertad de giro de la cadena, pero introduce la noción de morfología de cadena curva continua, con un ángulo formado entre los dos segmentos (o vectores unitarios tangentes a los segmentos), con una distancia l entre éstos. Esta distancia es mucho menor a la longitud total de la cadena, definida como: σ (l). Tanto en el caso de rotación libre de la cadena, como en la conformación tipo reptante, se presenta una relación, que se muestra en las Ecuaciones 28 y 29.
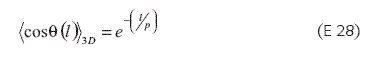
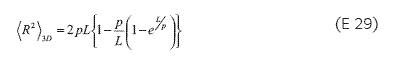
En la cual p es la longitud y R2 es el cuadrado medio de la distancia entre extremos cuando L tiende a infinito; la distancia es: R23D=2pL. Esta consideración da por sentado que todos los ángulos σ (l) son independientes entre sí.
También han sido utilizados diferentes conceptos de longitud, en los cuales la cadena se representa como una serie de n uniones de igual longitud λ, cuya configuración de equilibrio es una forma rectilínea. El cambio local en energía libre requerido para producir una curva a través de dos ángulos σ (i) en la i-ésima unión y está definido como: (E 30)
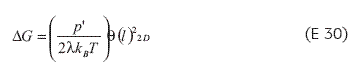
Ecuación en la cual p' es una expresión de la resistencia microscópica local al curvado y es comparable directamente a la cantidad p, utilizada en el modelo de cadena reptante, la cual ocasiona efectos de gran escala tales como exclusión por volumen, que se pueden ignorar. éste es el caso de polímeros a baja concentración para evitar el traslapamiento cuando se depositan sobre la superficie (conformaciones de equilibrio en soluciones diluidas) y cada unión es independiente de sus vecinas (19, 27).
3. Capacidad de formación de puentes de hidrógeno
La mucoadhesión de un polímero se encuentra en función de la capacidad para formar este tipo de uniones (8). Muchos investigadores han llegado a conclusiones similares pero no absolutas sobre el fenómeno. Se trata de moléculas lineales o poco ramificadas para evitar impedimentos estéricos, las cuales deben tener alto peso molecular y presentar grupos funcionales hidrófilos capaces de formar puentes de hidrogeno, tener flexibilidad suficiente para penetrar la malla mucosa o hendiduras del tejido y con características adecuadas de tensión superficial para mojar la superficie del tejido mucoso.
Los polímeros que han encontrado aplicación como bioadhesivos presentan en su estructura grupos hidroxilo y carboxilo. Algunos estudios presentan una clasificación de la capacidad de los polímeros bioadhesivos para unirse a tejidos, evaluada a partir de análisis por fluorescencia (8, 28). Se identificó que el parámetro que diferencia el potencial de unión de un polímero era el cambio en la relación entre el excímero (E) y el monómero (M) . Un valor alto en esta relación es indicativo de un potencial de unión que indirectamente se relaciona con una fuerte interacción bioadhesiva.
4. Densidad de entrecruzamiento
El tamaño de poro promedio, el peso molecular promedio de los polímeros entrecruzados y su densidad de entrecruzamiento son parámetros estructurales que están relacionados. Cuando se aumenta la densidad de entrecruzamiento, la difusión de agua entre la red del polímero se presenta a muy baja velocidad, se produce insuficiente hinchamiento y se disminuye la velocidad de interpenetración entre el polímero y la mucina (29, 30).
5. Carga
Dado que las moléculas de mucina se encuentran cargadas negativamente a pH neutro, se puede dar lugar a fuertes interacciones entre electrolitos de carga contraria; así los polímeros policatiónicos podrían ser excelentes mucoadhesivos a pH neutro; por el contrario, a bajos valores de pH, en los que la mucina no se encuentra cargada, los policatiónicos han mostrado poca efectividad (31-33).
6. Concentración del polímero bioadhesivo
En altas concentraciones, el polímero puede presentar poca bioadhesión al sustrato, pues adquiere una conformación replegada y no dispone de grupos suficientes para establecer interacciones adhesivas. Cuando la concentración del polímero es menor, las uniones se intensifican; sin embargo, una concentración muy baja favorece la interpenetración, pero la unión formada es inestable a causa del número escaso de moléculas que penetran por unidad de volumen (30).
7. Hidratación e hinchamiento
Las cargas de la red molecular del polímero facilitan la entrada de agua en cantidad suficiente para provocar la hidratación, el hinchamiento y expansión del gel, y hacen posible la movilización de las cadenas del polímero bioadhesivo que exponen todos los lugares de unión y facilitan la interdifusión o interpenetración del gel de mucus (5, 29, 34).
8. Solubilidad polímero-mucus
La penetración de polímeros, transporte de masa de largas cadenas de polímeros a través de la interfase bioadhesiva, ocurre por difusión regular o por interpenetración dentro de una red de glicoproteínas. Para que se produzca una difusión óptima, los polímeros deben ser miscibles entre sí (3, 9). La miscibilidad de los polímeros se puede cuantificar mediante la determinación del parámetro de solubilidad δ(s).
Los valores de los parámetros de solubilidad dependen del grado de interacciones intermoleculares en el disolvente o en el polímero. Dos polímeros, dos disolventes o un polímero y un disolvente son miscibles si tienen parámetros de solubilidad parecidos. Este modelo de difusión muestra que los polímeros con parámetros de solubilidad muy diferentes no presentan adhesión.
Estimar el parámetro de solubilidad de un polímero (δ2) puede llevarse acabo como una propiedad aditiva y constitutiva con base en las constantes de atracción molar F, de los grupos que lo constituyen (9, 19), empleando la Ecuación 31.
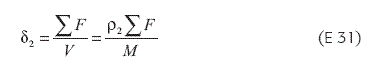
Para la expresión V y F corresponden al volumen molar y al peso molecular, respectivamente, y p2 es la densidad del polímero; los valores de F se encuentran en tablas especializadas.
FACTORES INDIRECTOS QUE PUEDEN AFECTAR LA UNION BIOADHESIVA
Existen algunas consideraciones desde la parte fisiológica que pueden interferir sobre la bioadhesión y se relacionan con la renovación natural de las moléculas de mucina de la capa de mucus (mucin turn-over), que limitan el tiempo de residencia de los bioadhesivos sobre el sustrato, e independientemente de la intensidad de la fuerza adhesiva, son despegados de la superficie a causa del recambio (35).
También es necesario considerar los factores asociados a estados patológicos, que pueden afectar las propiedades fisicoquímicas del mucus (5); de acuerdo con la vía de administración, se puede o no efectuar una presión inicial sobre la superficie de aplicación del mucoadhesivo, lo cual afecta la profundidad de la interpenetración. Se ha encontrado que al aplicar una presión alta durante períodos suficientemente largos, se puede presentar mucoadhesión aunque no exista atracción entre el polímero y la mucina (6).
Junto a la presión se estudia el tiempo de contacto, que puede afectar de forma decisiva la funcionalidad del sistema, determinando la extensión de la hidratación y del hinchamiento de los polímeros de alto peso molecular con estiramiento de las cadenas poliméricas y la interpenetración con la malla formada por las cadenas glicoproteícas de la mucina; por tanto, la fuerza adhesiva aumenta a medida que el tiempo de contacto inicial aumenta (12, 36).
PROPIEDADES DE UN SUSTRATO PARA BIOADHESION
Al ser crítico el efecto del sustrato sobre el cual se pretende realizar la unión adhesiva, es necesario realizar algunas consideraciones para la interacción entre un polímero bioadhesivo y el gel de mucus, como sustrato, para los procesos de mucoadhesión. En el caso de bioadhesión sobre la piel intacta, se deben tener en cuenta otras consideraciones (37).
Las membranas mucosas se caracterizan por ser superficies húmedas que recubren las paredes de las cavidades corporales. El mucus es secretado por células especializadas, directamente sobre la superficie del epitelio. La capa mucosa está compuesta principalmente de agua hasta el 95% en peso, glicoproteínas de mucina generalmente menos del 5% en peso, sales inorgánicas cerca del 1% en peso, carbohidratos y lípidos (37).
Las glicoproteínas de mucina son los componentes más importantes en la formación de estructura en el gel de mucus; son O-glicoproteínas que desde el punto de vista de la ciencia de los polímeros se comportan como copolímeros de bloque con bloques ramificados y sin ramificaciones; representan más del 80% de los componentes orgánicos del mucus y son responsables de sus características como gel y de las propiedades cohesivas y adhesivas (6, 8). Ambos tipos de bloques tienen uniones con proteínas, pero los bloques muy ramificados tienen cadenas de oligosacáridos unidas a ellos (10).
El análisis de las interacciones entre la mucina y las cadenas libres del polímero bioadhesivo en solución acuosa ayuda a dilucidar algunos de los problemas en mucoadhesión. Las interacciones se han explicado en términos de puentes de hidrógeno, interacciones hidrofóbicas, interacciones electrostáticas y reconocimiento de lecitinas-azúcares (38).
En algunas investigaciones (39, 40) se ha encontrado que la incorporación de polímeros mucoadhesivos a un gel de mucus induce un sinergismo reológico y refleja interacciones intermoleculares entre el polímero y el mucus. Como resultado de la interacción se forman enredamientos físicos y uniones no covalentes; también se ha identificado la dependencia de la temperatura y el pH como factores que inciden en la estructura y conformación tanto del polímero bioadhesivo como del mucus.
TECNICAS EXPERIMENTALES EMPLEADAS PARA LA DETERMINACION DE BIOADHESION
Dentro del estudio del comportamiento bioadhesivo de los polímeros, muchas de las apreciaciones teóricas que se han planteado son el resultado de las observaciones adelantadas mediante el empleo de diferentes metodologías analíticas conducentes a contribuir en la interpretación de los fenómenos observados. Dada la importancia del análisis instrumental en la compresión del comportamiento de los materiales, a continuación se presenta un resumen de las técnicas reportadas en diferentes estudios sobre el tema:
1. Análisis de la interfase
En esta clase de ensayos puede determinarse el ángulo de contacto de una gota de agua sobre el sistema bioadhesivo, o en el caso de sistemas líquidos bioadhesivos, el ángulo de contacto estático de una gota del sistema bioadhesivo sobre el sustrato biológico (41).
La determinación de la energía superficial de los materiales puede hacerse por el método de tensión superficial crítica o método de Zisman. Este método no considera la naturaleza diferente de las interacciones que tienen lugar en la interfase entre sólido y líquido. Otros métodos consideran las componentes de dispersión Ysd y polar Ysp de la energía superficial, como ya se señaló.
La utilización de técnicas espectroscópicas para realizar el estudio de polímeros y en bioadhesión ha encontrado una aplicación fundamental para la comprensión del fenómeno al permitir la observación de las estructuras poliméricas y sus superficies; incluyen análisis cuantitativos de átomos y la forma como ellos se unen. Las aplicaciones han sido fundamentalmente para estudiar la superficie química del polímero bioadhesivo, el establecimiento de uniones interfaciales y la identificación de los lugares de falla de la unión bioadhesiva; tal ha sido el caso de los estudios como la espectroscopia de rayos x (1, 12). El empleo de complejos de mucina marcados con oro coloidal en contacto con el polímero bioadhesivo permitió visualizar mediante el uso de un espectrofotómetro la cantidad de complejo que se adsorbe sobre la superficie en función del cambio en el valor de absorbancia. El resultado fue interpretado como indicativo de la interacción bioadhesiva.
2. Determinación de la formación de la unión bioadhesiva
Generalmente en estos ensayos se estudian las interacciones macroscópicas y que involucran la presencia de mucus. Las técnicas in vitro incluyen ensayos de destrucción de la unión adhesiva por fuerzas de corte, peeling y por tensión. Estos se caracterizan por la realización de pruebas mecánicas en las cuales se obtienen curvas de esfuerzo versus deformación a bajas longitudes, y esto dificulta diferenciar si se mide la fuerza de bioadhesión o el trabajo de bioadhesión. El ensayo más simple para medir macroscópicamente la adhesividad consiste en emplear máquinas de ensayo universal en las cuales se mide la fuerza necesaria para separar dos superficies (42-44).
Otro grupo de técnicas corresponde a los métodos reológicos (45), fundamentados en los cambios reológicos cuando se mezclan polímeros con mucina, que interpretan la respuesta reológica total del sistema como resultado de la contribución de cada uno de los polímeros presentes (38, 46). Aunque no dan una explicación completa para caracterizar las interacciones entre el polímero y el mucus, es posible obtener información útil sobre propiedades estructurales de los polímeros y los cambios que se presentan cuando éstos entran en contacto (34, 47-49). Estos ensayos incluyen la determinación de la viscosidad intrínseca de una solución diluida que emplea viscosímetros capilares con temperatura controlada, o en el caso de dispersiones más concentradas y geles, se determinan los parámetros reológicos (G) Módulo de Almacenamiento y (G') Módulo de Pérdida, para lo cual se han utilizado viscosímetros de tipo cono y plato.
Las técnicas ex vivo utilizan órganos aislados de animales para el estudio de las propiedades bioadhesivas de los polímeros. En algunos casos se realizan pruebas mecánicas sobre los sustratos o se emplean sistemas de células marcadas con fluoresceína en contacto con las soluciones de los polímeros potencialmente bioadhesivos, y en ellos se mide la relación excímero / monómero en función del tiempo (1, 12).
Las técnicas in vivo son mucho más complejas e incluyen la marcación del polímero con 99Tc para examinar su distribución en una región específica del organismo, como el tracto gastrointestinal, mediante el empleo de análisis de imágenes, después de una administración por vía oral del producto bioadhesivo a un reactivo biológico de prueba (1, 7).
SISTEMAS TERAPEUTICOS FARMACEUTICOS CON BASE EN POLIMEROS BIOADHESIVOS
Un sistema terapéutico farmacéutico (STF) consta fundamentalmente de un módulo de liberación, un programa terapéutico, un soporte o medio de transporte y uno o varios fármacos o principios activos (Figura 6).
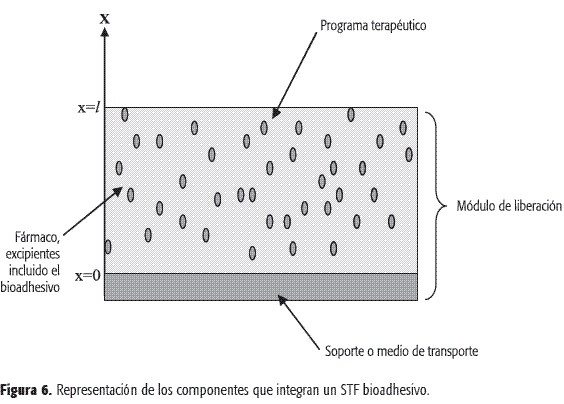
El módulo de liberación es la parte del sistema que garantiza la entrega del fármaco o sustancia activa de acuerdo con un programa terapéutico, establecido en el diseño. Allí puede encontrarse una cámara simple o múltiple que almacena el principio activo, el depósito; la vía o puerta de salida, que puede ser la superficie entera del dispositivo, uno o varios orificios o una cánula; los elementos que generan el potencial químico o mecánico para la liberación, que pueden ser gradientes de concentración, desplazamiento de émbolos, imanes o campos eléctricos (50-54).
El soporte integra todos los elementos y entra en contacto con el biosistema; requiere adaptación completa al lugar anatómico de emplazamiento final y ha de ser inerte ante el fármaco y el medio (50, 55).
La presencia de polímeros bioadhesivos define la funcionalidad principal de un STF, en cuanto a la capacidad de fijarse de manera estable y temporal a una superficie biológica sobre la que se espera ejerza su acción. Así, la tendencia en el desarrollo de nuevos STF se orienta al empleo de biopolímeros biodegradables y biocompatibles, como alternativa para mejorar la liberación de principios activos (56-58), aumentar los tiempos de contacto en el sitio de acción, reducir la frecuencia de administración, conseguir liberaciones tópicas, evitar efectos sistémicos y aprovechar las mucosas como vías de administración de fármacos (28).
Para diseñar sistemas terapéuticos farmacéuticos con características bioadhesivas, se han empleado biopolímeros, que de acuerdo con los investigadores del tema se clasifican como de primera y de segunda generación, en función de la selectividad que pueden presentar sobre las mucosas de estudio.
Dentro del grupo de primera generación se encuentra la mayoría de las moléculas de tipo hidrofílico, que presentan grupos capaces de formar puentes de hidrógeno, como los derivados del ácido poliacrílico (Carbomer®); también se encuentra una marcada tendencia al estudio de formas bioadhesivas con quitosano, polímero policatiónico derivado de la quitina, un polisacárido del exoesqueleto de las langostas y cangrejos.
Se han utilizado polímeros de celulosa como la hidroxipropilmetilcelulosa, sola y en combinación con otros polímeros (59, 60); con hidroxipropilcelulosa (61, 62) y con carboximetilceluosa (63, 64).
Con ácido hialurónico se han desarrollado algunos trabajos (65), y con alginatos (22, 33, 65). Los trabajos sobre polímeros conocidos como el almidón con gran contenido de amilosa han permitido hacer la modificación para mejorar las propiedades adhesivas, con potenciales aplicaciones para el control de la liberación de fármacos (66, 67).
El empleo de polímeros de estrella, aunque menos estudiado, encuentra una potencial aplicación al mejoramiento de las propiedades bioadhesivas, porque se considera que la existencia de múltiples brazos de unión de un polímero de estrella tendría mejor comportamiento que un polímero lineal (68), lo cual fue demostrado con un polímero derivado de dimetilaminoetilmetacrilato.
Los polímeros anteriores han sido incluidos en formulaciones como tabletas (69), parches, y microesferas (70, 71), en las cuales el polímero se encuentra formando una matriz con el fármaco disperso en ella; también se han presentado como ungüentos y pastas bioadhesivas y en formulaciones como geles, insertos vaginales y supositorios (72, 73).
Con el fin de superar las limitaciones de los polímeros bioadhesivos de primera generación, se han realizado algunas modificaciones que emplean grupos tiol, por acoplamiento con cisteína, ácido tioglicólico o cisteamina a polímeros como carbómeros, quitosanos y alginatos (74). Con estos polímeros se forman uniones disulfuro que pueden inhibir la sobrehidratación y formación de mucílagos resbalosos, y que hacen más estable la unión adhesiva.
La modificación química de polímeros con grupos funcionales tipo sulfhidrilo mejora las propiedades mucoadhesivas, característica que se ha demostrado mediante estudios in vivo sobre mucosas nasal, ocular y gástrica (74, 75).
También se han realizado estudios en los cuales se utiliza polietilenglicol (PEG) para hacer injertos sobre polímeros y copolímeros de ácido acrílico, lo cual ha mejorado la adhesión, debida a la interpenetración del polímero en el gel de mucus (76).
Un importante descubrimiento fue el empleo de las lecitinas, proteínas o glicoproteínas de origen no inmunológico, con la capacidad para reconocer moléculas de azúcar y unirse a componentes glicosilados de la membrana. Se consideran bioadhesivos de segunda generación porque tienen la capacidad de interactuar específicamente, con estos residuos mediante interacciones débiles (77). Según la señal biológica transmitida a la célula, los ligandos bioadhesivos específicos pueden producir solo adhesión, o por el contrario, internalización en la célula por diferentes vías, reconociendo estructuras de la membrana celular para unirse a células del epitelio; y por tanto, presentando preferentemente un comportamiento de adhesión sobre la capa mucosa (78).
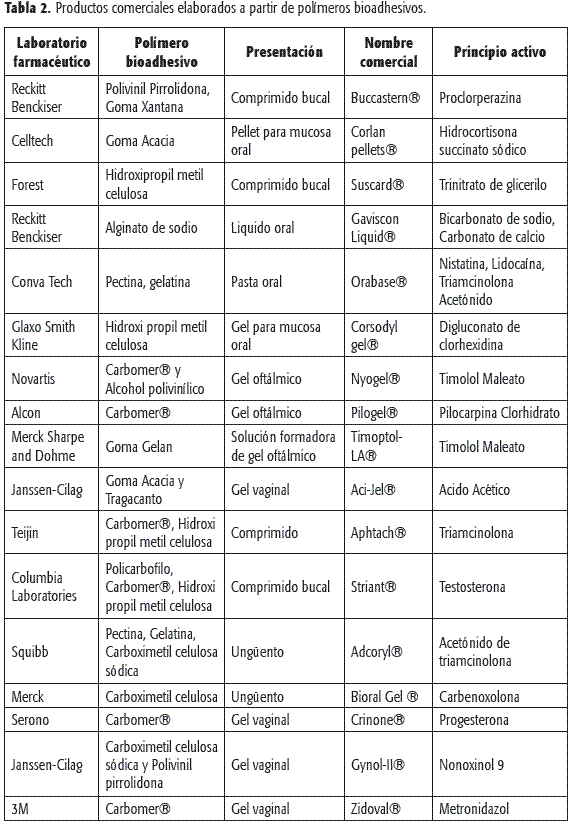
En la Tabla 2 se resumen algunos STF comercialmente disponibles que han sido catalogados como bioadhesivos; se indica el principio activo que contienen y los polímeros utilizados.
CONCLUSIONES
El objetivo de este artículo fue presentar los fundamentos conceptuales asociados con la presencia de fenómenos interfaciales entre materiales poliméricos y su incidencia en la formación de uniones adhesivas sobre sustratos de origen biológico. Se entiende que el empleo de un polímero implica comprender los fundamentos físicos y químicos que determinan la formación de uniones estables y permanentes en el tiempo y la interpretación de las relaciones de estos materiales con los sustratos sobre los cuales interactúa.
Se encontró que los materiales empleados como bioadhesivos tienen como característica la formación de entrecruzamientos a través de uniones físicas, formación de puentes de hidrógeno y otro tipo de uniones secundarias entre las cadenas poliméricas del material bioadhesivo y las cadenas poliméricas del mucus.
Se ha visto que las interacciones bioadhesivas se pueden estudiar en diferentes escalas, tanto microscópicas como macroscópicas, en función de las técnicas existentes; sin embargo, hasta el estado actual de desarrollo de la ciencia, no existe un único modelo que pueda describir el fenómeno interfacial estudiado, en su complejidad.
AGRADECIMIENTOS
Los autores agradecen formalmente a la Universidad Nacional de Colombia por el apoyo de la DIB al proyecto de investigación código 88071: "Estudio del Fenómeno de adhesión a superficies biológicas de películas obtenidas a partir de biopolímeros, para aplicación en el área de la salud".
BIBLIOGRAFIA
1. E. Mathiowitz, D. E. Chickering y C. M. Lehr, "Bioadhesive Drug Delivery Systems Fundamentals, novel approaches and development", Marcel Dekker Inc, New York, 1999, pp. 3-65. [ Links ]
2. A. W. Lloyd y J. Swarbrick, "Drug Delivery and Targeting". Edited by Anya M. Hillery, New York, 2001, pp. 154-156. [ Links ]
3. A. J. Kinloch, "Adhesion and Adhesives", Chapman and Hall, London, 1990, pp. 18-100. [ Links ]
4. V. N. Kestelman y R. A. Veselovsky, "Adhesion of Polymers", Mc Graw Hill, New York, 2002, pp. 1-20; 102-109. [ Links ]
5. I. C. Rodríguez, A. Cerezo y I. Salem, Sistemas de liberación bioadhesivos, ARS Pharmaceutica, 41, 115 (2000). [ Links ]
6. J. D. Smart, The basics and underlying mechanisms of mucoadhesión, Advanced Drug Delivery Reviews, 57, 1556 (2005). [ Links ]
7. N. A. Peppas y P. A. Buri, Surface, interfacial and molecular aspects of polymer bioadhesion on soft tissues, Journal of Controlled Release, 2, 257 (1985). [ Links ]
8. N. A. Peppas y J. Sahlin, Hydrogels as mucoadhesive and bioadhesive materials: a review, Biomaterials, 17, 1553 (1996). [ Links ]
9. P. J. Sinko, "Martin's Physical Pharmacy and Pharmaceutical Sciences". Lippincott Company, Baltimore, U.S.A. Fifth edition, 2006, pp. 20-24, 587-602, 437-447. [ Links ]
10. N. A. Peppas y Y. Huang, Nanoscale technology of mucoadhesive interactions, Advanced Drug Delivery Reviews, 56, 1675 (2004). [ Links ]
11. R. A. Jones y R. W. Richards, "Polymers at Surfaces and Interfaces", Cambridge University Press, United Kingdom, 1999, pp. 8-36. [ Links ]
12. S. E. Harding, Mucoadhesive Interactions, Biochemical Society Transactions, 31, part 5, 1036 (2003). [ Links ]
13. Y. Huang, W. Leobandung, A. Foss, y N. A. Peppas, Molecular aspects muco and bioadhesion: Tethered structures and site-specific surfaces, Journal of Controlled Release, 65, 63 (2000). [ Links ]
14. R. Bruinsma y E. Sackmann, "Bioadhesion and the dewetting transition", C.R. Acad.Sci.Paris, t. 2, Série IV, 2001, pp. 803-815. [ Links ]
15. W. F. Smith, "Fundamentos de la ciencia e ingeniería de materiales", Mc Graw Hill, Madrid, tercera edición, 1999, pp. 327-400. [ Links ]
16. A. T. Florence y D. Attwood, "Physicochemical Principles of Pharmacy", Pharmaceutical Press, London, fourth edition, 2006, pp. 177-183, 274-305. [ Links ]
17. S. Wu, Surface and interfacial tensions of polymer melts. II. Poly (methyl methacrylate), Poly (n-butil methacrylate), and Polystyrene., The Journal of Physical Chemistry, 74 (3), 632 (1970). [ Links ]
18. J. Welty, C. Wicks y R. Wilson, "Fundamentos de transferencia de momento, calor y masa", Limusa Wiley. México, segunda edición, 2004, pp. 560-595. [ Links ]
19. L. H. Sperling, "Introduction to physical polymer science", Wiley Interscience, New York, third edition, 2001, pp. 45-50, 63-102, 182-188. [ Links ]
20. D. Tiwari, R. Sauce y P. Madam, Evaluation of polioxyethylene homopolymers for buccal bioadhesive drug delivery device formulations, AAPS Pharmsci, 1 (3), article 3, 3 (1999). [ Links ]
21. B. Ratner, A.S. Hoffman, F. Schoen y J. Lemons, "Biomaterials Science, an Introduction to Materials in Medicine", Elsevier Academic Press, Oxford, 2004, pp. 67-79. [ Links ]
22. H. K. Batchelor, D. Banning, P. W. Dettmar, F. C. Hampson, I. G. Jollife y D. Q. Craig, An in vitro mucosal model for prediction of the bioadhesion of alginate solutions to the oesophagus., International Journal of Pharmaceutics, 238, 123 (2002). [ Links ]
23. L. Richert, A. Engler, D. Discher y C. Picart, Elasticity of native and cross - linked polyelectrolyte multilayer films, Biomacromolecules,5, 1908 (2004). [ Links ]
24. B. Akkok, S. Ugur y O. Peckan, Fast Transient Fluorescence Technique (FTRF) for studying vapor- induced latex film formation, Journal of Colloid and Interface Science, 246, 348 (2002). [ Links ]
25. C. Verdier, Rheological properties of living materials from cells to tissues, Journal of Theoretical Medicine, 5, 67 (2003). [ Links ]
26. A. N. Round, M. Berry, T. J. McMaster, S. Stoll, D. Gowers, A. P. Corfield y M. J Miles, Heterogeneity and persistence length in human ocular mucins, Biophysical Journal,83, 1661 (2002). [ Links ]
27. F. R. Eirich, "Rheology, theory and applications", Academic Press, New York, 1960, pp. 479-503. [ Links ]
28. S. E. Harding, S. S. Davis, M. P Deacon y I. Fiebrig, Biopolymer mucoadhesives, Biotechnology and Genetic Engineering Reviews, 16, 41 (1999). [ Links ]
29. J. D. Smart y S. A. Mortazavi, An investigation into the role of water movement and mucus gel dehydration in mucoadhesión, Journal of Controlled Release, 25, 197 (1993). [ Links ]
30. N. Salamat-Miller, M. Chittchang y T. P. Johnston, The use of mucoadhesive polymers in buccal drug delivery, Advanced Drug Delivery Reviews, 7, 1666 (2005). [ Links ]
31. R. G. Riley, J. D. Smart, J. Tsibouklis, P. W. Dettmar, F. Hampson, J. A. Davis y G. Kelly, An investigation of mucus/polymer rheological synergism using synthesized and characterized poly(acrylic acid)s, International Journal of Pharmaceutics, 217, 87 (2001). [ Links ]
32. X. Zhao, K. Kato, Y. Fukumoto y K. Nakamae, Synthesis of bioadhesive hydrogels from chitin derivates, International Journal of Adhesion & Adhesives, 21, 227 (2001). [ Links ]
33. C. Silva, A. J. Ribeiro, M. Figueiredo, D. Ferreira y F. Veiga, Microencapsulation of hemoglobin in chitosan - coated alginate microspheres prepared by emulsification / internal gelation, The AAPS Journal, 7 (4), article 88, E903 (2006). [ Links ]
34. P. Marshall, J. E. M. Snaar y Y. L. NG, A novel application of NMR microscopy: measurement of water diffusion inside bioadhesive bonds, Magnetic Resonance Imaging, 19, 487 (2001). [ Links ]
35. M. I. Ugwoke, R. U. Agu, N. Verbeke y R. Kinget, Nasal mucoadhesive drug delivery: Background, applications, trends and future perspectives, Advanced Drug Delivery Reviews, 57, 1640 (2005). [ Links ]
36. M. I. Ugwoke, N. Verbeke, R. Kinget, The biopharmaceutical aspects of nasal mucoadhesive drug delivery, Journal of Pharmacy and Pharmacology, 53, 3 (2001). [ Links ]
37. R. Bansil, E. Stanley y J. Thomas, La Mont, Mucin Biophysics, Annual Review Physiology, 57, 635 (1995) [ Links ]
38. F. Madsen, K. Eberth y J. A. Smart, Arheological assessment of the nature of interactions between mucoadhesive polymers and a homogenized mucus gel, Biomaterials, 19, 1083 (1998). [ Links ]
39. S. Tamburic y D. Q. M. Craig, An investigation unto the rheological, dielectric and mucoadhesive properties of poly (acrylic acid) gel systems, Journal of Controlled Release, 37, 59 (1995). [ Links ]
40. H. Hagerstrom, M. Paulsson y K. Edsman, Evaluation of mucoadhesion for two polyelectrolyte gels in simulated physiological conditions using a rheological method, European Journal of Pharmaceutical Sciences, 9, 301 (2000). [ Links ]
41. G. A. Abraham y T. R. Cuadrado, "Métodos de caracterización de biomateriales". Biomateriales, Faenza Editrice Ibérica S. L, Italia, 2004. [ Links ]
42. D. Dimas, P. Dallas, D. Rekkas y N. Choulis, Effect of several factors of the mechanical properties of pressure sensitive adhesives uses in transdermal therapeutic systems, AAPS PharmSciTech, 1 (2), article 16 (2000). [ Links ]
43. T. Khan, K. Peh, H. Ching, Mechanical bioadhesive strength and biologicals evaluations of chitosan films for wound dressing, J. Pharm. Pharmaceut. Sci, 3 (3), 303 (2000). [ Links ]
44. S. J. Pomfret, K. P. Plucknett, V. Normand, W. J. Frith y I. T. Norton, Interfacial adhesion of biopolymer gels measured using the peel test., Materials Research Society, 622, FF7.3.1 (2000). [ Links ]
45. E. E. Hassan y J. M. Gallo, A simple rheological method for the in vitro assessment of mucin-polymer bioadhesive bond strength, Pharmaceutical Research, 7, 491 (1990). [ Links ]
46. F. C. Mackintosh y C. F. Schmidt, Microrheology, Current Opinion, Colloid & Interface Science, 4, 300 (1999). [ Links ]
47. S. Rossi, M. C. Bonferoni y G. Lippoli, Influence of mucin type on polymer-mucin rheological interactions, Biomaterials, 16, 1073 (1995). [ Links ]
48. J. Kocevar-Nared, J. Kristl y J. Smid-Korbar, Comparative rheological investigation of crude gastric mucin and natural gastric mucus, Biomaterials, 18 (9), 677 (1997). [ Links ]
49. H. Hagerstrom, "Polymer gels as pharmaceutical dosage forms. Rheological performance and physicochemical interactions at the gel-mucus interface for formulations intended for mucosal drug delivery", Tesis de Doctorado, Universidad de Uppsala, 2003. [ Links ]
50. J. Bohórquez, "Tendencias en el desarrollo de sistemas terapéuticos", Tesis de Grado, Universidad Nacional de Colombia, 1996. [ Links ]
51. A. Gopferich y R. Langer, Modeling monomer release from bioerodible polymers, Journal of Controlled Release, 33, 55 (1995). [ Links ]
52. Y. Su y L. Lin, A water-powered micro drug delivery system, Journal of Micro Electromechanical Systems, 13, 75 (2004). [ Links ]
53. N. A. Pinzón, A. Espinosa, J. Perilla y I. Katime, Modelación del hinchamiento y difusion de solutos en hidrogeles, Revista Colombiana de Ciencias Químico-Farmacéuticas, 31, 43 (2002). [ Links ]
54. M. L. Zweers, "Biodegradable nanoparticles for intravascular drug delivery", Tesis doctoral, University of Twente, Enschede, The Netherlands, 2003. [ Links ]
55. V. Sáez, E. Hernández, L. Sanz y I. Katime, Liberación controlada de fármacos. Micropartículas, Revista Iberoamericana de Polimeros, 5, 87 (2004). [ Links ]
56. N. Fasiant, J. Siepmann y J. P. Benoit, PLGA-based microparticles: elucidation of mechanism and a new, simple mathematical model quantifying drug release, European Journal of Pharmaceutical Sciences, 15, 355 (2002). [ Links ]
57. R. Langer y D. A. Tirrell, Designing materials for biology and medicine, Nature, 428, 487 (2004). [ Links ]
58. V. Sáez, E. Hernández y L. López, Liberación controlada de fármacos. Aplicaciones biomédicas, Revista Iberoamericana de Polímeros, 4, 111 (2003). [ Links ]
59. A. Koffi, F. Agnely, G. Ponchel y J. L. Grossiord, Modulation of the rheological and mucoadhesive properties of thermosensitive poloxamer-based hydrogels intended for the rectal administration of quinina, European Journal of Pharmaceutical Sciences, 27, 328 (2006). [ Links ]
60. M. D Chavanpatil, P. Jain, S. Chaudari y S. R. Shear, Novel sustained release, swellable and bioadhesive gastroretentive drug delivery system for ofloxacin, International Journal of Pharmaceutics, 316, 86 (2006). [ Links ]
61. M. A. Repka y J. W. McGinity, Physical-mechanical, moisture absorption and bioadhesive properties of hydroxypropylcellulose hot-melt extruded films, Biomaterials, 21, 517 (2000). [ Links ]
62. J. Bajdik, G. Regdon, T. Marek, I. Eros y K. Suvegh, The effect of the solvent on the film forming parameters of hydroxypropyl-cellulose, Internacional Journal of Pharmaceutics, 301, 192 (2005). [ Links ]
63. A. El-Kamel, M. Sokar, V. Naggar y S. Al Gamal, Chitosan and sodium alginate-based bioadhesive vaginal tablets, AAPS PharmSci, 4 (4) article 44 (2002). [ Links ]
64. B. Singh, S. K. Chakkal y N. Ahuja, Formulation and optimization of controlled release mucoadhesive tablets of atenolol using response surface methodology, AAPS PharmSciTech, 7 (1), article 3, E1-E10 (2006). [ Links ]
65. S. Barbault-Foucher, R. Gref, P. Russo, J. Guechot y A. Bochot, Design of poly -e-caprolactone nanospheres coated with bioadhesive hyaluronic acid for ocular delivery, Journal of Controlled Release, 83, 365 (2002). [ Links ]
66. D. Ameye, D. Mus, P. Foreman y J. P. Remon, Spray-dried Amioca starch / Carbopol 974P mixtures as buccal bioadhesive carriers, International Journal of Pharmaceutics, 301, 170 (2005). [ Links ]
67. J. Mulhbacher, P. Ispas-Szabo, M. Oullet, S. Alex y A. Matesscu, Mucoadhesive properties of cross-linked high amylose starch derivates, International Journal of Biological Macromolecules, In Press, No. of pages 6 (2006). [ Links ]
68. A. Limer, A. K. Rullav, V. Sanmiguel, C. Peinado, S. Keely y E. Fitzpatrick, Fluorescently tagged star polymers by living radical polymerisation for mucoadhesión and bioadhesión, Reactive & Functional Polymers, 66, 51 (2006). [ Links ]
69. A. Tunon, "Preparation of tablets from reservoir pellets with an emphasis on the compression behaviour and drug release", Dissertations from the Faculty of Pharmacy 288, Acta Universitatis Upsaliensis, Uppsala 2003. [ Links ]
70. W. Tong, L. Wang, M. D'Souza, Evaluation of PLGA microspheres as delivery system for antitumor agent-camptothecin, Drug Development and Industrial Pharmacy, 29, 745 (2003). [ Links ]
71. I. Galeska, T. K. Kim, S. D. Patil y U. Bhardwaj, Controlled release of dexamethasone from PLGA microspheres embedded within polyacid containing PVA hydrogels, The AAPS Journal, (1), article 22 E231 -E240 (2005). [ Links ]
72. C. Valenta, The use of mucoadhesive polymers in vaginal delivery, Advanced Drug Delivery Reviews, 57, 1692 (2005). [ Links ]
73. A. Ludwig, The use of mucoadhesive polymers in ocular drug delivery, Advanced Drug Delivery Reviews, 57, 1595 (2005). [ Links ]
74. A. Bernkop-Schnurch, Thiomers: A new generation of mucoadhesive polymers, Advanced Drug Delivery Reviews, 57, 1569 (2005). [ Links ]
75. C. M. Lehr, Lectine-mediated drug delivery: The second generation of bioadhesives, Journal of Controlled Release, 65, 19 (2000). [ Links ]
76. K. Yoncheva, E. Lizarraga y J. M. Irache, Pegylated nanoparticles based on poly(methyl vinyl ether-co-maleic anhydride): preparation and evaluation of their bioadhesive properties, European Journal of Pharmaceutical Sciences, 24, 411 (2005). [ Links ]
77. R. Kumar y O. P. Katare, Lecithin Organogels as a potential phospholipid structured system for topical drug delivery: A review, AAPS PharmSci Tech, 6 (2) article 40, E298-E310 (2005). [ Links ]
78. C. Bies, C. M.Lehr y J. F. Woodley, Lectin-mediated drug targeting: history and applications, Advanced Drug Delivery Reviews, 56, 425-435 (2004). [ Links ]














