INTRODUCCIÓN
El estilo de vida actual de la humanidad ha causado la sobreproducción de radicales libres y de especies reactivas de oxígeno (EROs) en el cuerpo humano, incrementando los niveles de estrés oxidativo [1]. El estrés oxidativo está asociado con el incremento de enfermedades tales como: diabetes, hipertensión, obesidad, cáncer, entre otras [2]; sin embargo, los antioxidantes son capaces de neutralizar y eliminar radicales libres y otras especies reactivas de oxígeno [3], protegiendo el cuerpo humano y evitando así el estrés oxidativo y las enfermedades asociadas [4].
El arándano (Vaccinium meridonale) forma parte de la familia Ericaceae, es un fruto nativo, que en Colombia se conoce como agraz o mortiño [1]; es aprovechado por comunidades rurales, que recolectan sus frutos en regiones (Departamentos) como Boyacá, Antioquia y Cundinamarca, de forma silvestre. Este fruto crece en altitudes de (2200-3400 m s.n.m.) [5, 6] y se puede considerar como una fruta rica en compuestos interesantes, antocianinas y flavonoides, los cuales contienen compuestos antioxidantes [7], con estructuras químicas que presentan algunas características que los hacen idóneos para estabilizar o desactivar radicales libres en el cuerpo humano [2].
En cuanto a técnicas de extracción de antioxidantes, se destaca la extracción asistida por microondas (MAE, por sus siglas en inglés) [8, 9]. En este tipo de procesos, una muestra de material vegetal inmerso en un solvente de naturaleza orgánica se expone a radiación microondas bajo condiciones controladas de temperatura y presión [10].
Consecuentemente, las moléculas de agua presentes en los sistemas vasculares de las plantas rompen los tejidos, liberan las biomoléculas allí contenidas y son progresivamente incorporadas al solvente [11]. Las ventajas de este proceso son los cortos tiempos de extracción, y una mayor eficiencia en uso de reactivos, y consecuente rendimiento de la reacción, así como una disminución en los costos, entre otras [12].
La metodología de diseño factorial 2K se ha convertido en una herramienta útil para la realización de diseños experimentales [13] que permiten la determinación de puntos altos y bajos de las condiciones de operación, a partir del análisis de los factores que afectan el valor de respuesta determinada, y un número de puntos experimentales relativamente pequeño [14]. En este caso, la metodología de diseño factorial 2K se ha empleado para determinar las condiciones de operación del equipo de microondas y extraer antioxidantes del fruto Vaeeinium meridionale mediante MAE [15], en la que intervienen 3 variables.
El objetivo de este trabajo fue evaluar las condiciones de extracción de antioxidantes vía MAE teniendo en cuenta diferentes rangos de factores como: temperatura (T), tiempo (t) y concentración del solvente de extracción (% etanol) [16], en la obtención de antioxidantes a partir de frutos de Vaeeinium meridionale, con ayuda de un procedimiento colorimétrico, que emplea el reactivo de DPPH- (2,2-difenil-1-picrilhidrazilo) [17,18].
El método de DPPH- se basa en la reducción del radical DPPH- por los antioxidantes contenidos en la muestra. El radical es estable y tiene una coloración púrpura que se pierde progresivamente cuando se añade la muestra conteniendo sustancias antioxidantes [19]. La decoloración del radical se determina a la longitud de onda (λ) de 515 nm, hasta alcanzar el equilibrio. Las ventajas de este método son que el ensayo DPPH-es un método rápido y sencillo y que no requiere de un equipamiento sofisticado [20]. La desventaja, es que el reactivo sólo puede disolverse en medio orgánico y en algunos casos la interpretación resulta complicada, ya que algunos antioxidantes pueden causar interferencias si poseen un espectro de absorción similar al DPPH- [21].
METODOLOGÍA
El diseño experimental utilizado es un diseño tipo factorial 2K, con un valor de k=3. Se evaluaron los efectos de las variables seleccionadas: temperatura, tiempo y %EtOH en frutos secos de Vaccinium meridionale con variables codificadas A, B y C respectivamente. En la tabla 1 se presentan los valores límite de estas variables, desde los niveles altos (+) y bajos (-) de experimentación [13, 14].
Tabla 1 Variables y niveles del diseño experimental.
| Variable | Nivel bajo (-1) | Nivel alto (+1) |
|---|---|---|
| A = temperatura (K) | 343,15 | 383,15 |
| B = tiempo (min) | 5 | 15 |
| C= % etanol (%EtOH) | 0 | 80 |
Tabla 2 Diseño experimental factorial codificado y variables reales.
| Orden | Temperatura (K) | Tiempo (min) | % etanol (%EtOH) |
|---|---|---|---|
| 1 | -1 (343,15) | -1 (5) | -1 (0) |
| 2 | 1 (383,15) | -1 (5) | -1 (0) |
| 3 | -1 (343,15) | 1 (15) | -1 (0) |
| 4 | 1 (383,15) | 1 (15) | -1 (0) |
| 5 | -1 (343,15) | -1 (5) | 1 (80) |
| 6 | 1 (383,15) | -1 (5) | 1 (80) |
| 7 | -1 (343,15) | 1 (15) | 1 (80) |
| 8 | 1 (383,15) | 1 (15) | 1 (80) |
Se logró encontrar una aproximación adecuada de la verdadera relación funcional entre la variable de respuesta TEAC (capacidad antioxidante equivalente a Trolox) y el conjunto de variables seleccionadas [22]. Se modeló la respuesta mediante regresión lineal de los factores, por medio de análisis de regresión lineal del diseño factorial, cuya función de aproximación es un modelo empírico de primer orden con interacciones según la ecuación (1). Los ensayos se ejecutaron por triplicado, aleatoriamente, para garantizar la validez estadística de los resultados [13, 22]:
Y: variable dependiente, TEAC Trolox (mg/g fruto seco)
A, B, C: variables independientes, (temperatura, tiempo, %EtOH)
β°: punto en el cual la recta intercepta el eje (ordenada en el origen)
β 1 : pendiente de la recta
ε: error aleatorio.
INSTRUMENTOS Y EQUIPOS
Se empleó Trolox (ácido 6-hidroxi-2,5,7,8-tetrametilcromo-2-ácido carboxílico 97%), de marca Merck™ como antioxidante de referencia, y DPPH- (2,2- Difenil-1-picrilhi-drazilo, D-9132), Merck™. Los frutos frescos de la especie Vaccinium meridionale fueron adquiridos en el mercado local de la ciudad de Tunja (Boyacá); posteriormente se analizaron en el Laboratorio de Química y Tecnología de Alimentos de la Universidad Pedagógica y Tecnológica de Colombia (Tunja, Boyacá) [14, 16, 19].
Los frutos se lavaron con agua destilada para remoción de impurezas tales como hojas, tierra y cuerpos extraños. Las muestras se sometieron a un proceso de secado bajo estufa con recirculación de aire, durante 2 horas a una temperatura de 45 °C grados. El registro de los espectros de absorción y las medidas de absorbancia, a longitud de onda fija, se llevaron a cabo con un espectrofotómetro Hach DR 5000. Los análisis estadísticos se realizaron con ayuda del software R Studio® versión libre [14, 23].
Para la obtención de los extractos del fruto Vaccinium meridionale se pesaron 200 mg de fruta seca y se mezclaron con 20 ml de la mezcla solvente {EtOH (del 96%) + agua} en porcentajes EtOH 0% (-1) y EtOH 80% (+1) a tiempo de 5 minutos (-1) y 15 minutos (+1) y temperatura de 343,15 K (-1) y 383,15 K (+1). Posteriormente, las muestras se llevaron al sistema microondas Sineo MDS-8G empleando las condiciones propuestas para el diseño experimental [14, 16]. Finalmente, la mezcla se centrifugó a 4000 rpm, durante de 15 min, en una Centrífuga Hettich Rotina™. El sobrenadante obtenido se conservó para análisis posteriores y se denominó el extracto. Los extractos totalmente acuosos se almacenaron en un refrigerador a 4 °C, y los extractos con etanol en un congelador a -4 °C. Estos últimos extractos fueron analizados dentro de un período no superior a 24 horas después de la extracción para no comprometer la integridad de los analitos.
Actividad antioxidante método DPPH-: este método, desarrollado por Brand et al. [23], se basa en la reducción de la absorbancia medida a 515 nm del radical DPPH-, por los antioxidantes presentes en la muestra. Con modiicaciones el método descrito por Kim et al. [24], se basa en la medida de la absorbancia del radical DPPH- 100 mmol/L disuelto en metanol al 80%, a la longitud de onda de 517 nm. Después, se añade 0,2 mmol/L de la muestra o patrón, la mezcla se homogeniza cuidadosamente, y se mantiene en la oscuridad durante 30 minutos. Las medidas de absorbancia a 517 nm se realizan antes de añadir la muestra (A0) y pasados los 30 minutos (Af). La concentración de DPPH- en el medio de reacción se calcula a partir de una curva de calibrado obtenida por regresión lineal. Los resultados se expresan en TEAC, o actividad equivalente a Trolox (mg/g de muestra peso seco). El antioxidante sintético de referencia Trolox, a una concentración de 0,08-1,28 mmol/L en disolución de metanol al 80%, se analiza bajo las mismas condiciones, expresándose los resultados en TEAC (capacidad antioxidante en equivalentes Trolox) (mg/g fruto seco) [19].
Finalmente, para la determinación de actividad antioxidante por DPPH- se traza una curva de calibración para la técnica utilizando Trolox como compuesto antioxidante de referencia.
RESULTADOS Y DISCUSIÓN
Después de obtener los diferentes extractos de Vaccinium meridionale se preparó una curva de calibración para la técnica utilizando Trolox como compuesto antioxidante de referencia [23], utilizando 5 soluciones patrón. La curva obtenida presenta un coeficiente de correlación R2 = 0,9981 (ver figura y tabla 3).
Tabla 3 Resumen del ANOVA, curva de calibración DPPH-.
| S | R-cuad. | R-cuad. (ajustado) | Fuente | GL | SC | MC | F | P |
|---|---|---|---|---|---|---|---|---|
| Regresión | 1 | 0,504212 | 0,504212 | 1540,91 | 0,000 | |||
| 0,01808 | 99,81 | 99,74 | Error | 3 | 0,000982 | 0,000327 | ||
| Total | 4 | 0,505193 |
Posteriormente se determinó el % de inhibición de acuerdo con la ecuación (2):
Donde:
Am: absorbancia de la muestra control, se toma al inicio de la prueba.
Ap: absorbancias del patrón o muestras de los extractos las diferentes concentraciones.
Se graficó concentración de Trolox (mmol/L) y el porcentaje de inhibición para determinación de la actividad antioxidante TEAC. La curva de calibración, con las variables %inhibición vs. concentración de Trolox, mostró un coeficiente de correlación R2 = 0,9981 (ver tabla 4).
Tabla 4 Resumen del ANOVA, curva de calibración DPPH- % de inhibición.
| S | R-cuad. | R-cuad. (ajustado) | Fuente | GL | SC | MC | F | P |
|---|---|---|---|---|---|---|---|---|
| 1,67101 | 99,81 | 99,74 | Regresión | 1 | 4290,32 | 4290,32 | 1536,49 | 0,000 |
| Error | 3 | 8,38 | 2,79 | |||||
| Total | 4 | 4298,70 |
Determinación de la actividad antioxidante de los compuestos obtenidos por MAE
Espectroscopia UV-Vis. La actividad antioxidante de los extractos obtenidos por MAE de Vaccinium meridionale se midió frente a los radicales libres DPPH-. La medida de la actividad antioxidante por el método permite confirmar la contribución relativa de los diferentes compuestos presentes en el fruto estudiado. En la tabla 5 se presentan los resultados obtenidos de la actividad antioxidante por el método y de acuerdo con el diseño experimental utilizado en la investigación.
Análisis del modelo de regresión codificado para el diseño factorial 23, de primer orden, en la extracción de antioxidantes de frutos de vaccinium meridionale, según las variables consideradas
El objetivo del análisis de regresión es modelar de manera matemática el comportamiento de una variable de respuesta en función de una o más variables independientes. Los datos codificados a partir del diseño factorial 23 contemplan el número de tratamientos entre las combinaciones de las variables independientes codificadas como temperatura (A), tiempo (B) y % de EtOH (C) tabla (2). La respuesta como TEAC mostró diferencias significativas entre todos los tratamientos con un (p < 0,001). Según el análisis de regresión codificado de la tabla 6, las variables A y C tienen un mayor efecto en el sistema, generando una mejora en la respuesta TEAC. Se observa que el único factor que no tiene un efecto significativo es B ya que su P-value es el único que se acerca a 0,001 [13, 25].
Tabla 6 Análisis del modelo de regresión codificado. Fórmula TEAC = A + B + C.
| Error estándar estimado | Error del modelo | t value | Pr(>|t|) | |
|---|---|---|---|---|
| Intercepto | 1,5975 | 0,1916 | 8,340 | 0,00113 ** |
| A | 1,4600 | 0,1916 | 7,622 | 0,00159 ** |
| B | 1,3600 | 0,1916 | 7,100 | 0,00208 ** |
| C | 1,5050 | 0,1916 | 7,857 | 0,00142 ** |
Códigos nivel significancia: 0 '***' 0,001 '**' 0,01 '*' 0,05 '.' 0,1 ' ' Error residual del modelo: 0,2709 en 4 grados de libertad (DF), R2: 0,977, R2 ajustada: 0,9598 F-estadística: 56,77 en 3 y 4 DF p-value: 0,0009807.
Se observa en la figura 3 que el modelo no es lineal y q hay una tendencia en los datos diferente a cero. La gráfica de distribución (normal Q-Q) muestra que el modelo no tiene comportamiento normal ya que todos los valores de TEAC no tienen un comportamiento lineal. Por ello, se realiza el análisis de residuales, comprobando que no hay evidencia para creer que los residuos no siguen la distribución normal. Los resultados obtenidos se llevaron a una gráfica de efectos (ver figura 4) que muestra la magnitud de la influencia de cada factor presente en el estudio, observando que no todos los factores son significativos ya que sus efectos son iguales [26], por tanto es necesario ajustar el modelo a un modelo lineal con interacciones y variables reales para determinar los factores de importancia en los niveles de estudio alto y bajo con los valores reales del diseño experimental planteado en la investigación [13, 18, 27].
El modelo lineal sin interacciones no es estadísticamente significativo para la variable de respuesta TEAC. Se puede observar en la tabla 6, que si bien en la ecuación (1) el valor del error aleatorio es diferente de cero y que el valor R2 = 0,977, con R2 ajustado = 0,9598, el modelo matemático no se ajusta en su totalidad a los valores experimentales de la investigación [28]. De esta forma, el modelo obtenido con un ajuste lineal, que considera los efectos y las interacciones significativas en el desempeño del método está enunciado en la ecuación (3) [13, 29].
Desarrollo de la ecuación (3) utilizando variables codificadas, para el nivel alto.
Determinación de la actividad antioxidante de los compuestos obtenidos por MAE (variables originales)
En la tabla 7 se observan los resultados del diseño experimental 23 con las variables originales que se utilizaron en el procedimiento analítico llevado a cabo en el equipo de MAE.
Tabla 7 Resultados variables originales del diseño 23 por DPPH-.
| Ensayo | Temperatura (K) | Tiempo (min) | Etanol (% EtOH) | TEAC |
|---|---|---|---|---|
| 1 | 343,15 | 5 | 0 | 1,78 |
| 2 | 383,15 | 5 | 0 | 2,78 |
| 3 | 343,15 | 15 | 0 | 2,82 |
| 4 | 383,15 | 15 | 0 | 4,65 |
| 5 | 343,15 | 5 | 80 | 2,97 |
| 6 | 383,15 | 5 | 80 | 4,79 |
| 7 | 343,15 | 15 | 80 | 4,55 |
| 8 | 383,15 | 15 | 80 | 5,74 |
TEAC: actividad antioxidante equivalente al Trolox (mg /g fruto seco).
Análisis del modelo de regresión del diseño factorial 23 de primer orden con interacciones (variables reales)
Actividad antioxidante TEAC. El análisis de regresión demostró que el modelo es altamente significativo como se puede observar en la tabla 8 y que, además, es evidente a partir del test de Fisher (F modelo = 7) con un muy bajo valor de probabilidad (P modelo> 0,000) [30]. El valor del coeficiente de determinación ajustada (R2 ajustada) es de 1, estadística que ofrece cierto indicio de la capacidad predictiva del modelo de regresión de la ecuación (5) que no presenta error aleatorio (s), como se puede observar en la tabla 9 y en el desarrollo de la ecuación (5) utilizando variables reales, para el nivel bajo y alto [31].
Tabla 8 Análisis de regresión unidades originales con interacciones: fórmula TEAC= temperatura * tiempo * %EtOH.
| Error estándar estimado | Error del modelo | t value | Pr(>|t|) | |
|---|---|---|---|---|
| Intercepto | - 3,759 | NA | NA | NA |
| Temperatura | 0,01463 | NA | NA | NA |
| Tiempo | -0,608 | NA | NA | NA |
| %EtOH | -0,1547 | NA | NA | NA |
| Temperatura* tiempo | 0,002075 | NA | NA | NA |
| Temperatura* %EtOH | 0,0004844 | NA | NA | NA |
| Tiempo*%EtOH | 0,01633 | NA | NA | NA |
| Temperatura*tiempo*%EtOH | 0,00004563 | NA | NA | NA |
(NA): no aplica error residual del modelo: NA en 0 grados de libertad (DF), R2: 1, R2 ajustada: NA F-estadística: NA, en 7 y 0 DF p-value: NA.
En cuanto el resultado del análisis experimental y el valor predicho por el modelo matemático de primer orden con interacciones se ajusta el modelo un nivel de confianza del 100% como se observa en la tabla 9, de otro lado, la figura 4 muestra que las variables que tienen un efecto más significativo son el tiempo y el %EtOH. Estos resultados son comparables a los reportados por otros autores, cuyo objetivo era extraer por MAE polifenoles de especies vegetales como Rosemary (Rosmarinus officinalis L.) [32].
Tabla 9 Resultados obtenidos del diseño factorial 23 y predicción del modelo para actividad antioxidante sobre la variable de respuesta en TEAC.
| Obser | Temperatura (K) | Tiempo (min) | %etanol (%EtOH) | TEAC (mg/g) | Ecuación 5 ajustada | ε.(±) |
|---|---|---|---|---|---|---|
| 1 | 343,15 | 5 | 0 | 1,78 | 1,78 | 0,00 |
| 2 | 383,15 | 5 | 0 | 2,78 | 2,78 | 0,00 |
| 3 | 343,15 | 15 | 0 | 2,82 | 2,82 | 0,00 |
| 4 | 383,15 | 15 | 0 | 4,65 | 4,65 | 0,00 |
| 5 | 343,15 | 5 | 80 | 2,97 | 2,97 | 0,00 |
| 6 | 383,15 | 5 | 80 | 4,79 | 4,79 | 0,00 |
| 7 | 343,15 | 15 | 80 | 4,55 | 4,55 | 0,00 |
| 8 | 383,15 | 15 | 80 | 5,74 | 5,74 | 0,00 |
TEAC: actividad antioxidante equivalente al Trolox (mg/g fruto seco).
Es necesario realizar un análisis de los mecanismos de reacción de la forma como cada una de estas variables se comportan en relación con los sistemas solvente-variables físicas, y su efecto significativo en procesos de extracción asistida por microondas (MAE) de frutos de la especie Vaccinium meridonale, para determinar actividad antioxidante por el método DPPH- sobre la variable de respuesta en TEAC [13, 28].
Desarrollo de la ecuación (4) utilizando variables reales, para el nivel bajo y alto.
Etanoly tiempo
El coeficiente de correlación, R, mide la intensidad de la relación lineal entre las variables y varía entre -1 y 1, si R fue próximo a -1 indica que existió una fuerte relación lineal negativa entre las variables, señalando una disminución de TEAC al aumentar el tiempo de calentamiento o almacenamiento; si fue próximo a 0, no hubo correlación lineal; y si fue próximo a + 1, hubo una fuerte relación lineal positiva entre las variables, por lo que un aumento del tiempo y la concentración de etanol, implicaría un aumento de la TEAC [13, 29].
Análisis de regresión unidades originales interacción tiempo*%EtOH
La finalidad del modelo de la ecuación 4 es reproducir el comportamiento de las variables tiempo* %etanol. El modelo de primer orden con interacciones muestra que estas variables son las que tienen mayor importancia con respecto a la variable dependiente TEAC lo cual, a partir del análisis de regresión de la tabla 10, indica que el modelo R2 es de 64% de la variabilidad en la respuesta del porcentaje de extracción de compuestos con propiedades antioxidantes, mientras que el R2 ajustado es de 37%, lo que indica que las variables son altamente significativas.
Tabla 10 Análisis de regresión unidades originales interacción tiempo* %etanol. Fórmula = TEAC ~ tiempo *% etanol.
| Error estándar estimado | Error del modelo | t value | Pr(>|t|) | |
|---|---|---|---|---|
| Intercepto | 1,5525000 | 1,1909424 | 1,304 | 0,262 |
| Tiempo | 0,1455000 | 0,1065211 | 1,366 | 0,244 |
| %etanol | 0,0211875 | 0,0210531 | 1,006 | 0,371 |
| Tiempo*%etanol | -0,0002375 | 0,0018830 | -0,126 | 0,906 |
Error residual del modelo: 1,065 en 4 grados de libertad (DF), R2: 0,645, R2 ajustada: 0,3788F-estadística: 2,423, en 3 y 4 DF p-value: 0,2061.
Los p-value obtenidos para las variables: tiempo (p<0,244), %EtOH (p<0,375) y la interacción tiempo*%etanol (p<0,906) muestran que el tiempo es la variable que tiene mayor influencia en la respuesta TEAC seguido del %EtOH. La influencia en la respuesta del sistema ante cambios en las variables puede ser observada claramente en la siguiente figura:
Se desarrolló la ecuación 5 para las variables que tienen un efecto más significativo, para el nivel bajo y alto.
Se observa que el impacto de la interacción de los factores tiempo y %EtOH es altamente positiva para el sistema, aumentando considerablemente el desempeño de procesos de MAE en frutos de la especie Vaccinium meridionale, para determinar actividad antioxidante por el método DPPH- sobre la variable de respuesta en TEAC.
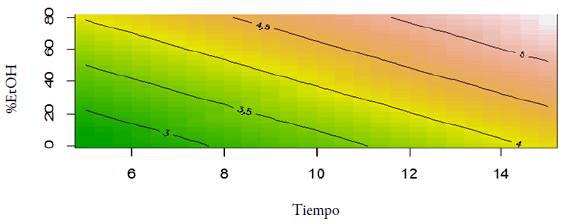
Tiempo vs. %etanol
El modelo obtenido del análisis de superficie de respuesta figura 7 y el análisis de contornos de la figura 8, de un modelo de primer orden con interacciones, indica que el comportamiento de las variables tiempo y etanol es directamente proporcional en el proceso, demostrando que estas son las variables con mayor un efecto sobre a la variable de respuesta, y en menor medida la temperatura ya que en el nivel bajo se tiene una respuesta de 2,8 TEAC y a medida que aumenta el tiempo y el %EtOH la variable de respuesta aumenta hasta 5,4 TEAC aportando cerca del 64% de eficiencia en la extracción [13, 31].

Figura 7 Gráfica de superficie de respuesta efecto del tiempo (min)* %EtOH sobre la extracción de antioxidantes.
La superficie de respuesta obtenida muestra que el método propuesto para la extracción de antioxidantes de la especie Vaccinium meridionale no tiene un desplazamiento hacia puntos máximos o mínimos de las variables que intervienen en el proceso; por lo tanto, es posible observar que el comportamiento del método es directamente proporcional a los cambios en las variables.
CONCLUSIONES
En comparación con los métodos convencionales empleados para la extracción de compuestos con actividad antioxidante, presentes en frutas, el método de extracción asistida por microondas ofrece una alternativa con mayores atractivos en términos del ahorro energético, la reducción considerable de disolventes que pueden afectar las condiciones medioambientales y unos tiempos significativamente menores de proceso, que redundan de modo definitivo en la eficiencia del proceso.
La aplicación de un diseño factorial 23 en la extracción asistida por microondas y evaluación de la actividad antioxidante de los compuestos presentes en frutos de Vaccinium meridionale Swartz demuestra que, en términos de diseño y modelamiento, puede ofrecer alternativas con resultados comparables con la aplicación de otros diseños estadísticos.