Introducción
La contaminación del agua en el Perú se ha convertido en un grave problema que alcanza distintos territorios y genera diferentes dificultades. Una de estas dificultades está relacionada con el deterioro de la calidad del agua del Río Tumbes por el vertimiento de metales pesados y otros elementos, producto de la minería artesanal, y por la carga orgánica y microbiana, producto de la actividad urbana en la parte alta de la cuenca.
El Río Tumbes es un río binacional que nace en Ecuador en cuya parte alta, cerca de las poblaciones de Portobello y Zaruma, se desarrolla ilegalmente minería aurífera artesanal. A su vez, las poblaciones ubicadas en la parte alta de la cuenca vierten sus aguas residuales, tratadas y sin tratar, al cauce del Río Tumbes cargándolo de materia orgánica y bacterias fecales 1.
Durante el año 2014, el Proyecto de Modernización del Recurso Hídrico, manejado por la Autoridad Nacional del Agua 2, estableció que 52% de los parámetros analizados en el Río Tumbes excedieron los estándares de calidad ambiental de agua 3. Dentro de estos parámetros se encontraron niveles altos de los coliformes fecales y cantidades totales de elementos como: P, Al, Sb, As, Cd, Fe, Mn y Pb. Esto afecta a las poblaciones rurales que toman el agua del río de manera directa o con un tratamiento muy precario. A pesar de este problema sanitario, no se han establecido medidas concretas que puedan servir para mitigar los efectos de la contaminación del Río Tumbes.
Los metales pesados y los metaloides son uno de los principales grupos inorgánicos contaminantes del agua y son altamente peligrosos para el ser humano. Este peligro se debe a que pequeñas concentraciones metálicas tienen la capacidad de bioacumularse en el organismo y son causa de varios problemas de salud que pueden derivar incluso en cáncer 4, como ocurre con el As, Cd y Pb, entre los más peligrosos. Al respecto, los estándares de calidad ambiental 5 definen para la categoría A: poblacional y recreacional; subcategoria A1: aguas que pueden ser potabilizadas con desinfección, que las concentraciones máximas permitidas de As, Cd y Pb son 10, 3 y 10 μg/L, respectivamente.
El agua potable en el Perú ha sido definida en el Reglamento de la Calidad del Agua para Consumo Humano establecido en la norma vigente (Decreto Legislativo Supremo N° 031-2010-SA) 6, que establece como límites permisibles un máximo de 500 bacterias heterotróficas por mL y ausencia absoluta de coliformes totales y fecales. De los muchos microorganismos infecciosos que se pueden encontrar en el agua destacan bacterias como Escherichia coli, Salmonella typhimurium y Shigella flexneri. Estos microorganismos pueden provocar síntomas como náuseas, vómitos, diarrea y calambres estomacales. En personas adultas, con un buen estado de salud, pueden ocasionar enfermedades leves y de poca duración, mientras que en bebés, niños, ancianos y personas con el sistema inmunológico deprimido pueden revestir mayor gravedad.
Actualmente existe una serie de filtros comerciales en el mercado que contienen distintos materiales adsorbentes, algunos de ellos con propiedad antibacteriana, los cuales han sido diseñados para el tratamiento final del agua para consumo humano. Estos filtros son usualmente colocados a la salida del grifo de agua potable para dar un tratamiento final al agua de consumo y, aparentemente, aseguran la reducción de compuestos orgánicos e inorgánicos que podría contener el agua, así como la eliminación del 99,9 % de los microorganismos presentes. Por lo anterior, estos filtros han sido considerados como una opción viable para ser usados en las áreas rurales de Tumbes y conseguir agua apta para el consumo humano.
Así, la presente investigación tiene por objetivo caracterizar los materiales que componen los filtros comerciales (A, B, C y D) que reportan usar carbón activado como material adsorbente y evaluar su potencial uso en el tratamiento del agua del Río Tumbes. Son muy escasas las investigaciones realizadas con soluciones multicomponentes como agua real contaminada, evaluando la presencia de otros cationes y aniones en ella. Además, se evaluó la relación entre las propiedades de los carbones, su capacidad de adsorción de metales y su actividad antibacteriana.
Materiales y métodos
Fueron extraídos de sus respectivos cartuchos cuatro materiales procedentes de filtros comerciales (A, B, C y D), utilizados en el tratamiento final del agua para consumo humano y comercializados en los principales centros comerciales del país. Después fueron molidos y finalmente tamizados a un tamaño de partícula menor de 0,25 mm. A pesar de que sus propiedades puedan variar, debido a que el tamaño de partícula influye en la adsorción, es necesario homogenizar los tamaños de grano de las muestras en estudio para luego poder compararlos.
Estos materiales se caracterizaron desde el punto de vista morfológico, estructural, textural y químico. Las propiedades morfológicas fueron determinadas mediante microscopía electrónica de barrido, utilizando un microscopio electrónico con emisión de campo (FESEM, por sus siglas en inglés) marca Zeiss modelo Ultra Plus (Carl Zeiss AG, Alemania). Este microscopio electrónico tuvo acoplado un espectrómetro de energía dispersa (EDS) INCA® x-act (Oxford Instruments, Reino Unido) que permitió la determinación de algunos de los componentes superficiales de los materiales estudiados. Para obtener las imágenes con el FESEM las muestras fueron recubiertas con platino, mientras que para la obtención de los espectros EDS se utilizó un recubrimiento de carbono con las muestras en su tamaño original.
El estudio estructural de los materiales se realizó empleando un difractómetro de rayos X marca Siemens (Siemens AG, Alemania) modelo D5000 operado con radiación CuKα.
Para el análisis textural se utilizó la técnica de adsorción-desorción con N2 a 77 K en un analizador de área superficial Gemini VII 2390 (Micromeritics, USA). El área superficial específica (SBET) fue determinada con el método desarrollado por Brunauer-Emmett-Teller (BET) de acuerdo a lo recomendado por la IUPAC 7. El valor del volumen total o neto (Vnet) se calculó a partir del valor del volumen (de gas) en la isoterma de adsorción de N2 para la presión relativa más cercana al valor 0,999. Los valores del volumen de microporos (Vmicro) y área superficial mesoporosa (Smeso) se calcularon mediante el método de t-plot usando la ecuación de la norma ASTM standard D-6556-01 8 ). La distribución de tamaños de mesoporos se realizó utilizando el modelo de Horvath-Kawazoe, suponiendo una geometría de poros de ranura (slit pore geometry) ( 9.
El punto de carga cero (pHPZC) fue determinado mediante el metodo de pH drift, para lo cual se prepararon soluciones 0,01 M de KNO3 burbujeadas con N2 durante 40 min. Se pusieron 50 mL de estas soluciones en diferentes frascos y se modificó el pH para alcanzar valores entre 3 y 10 (8 puntos en total). Estos valores de pH fueron alcanzados mediante la adición de soluciones de 0,1 y 0,01 M de NaOH y H2SO4, respectivamente.
Se colocó en cada frasco 0,1 g de las muestras de carbón activado y se mantuvo en agitación por 48 h hasta alcanzar el equilibrio. Luego, las muestras fueron filtradas y el pH final fue medido. El pHPZC fue calculado de la intercepción entre la curva pHinicial vs pHfinal y la curva resultante del supuesto que pHinicial es igual a pHfinal10 ).
Para las medidas de cinética de adsorción, la recolección de la muestra de agua se realizó en el Río Tumbes en la zona de Cabo Inga (Frontera Peru-Ecuador), durante la época de estiaje (mes de Diciembre), considerando que en esta época se tiene la concentración máxima de contaminantes en el agua, a diferencia de la época lluviosa donde esta concentración se diluye. Inmediatamente después del muestreo del agua, esta fue acidificada con ácido nítrico hasta llegar a un pH < 3, con la finalidad de evitar la precipitación de los metales pesados y otros elementos. Antes de los experimentos, el pH del agua se reguló a valores entre 6 y 6,5 para acercarse al valor de pH real del río de 7.
Para las pruebas cinéticas se utilizó un volumen de agua de 200 mL en erlemeyers de 250 mL y se les adicionó una concentración de carbón activado de 1 g/L; la mezcla se mantuvo en agitación constante en un agitador magnético. Se tomaron 9 alícuotas de 10 mL por vez, a diferentes periodos de tiempo entre el inicio y los 300 min de duración de los experimentos. Estas alícuotas se filtraron a través de papel filtro Whatman® 1. Los porcentajes de adsorción (%Ads) fueron calculados para los distintos tiempos de muestreo en base a la ecuación [1] 9:
donde Ci es la concentración inicial del elemento contaminante (μg/L) y Ct es la concentración del elemento contaminante (μg/L) en el tiempo t (min).
Se midieron específicamente los contenidos de As y Pb durante las pruebas cinéticas, sin embargo, se hizo un análisis elemental completo al inicio y al final, luego de los 300 min de adsorción. Todos los análisis elementales en el agua se realizaron en un equipo ICP-MS (Inductively Coupled Plasma Mass Spectrometer) marca Thermo Fisher Scientific (USA) modelo X Series 2 ICP-MS.
La determinación de las propiedades antibacterianas de los materiales se realizó utilizando las siguientes cepas bacterianas fecales estandar gram negativas; Escherichia coli (ATCC® 25922™), Salmonella typhimurium (ATCC® 14028™) y Shigella flexneri (ATCC® 12022™). Las cepas bacterianas se cultivaron en caldo Luria (Luria broth) a 36 °C ± 1 por 24 h. Luego se centrifugaron por 15 min a 3500 rpm, y el sedimento resultante se resuspendió en 3 mL de solución salina fisiológica (0,9% NaCl); este procedimiento se realizó dos veces. A partir de las células lavadas en suspensión, se prepararon diluciones de 10 mL para obtener concentraciones de aproximadamente 105 UFC/mL para las tres cepas, de acuerdo al método del tubo de McFarland (con un 10% de variación), a las cuales se le agregaron 10 mg del material a evaluar. Las suspensiones se agitaron a temperatura ambiente por 2 h. Los conteos de los microorganismos viables de las cepas se realizaron cada 30 min hasta un tiempo de 120 min. Para ello se tomó 0,1 mL de la solución tratada y se diluyó para asegurar que el crecimiento de las colonias permitiera el conteo fácil y correcto. La solución diluida se sembró en 15 mL de agar Mueller-Hinton, y se incubó a 37 °C por 24 h. Cada evaluación se realizó por triplicado y los valores obtenidos se promediaron 11 - 13. Lo que se reportó en resultados corresponde a la eliminación de microorganismos a traves del tiempo expresada en porcentaje (%) respecto de la concentración inicial de microorganismos.
Resultados y discusión
Caracterización de los carbones activados comerciales
En la Figura 1 se muestran las imágenes FESEM de los carbones activados comerciales estudiados. Para el caso del carbón activado A se identificaron dos tipos de estructuras; una de morfología irregular (que en la micrografía de menos magnificación se muestra algo triangular) correspondiente al carbón activado, y la otra de forma perfectamente esférica del orden de 500 μm de diámetro. En el caso de las partículas de carbón activado, estas mostraron una estructura altamente porosa con poros irregulares que estaban en el orden de 0,5 a 3,0 μm, mientras que las esferas no presentaron porosidad, pero en su superficie se encontraron partículas de 0,5 a 1,0 μm distribuidas homogeneamente.

Figura 1 Micrografias de FESEM de las muestras de los materiales contenidos en los filtros comerciales A, B, C y D, tomadas a diferentes magnificaciones
La muestra B resultó altamente porosa, característica del carbón activado. Se observaron superficies con relieves escarpados sobre las cuales se reconocieron poros con un tamaño promedio de ~1 μm con formas irregulares. Además, se reconoció la presencia de pequeños trozos en la superficie del carbón los cuales, en base al análisis de EDX, se han identificado como trozos del mismo carbón y otros son impurezas que podrían provenir de la materia prima o de la interacción de los componentes de la materia prima durante el proceso de carbonización en la producción del material. Estas impurezas fueron compuestos a base de Al y Si.
La estructura del material C mostró una fibra de tejido que soportaba un material amorfo y poroso. Este material se conoce como tejido de carbón activado (cloth activated carbon) ( 14, constituido por fibras de un polímero (que por lo general es celulosa) cubiertas con carbón activado. Es posible apreciar cierta porosidad en los carbones activados, sin embargo, los poros no son tan prominentes como en los casos anteriores.
La muestra D presentó a baja magnificación la estructura rocosa típica del carbón activado. Este material se distinguió por mostrar una estructura porosa muy ordenada con formaciones tipo panal de abejas; la forma de los poros fue bastante regular y tipo ovoide.
Esta porosidad identificada en los carbones activados de los filtros comerciales analizados es importante desde el punto de vista de acceso de los agentes contaminantes (de naturaleza inorgánica y/o orgánica) del medio acuoso hacia el interior de los mismos y su contacto con los sitios activos de adsorción o agentes antimicrobianos que podrían contener estos materiales y a los que se debe su capacidad descontaminante.
La determinación elemental de algunas zonas superficiales de los materiales estudiados se realizó a través de EDS. La Figura 2 muestra los espectros obtenidos para las zonas indicadas en las imágenes respectivas. Así, se confirma que el material corresponde a una matriz de carbón que contiene Al como impureza (Figura 2a). La estructura esférica del material (Figura 2b) contiene elementos como K, Cl y Ag (Figura 2c); estos dos últimos con propiedades antibacterianas conocidas 15.

Figura 2 La micrografias a la izquierda muestran la region donde se realizó el análisis EDS de la muestra A, cuyos espectros se representan en las figuras de la derecha. La figura (a) muestra el analisis EDS de las partículas de carbón activado, mientras que las figuras (b) y (c) corresponde a distintas regiones de las partículas esféricas
El material B está constituido básicamente por carbono (el cual fue extraído de la composición elemental, Figura 3), contiene elementos como Mg, Al, Fe, K y Si, los que podrían provenir básicamente de la composición de la materia prima precursora (que por lo general es carbón mineral) o del agente químico activador en el caso que haya sido activado químicamente.

Figura 3 La micrografias a la izquierda muestran las dos regiones (a,b) donde se realizó el análisis EDS de la muestra B, cuyos espectros se representan en las figuras de la derecha
El material C (Figura 4a-c) muestra mayor cantidad de elementos entre los que se encuentran Cu, Si, P, S, Cl, Mg, Al y Ca, los cuales también podrían derivarse de la composición propia del agente precursor, así como de los posibles insumos químicos utilizados durante la producción del carbón.

Figura 4 La micrografias a la izquierda muestran las tres regiones (a-c) donde se realizó el análisis EDS de la muestra C, cuyos espectros se representan en las figuras de la derecha
La composición de la muestra D se observa en la Figura 5a-c. En estas micrografías destaca la presencia de Ag que se presenta en forma de cúmulos cristalinos en la superficie de una matriz de carbón que corresponde al carbón activado. Adicionalmente se aprecia la presencia de S y Cl.

Figura 5 La micrografias a la izquierda muestran las tres regiones (a-c) donde se realizó el análisis EDS de la muestra B, cuyos espectros se representan en las figuras de la derecha
En la Tabla 1 se resumen los elementos, distintos de C y O, encontrados en los carbones activados analizados con EDS.
Tabla 1 Elementos (distintos de C y O) presentes en los materiales adsorbentes estudiados usando la técnica de EDS

La Figura 6 muestra las isotermas de adsorción de N2 a 77 K (Fig. 6a) y la distribución de tamaño de poros en la región mesoporosa (Fig. 6b) para las muestras analizadas. Las isotermas de adsorción de nitrógeno de todos los carbones concuerdan con la forma de la isoterma tipo I(b) de acuerdo a la IUPAC (7) que corresponde a materiales con un amplio rango de poros que incluyen microporos cercanos a los 2 nm y mesoporos estrechos (≤ 2,5 nm). Sin embargo, las isotermas presentan histéresis tipo H4, lo que hace suponer la presencia de mesoporos en la estructura. Esta histéresis es más notoria en el caso de los carbones B, C y D, mientras que en la muestra A es menos perceptible.
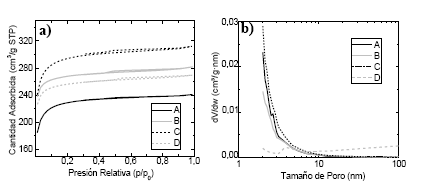
Figura 6 (a) Isotermas de adsorción de nitrógeno (77 K) y (b) distribución de poros en la región mesoporosa de las muestras analizadas
La Figura 6b muestra la distribución de mesoporos en los materiales estudiados. Las muestras A, B y C presentan una distribución de poros similar con una mayor cantidad de poros con tamaños entre 2 y 10 nm, mientras que en la muestra D la cantidad de poros está casi homogéneamente distribuida en todo el rango mesoporoso (2-50 nm). Incluso en la muestra D se muestra mayor cantidad de poros en la región macroporosa (mayor de 50 nm) comparado con el resto de muestras, coincidiendo con las micrografías de microscopía electrónica de la muestra en cuestión (Figura 1).
En la Tabla 2 se muestran los valores medidos de las propiedades texturales de los materiales estudiados. Todos los materiales mostraron valores de área superficial menores de 1000 m2/g. Los valores obtenidos de la razón entre el área mesoporsa respecto al área específica total ( ) y la razón del volumen de microporos respecto al volumen total de poros (
) y la razón del volumen de microporos respecto al volumen total de poros ( ) de los materiales estudiados verifica lo mencionado respecto de la naturaleza principalmente microporosa de las muestras con presencia de mesoporos.
) de los materiales estudiados verifica lo mencionado respecto de la naturaleza principalmente microporosa de las muestras con presencia de mesoporos.
Tabla 2 Propiedades texturales y valores de pH del punto de carga cero (pHPZC) de los carbones activados estudiados

El punto de carga cero, además de indicar el valor de pH donde la carga del material es igual a cero a nivel de su superficie interna y externa, indica el carácter ácido o básico de los materiales relacionado con la naturaleza de los grupos funcionales 16 ). De acuerdo a los valores de la Tabla 2, para este parámetro los carbones C y D presentan un carácter neutro, mientras que el carbón B un carácter ligeramente ácido y el carbón Aun carácter ácido.
Los difractogramas de rayos X de los materiales provenientes de los filtros comerciales se muestran en la Figura 7. Los picos anchos que se observan y que están aproximadamente en 23° y 42° corresponden a los planos (002) y (101) correspondientes al grafito17 ).

Figura 7 Difractogramas de rayos X de los materiales provenientes de los filtros comerciales A, B, C y D
Los picos anchos de difracción sugieren que la muestra tiene una estructura muy desordenada y amorfa. Se observa que la muestra A es amorfa y tiene el pico ancho correspondiente al carbón activado superpuesto a otro pico ancho que aparece en 18°, este puede ser correspondiente a las esferas que se observan por microscopia electrónica. Las muestras B y C son amorfas, mientras que la muestra D, además de los picos anchos correspondientes al carbón activado, presenta los picos característicos de la Ag metálica (identificado con *) ( 18 ).
A pesar de que la muestra A contiene Ag de acuerdo al analisis de EDS, al parecer las cantidades de este elemento son menores del límite de detección de la difracción de rayos X, que corresponde a contenidos mayores a 1% p/p de los compuestos cristalinos presentes en la muestra.
Adsorción de metales pesados por los materiales estudiados
El porcentaje de adsorción de As y de Pb obtenido con todos los materiales se muestra en la Figura 8. Específicamente para el caso del As (Figura 8a) se obtuvo una remoción cercana al 100% a los 10 min. Para el caso del Pb (Figura 8b) las muestras de carbones B, C y D también alcanzaron valores de remoción cercanos al 100% en menos de 10 min. Sin embargo, en el caso de la muestra A el porcentaje de remoción fue cercano a 80% en los primeros 5 min, luego disminuyó hasta los 50 min para finalmente aumentar progresivamente y llegar a un valor cercano a 100% a los 300 min.

Figura 8 Porcentaje de adsorción de As (a) y Pb (b) contenido en el agua del Rio Tumbes utilizando los materiales comerciales estudiados A, B, C y D
El pH es un factor relevante sobre los estados de oxidación en el que se encuentran presentes los metales, así como sobre las propiedades superficiales del adsorbente, de ahí que influya en el porcentaje de adsorción 19 ). En la Figura 9 se muestra el comportamiento del pH durante el experimento de adsorción, así como los valores de pHPZC para cada muestra de carbón. Para el caso de los carbones activados B, C y D los valores de pH aumentaron ligeramente respecto del valor inicial 6, llegando en algunos casos hasta valores ~7, mientras que para la muestra A el valor de pH se redujo respecto del pH inicial hasta valores ~ 4.

Figura 9 Comportamiento del pH durante los experimentos y los respectivos pHPZC de los materiales estudiados A, B, C y D
Cuando el pH de la solución se encuentra por debajo del pHPZC del carbón activado, la carga neta es predominantemente positiva, favoreciendo la adsorción de aniones, pero cuando el pH es superior al valor del pHPZC, la carga neta del carbón es negativa favoreciendo la adsorción de cationes 19 ). Sin embargo, cuando el pH de la solución está cerca del valor del pHPZC, el carbón presenta carga neutra, pudiendo adsorber tanto aniones como cationes. Este hecho permitiría explicar la situación particular del comportamiento del porcentaje de adsorción de Pb por parte de la muestra de carbón A. De acuerdo a las condiciones de las soluciones utilizadas en las pruebas de adsorción de Pb, se encuentra como cation Pb2+20 y el carbón tendría una carga neta positiva. Por esto, debido a la repulsión electrostática entre la superficie del carbón y el catión Pb2+, se dificulta la adsorción del mismo.
Como se muestra para los carbones B, C y D el cambio del pH osciló a un nivel cercano de sus respectivos pHPZC, por lo que fueron capaces de adsorber el catión Pb2+ y el anión arsénico (AsO4 3-), el cual en las condiciones del experimento se encontraría como oxianiones negativos 21 ).
Otro de los factores a tener en cuenta en los procesos de adsorción es la caracterización textural de los materiales adsorbentes. En este caso todos los materiales son micro-mesoporosos, característica que permite facilitar el acceso del agua de río con los contaminantes hacia los sitios activos de los materiales para su adsorción; una menor área superficial denota una menor presencia de sitios activos para la adsorción de contaminantes. En este sentido, el carbón A presenta la menor área superficial específica, área mesoporosa y volumen de poros, respecto a los demás carbones. Esto reduce la posibilidad de acceso del agua hacia los sitios activos, así como también disminuye la presencia de sitios activos de adsorción sobre su superficie. Este factor, junto a la relación del pH de la solución (agua del río) durante los experimentos y el pHPZC de la muestra, explicarían la menor adsorción de As por parte de la muestra.
En la Tabla 3 se muestran los resultados de la caracterización inicial del agua contaminada del Río Tumbes y de las diferentes muestras de agua luego de los 300 min de duración de los experimentos de adsorción acorde al material utilizado. Se observa que las concentraciones de As y Pb son reducidas en todos los casos hasta valores cercanos o por debajo del estándar de calidad de agua (Categoría A y Subcategoría A1, 10 μg para los dos elementos) 5.
Tabla 3 Contenido de metales pesados y de otras especies metálicas presentes en el agua del Río Tumbes después de un tiempo de contacto de 300 min con los materiales adsorbentes estudiados

(*) Estándar de Calidad de Agua (Categoría A-Aguas superficiales destinadas a la producción de agua potable, Subcategoría A1-Aguas que pueden ser potabilizadas con desinfección) (6)
La cantidad de Al en la muestra inicial de agua del Río Tumbes fue de 1750 μg/L, un nivel más alto del estipulado en la normatividad (900 μg/L), sin embargo, todos los materiales en las condiciones experimentales redujeron el nivel de Al hasta niveles menores al estipulado en la norma.
Para el caso del Fe, el valor inicial estuvo por encima del estándar de calidad de agua, sin embargo, la mayoria de materiales, a excepción del A, redujeron su concentración hasta valores por debajo de este estándar.
A pesar de que el carbón A redujo los niveles de Al y Fe, siendo cationes a las condiciones del experimento, la remoción de estos metales resultó ser de solo 26,3 y 17,4 %, respectivamente. Esto corrobora lo antes mencionado respecto a que la carga superficial neta del carbón A es positiva y la adsorción de cationes se ve limitada por las fuerzas de repulsión.
Capacidad antibacteriana de los materiales
Los resultados de las pruebas antibacterianas de los materiales evaluados se muestran en la Figura 10. Aquí se puede apreciar la reducción en la carga microbiana luego de diferentes tiempos de siembra 0, 30, 60, 90 y 120 min. Es evidente que, en general, la carga microbiana se redujo a medida que el tiempo de contacto entre los materiales (basicamente carbones activados) y la solución de microorganismos aumentaba.

Figura 10 Remoción de bacterias fecales estándar gram negativas: (a) Escherichia coli, (b) Salmonella typhimurium, (c) Shigella flexneri en porcentaje (%) para las cuatro muestras de filtros comerciales (A, B, C y D)
En la Figura 10a se muestra el comportamiento de las cuatro muestras estudiadas en contacto con Escherichia coli. Es evidente que la muestra C tiene la mayor efectividad para la eliminación de esta cepa, llegando hasta valores de eliminación cercanos a 70% después de 120 min. Luego le siguen la muestra D, B y finalmente A en orden decreciente de efectividad. Así, para el caso de la muestra A se alcanzaron valores de eliminación de Escherichia coli que no superaron el 30%. En ninguno de los casos se llega a una condición de equilibrio, sin embargo, el carbón A se aproximó a ese comportamiento después de 120 min.
Los niveles de eliminación de la cepa Salmonella typhimurium se presentan en la Figura 10b. Se observa que los materiales C y A mostraron comportamientos similares y con niveles de remoción superiores a 70% después de 120 min. El carbón D mostró valores de eliminación cercanos al 50%, mientras que el material B solo presentó niveles que apenas superaron el 30% de eliminación después de 120 min.
Finalmente, la Figura 10c muestra los niveles de eliminación de la cepa Shigella flexneri para los materiales analizados. Se observa que la muestra D alcanza aproximadamente un 70% de eliminación a los 120 min y además se observa que el incremento de la remoción se desarrolla en forma casi lineal. Este comportamiento lineal también se presentó para el material B, pero su máxima remoción no superó el 40% a los 120 min. La muestra C presentó un máximo de remoción a los 30 min con un valor ligeramente mayor a 40%.
En general, las muestras de carbón activado CyD mostraron mejor capacidad antibacterial frente a las cepas de enterobacterias estudiadas. Para la muestra C la capacidad antibacteriana se basaría en la presencia de Cl, Cu y Si que conforman parte de su composición superficial; el Cl y el Cu son elementos con capacidad antibacteriana demostrada 22,23 ). La capacidad antibacteriana del Cl reside en sus propiedades antioxidantes moderadas y la reacción del mismo con componentes de las células microbianas, como lípidos y proteínas 22 ), mientras que los mecanismos que le confieren actividad antibacteriana al Cu no han sido claramente delucidados. En relación con el Si, también se han demostrado sus propiedades antibacterianas, basadas en la inducción de estrés oxidativo debido a que el Si es una especie reactiva de oxígeno 24 ). En este compuesto también se basaría la capacidad antibacteriana de la muestra de carbon B.
En el caso de la muestra D, la capacidad antibacteriana se basaría en la presencia de partículas de Ag soportadas en la superficie del carbón activado, tal como se observa en los espectros EDS. La muestra A también tendría Ag en su composición, pero en cantidades menores a la muestra D. Por esta razón, sólo se detectan trazas en los análisis de EDS, en los análisis de rayos X no es posible la detección. La capacidad antibacteriana de la Ag ha sido demostrada anteriormente 25. El mecanismo en el cual se sustenta esta actividad de la Ag se basa en el efecto desnaturalizador de los iones de Ag sobre las moléculas de ADN y la inactivación del grupo tiol de las proteínas 26 ). La mayor capacidad antibacteriana de la muestra de carbón C sobre el carbón D que contiene Ag en algunos casos, se basaría en el posible efecto combinado por la presencia de Cl, Cu y Si.
Conclusiones
Se caracterizaron cuatro muestras de carbones activados (A, B, C y D) extraídos de filtros comerciales utilizados para el tratamiento del agua y se evaluó su porcentaje de adsorción de metales pesados presentes en el agua del Río Tumbes - Perú y su capacidad de eliminación de microorganismos. Todas las muestras mostraron gran área superficial (entre 705 y 906 m2/g) y contaban con estructura micro y mesoporosa desarrollada, además, fueron amorfas. Solo la muestra D presentó picos asignados a Ag metálica. Se determinaron diferentes morfologías en los carbones, además de la presencia de poros en las muestras A, B y D. En la muestra A se identificó la presencia de un material de geometría esférica (con un diámetro ~500 μm) conteniendo Cl, Ag y K. La muestra C mostró ser un tejido de carbón activado, con fibras que soportan partículas de carbón.
De la evaluación de los experimentos de adsorción de los materiales analizados se determinó que para el caso del As y del Pb, cuyas concentraciones iniciales en el agua contaminada fueron 56,7 y 224,0 μg/L, respectivamente, el porcentaje de adsorción fue cercano al 100%. Las propiedades texturales y la relación entre el pHPZC de los carbones y el pH del agua del río durante los experimentos tuvieron influencia en el proceso de adsorción.
Por otro lado, la capacidad antibacteriana fue evaluada satisfactoriamente frente a las siguientes cepas fecales de bacterias gram negativas; Escherichia coli (ATCC® 25922™), Salmonella typhimurium (ATCC® 14028™) y Shigella flexneri (ATCC® 12022™). Esta capacidad se basa en la presencia superficial en los carbones de Ag, Cu, Cl y/o Si. Los materiales estudiados son de potencial uso en el tratamiento del agua del Río Tumbes, en orden descendente de efectividad los materiales C, B, D y A.















