Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Boletín de Ciencias de la Tierra
Print version ISSN 0120-3630
Bol. cienc. tierra no.40 Medellín July/Dec. 2016
https://doi.org/10.15446/rbct.n40.55999
DOI: http://dx.doi.org/10.15446/rbct.n40.55999
Glycerol effect on the inhibition of spontaneous combustion of sub-bituminous coal
Efecto del glicerol en la inhibición de la combustión espontánea de carbón sub-bituminoso
Esteban Alberto Taborda-Acevedo a, William J. Jurado b & Farid B. Cortés a
a Grupo de Fenómenos de Superficie - Michael Polanyi, Facultad de Minas, Universidad Nacional de Colombia, Medellín, Colombia. fbcortes@unal.edu.co
b Departamento de Optimización de Procesos, Grupo Argos S.A, Medellín, Colombia. wjurado@argos.com.co
Received: March 01th, 2016. Received in revised form: May 8th, 2016. Accepted: May 25th, 2016.
This work is licensed under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.

How to cite: Taborda-Acevedo, E.A., Jurado, W.J. & Cortés-Correa, F.B., Efecto del Glicerol en la Inhibición de la Combustión Espontánea de Carbón Sub-Bituminoso. Boletín de Ciencias de la Tierra, (40), 64-74, 2016.
Abstract
Factors favoring the phenomenon of spontaneous combustion in coal mainly depend on the intrinsic properties such as coal particle size, moisture content, among others; the medium in which it is located and how it is stored. Consistent with this, the objective of this work is to evaluate the effect of glycerol on the inhibition of self-combustion as water re-adsorption reducer through the addition of glycerol in different amounts (4, 8, 18 and 28% wt). The coal sample was extracted from the Córdoba department, Colombia. Incipient impregnation method was used to perform the addition of glycerol to the desired quantities. Characterizing the coal samples was performed by: TGA-DTG, nitrogen adsorption at -196 °C, C-H-N-O, FTIR, and SEM. The TGA of the coals evaluated in an air atmosphere, show changes in combustion properties of each sample. Di ignition index is reduced as the coal is impregnated with glycerol, obtaining its lowest value for 8wt% of glycerol. The effect of glycerol in inhibiting the spontaneous combustion of coal is exposed in the adsorption equilibrium; the sample with 8wt% glycerol shows the highest reduction of water adsorption in coal validating the proposed technology as inhibitor agent spontaneous combustion phenomenon found in Colombian coal.
Keywords: Adsorption; Coal; Isotherm; Water
Resumen
Factores que favorecen el fenómeno de auto-combustión del carbón depende principalmente de las propiedades intrínsecas, tales como tamaño de partícula, contenido de humedad, entre otros; el medio en el que se encuentra y cómo se almacena. De acuerdo con esto, el objetivo de este trabajo es evaluar el efecto del glicerol en la inhibición de auto-combustión del carbón como reductor de re-adsorción de agua, mediante la adición de glicerol en diferentes cantidades (4, 8, 18 y 28% en peso). El método de impregnación incipiente se utilizó para adicionar el glicerol a las cantidades deseadas. La caracterización de las muestras se realizó mediante: TGA-DTG, adsorción de nitrógeno a -196 ° C, C-H-N-O, FTIR, y SEM. El TGA de los carbone refleja cambios en las propiedades de combustión de cada muestra. El índice de ignición Di presenta su valor más bajo para la muestra con 8% en peso. El efecto del glicerol en la inhibición de la combustión espontánea del carbón está expuesto en el equilibrio de adsorción; la muestra con 8% en peso de glicerol presenta la mayor reducción de la adsorción de agua en el carbón validando la tecnología propuesta como agente inhibidor del fenómeno de auto-combustión en carbones colombianos.
Palabras clave: Adsorción; Carbón; Isoterma; Agua
1. Introducción
El carbón es el combustible fósil más abundante en la naturaleza, con 750.000 millones de toneladas en reservas globales medidas a finales de 2014 [1,2]. Las mayores reservas por país se encuentran en los Estados Unidos con el 27,6% la Federación de Rusia 18,2%, China 13,3%, Australia 8,9% y la India 7,0%, mientras que Colombia se encuentra en el undécimo lugar con 6,593.4 millones de toneladas equivalente al 0,8% [1-3]. De estas reservas, se puede ver que la mayor región de concentración es Europa y Euro Asia, seguida de Asia Pacífico, América del Norte, África y América del Sur y Central.
Colombia tiene las mayores reservas de carbón en América del Sur y ocupa el puesto undécimo en todo el mundo [1,3]. Uno de los principales problemas para los productores de carbón y los consumidores industriales en general está relacionado con la combustión espontánea del carbón [4]. La auto-combustión del carbón es la causa más importante de los incendios en las pilas de carbón en todo el mundo [4], estos incendios pueden tener efectos perjudiciales significativos sobre la salud, el medio ambiente y la economía [5].
El carbón tiene sitios activos con en alto contenido de agua, debido a su alta afinidad por las moléculas polares [6,7]. Existen riesgos asociados con altos contenidos de agua en carbones: el sobrecosto de la energía excesiva utilizada en el proceso de secado carbón, sobrecostos en los procesos de almacenamiento y transporte y los problemas ambientales relacionados con la auto-combustión de carbón, debido a la oxidación del material carbonoso a una cierta temperatura. Esto ocurre cuando el carbón se expone al aire y se somete a quimisorción exotérmica de oxígeno. Las pilas de carbón grandes, especialmente aquellas almacenados durante largos períodos, pueden desarrollar puntos calientes debido a un calentamiento espontáneo [8-10]. Varios estudios se han reportado en la literatura sobre la combustión espontánea del carbón y las formas de evitarlos. [4,11-14]. Fei et al. [15] compararon la combustión espontánea de dos muestras de carbón con diferentes contenidos de humedad. Se determinó la temperatura crítica de encendido a partir de dos métodos, el método de punto de cruce y el método de liberación de calor. Para ambos métodos, los autores encontraron que las tendencias de la temperatura crítica, principalmente se pueden explicar en términos de los efectos del contenido de humedad de las muestras, a menos contenido de humedad, se reduce su propensión a la combustión espontánea. Fierro et al. [16] estudiaron la combustión espontánea de cinco pilas de carbón de prueba y la medida para evitar la pérdida del calor producido, desarrollaron un método directo para determinar el coeficiente de pérdidas totales y determinar los coeficientes de pérdidas de calor. Para evitar la combustión espontánea, las reservas se estaban protegiendo para evitar al máximo el flujo de aire con una barrera artificial o eran cubiertas con una suspensión de cenizas húmedas de la misma planta de energía. Los resultados sugieren que los métodos de protección aplicados a las pilas experimentales han demostrado ser muy eficiente. La pila se cubre con una capa húmeda de las cenizas volantes de la misma central térmica ha demostrado ser la medida más eficaz con el menor coeficiente de pérdidas totales del 3%. Pone et al. [17] estudió la combustión espontánea de las vetas de carbón en las minas de Witbank y Sasolburg con el fin de determinar si los elementos químicos tóxicos y compuestos están siendo movilizados en el medio ambiente, los minerales de gas de carbón al fuego (CFGM) identificados incluyen compuestos de azufre y sal amoniacal. Mediante difracción de rayos X (XRD) los estudios de los subproductos CFGM confirmaron la presencia de mascagnita ((NH4) 2SO4), illita ((Al, Si) 4O10 [(OH) 2, H2O]) letovicita ((NH4) 3H (SO4) 2), flogopita (KMG), dióxido de titanio (TiO2), barita (BaSO4), sulfato de hierro (FeSO4), yeso (CaSO4 2HO) y silicato. Este estudio identificó que durante la combustión espontánea del carbón en los yacimientos de carbón Witbank y Sasolburg, la quema de carbón liberado altas concentraciones de gases tóxicos, incluyendo benceno, tolueno, xileno, etilbenceno, metano y óxidos de carbono. Se detectaron treinta y dos compuestos alifáticos y otros compuestos halogenados. La naturaleza de los riesgos para la salud humana y el medio ambiente de la mayoría de los compuestos de gas y los subproductos CFGM producidos de la combustión espontánea en las minas de carbón y Witbank Sasolburg son aún desconocidos y merecen ser investigados. Arisoy [18] utilizó la prueba R para evaluar el riesgo de combustión espontánea y la propensión de combustión espontánea del carbón. Esta prueba también se ha utilizado para investigar los efectos de diferentes propiedades del carbón sobre la tasa de auto-calentamiento. Estos efectos se pueden dividir en dos grupos. El primer grupo está relacionado con las propiedades del carbón, tales como el rango, materia mineral, contenido de pirita y el tipo de carbón. En segundo grupo está relacionado condiciones de la pila, como la temperatura de la pila, el envejecimiento de carbón, tamaño de partícula, contenido de humedad, la profundidad de la pila de carbón almacenado y la cantidad de flujo de aire que pasa a través de la masa de carbón. El autor encontró que el factor de riesgo más importante para la combustión espontánea es el contenido de humedad y tamaño de partícula de la muestra. Bath y Agarwal [19] identificaron el efecto de condensación de humedad en la combustión espontánea del carbón a través de un modelo matemático desarrollado para investigar la influencia de la migración de la humedad en la combustión espontánea del carbón. Se muestra que la humectación parcial de carbón o de condensación de la humedad ejerce dos influencias que compiten en la tasa global de oxidación. Por un lado, una parte del carbón se llena de agua líquida; en esta región, la velocidad de oxidación se convierte en insignificante, ya que el oxígeno tiene que disolverse en el agua antes de que pueda acceder a un sitio activo en la superficie del carbón y la solubilidad del oxígeno en el agua es baja. Por otra parte, la condensación conduce también a la liberación del calor latente de vaporización. Este efecto de calor eleva la temperatura de la partícula y aumenta la velocidad de oxidación. Los autores también encontraron que tipo de carbón y rango, como se caracteriza por el comportamiento de adsorción de humedad, juegan un papel muy importante. Carbones de bajo rango, cuya isoterma de adsorción de humedad muestra una mayor desviación del comportamiento de tipo III, tienen una mayor tendencia a la auto-ignición. Cuanto más grande esta desviación, mayor será el potencial para la combustión espontánea. Ávila et al. [4] utilizaron el análisis termogravimétrico para estimar el potencial de la combustión espontánea del carbón, utilizando dos métodos termogravimétricos no isotérmicos. La prueba de "adsorción de oxígeno" consistió en la exposición de muestras de carbón para reducir las tasas de calentamiento en el aire mientras se mide el aumento de peso producido por la adsorción de oxígeno, con frecuencia dando a los más altos niveles de adsorción. Se realizó una segunda prueba termogravimétrica para el cálculo del potencial de ignición espontánea (TGspi), que se centró en el segmento lineal de la curva derivada de peso entre 150 y 350 ° C a diferentes velocidades de calentamiento en aire (3, 5, 7, 10, y 20 ° C min-1). A partir de estos resultados, se obtuvo una relación entre la tasa de pérdida de masa y la temperatura (TGindex), donde los valores altos fueron producidos por carbones altamente reactivos.
Como se evidencia en esta serie de trabajos, existe una relación directa entre la capacidad de adsorción de agua en los carbones y su potencial riesgo de combustión espontánea. En ese sentido, este trabajo evalúa el riesgo de combustión espontánea en carbones impregnados con glicerol a través de una serie de análisis como termogravimetría, análisis diferencial termogravimétrico, y espectroscopía infrarroja y su relación con la capacidad de adsorción de agua. El comportamiento de la combustión del carbón se describe con el cálculo de los parámetros relacionados con el proceso térmico de carbones. El índice de ignición Di y el índice de la combustión final Df que se presentan por Jun-Lin et al. [20]. Además, se calculó el índice de combustión espontánea TGspi y la energía de activación de combustión para cada muestra evaluada.
2. Experimentos
2.1. Preparación y modificación del carbón
Una muestra de carbón obtenida de la región de Córdoba en el noroeste de Colombia fue utilizada en este estudio. La preparación de la muestra de carbón fue realizada por separación y posterior cuarteo por cuatro veces. El tamaño de partícula fue subsecuentemente reducido a 250 mm aproximadamente, utilizando un cortador y un Molino de bolas de acuerdo a la norma ASTM D2013-01. Posteriormente, el carbón fue secado en una atmósfera de aire a 120ºC por 12 horas y fue transferido a un sistema de desecado hasta alcanzar la temperatura ambiente. El glicerol (86%, Merck KGaA, Alemania) se utilizó como el material de impregnación. La superficie del carbón fue modificada por el método de impregnación incipiente [21-24]. El glicerol se diluyó en agua destilada, fue añadido gota a gota al carbón y se coloca en un vidrio de reloj. Durante la adición de la solución de glicerol, la muestra de carbón se agitó continuamente de forma manual para asegurar el máximo contacto. A continuación, la muestra se lavó con agua y se seca a 120 °C durante 12 h para eliminar el solvente usado. El porcentaje de impregnación se calculó por la diferencia de peso antes y después del secado y corroborado por mediciones termogravimétricas. Cuatro muestras de carbón fueron impregnadas con concentraciones de glicerol de 4, 8, 18 y 28% en peso, respectivamente. Las muestras impregnadas se denominan por el nombre del carbón seguido por el porcentaje en peso de glicerol. Por ejemplo, C4 denota el carbón con un 4% en peso de glicerol.
2.2. Caracterización de la muestra
La muestra de carbón fue caracterizada con análisis elemental realizado utilizando un 5000A TOC (CHN Shimadzu, Japan) para obtener los elementos C-H-N, el oxígeno fue obtenido calculando la diferencia. La fisisorción de nitrógeno a 77 K fue realizada utilizando un ASAP 2010 (Micromeritics, USA). El área superficial (SBET) fue obtenida después de desgasificar la muestra por 12 horas aproximadamente a 140°C bajo ultra vacío (10-6 mbar). SBET fue estimada utilizando el método Brunauer, Emmett y Teller (BET) [25,26]. El límite mínimo de confiabilidad del equipo detecta áreas superficiales de 1 m2/g. Para determinar los grupos funcionales presentes en el carbón, la muestra fue caracterizada por espectroscopía infrarroja (IRAffinity-1S Shimadzu, Japan) [5,27] Microscopía electrónica de barrido (JSM-5910JL, JEOL Japón) fue utilizada para obtener imágenes de la muestra de carbón para confirmar que se trata de una muestra no porosa. Los efluentes gaseosos productos de la oxidación del carbón se analizaron por espectroscopía infrarroja de transformada de Fourier para determinar su composición química.
2.3. Isotermas de adsorción
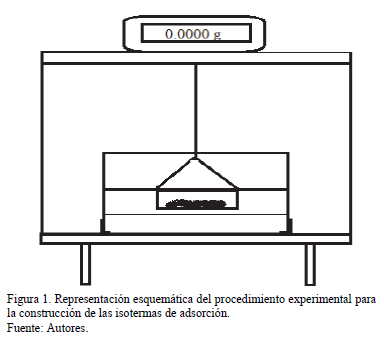
El método termogravimétrico estático fue utilizado para la construcción de las isotermas de adsorción a 21°C. Este método involucra la determinación del peso ganado por una muestra de carbón sometida a varios ambientes con actividades de agua diferentes (Aw) a una temperatura definida. Ocho contenedores con soluciones salinas sobresaturadas determinaron un rango de actividad acuosa entre 0.113 y 0.842 (Tabla 1) a 21°C por 24 horas. Después de la preparación de las soluciones salinas, la actividad fue medida continuamente hasta que alcanzara un valor constante. Después, 0.5 g de carbón fueron colocados en el interior de los contenedores hasta alcanzar el equilibrio. La muestra de carbón fue pesada cada 8 horas en una balanza analítica (OHAUS - precisión of 0.0001 g) hasta que el peso no variara más de 1%. Este procedimiento fue realizado por triplicado para confirmar la reproducibilidad, y su desviación estándar fue calculada y presentada en forma de barras de error en la figura de las isotermas. Finalmente, la cantidad de agua adsorbida fue estimada calculando la diferencia entre el valor en peso final e inicial de la muestra. La cantidad adsorbida (Nads) fue calculada como g de agua por g de carbón [6-12,28]. La Fig. 1 muestra una representación esquemática del procedimiento experimental. La Tabla 1 presenta las sales higroscópicas utilizadas para acondicionar cada sistema a la actividad acuosa deseada.
3. Resultados y Discusión
3.1. Caracterización de la muestra
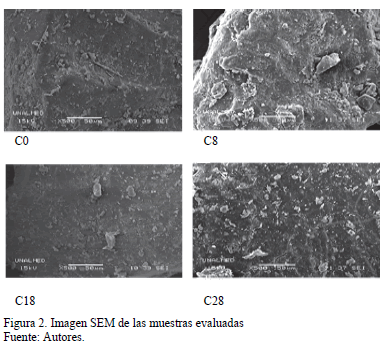
La Fig. 2 presenta las imágenes por espectroscopía electrónica de barrido (SEM) del carbón. De acuerdo con ella parece que el carbón tiene una estructura propia de un material no poroso. La Tabla 2 muestra que el área superficial (BET) del carbón disminuyó a medida que el contenido de glicerol en la superficie aumenta, y los valores bajos de SBET apoyan de nuevo que los materiales son no porosos. La reducción del área superficial de las muestras sugiere que el glicerol ha bloqueado los sitios polares del carbón virgen. La Fig. 2 muestra imágenes de microscopía electrónica de barrido (SEM) de las muestras de carbón en diferentes cargas de glicerol. Por consiguiente, parece que los carbones vírgenes y funcionalizados con glicerol son un material no poroso.
La Tabla 2 también presenta el análisis elemental de las muestras de carbón. Como se ve, ya que el contenido de glicerol en el carbón aumenta, las proporciones de O/C y H/C aumentó, debido a que el glicerol tiene una mayor relación O/C y H/C en comparación con el carbón seco vírgen. A medida que la relación O/C aumenta, se espera que aumenten los grupos de aromaticidad y carbonilo [27]. En consecuencia, la afinidad entre la superficie del carbón y el agua disminuiría.
3.2. Análisis termogravimétricos
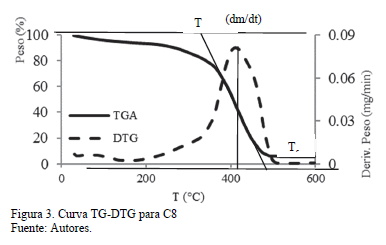
Hay muchos métodos para estudiar el comportamiento de la combustión de carbones. Para obtener la temperatura de ignición en las pruebas de combustión de carbón, se utilizó el método TG-DTG. Una línea vertical se extrae del pico de la curva DTG y se cruza con las curvas de TG, y luego desde el punto de cruce se dibuja una tangente de la curva de TG. El punto de cruce entre la tangente y las líneas paralelas de la pérdida de masa se define la temperatura de ignición. La Fig. 3 muestra el proceso de fijación de la temperatura de ignición.
Los parámetros característicos de la combustión de TG y DTG curvas incluyen: la temperatura inicial Ti al tiempo correspondiente to, la tasa máxima de combustión (dm/dt)max al tiempo correspondiente tm, la temperatura final de combustión Tf y el tiempo correspondiente tf y Dt1/2 que es la diferencia de tiempo entre dos temperaturas cuando (dm/dt)/(dm/dt)max = ½ se denomina como un pico medio, que representa el grado de combustión de un producto. Según estos parámetros, el índice de ignición Di y combustión final Df, que son presentados por Jun-Lin, et al. [20].
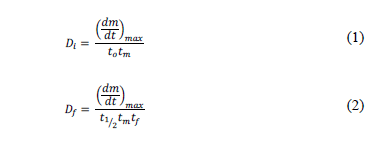
El valor más alto del índice de Di y Df presenta una mejor combustión.
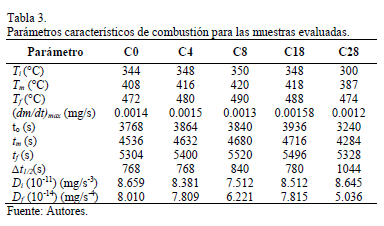
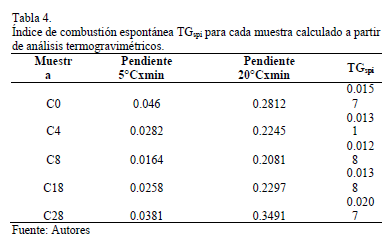
El índice de indición Di presenta una tendencia a decreciente a medida que el contenido de glicerol se aumenta en la superficie de carbono, a excepción de la muestra con 28wt%. Sugiriendo una disminución en el riesgo de ignición a medida que aumenta el contenido de glicerol en el carbón, los valores más bajos se obtienen en para la muestra C8, lo que sugiere una mayor dificultad para que ocurra la auto-ignición. La Tabla 3 presenta los parámetros de combustión donde que se pueden ver diferencias entre cada muestra evaluada.
3.3. Análisis FT-IR
Los efluentes gaseosos productos de la combustión de las muestras de carbón, se analizaron por espectroscopía de infrarrojo con transformada de Fourier (FT-IR) con el fin de determinar los gases que se producen a medida que la combustión avanza. La Fig. 4 presenta la pérdida de masa de gas asociado para C0 y C8 en comparación con el análisis gravimétrico diferencial.
El comportamiento que se encuentra en la Fig. 4 es similar para todos los carbones tratados, muestra que el producto principal es el CO2 y se obtiene una mayor producción a temperaturas donde se produce el cambio de masa más grande, siendo coherente con las curvas de termogravimétricas presentadas anteriormente.
Para estar completamente seguros de esta hipótesis, a continuación, se calcula el índice de combustión espontánea mediante un procedimiento compuesto por pruebas termogravimétricas al menos a dos velocidades de calentamiento diferentes.
3.4. Índice de Combustión Espontánea
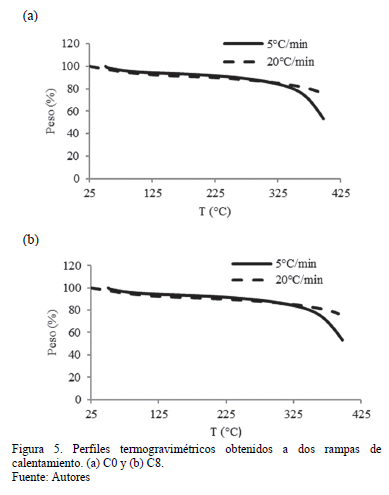
Para comprender mejor el efecto del contenido de glicerol en la superficie de carbón, en el riesgo de combustión espontánea, se realizó un análisis termogravimétrico para calcular el potencial de combustión espontánea. La Fig. 5 muestra los perfiles de termogravimetría para muestras en dos rampas en atmósfera de aire.
Se obtuvieron perfiles termogravimétricos derivados para todas las muestras de carbón utilizando dos velocidades de calentamiento en atmósfera de aire. (5 a 20 ° C / min), en la Fig. 6 se presentan dos ejemplos C0 y C8.
La Fig. 5 revela una pérdida de peso lineal que comienza inmediatamente después de la liberación de la humedad (~ 110 °C) y termina con un aumento brusco de la velocidad de volatilización producido por la etapa de combustión completa (después de la ignición, que varían desde 300 hasta 400 °C, depende de cada tipo de muestra). La forma de la derivada del perfil termogravimétrico a bajas temperaturas (Fig. 6) depende de las propiedades reactivas de la muestra. En cada velocidad de calentamiento, una pendiente se produce en el "segmento" inicial de la curva derivada. El análisis de una muestra en un número de diferentes rampas de calentamiento (como se muestra en la Fig. 6 para cada carbón) produce un conjunto de pendientes asociadas con el conjunto de condiciones de calentamiento. Al representar esta información, la relación encontrada tiende a ser también lineal, con un coeficiente de regresión cerca de 1 para todas las muestras. La pendiente de la segunda derivada, se definió como el índice de combustión espontánea TGspi, y su magnitud representa la reactividad intrínseca de cada carbón en particular, y se calcula así (Ver fig. 5):

Se encontraron altos valores de TG cuando las tasas de pérdida de peso tienden a ser en gran medida influenciada por un cambio de temperatura preestablecida, lo que significa que la reacción química se desarrolló más rápido debido a la alta reactividad de la muestra.
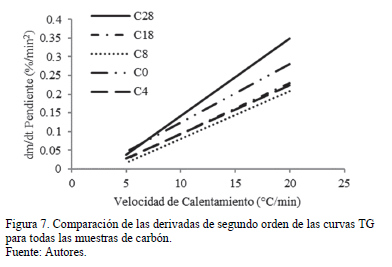
Con la Fig. 7 es posible determinar la reactividad de cada muestra de carbón, y por lo tanto definir el riesgo de combustión espontánea. La muestra con mayor pendiente representa un carbón más reactivo debido a que su índice de combustión espontánea es mayor, por esta razón será más probable para promover la combustión espontánea. Del mismo modo, la pendiente más baja dada para C8 representa un carbón menos reactivo y menos propenso a producir combustión espontánea.
La Tabla 4 presenta los resultados de las pruebas de combustión espontánea. Los resultados sugieren que la C8 muestra tiene la reactividad más baja.
3.5. Cinética de Combustión
En el proceso del estudio cinético, la combustión es considerada como una reacción simple, y no existe ningún obstáculo difuso en las condiciones de este experimento. La ecuación de Arrhenius se usa para describir la velocidad aparente de reacción:

El método de Freeman y Carroll [29] se utiliza para obtener los parámetros cinéticos con datos termogravimétrico
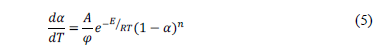
Donde k es la velocidad de reacción aparente, A el factor pre-exponencial, E la energía de activación, R la constante de los gases, T es la temperatura, a el porcentaje restante, j la velocidad de calentamiento lineal y n el orden de reacción. Basado en la experiencia, n = 1, e integrando

Se puede obtener un gráfico de línea recta de ln[-(ln(1-a))/T2] vs. 1/T (se muestra en la Fig 8), en la que -E/R es la pendiente de la línea y a es la intersección [30, 31].
Los parámetros cinéticos obtenidos de la combustión se enumeran en la Tabla 5.
La energía de activación de la combustión es diferente para cada muestra impregnada con glicerol. A medida que el contenido de glicerol en la superficie aumenta, también aumenta la energía de activación de la combustión, lo que retrasa la combustión normal de carbón sin glicerol. La muestra C8 nuevamente es la que presenta un mejor resultado en la búsqueda para inhibir la combustión espontánea del carbón.
3.6. Isotermas de Adsorción
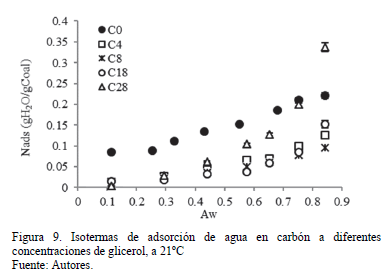
La Fig. 9 presenta las isotermas de adsorción de agua sobre el carbón a 21 °C a lo largo de diferentes concentraciones de glicerol para una actividad de agua entre 0,10 a 0,90. La adsorción aumentó con el aumento de la actividad del agua. Estos resultados están en de acuerdo con los estudios de adsorción de carbón/agua disponibles [32-38]. La cantidad de vapor de agua en el recipiente de adsorción aumenta debido al aumento de presión de vapor (actividad de agua). Las colisiones con la superficie de la muestra son favorecidas, lo que lleva a una mayor cantidad adsorbida. Las isotermas de adsorción exhiben comportamiento Tipo III, según la clasificación IUPAC [6, 39]. La forma resultante de la isoterma de sorción de agua indica una baja afinidad entre el adsorbato y adsorbente, que se produjo principalmente a una humedad relativa baja (actividad de agua). El comportamiento de la isoterma muestra diferentes interacciones, incluyendo la interacción de agua sobre los sitios activos, junto con varias capas humedad adsorbida en la superficie de carbón.
La reducción de la superficie después del proceso de impregnación de glicerol se refleja principalmente en las regiones de alta actividad de agua, mientras que es mínima en la región de baja actividad de agua (la ley de Henry). De hecho, los datos de isotermas con desviación estándar correspondiente son menores que 5%.
Los resultados de la Tabla 2 también muestran que para todas las muestras de glicerol, la relación O/C aumenta. Sin embargo, el material funcionalizado exhibió baja afinidad entre el agua y la superficie debido al bloqueo de los sitios activos en la superficie del carbón por la adición de glicerol en el intervalo de 4-8% en peso. Para las muestras C18 y C28, la afinidad por el agua aumentó, probablemente debido a la formación de grupos a través de enlaces de hidrógeno de adsorbato que son adsorbidos sobre carbón modificado con glicerol.
La reducción en la re-adsorción de agua sobre el carbón modificado con glicerol es mayor para C4, C8 y C18 en toda la gama de Aw. En el caso de C28, la reducción fue significativa a bajas actividades. Para C4, C8 y C18, a una baja actividad de agua (menos de 0,40), la reducción de la cantidad adsorbida de agua fue de aproximadamente 70% en comparación con el carbón virgen. Por el contrario, en las actividades superiores, tales como 0,75, la reducción fue de aproximadamente 6, 53, 59 y 63% para las muestras C28, C4, C18 y C8, respectivamente. Los resultados muestran que el punto de impregnación óptima de glicerol sobre la superficie del carbón estaba en 8% en peso. Cuando la concentración de glicerol aumentada por encima de 8% en peso, se observó re-adsorción de agua significativo, lo que se hizo más notable en una actividad más alta que 0,7. Esto se puede explicar por la estructura de glicerol. Cuando los grupos funcionales OH están expuestos a contacto directo con el agua, la probabilidad de la formación de nuevos enlaces de hidrógeno se incrementa, aumentando así la cantidad de agua en la estructura. Esto parece ocurrir principalmente para C28. Para un contenido de glicerol inferior a 8% en peso, la cantidad de agua adsorbida disminuyó debido a la obstrucción o el relleno de los sitios polares de carbón con el grupo hidroxilo de glicerol en la superficie de carbón, generando así una superficie con más afinidad por los compuestos no polares. Al contenido de glicerol mayor que 8% en peso en la superficie del carbón, los sitios polares de carbón se llenan inicialmente con OH- grupos de la glicerina. El glicerol está anclado al glicerol impregnado en la superficie del carbón a través de interacciones no polares, que se basan en el tipo de múltiples capas de impregnación. Por lo tanto, los carbones modificados muestran una alta afinidad por las moléculas polares debido a la reorganización del glicerol sobre su superficie.
La isoterma de adsorción fue modelada utilizando el modelo propuesto por Talu y Meunier [39]. Este modelo puede ser expresado como una teoría general para la adsorción de moléculas auto-asociativas sobre estructuras sólidas. La aproximación es similar a la interpretación "química" de fases no ideales de líquido y vapor. La teoría puede explicar el comportamiento de las isotermas Tipo I a Tipo V, incluyendo isotermas tipo III características de adsorbentes no porosos, como es el caso de este trabajo. Los datos de las isotermas son dependientes únicamente en tres parámetros: El inverso de la constante de Henry, la capacidad de saturación y la constante de reacción de formación de "clúster". El modelo es descrito a continuación:

Donde, N (g/g) es la cantidad adsorbida, Nm (g/g) es la cantidad de saturación adsorbida por el monómero, K (g/g) es la constante de reacción relacionada con la agregación de las moléculas autoasociativas, P (kPa) es la presión de equilibrio del sistema, y H (kPa) es el inverso de la constante de la ley de Henry.
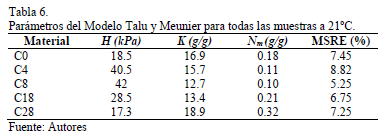
La Fig. 10 muestra la comparación entre los datos experimentales y el modelo de Talu y Meunier [39]. La Tabla 5 muestra los valores de los parámetros obtenidos del modelo Talu y Meunier. Los valores de los parámetros están de acuerdo con las características de los carbones en la que el valor K es alta. Esto indica una rápida asociación de moléculas de agua una vez que los sitios primarios están ocupados y es similar al comportamiento descrito por las isotermas de adsorción. Por otro lado, los valores de H son también altos (el inverso de la constante de la ley de Henry común). Los valores más altos del parámetro H indican menor afinidad de las moléculas de agua por estar en la fase adsorbida. Los sitios activos se encuentran en lugares que no son de fácil acceso al agua.
Los parámetros del modelo Talu y Meunier muestran una tendencia consistente con isotermas de sorción. Está claro que la pendiente de las isotermas en la región de Henry es mayor a medida que la cantidad adsorbida se incrementa; es por esto que los parámetros H aumenta (es decir, disminuye la afinidad) en el orden C28 < C0 < C18 < C4 < C8, lo que indica que la afinidad adsorbato-adsorbente se reduce en gran medida con la muestra C8. El parámetro Nm está relacionada con la capacidad de adsorción de la monocapa, esto de acuerdo con las isotermas, como el carbón adsorbe más agua, este parámetro es mayor. Por lo tanto, muestra que el parámetro Nm para C8 es menor que para otras muestras
4. Conclusiones
La reactividad en carbones con la superficie modificada con glicerol se estudió a partir de ensayos termogravimétricos para determinar su riesgo de combustión espontánea mediante el cálculo del índice de ignición, el índice de combustión espontánea y la energía de activación de la combustión. Un punto de impregnación óptimo se encontró (C8), con una reducción de la re-adsorción era más del 70% en comparación con el carbón no tratado. En el caso de la impregnación con 8% en peso de glicerol, un porcentaje más alto (aproximadamente 40%) de la reducción de la humedad absorbida fue encontrado. La adición de glicerol a la superficie de carbón reduce la afinidad de los sitios activos altamente polares para el agua, reduciendo así el área de la superficie de las muestras tratadas y la adsorción de humedad. El aumento de la cantidad de glicerol en el carbón resultó en la capacidad de los grupos OH para formar enlaces de hidrógeno con moléculas de agua presentes en la atmósfera. Si la cantidad de agua en la atmósfera era alta, entonces la adsorción de agua se incrementó.
Estos resultados muestran que la adición de glicerol a carbones disminuye la humedad, lo que resulta en la disminución de la re-adsorción de agua en comparación con el carbón seco. Estos dos hechos implican un aumento en las propiedades del carbón en los procesos térmicos. Los resultados también implican que la auto-combustión de carbón se inhibe, esto fue demostrado mediante el cálculo de la velocidad de combustión espontánea, obteniendo el valor más bajo de la reactividad de las muestras analizadas. Existe una relación directa entre la capacidad de adsorción de agua y el riesgo potencial de la combustión espontánea.
Agradecimientos
Los autores agradecen a La Universidad Nacional de Colombia y a ARGOS S.A. por su apoyo logístico y financiero
Bibliografía
[1] Rutledge, D., Hubbert's peak, the coal question, and climate change, Excel Workbook (permission is given to copy this work provided that attribution is given and the following web link is included). Website: http://rutledge.caltech.edu, 2007. [ Links ]
[2] Shafiee, S. and Topal, E., When will fossil fuel reserves be diminished?, Energy policy, 37, pp. 181-189, 2009. DOI: 10.1016/J.ENPOL.2008.08.016 [ Links ]
[3] Castro, J., Perspectivas de la demanda energética global, Petrotecnia, pp. 54-70, 2011. [ Links ]
[4] Avila, C., Wu, T. and Lester, E., Estimating the spontaneous combustion potential of coals using thermogravimetric analysis, Energy & Fuels, 28, pp. 1765-1773, 2014. DOI: 10.1021/ef402119f [ Links ]
[5] Stracher, G.B. and Taylor, T.P., Coal fires burning out of control around the world: Thermodynamic recipe for environmental catastrophe, International Journal of Coal Geology, 59, pp. 7-17, 2004. DOI: 10.1016/J.COAL.2003.03.002 [ Links ]
[6] Dubinin, M., Inhomogeneous microporous structures of carbonaceous adsorbents, Carbon, 19, pp. 321-324, 1981. [ Links ]
[7] Dubinin, M. and Serpinsky, V., Isotherm equation for water vapor adsorption by microporous carbonaceous adsorbents, Carbon, 19, pp. 402-403, 1981. [ Links ]
[8] Bowes, P., Self-heating: Evaluating and controlling the hazards: Department of the environment, building research establishment, 1984. [ Links ]
[9] Carras, J.N. and Young, B.C., Self-heating of coal and related materials: Models, application and test methods, Progress in Energy and Combustion Science, 20, pp. 1-15, 1994. DOI: 10.1016/0360-1285(94)90004-3 [ Links ]
[10] Nalbandian, H., Propensity of coal to self-heat: IEA Clean Coal Centre London, 2010. [ Links ]
[11] Krishnaswamy, S., Agarwal, P. K. and Gunn, R.D., Low-temperature oxidation of coal. 3. Modelling spontaneous combustion in coal stockpiles, Fuel, 75, pp. 353-362, 1996. DOI: 10.1016/0016-2361(95)00249-9 [ Links ]
[12] Küçük, A., Kadıoğlu, Y. and Gülaboğlu, M., A study of spontaneous combustion characteristics of a Turkish lignite: Particle size, moisture of coal, humidity of air, Combustion and Flame, 133, pp. 255-261, 2003. DOI: 10.1016/S0010-2180(02)00553-9 [ Links ]
[13] Ray, S. and Bhowmick, B., Indian coals vis-a-vis spontaneous heating problems, Journal of Mines, Metals & Fuels, 49, pp. 123-128, 2001. [ Links ]
[14] Sujanti W. and Zhang, D.K., A laboratory study of spontaneous combustion of coal: The influence of inorganic matter and reactor size, Fuel, 78, pp. 549-556, 1999. DOI: 10.1016/S0016-2361(98)00188-4 [ Links ]
[15] Fei, Y., Aziz, A.A., Nasir, S., Jackson, W., Marshall, M.J. and Hulston, J., The spontaneous combustion behavior of some low rank coals and a range of dried products, Fuel, 88, pp. 1650-1655, 2009. DOI: 10.1016/J.FUEL.2009.03.017 [ Links ]
[16] Fierro, V., Miranda, J., Romero, C., Andres, J., Arriaga, A. and Schmal, D., Model predictions and experimental results on self-heating prevention of stockpiled coals, Fuel, 80, pp. 125-134, 2001. DOI: 10.1016/S0016-2361(00)00062-4 [ Links ]
[17] Pone, J.D.N., Hein, K.A., Stracher, G.B., Annegarn, H.J. and Finkleman, R.D. and Blake, D.R., The spontaneous combustion of coal and its by-products in the Witbank and Sasolburg coalfields of South Africa, International Journal of Coal Geology, 72, pp. 124-140, 2007. DOI: 10.1016/J.COAL.2007.01.001 [ Links ]
[18] Arısoy, A., Coal mine safety and preventing self-combustion of coal. In: Conference: Inerma, At Istanbul, Turkey, 2010. [ Links ]
[19] Bhat, S. and Agarwal, P.K., The effect of moisture condensation on the spontaneous combustibility of coal, Fuel, 75, pp. 1523-1532, 1996. DOI: 10.1016/0016-2361(96)00121-4 [ Links ]
[20] Jun-Ling, X., Feng, H. and Run-Zhang, Y., Relationship between coal powder and its combustibility, Journal of Wuhan University of Technology-Mater. Sci. Ed., 17, pp. 72-75, 2002. DOI: 10.1007/BF02852641 [ Links ]
[21] Franco, C., Martínez, M., Benjumea, P., Patiño, E. and Cortés, F., Water remediation based on oil adsorption using nanosilicates functionalized with a petroleum vacuum residue, Adsorption Science & Technology, 32, pp. 197-208, 2014. DOI: 10.1260/0263-6174.32.2-3.197 [ Links ]
[22] Franco, C., Patiño, E., Benjumea, P., Ruiz, M.A. and Cortés, F., Kinetic and thermodynamic equilibrium of asphaltenes sorption onto nanoparticles of nickel oxide supported on nanoparticulated alumina, Fuel, 105, pp. 408-414, 2013. DOI: 10.1016/J.FUEL.2012.06.022 [ Links ]
[23] Franco, C., Montoya, T., Nassar, N.N., Pereira-Almao, P. and Cortés, F., Adsorption and subsequent oxidation of colombian asphaltenes onto nickel and/or palladium oxide supported on fumed silica nanoparticles, Energy & Fuels, 27, pp. 7336-7347, 2013. DOI: 10.1021/ef4018543 [ Links ]
[24] Franco, C., Nassar, N.N. and Cortés, F., Removal of oil from oil-in-saltwater emulsions by adsorption onto nano-alumina functionalized with petroleum vacuum residue, Journal of Colloid and Interface Science, 433, pp. 58-67, 2014. DOI: 10.1016/j.jcis.2014.07.011 [ Links ]
[25] Brunauer, S., Emmett, P.H. and Teller, E., Adsorption of gases in multimolecular layers, Journal of the American chemical society, 60, pp. 309-319, 1938. [ Links ]
[26] Cortés, F., Rojano, B. and Chejne-Janna, F., Advantages and thermodynamic limitations of the experimental sorption isosteric method, DYNA, 80(182), pp. 155-162, 2013. [ Links ]
[27] Parshetti, G.K., Quek, A., Betha, R. and Balasubramanian, R., TGA-FTIR investigation of co-combustion characteristics of blends of hydrothermally carbonized oil palm biomass (EFB) and coal, Fuel Processing Technology, 118, pp. 228-234, 2014. DOI: 10.1016/J.FUPROC.2013.09.010 [ Links ]
[28] Kaymakci, E. and Didari, V., Relations between coal properties and spontaneous combustion parameters, Turkish Journal of Engineering and Environmental Sciences, 26, pp. 59-64, 2002. [ Links ]
[29] Freeman, E.S. and Carroll, B., The application of thermoanalytical techniques to reaction kinetics: the thermogravimetric evaluation of the kinetics of the decomposition of calcium oxalate monohydrate, The Journal of Physical Chemistry, 62, pp. 394-397, 1958. DOI: 10.1021/j150562a003 [ Links ]
[30] Arias, B., Pevida, C., Rubiera, F. and Pis, J., Changes in coal char reactivity and texture during combustion in an entrained flow reactor, Journal of Thermal Analysis and Calorimetry, 90, pp. 859-863, 2007. DOI: 10.1007/s10973-006-8265-z [ Links ]
[31] Sis, H., Evaluation of combustion characteristics of different size elbistan lignite by using TG/DTG and DTA, Journal of thermal analysis and calorimetry, 88, pp. 863-870, 2006. DOI: 10.1007/s10973-005-7447-4 [ Links ]
[32] Allardice, D., Clemow, L., Favas, G., Jackson, W., Marshall, M. and Sakurovs, R., The characterisation of different forms of water in low rank coals and some hydrothermally dried products, Fuel, 82, pp. 661-667, 2003. DOI: 10.1016/S0016-2361(02)00339-3. [ Links ]
[33] Charrière, D. and Behra, P., Water sorption on coals, Journal of colloid and interface science, 344, pp. 460-467, 2010. DOI: 10.1016/j.jcis.2009.11.064 [ Links ]
[34] Chen, X.D., A new water sorption equilibrium isotherm model, Food research international, 30, pp. 755-759, 1997. DOI: 10.1016/S0963-9969(98)00042-8 [ Links ]
[35] Karthikeyan, M., Minimization of moisture readsorption in dried coal samples, Drying Technology, 26, pp. 948-955, 2008. DOI: 10.1080/07373930802142846 [ Links ]
[36] Marchessault, R., Application of infra-red spectroscopy to cellulose and wood polysaccharides, Pure and Applied Chemistry, 5, pp. 107-130, 1962. DOI: 10.1351/pac196205010107 [ Links ]
[37] McCain, W.D., The properties of petroleum fluids: PennWell Books, 1990. [ Links ]
[38] Shigehisa, T., Inoue, T. and Kumagai, H., Mathematical model of water sorption isotherms of UBC, Fuel Processing Technology, 131, pp. 133-141, 2015. DOI: 10.1016/J.FUPROC.2014.11.023 [ Links ]
[39] Talu, O. and Meunier, F., Adsorption of associating molecules in micropores and application to water on carbon, AIChE Journal, 42, pp. 809-819, 1996. DOI: 10.1002/aic.690420319 [ Links ]
E.A. Taborda-Acevedo, es Ing. Químico en 2007 de la Universidad Nacional de Colombia. MaSc. en Ingeniería Química em 2014, de la Universidad Nacional de Colombia. Actualmente estudiante de doctorado en Sistemas Energéticos de la Universidad Nacional de Colombia, perteneciente al Grupo de Investigación en Fenómenos de Superficie - Michael Polanyi con experiencia en proyectos de investigación y extensión en el área de fenómenos de superficie como adsorción, humectabilidad, reología, entre otros. ORCID: 0000-0001-5920-0830
W.J. Jurado, es Ing. Químico de la Universidad Nacional de Colombia. MSc. en Ingeniería Química em 2014, de la Universidad Nacional de Colombia. Actualmente, perteneciente al Departamento de optimización de procesos del grupo ARGOS. Experiencia como líder de proyectos de investigación en cementos ARGOS. ORCID: 0000-0001-9236-7042
F.B Cortes, es Ing. Químico de la Universidad Nacional de Colombia. Dr. en Ingeniería: Sistemas Energéticos de la Universidad Nacional de Colombia. Profesor asociado del Departamento de Química y Petróleos, Facultad de Minas, de la Universidad Nacional de Colombia sede Medellín. Director del Grupo de Investigación en Fenómenos de Superficie - Michael Polanyi con experiencia en proyectos de investigación y extensión en el área de fenómenos de superficie aplicados a la productividad de yacimientos y áreas afines. ORCID: 0000-0003-1207-3859