El lago de Coatepeque presenta 2485 hectáreas de espejo de agua, se localiza a 740 m.s.n.m., y se originó por el colapso de una caldera volcánica en El Salvador, Centroamérica (Bergoeing, 2015). Las orillas son principalmente arenosas y rocosas con diferentes pendientes (Ministerio de Medio Ambiente y Recursos Naturales [MARN], 2018). Este lago alberga una importante riqueza de fauna y flora acuática que se distribuye en diferentes profundidades. La fauna acuática incluye macroinvertebrados bentónicos que se asocian a rocas, algas, plantas, restos vegetales y fondos blandos (arena o ceniza). La vegetación litoral incluye a la especie emergente Typha domingensis Persoon 1807, así como a las sumergidas: Chara zeylanica Klein ex Willdenow, 1805, Hydrilla verticillata (L. f.) Royle, 1839, Najas marina Linaeus 1753, Ruppia marítima Linnaeus, 1753 (MARN, 2018). A pesar de que la literatura sobre macroinvertebrados bentónicos de este lago es escasa, existen registros de gasterópodos de las familias Cochliopidae, Hydrobiidae, Planorbidae y Physidae (Thompson, 2011). También se ha documentado la presencia de un cangrejo Potamocarcinus magnus Rathbun, 1896 (Bott, 1956; Carranza-Noyola y Pocasangre, 1988; Jiménez et al., 2004). El objetivo de este estudio preliminar fue determinar la abundancia, hábitats y distribución vertical de macroinvertebrados asociados al sustrato de la zona noroeste de este lago.
Todos los muestreos y observaciones se completaron en tres diferentes profundidades en los meses de julio, noviembre y diciembre de 2019, así como entre marzo y abril de 2022, en el sector denominado "Segundo Anteojo" del lago de Coatepeque (13o 52' 22.1" N, 89o 31' 18.7" W), departamento de Santa Ana, El Salvador. Se establecieron tres franjas de muestreo paralelas a la línea litoral. La primera de ellas en la orilla rocosa y arenosa, incluyendo vegetación emergente y sumergida (T domingensis y C. zeylanica, respectivamente); la segunda franja, entre 0,5 a 2,0 m de profundidad, presentó rocas, mezcla de arena y fango fino con todas las especies vegetales sumergidas mencionada en el párrafo anterior; en la tercera, ubicada a 10 m de profundidad, la vegetación disminuyó, presentando principalmente ejemplares dispersos de C. zeylanica sobre sedimento fino. Las recolectas de macroinvertebrados se realizaron con la autorización de las Resoluciones ADENDA-MARN-DEV-GVS-108-2018 y MARN-DEB-GVS-AIMA-1-2022, emitidas por el Ministerio de Medio Ambiente y Recursos Naturales de El Salvador.
En la franja de muestreo superficial se capturaron ejemplares de macrofauna con un cuadrante de 400 cm2 en tres diferentes zonas seleccionadas al azar, girando rocas de ser necesario y también utilizando un tamiz de 0,5 mm de diámetro de poro. En la segunda franja, se extrajeron macroinvertebrados de rocas en forma manual con igual cantidad de repeticiones (tres) que la estación anterior, utilizando el mismo cuadro y tamiz. En la última estación se recolectaron muestras de sedimento fino con tres nucleadores de 12 cm de diámetro (área total: 339,3 cm2) y con un grosor de cinco cm aproximados de sedimento superficial, incluyendo rocas pequeñas, que se tamizaron para separar el macrozoobentos (> 0,5 mm). En la segunda y tercera franja se utilizó buceo autónomo para tomar las muestras. El material biológico recolectado se preservó y fijó en etanol al 90 %. Las muestras se clasificaron en el nivel taxonómico más preciso posible (Tabla 1), utilizando las descripciones de Hanson et al. (2010), Sermeño-Chicas et al. (2010), Pessacq et al. (2018) y Thorp et al. (2020).
Los taxones más abundantes en la primera y segunda franja (<0,5 m y 0,5-2,0 m, respectivamente) fue una especie de gasterópodo de la familia Thiaridae, incluyeron a un anfípodo del género Hyalella S.I. Smith, 1874 (Hyalellidae) y larvas de insectos de las familias Chironomidae (Diptera) y Coenagrionidae (Odonata) (Tabla 1).
Tabla 1 Taxones registrados a diferentes estratos de profundidad (O, M, F) en zona noreste del lago de Coatepeque. A: abundancia, D: densidad (ind/m2), H: superficies duras, H': Indice de Shannon-Weaver, nd: no determinado, R: rocas, S: sedimento, V: vegetación emergente o sumergida. Fila en letra negrita.
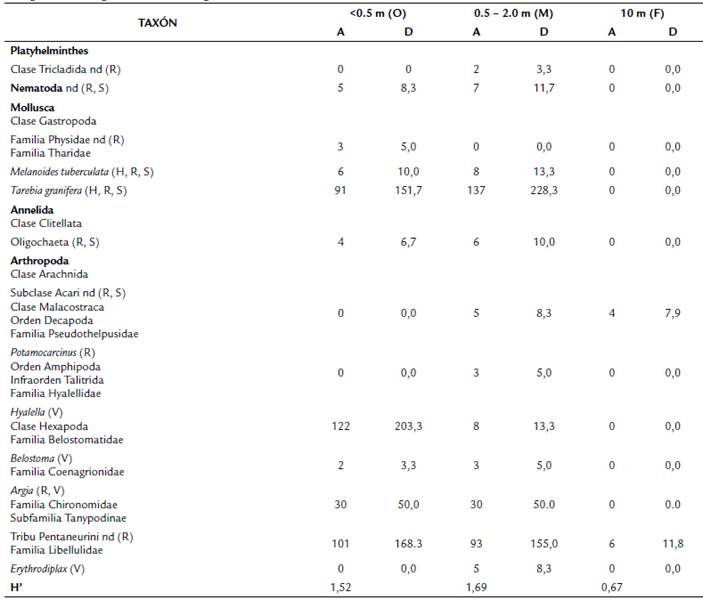
El caracol Tarebia granifera (Lamarck, 1816) (Thiaridae) que según López-López et al., (2009) es un gasterópodo invasor en México, fue la especie más abundante en las franjas de muestreo OyM (Tabla 1), reflejando su establecimiento en el lago de Coatepeque, ya que se presentó en diferentes franjas entre 0,0 a 5,0 m de profundidad, tanto en fondos blandos como duros, incluyendo desechos sólidos sumergidos. T. granifera y la especie Melanoides tuberculata (O. F. Müller, 1774), que según Quirós-Rodríguez et al. (2018) es otra especie invasora, han colonizado exitosamente diferentes cuerpos de agua dulce de El Salvador (Barraza, 2021), incluyendo este cuerpo léntico. Se desconoce fechas y mecanismos de introducción al país para ambas especies. La ocurrencia de ambas especies presenta riesgos para la salud de humanos, peces y aves ictiófagas por la facilidad con que albergan diferentes tipos de parásitos, así como la posibilidad de desplazar a especies de macroinvertebrados acuáticos nativos (López et al., 2019). El segundo grupo con importancia numérica fue la familia Chironomidae (Subfamilia Tanypodinae) que se encontró en las tres profundidades en estudio, particularmente asociado a fondos blandos. Estos insectos también se encontraron en sedimentos blandos del lago Cote (650 m.s.n.m., 15 m profundidad), Costa Rica, aunque con menor abundancia (Sibaja-Cordero y Umaña-Villalobos, 2008). Esta familia se considera indicadora de contaminación orgánica en ríos de El Salvador debido a su capacidad de adaptarse a bajas concentraciones de oxígeno disuelto en el agua, y también se encuentra en diferentes tipos de hábitats acuáticos lénticos i.e. lagos (Sermeño-Chicas, Serrano-Cervantes, et al., 2010); estas características podrían explicar su presencia entre la orilla y 10 m de profundidad en la zona de estudio.
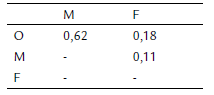
El tercer organismo con mayor abundancia fue el anfípodo del género Hyalella, particularmente en profundidad menor a 0,5 m y asociado a la macroalga C. zeylanica (Charophyta: Charophyceae: Charales: Characeae). En el área natural protegida Laguna El Jocotal se encontraron especímenes de este género en un hábitat semejante (Barraza y López, 2017). Una similar asociación a macrófitas sumergidas de al menos dos especies de este género fueron mencionadas por Soucek et al. (2015) para la zona este de Estados Unidos de América. El cuarto taxón en abundancia pertenece al género Argia (Coenagrionidae) que se encontró en la franja O y M asociado a T. domingensis y otras macrófitas sumergidas, así como bajo rocas. La presencia de la familia Coenagrionidae fue documentada también en ambientes con vegetación acuática de lagos tropicales de Costa de Marfil (Kouamé et al., 2011), Zimbaue (Makaure et al., 2015) y Costa Rica (Román-Herácleo, 2020). Adicionalmente, se han registrado 16 especies del género Argia en varios cuerpos de agua de El Salvador (Sermeño-Chicas et al., 2010). El índice de similitud de Jaccard entre la zona O y M (Tabla 2) fue de 0,62, reflejando cierta semejanza en la composición de los taxones que habitan en la orilla y la franja de 0,5 a 2,5 m, ya que en ambos casos se observaron organismos bentónicos asociados fondos rocosos, parches arenosos y vegetación acuática. El mismo índice determinado entre las zonas O y F, así como M y F, presentó valores bajos (0,18 y 0,11, respectivamente), reflejando bajas similitudes en la composición de especies. El estrato F (10 m), caracterizado por escasa vegetación y rocas cubiertas por abundante sedimento blando, presentó menor riqueza y abundancia de taxones (Tabla 1), posiblemente asociado a la disminución de microhábitats y a la naturaleza geoquímica de este lago (Cabassi et al., 2019). Además, en esta franja se encontró una alta cantidad de conchas vacías de los gasterópodos M. tuberculata y T. granifera, así como cápsulas cefálicas de quironómidos en el sedimento, que podrían servir en futuros estudios de paleolimnología (Hamerlik et al., 2018). Además, el índice de diversidad de Shannon-Weaver en los estratos O, M y F fue 1,52, 1,69 y 0,67, respectivamente, reflejando baja diversidad de taxones con algunos de ellos dominantes (<2,00) (Tabla 1) (Mora-Donjuán et al., 2017).
Tabla 2 Indice de similitud de Jaccard determinado para los tres estratos de profundidad (O, M, F) en el área noreste del lago de Coatepeque.
Similares valores del mismo índice se observaron en la zona litoral de menos de 1 m (1,26), sublitoral entre 1,5 a 2,7 m (0,60) y más de 3 m de profundidad (0,58) de un lago tropical (Kuriftu) en Etiopía (Ayele y Mengistou, 2013), donde el grupo con mayor dominio numérico fue la familia Chironomidae la cual fué también detectada en este estudio.
Los estratos de orilla (O) y profundidad media (M) presentaron mayor diversidad y abundancia de especies en comparación a la franja más profunda (F), lo que puede estar asociado a la presencia de vegetación sumergida y emergente, substrato blando y rocoso, lo que facilita una mayor disponibilidad de hábitats para macroinvertebrados bentónicos. Similar resultado se encontró en un estudio con la misma temática en el lago tropical Nguru de Nigeria, en el cual el grupo dominante también fue la familia Chironomidae (Abubakar et al., 2013).
Los resultados obtenidos indican la importante abundancia de la familia Thiaridae, también la familia Hyalellidae representada por anfípodos del género Hyalella y las fases acuáticas de libélulas de la familia Coenagrionidae en áreas rocosas y arenosas asociadas a vegetación de poca profundidad (0,0 - 2,5 m) del sector noroeste del lago de Coatepeque.
CONCLUSIONES
Este estudio preliminar incursiona en el área de ecología del macrozoobentos del lago de Coatepeque, refleja la distribución de taxones en forma estratificada en un gradiente de profundidad entre los 0 y los 10 m, resalta la importancia de la vegetación sumergida y la reducción de la riqueza de especies en los estratos más profundos.
Se requieren estudios con mayor amplitud en ese cuerpo léntico y otros del país, particularmente la profundización en la taxonomía de odonatos y quironómidos. Para ello es indispensable el estudio no solamente de las larvas acuáticas, sino también de los adultos y así lograr determinar las especies.















