Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Col. Cardiol. vol.13 no.1 Bogota Aug. 2006
Universidad Militar Nueva Granada.Departamento de Cirugía Vascular y Angiología. Hospital Militar Central, Bogotá, DC., Colombia.
Correspondencia: Luis Fernando García Valencia, MD. Departamento de Cirugía Vascular y Angiología, Hospital Militar Central, Carrera 5a. Calle 49, Bogotá, DC., Colombia. Teléfono: 348 68 68, Extensión: 5185-5186.
Recibido: 20/12/05. Aprobado: 04/08/06
Objetivo: reportar la experiencia del manejo endovascular en pacientes con síndrome de compresión iliocava.
Materiales y métodos: durante tres años se evaluaron 84 pacientes con sospecha de compresión iliocava, cuyo diagnóstico se confirmó mediante flebografía ascendente e Iliocavografía.
Se trataron 17 pacientes por vía endovascular, terapia de anticoagulación y seguimiento radiológico seriado.
Resultados: en un total de 17 pacientes con edad promedio de 43 años, se observó mejoría clínica completa en 88%, parcial en 6% y ninguna en 6%. Permeabilidad del stent en 94,12% a 36 meses.
Conclusión: la terapia endovascular muestra excelente permeabilidad y baja morbilidad en el tratamiento de pacientes con síndrome de compresión iliocava.
Palabras clave: cockett, iliocava, iliocavografia, endovascular, stent.
Objective: to report our experience in the intravascular management in patients with iliocaval compression syndrome.
Material and methods: 84 patients with suspicion of iliocaval compression were evaluated during a three years period. This diagnosis was confirmed by ascendant phlebography and iliocavography.
17 patients received endovascular treatment, anticoagulants and serial radiological follow-up.
Results: from 17 patients with mean age of 43 years, 88% had a complete clinical recovery; it was partial in 6% and absent in 6%. Stent’s patency was 94.12% after 36 months.
Conclusion: endovascular therapy shows excellent patency and low morbidity in the treatment of patients with iliocaval compression syndrome.
Key words: cockett, iliocaval, iliocavography, endovascular, stent.
Introducción
El síndrome de Cockett o síndrome de compresión iliocava, es aquella alteración anatómica, compresiva o endoluminal de la vena ilíaca común izquierda, que produce obstrucción y/o trombosis venosa iliofemoral (1-7, 12-15).
Desde Virchow, se han investigado las causas de dicha patología y a través del tiempo se han hallado alteraciones anatómicas como la relación que existe entre la arteria ilíaca derecha que comprime la vena ilíaca común izquierda (1, 15).
Los trabajos iniciales de May–Thurner en 1955 (4), realizados en cadáveres, permitieron demostrar la presencia de espolones en la unión iliocava izquierda, asociada a trombosis venosa iliofemoral, postulando que esta deformidad de la vena se debía a irritación producida por el golpe permanente de la arteria ilíaca derecha sobre la vena ilíaca izquierda.
El origen congénito de los espolones (demostrado histológicamente por la presencia de fibras de músculo liso dentro de las sinequias) así como la clasificación clínica y radiológica del síndrome, fueron postulados en 1965 por Cockett y Lea Thomas (5, 6).
Dentro de las causas extrínsecas que producen compresión iliocava izquierda, se debe considerar el cruce arteriovenoso de la arteria ilíaca derecha sobre la vena ilíaca izquierda, la impronta de L4 sobre la vena ilíaca izquierda (por hiperlordosis lumbar) y las masas tumorales intra y extraperitoneales (1, 15).
El grado de severidad de las manifestaciones clínicas de este síndrome, depende de la eficiencia con que la circulación colateral de la pelvis logre llevar el retorno venoso desde la extremidad inferior izquierda hacia la vena cava inferior, dando la posibilidad de encontrar pacientes que aunque tengan evidente malformación endoluminal o compresión extrínseca, no presenten hiperpresión venosa de dicha extremidad que justifique la realización de la corrección endoluminal (5, 6, 12).
Aunque en la actualidad no hay estudios que definan la mejor opción terapéutica para el síndrome de Cockett, ésta puede ser médica, quirúrgica o endovascular (12).
En este trabajo se presenta la experiencia dirigida a la terapia endovascular en dicha patología.
Materiales y métodos
Objetivo
Reportar la experiencia del manejo endovascular en el síndrome de compresión iliocava (síndrome de Cockett) en el Hospital Militar Central, por un período de 36 meses durante los años 2001 a 2004.
Tipo de estudio
Estudio observacional, descriptivo y reporte de casos clínicos.
Criterios de inclusión
Se incluyeron todos los pacientes que consultaron al Servicio de Consulta Externa de Cirugía Vascular del Hospital Militar Central, con signos y/o síntomas de hipertensión venosa como: circulación colateral prepúbica y de la pared abdominal, pesadez, claudicación venosa y edema; trombosis venosa profunda iliofemoral y síndrome postrombótico del miembro inferior izquierdo. A estos pacientes se les sospechó síndrome de compresión iliocava, diagnóstico confirmado mediante flebografía ascendente e iliocavografía.
Criterios de exclusión
Se excluyeron pacientes a quienes se les confirmó síndrome de hipercoagulabilidad, aquellos en quienes no se demostró por flebografía alteración morfológica de la unión iliocava izquierda, quienes no presentaron un gradiente de presión significativo o en quienes no fue posible realizar el paso de la guía hidrofílica a través de la lesión después de múltiples intentos.
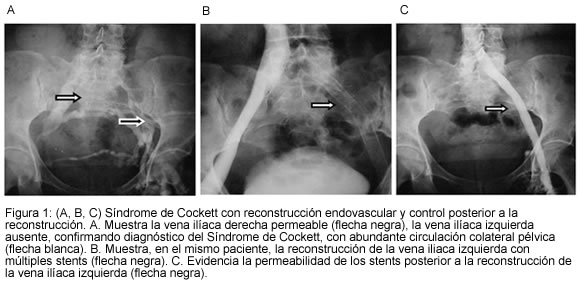
En la Consulta Externa del Servicio de Cirugía Vascular y Angiología del Hospital Militar Central de Bogotá, por un periodo de 36 meses, comprendido entre los años 2001 y 2004, se seleccionaron 84 pacientes con síntomas como pesadez, edema, claudicación venosa, trombosis venosa iliofemoral (como primera manifestación) y síndrome postrombótico del miembro inferior izquierdo, que presentaban, al examen físico, várices de miembro inferior izquierdo, edema con diferencia en el diámetro del muslo y pierna mayor de 2 centímetros con respecto a la extremidad contralateral y circulación colateral prepúbica y de la pared abdominal (Figura 1A). A estos pacientes se les sospechó síndrome de compresión iliocava, diagnóstico confirmado según protocolo de nuestro servicio, mediante flebografía ascendente de miembros inferiores e iliocavografía con medición de presiones. Se diagnosticó síndrome de Cockett de tipo no trombótico y trombótico, que según la clasificación CEAP son: C3 EC AD Po y C3 ES AD Po respectivamente (18-21). A los pacientes con síndrome de Cockett trombótico, se les realizó tamizaje para síndrome de hipercoagulabilidad de tipo hereditario, mediante pruebas sanguíneas como: factor V de Leiden, factor 8, antitrombina III, proteína C y proteína S libre realizadas por técnicas de coágulo, sustratos cimógenos y Elisa, según la fracción estudiada. Para el tipo adquirido, se realizaron pruebas de anticoagulante lúpico por técnica de coágulo y anticuerpos anticardiolipina y antifosfolípidos por técnica de Elisa.
El tamizaje del síndrome de plaquetas pegajosas, se realizó mediante la técnica de agregometría plaquetaria con sustratos de adenosín-difosfato y epinefrina.
Los pacientes con positividad de alguna de las pruebas descritas, s excluyeron del estudio y recibieron manejo médico por nuestro servicio y por hematología.
Todos los pacientes seleccionados se presentaron en junta quirúrgica, con el fin de establecer la mejor opción terapéutica para cada uno.
La indicación para realizar manejo endovascular fue la confirmación clínica y radiológica del síndrome de compresión iliocava (Figura 1), además de la presencia de un gradiente de presión con valores mínimos de 2 mm Hg, entre la vena cava inferior y el segmento iliofemoral distal a la alteración anatómica. Dichas presiones se hicieron con el paciente en decúbito supino, durante la realización de la iliocavografia y mediante un catéter con orificio único terminal, conectado a un transductor Transpac IV. Los valores de las presiones se visualizaron en un monitor de presiones invasivas, POET PLUS 8100, calibrado a presión venosa central (PVC), determinando así la diferencia de presiones proximal y distal a la estenosis.
Del manejo endovascular se excluyeron 67 pacientes, de los cuales 23 no presentaron evidencia flebográfica de alteración morfológica de la unión iliocava izquierda, 31 pacientes no tuvieron un gradiente de presión significativo a pesar de presentar alteración morfológica, 8 pacientes a quienes no fue posible realizar el paso de la guía hidrofílica a través de la lesión después de múltiples intentos y 5 pacientes a quienes se les confirmó el diagnóstico de síndrome de hipercoagulabilidad, los cuales presentaban alto riesgo de trombosis del stent.
Los 17 pacientes restantes fueron manejados por vía endovascular (angioplastia con balón y stent único o múltiples de acuerdo con el tipo de lesión y su extensión).
Previo a la intervención, cada paciente recibió información acerca del procedimiento, riesgos y beneficios, con aceptación y firma del consentimiento informado.
El tamaño del stent se escogió de acuerdo con el diámetro de la vena, según la iliocavografía; todos los stents fueron impactados con balón. Es de anotar que hubo pacientes que se manejaron con uno, dos, tres y hasta cuatro stents dependiendo de la longitud de la estenosis (Figura 1B).
Los stents utilizados para la unión iliocava fueron stents de Palmaz en acero inoxidable, con un diámetro promedio de 14-25 mm montados sobre un balón de 20 mm. Los stents usados para la reconstrucción de la vena ilíaca fueron stents de nitinol autoexpandibles, con diámetro promedio de 12-14 mm.
Todos los pacientes fueron tratados por el mismo cirujano vascular, en la sala de hemodinamia y sobre la mesa angiográfica. Se realizó punción de la vena femoral en forma bilateral, mediante la técnica de Seldinger. Se emplearon introductores 6Fr en el lado derecho y 12Fr en el lado izquierdo, logrando el paso de la guía hidrofílica a través de la lesión hasta la vena cava inferior. Por protocolo de nuestro servicio, todos los pacientes recibieron 5.000 UI de heparina intravenosa en bolo previo al implante del o de los stents.
De los 17 pacientes manejados con terapia endovascular, 10 presentaron alteración morfológica de la unión iliocava izquierda, asociada a estenosis y fibrosis de la vena ilíaca primitiva y externa. Éstos requirieron angioplastia progresiva con balones de 4 mm, 6 mm, 8 mm y 12 mm, que permitieran el paso del stent de Palmaz montado sobre el balón, el cual fue implantado a nivel de la unión iliocava izquierda, seguido de la colocación de 2 o más stents de nitinol autoexpandibles de 12 mm y 14 mm de diámetro, hasta lograr la completa repermeabilización y cubrimiento de la lesión estenótica de la vena ilíaca izquierda (Figura 1B).
Los 7 pacientes restantes presentaron sinequias endoluminales o espolones de la unión iliocava izquierda, sin presencia de trombosis asociada. Estos pacientes se trataron mediante angioplastia de la lesión, con balón de 20 mm de diámetro y el posterior implante de un stent de Palmaz en acero inoxidable montado sobre dicho balón.
Inmediatamente concluido el procedimiento, se realizó en todos los casos, control angiográfico con inyección de medio de contraste no iónico, corroborando la adecuada posición de los stents y el correcto paso del medio a través de éstos hacia la vena cava inferior (Figura 1C).
Durante el postoperatorio, los pacientes recibieron terapia de anticoagulación con heparina en infusión venosa continua, hasta lograr prolongación del tiempo parcial de tromboplastina (PTT) 2,5 veces el control. Posteriormente, se continuó la anticoagulación con warfarina sódica oral, con control periódico del tiempo de protrombina (PT) y mediante el método de rango normalizado internacional (INR) entre 2,5 a 3 por un período de seis meses.
A todos los pacientes se les realizó seguimiento quincenal, manteniendo INR entre 2,5 y 3, suspendiendo la terapia con warfarina luego de seis meses. Después se continuó con el seguimiento clínico y se verificó la permeabilidad del stent por medio de iliocavografía a los seis meses y luego anualmente hasta los 36 meses (Figura 2).

Síndrome de Cockett o síndrome de compresión iliocava
Alteración anatómica, compresiva o endoluminal de la vena ilíaca común izquierda, que produce obstrucción y/o trombosis venosa iliofemoral (1-7, 12-15).
Edema de origen vascular
Acumulación de líquido en el espacio extravascular predominantemente en las piernas, frío, con fóvea, cianótico, vespertino, que cede al mejorar la circulación venosa (reposo), producido por un disbalance entre las presiones hidrostáticas y oncóticas a nivel intravascular (22, 23).
Síndrome de hipercoagulabilidad
Situación anormal de la sangre circulante, en la que comparada con el estado normal, requiere un menor estímulo para provocar la aparición de trombosis. Puede diferenciarse en síndrome de tipo hereditario y adquirido (24).
Claudicación venosa
Dolor muscular, calambre y/o tensión en miembros inferiores, que obliga al paciente a detenerse después de caminar cierto trayecto, esto en ausencia de obstrucción arterial y con presencia de congestión venosa (22, 23).
Síndrome postrombótico
Manifestación de la insuficiencia venosa crónica, como complicación tardía de la trombosis venosa profunda, que se manifiesta con cambios cutáneos, úlceras, edema y dolor. La severidad de los síntomas se relaciona con la extensión de la trombosis venosa profunda (25, 26).
Pesadez
Sensación de plenitud y de peso, generalmente acompañada de cansancio en las piernas (22, 23).
Resultados
Del primero de enero de 2001 al treinta y uno de diciembre de 2004, se trataron 17 pacientes con terapia endovascular, 16 mujeres y 1 hombre, con un promedio de edad de 43 años (rango entre 22 y 58 años).
Diez pacientes presentaron síndrome de Cockett con trombosis y 7 fueron no trombóticos (58,82% y 41,18% respectivamente).
Durante la hospitalización, los pacientes tuvieron evaluación clínica a diario, hasta lograr adecuados niveles de anticoagulación. El control ambulatorio se realizó cada quince días y se suspendió la anticoagulación a los seis meses para continuar con valoraciones clínicas hasta los 36 meses. La mejoría clínica de síntomas como pesadez, dolor y claudicación venosa se evaluó mediante la escala visual análoga del dolor: 0 para ausencia de dolor y 10 para dolor severo e intolerable (16,17), evidenciándose mejoría completa en el 88%, parcial en el 6% y ninguna en el 6% restante.
La diferencia de diámetros a nivel del muslo izquierdo comparado con el derecho, fue en promedio 2,35 cm y a nivel de la pierna de 3 cm antes del tratamiento; posterior al implante del o de los stent el promedio de los diámetros fue de 1,25 y 1 cm respectivamente, tomados al mismo nivel.
La permeabilidad del stent se corroboró a los 6, 12, 24 y 36 meses (Figura 2), mediante iliocavografía por punción femoral bilateral. El 94,12% presentó adecuada permeabilidad, mientras que el 5,88% mostró trombosis de los stents (1 paciente), complicación presentada por el suministro inadvertido de dosis subóptimas de anticoagulación. Dicho paciente presentaba cambios postrombóticos extensos y antiguos de la vena ilíaca común y externa izquierda.
En toda la serie reportada no hubo ningún caso de reacción alérgica al medio de contraste, falla renal, ruptura de los vasos tratados, migración ni mal posición de los stents o mortalidad, ni tampoco fue necesario realizar procedimientos adicionales.
Discusión
En nuestro estudio se evaluó una serie de casos de pacientes con síndrome de Cockett, de los cuales se incluyeron 17 para tratamiento por vía endovascular. En el análisis de los resultados se encontró evidente mejoría clínica, baja morbilidad y permeabilidad del stent a corto, mediano y largo plazo en quienes recibieron este tipo de manejo.
El síndrome de compresión iliocava fue descrito por primera vez en 1851 por Virchow (1), quien evidenció mayor trombosis venosa iliofemoral izquierda (cinco veces más) en comparación con la derecha. Esta diferencia se debe a la relación anatómica de la vena ilíaca común izquierda, que hace que sea comprimida por la arteria ilíaca común derecha contra la quinta vértebra lumbar, lo cual produce estasis venosa y por ende mayor frecuencia de trombosis venosa profunda.
En 1908 Murrich (2), planteó la hipótesis sobre el origen congénito de esta patología al encontrar 35 cadáveres de los 107 examinados, con adherencias o espolones, 32 de los cuales estaban en la vena ilíaca común izquierda y presentaron mayor frecuencia de trombosis venosa profunda.
En 1943, Ehrich y Krumbhaar (3) realizaron 412 autopsias, en las cuales evidenciaron 23,8% de obstrucción de la vena ilíaca común izquierda y concluyeron que la patología era adquirida y no congénita, al encontrar en el análisis microscópico defectos del colágeno, elastina, reacción inflamatoria y cicatriz de organización irregular, además de aparecer después de la primera década de la vida en un 33,8%.
En 1957, May y Thurner (4) examinaron 430 cadáveres y encontraron en 22% lesiones obstructivas, denominadas «spurs» o espolones, formaciones callosas que comprometían el diámetro de la luz de la unión iliocava izquierda.
Los espolones fueron clasificados en tres tipos, I: laterales en la pared de la vena, II: centrales, que dividen la vena en dos lúmenes y III: sinequias completas con fenestración única o múltiple. Ellos consideraron que los espolones se presentaban por el frote de las paredes de la vena, dado por la obstrucción y la pulsación de la arteria ilíaca común derecha, ocasionando daño, proliferación endotelial y mayor frecuencia de trombosis venosa profunda.
En 1965 y 1967, Cockett y Lea Thomas (5, 6) reportaron la primera serie de 57 pacientes con trombosis venosa profunda iliofemoral, dada por síndrome de compresión de la vena ilíaca. En esta serie se evidenció mayor frecuencia de esta patología, en mujeres entre la segunda y cuarta décadas de la vida, con mayor afectación del lado izquierdo que el derecho, notándose que podía cursar sintomático o asintomático dependiendo de la presencia de drenaje adecuado o no por venas colaterales. Histológicamente demostraron el origen congénito de los espolones, al encontrar fibras de músculo liso dentro de las sinequias, así como la clasificación clínica y radiológica del síndrome.
Los síntomas de la enfermedad dependen de la fase de obstrucción; en la fase aguda se presentan dolor y edema súbito, mientras que en la fase crónica hay dolor, edema, hipertensión venosa, estasis venosa, claudicación venosa y cambios en el color de la piel. No es infrecuente que la trombosis venosa profunda iliofemoral izquierda, sea la primera manifestación del síndrome de Cockett (5, 6, 12).
Cockett (5, 6), reportó que el manejo de las dilataciones varicosas, úlceras y ligadura de perforantes no está indicado hasta no resolver la obstrucción iliofemoral.
Se han determinado múltiples planes de manejo; en la fase aguda se indica la trombectomía y en la fase crónica el bypass con safena, el parche venoso, la cirugía De Palma, la reacomodación de la arteria ilíaca común derecha y las angioplastias entre otros (12).
La indicación del manejo quirúrgico, está dada por un gradiente de presión mayor de 2 mm Hg entre la vena cava inferior y el segmento iliofemoral, distal a la alteración anatómica (5, 6, 12).
Mikley (7), reportó su experiencia en 30 pacientes (espolones) con manejo quirúrgico y endovascular combinado (Tabla 1).
Hurst y Darren (8), durante un periodo de tres años, presentaron 18 pacientes con síndrome de Cockett y concluyeron que la venografía, la resonancia magnética (Wolpert, Lorraine M. Sensibilidad del 100%) y la ultrasonografía intravascular tuvieron una alta sensibilidad para el diagnóstico (9, 13, 14).
La terapia endovascular proporcionó un manejo efectivo y seguro a temprano y mediano plazo para los pacientes con síndrome de Cockett (8, 9) (Tabla 1).
Rilinger, Görich, Mickley y colaboradores (10) reportaron su experiencia (tres mujeres) en el manejo del síndrome de Cockett (Tabla 1).
Feghaly, Soula, Rousseau, Chaiban, Otal, Joffre y Cerene (11) encontraron como complicaciones de la angioplastia con stent venoso, la migración en dos pacientes, uno a cavidades cardiacas derechas y otro a la arteria pulmonar, los cuales se recuperaron con balón de angioplastia de manera adecuada (Tabla 1).
Patel, Stookey, Ketchman y Cragg (12) presentaron 10 pacientes con trombosis venosa profunda iliofemoral estudiados durante un año con manejo con trombólisis y posterior stent (Tabla 1).
En nuestro grupo de 17 pacientes con síndrome de Cockett, manejados con terapia endovascular, se encontró alta prevalencia de esta patología en el género femenino (acorde con la literatura mundial), con un promedio de edad de 43 años.
Se evidenciaron además dos presentaciones del síndrome, aquellos con trombosis (58,82%) y los no trombóticos (41,18%), cuya sintomatología fue similar a la descrita por otros autores. Los pacientes cuya presentación fue de características trombóticas, consultaron por síntomas crónicos. No se encontró ninguna extensión a la vena cava inferior y ninguno de los pacientes recibió algún tipo de manejo quirúrgico o mecánico del trombo previo al implante del stent.
El seguimiento clínico de los pacientes, se realizó hasta los 36 meses, tiempo durante el cual se observó mejoría clínica completa en el 88% de los casos, ninguna mejoría en el 6% y mejoría parcial en el 6% restante.
Por medio de la iliocavografía ascendente realizada a los 6, 12, 24 y 36 meses se corroboró la permeabilidad del stent en el 94,12%.
Un paciente con cambios postrombóticos extensos y antiguos de la vena ilíaca común y externa izquierda, mostró tempranamente trombosis del stent por dosis subóptimas de anticoagulación (5,88%); ésta fue la única complicación.
A diferencia de otros estudios no se encontraron otras complicaciones del procedimiento, como tampoco de su manejo postoperatorio (Tabla 1).
Conclusiones
El síndrome de compresión iliocava o síndrome de Cockett, es una patología frecuente, altamente incapacitante, en la cual la presentación de los síntomas depende de la existencia de circulación colateral.
De la muestra seleccionada en nuestro trabajo, es decir 84 pacientes que presentaban signos y síntomas de hipertensión venosa, a 61 pacientes se les confirmó síndrome de Cockett, lo que representa alta frecuencia de dicha patología en nuestro grupo poblacional de estudio.
La alta sospecha diagnóstica y el interés por esta patología, han dejado identificar con frecuencia el síndrome de compresión iliocava, así como la estenosis de la vena ilíaca, permitiendo de esta manera la corrección endovascular del síndrome de Cockett, así como en algunos casos la reconstrucción completa de la vena.
Igualmente, se halló gran diversidad en la presentación de los síntomas, desde aquellos leves como hipertensión venosa hasta trombosis venosa profunda.
La flebografía ascendente de miembros inferiores y la iliocavografía, fueron los métodos diagnósticos confirmatorios del síndrome de Cockett en nuestro estudio.
El objetivo terapéutico de la patología fue disminuir la presión venosa, con resolución de los síntomas; se observó que la terapia endovascular es una alternativa de manejo promisoria, con resultados de permeabilidad excelentes a largo plazo y con disminución de la morbilidad.
Nuestro estudio es el primer reporte acerca de esta patología en Colombia.
Creemos que el número de pacientes manejados de esta manera por vía endovascular, es superior al resto de los estudios encontrados sobre esta patología.
Para concluir, podemos afirmar que los resultados que se obtuvieron al realizar el manejo endovascular en los pacientes con síndrome de Cockett, son comparables con otras publicaciones a nivel mundial.
Reconocimientos
A los doctores Javier Leal Monedero y Santiago Zubicoa Ezpeleta, cirujanos vasculares de la Unidad de Cirugía Vascular y Angiología del Hospital Ruber de Madrid España, por habernos iniciado en las técnicas para el diagnóstico y manejo del síndrome de Cockett.
Bibliografía
1. Virchow R. Uber die erweiterung kleinerer gefasse. Arch Anatom Patol 1851; 3: 427. [ Links ]
2. McMurrich JP. The occurrence of congenital adhesions in the common iliac veins, and their relation to thrombosis of the femoral and iliac veins. Am J Med Sci 1908; 135: 342-346. [ Links ]
3. Ehrich WE, Krumbhaar EB. A frequent obstructive anomaly of the mouth of the left common iliac vein. Am Heart J 1943; 26: 737-750. [ Links ]
4. May R, Thurner J. the cause of the predominantly sinistral occurrence of the thrombosis of the pelvic veins. Angiology 1957; 8: 419-427. [ Links ]
5. Cockett FB, Lea Thomas M, Negus D. Iliac vein compression: its relation to iliofemoral thrombosis and the post-thrombotic syndrome. Br Med J 1967; 2: 14-19. [ Links ]
6. Cockett FB, Lea Thomas M. The iliac compression syndrome. Br J Surg 1965; 52: 816-821. [ Links ]
7. Mikley V, Schwagierek R, Rilinger N, Gorich J, Sunder – Plassmann L. Left iliac venous thrombosis caused by venous spur: treatment with thrombectomy and stent implantation. J Vasc Surg 1998; 28: 492-497. [ Links ]
8. Hurst DR, Forauer AR. Bloom JR, Greenfield LJ, Wakefield TW, Williams DM. Diagnosis and endovascular treatment of iliocava compression syndrome. J Vasc Surg 2001; 34: 106-113. [ Links ]
9. Wolpert LM, Rahmani O, Stein B, Gallagher JJ, Drezner AD. Magnetic resonance venography in the diagnosis and management of May-Thurner syndrome. J Vasc Surg 2002; 36: 51-57. [ Links ]
10. Rilinger N, Görich J, Mickley V et al. Endovascular stenting in patients with iliac compression syndrome: experience in three cases. J Vasc Interv Radiol 1997; 8: 484. [ Links ]
11. El FM, Soula P, Rousseau H, Chaiban F, Otal P, Joffre F, et al. Endovascular retrieval of two migrated venous stents by means of balloon catheters. J Vasc Surg 1998; 28: 541- 546. [ Links ]
12. Patel NH, Stookey KR, Ketcham DB, Cragg AH. Endovascular management of acute extensive iliofemoral deep venous thrombosis caused by May-Thurner syndrome. J Vasc Interv Radiol 2000; 11: 1297-1302. [ Links ]
13. Fraser DG, Moody AR, Martel A, Morgan PS. Re-evaluation of iliac compression syndrome using magnetic resonance imaging in patients with acute deep venous thromboses. J Vasc Surg 2004; 40: 604-611. [ Links ]
14. Fraser DG, Moody AR, Morgan PS, Martel A. Iliac compression syndrome and recanalization of femoropopliteal and iliac venous thrombosis: a prospective study with magnetic resonance venography. J Vasc Surg 2004; 40: 612-619. [ Links ]
15. Akers DL Jr, Creado B, Hewitt RL. Iliac vein compression syndrome: case report and review of the literature. J Vasc Surg 1996; 24: 477-481. [ Links ]
16. Edibe Y, et al. Reliability and validity of reverse visual analog scale (right to left) in different intensity of pain. The Pain Clinic 2003; 15 (1):1-6. [ Links ]
17. Chapman CR; Dunbar PJ. Measurement in pain therapy: is pain relief really the endpoint? Current Op Anaesthesiol 1998; 11 (5): 533-537. [ Links ]
18. Vedantham S, Grassi CJ, Ferral H, Patel NH, et al. Reporting standards for endovascular treatment of lower extremity deep vein thrombosis. J Vasc Interv Radiol 2006; 17: 417-434. [ Links ]
19. Kistner RL, Eklof B, Masuda EM. Diagnosis of chronic venous disease of the lower extremities: The CEAP classification. Mayo Foundation for medical education and research 1996; 71 (4): 338-345. [ Links ]
20. Eklof B, Rutherford RB, Bergan JJ, Carpentier PH, Gloviczki P, Kistner RL, et al. for the American Venous Forum International Ad Hoc Committee for Revision of the CEAP Classification. Revision of the CEAP classification for chronic venous disorders: Consensus statement. J Vasc Surg 2004; 40 (6): 1248-1252. [ Links ]
21. Carpentier PH, Cornu-Thenard A, Uhl JF, et al. Societe Francaise de Medecine Vasculaire and the European Working Group on the Clinical Characterization of Venous Disorders. Appraisal of the information content of the C classes of CEAP clinical classification of chronic venous disorders: A multicenter evaluation of 872 patients. J Vasc Surg 2003; 37(4): 827-833. [ Links ]
22. Mazzei ES, Rozman C. Estudio fisiológico del metabolismo del agua. En: Semiotecnia y fisiopatología. Segunda edición. Buenos Aires: Ateneo editorial. p. 764-782. [ Links ]
23. Batlló JS, Batlló AS. Aparato circulatorio. En: Semiología médica y técnica exploratoria. Séptima edición. Barcelona: Masson, S.A. p, 201-339. [ Links ]
24. Espinos D, Díaz-Rubio M. Estados de hipercoagulabilidad. Clín Méd España 1996; 1 (3): 27-51. [ Links ]
25. Calvin BE, Stanley JC. Nonoperative treatment of lower extremity venous thrombosis in venous disease. Current Therapy in Vascular Surgery, Fourth Edition, Michigan: Mosby; 2001. p. 830-834. [ Links ]
26. Bergan JJ, et al. Complex problems involving varicose veins: varicose veins and telangiectasias, diagnosis and treatment. St Louis, Missouri: QMP Edition; 1993. p. 326-369. [ Links ]














