Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colom. Cardiol. vol.18 no.2 Bogota Mar./Apr. 2011
Derrame pericárdico con inminente taponamiento cardiaco secundario a inhibidor de la tirosina quinasa. Reporte de un caso
Pericardial effusion secondary to tyrosine kinase inhibitor with imminence of cardiac tamponade: case report
Trabajo realizado en el Hospital Universitario Fundación Santa Fe de Bogotá, Departamento de Medicina Interna. Bogotá, Colombia.
(1) Hospital Universitario Fundación Santa Fe de Bogotá. Bogotá, Colombia.
(2) Universidad de Los Andes. Bogotá, Colombia.
(3) Universidad El Bosque. Bogotá, Colombia.
Correspondencia: Dr. Andrés Felipe Buitrago Sandoval, Hospital Universitario Fundación Santa Fe, Calle 119 No. 7-75. Bogotá, Colombia. Tel.: (57-1) 6 03 03 03. Ext.: 5492. Correo electrónico: abuitrag@uniandes.edu.co
Recibido: 03/08/2010. Aceptado: 30/11/2010.
La leucemia es una enfermedad maligna que se caracteriza por una proliferación no controlada de una clona iniciada en una etapa precoz de la diferenciación linfoide. Es importante determinar si hay una alteración genética conocida como cromosoma Filadelfia, para pronóstico y tratamiento. El imatinib, un inhibidor de la tirosina kinasa, tiene buena respuesta terapéutica y pocos efectos adversos. Uno de frecuente aparición es la serositis manifestada como derrame pleural, aunque es de menor incidencia asociada con derrame pericárdico. El tratamiento se debe individualizar, pero en caso de inminente taponamiento cardiaco se realiza pericardiocentesis.
PALABRAS CLAVE: imatinib, inhibidores de la tirosina quinasa, derrame pericárdico.
Leukemia is a malignant disease characterized by uncontrolled proliferation of a clone initiated at an early stage of lymphoid differentiation. It is important to determine if there is a genetic disorder known as the Philadelphia chromosome, for both prognosis and treatment. Imatinib, a tyrosine kinase inhibitor has good therapeutic response and few adverse effects. An adverse event is the frequent occurrence of serositis manifested as pleural effusion, but its association with pericardial effusion has a lower incidence. Treatment should be individualized, but in case of imminent cardiac tamponade pericardiocentesis is performed.
KEY WORDS: imatinib, tyrosine kinase inhibitors, pericardial effusion.
Introducción
Las leucemias linfoides agudas predominan en los niños y adultos jóvenes, siendo poco frecuentes en los adultos de mediana edad (1); en este grupo se comporta y manifiesta de manera diferente, es más agresiva y con menor repuesta terapéutica para remisión completa y cura, con tasas de mortalidad cercanas a 38%. A lo anterior se añade que 20% de pacientes con leucemias linfoides agudas, tienen alteraciones genéticas como el cromosoma Filadelfia positivo, lo cual la convierte en una enfermedad más agresiva y de peor pronóstico (2).
Este cromosoma es una alteración genética que se traduce en un desplazamiento recíproco entre los brazos largos de los cromosomas 9 y 22, que permite la formación de un gen de fusión conocido como BCR/ABL, creando la alteración designada como traslocación (9, 22) (q34; q11). Esta transformación génica es la encargada de la producción de una proteína anormal con acción tirosina quinasa, que tiene como función aumentar el crecimiento celular y la angiogénesis, y reducir la respuesta a estímulos inductores de apoptosis, creando finalmente una célula con fenotipo maligno (2-5).
Caso clínico
Paciente de género femenino, de 46 años de edad, con diagnóstico de leucemia linfoide aguda cromosoma Filadelfia positivo, en tratamiento con imatinib 600 mg al día por cuatro años, quien presentó cuadro de disnea de pequeños esfuerzos acompañada de opresión precordial relacionada con los cambios de posición, de una semana de evolución. Al examen físico presentó tensión arterial de 120/70 mm Hg, sin pulso paradójico, frecuencia cardiaca de 90 latidos por minuto y frecuencia respiratoria de 18 respiraciones por minuto. Se observó ingurgitación yugular grado II a 45º y se encontró signo de Kussmaul positivo. A la auscultación se encontraron ruidos cardiacos rítmicos, sin soplos, y ruidos respiratorios con hipoventilación bibasal. No se halló ascitis ni hepatomegalia ni edema en miembros inferiores. Inicialmente se solicitó una radiografía de tórax que mostró infiltrados intersticiales bibasales sin consolidación, y se observó cardiomegalia de las cuatro cavidades. Con estos hallazgos se inició manejo antibiótico y se solicitó ecocardiograma transtorácico (Figura 1), en el que se encontró ventrículo izquierdo con dimensiones normales, función sistólica normal con fracción de eyección de 60%, sin trastornos de la contractilidad segmentaria, dilatación moderada de la aurícula izquierda, insuficiencia mitral y tricúspide leve, derrame pericárdico con cerca de 1.000 mL, con colapso de la aurícula derecha, algunos depósitos de fibrina, y líquido en la pleura (Figuras 2 y 3).


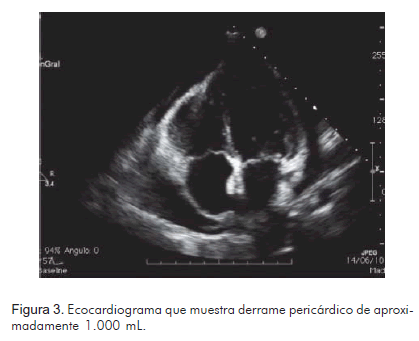
Adicionalmente se solicitó una tomografía de tórax de alta resolución para evaluar los infiltrados que se observaron en la radiografía; este estudio reportó corazón de tamaño normal, líquido pericárdico, no adenomegalias mediastinales, hiliares ni axilares y derrame pleural bilateral de predominio derecho, asociado a opacidades parenquimatosas bibasales por atelectasia o focos neumónicos (Figura 4).

Ante estos hallazgos se hizo pericardiocentesis evacuadora y diagnóstica, por vía subxifoidea y con guía ecográfica, obteniéndose 400 mL de líquido serohemático, y se dejó catéter para drenaje por Hemovac®. Se envió líquido para citológico, histoquímico y cultivo. En éste se encontraron 644 leucocitos, 99% de neutrófilos y 34.400 eritrocitos, de los cuales 60% eran frescos y 40% crenados. Relación LDH líquido/LDH sérica de 2,18, relación proteínas líquido/proteínas séricas de 0,82 y proteínas totales de 5,1 g/dL. Según estos hallazgos el líquido pericárdico es de características de exudado. Posterior al procedimiento la paciente mejoró su sintomatología. Se realizó radiografía de tórax de control en la que no se evidenció neumopericardio, y ecocardiograma transtorácico de control que mostró derrame pericárdico de aproximadamente 180 mL sin repercusión hemodinámica. Su condición actual es estable, no ha presentado recurrencia de la serositis y tiene un adecuado control de su enfermedad de base (Figuras 5 y 6).

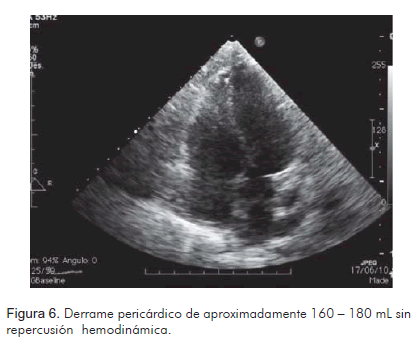
Discusión
El imatinib es uno de los primeros medicamentos antineoplásicos desarrollados para un blanco molecular específico, que funciona como inhibidor de la transducción de señales. Su principio activo es el mesilato de imatinib, que actúa bloqueando el sitio de unión a ATP en la proteína kinasa ABL, inhibiendo su capacidad para transferir un grupo fosfato desde el ATP y así fosforilar residuos de tirosina en proteínas sustrato, lo que impide la transducción de señales necesarias para inducir proliferación celular y apoptosis (6). Paralelamente, funciona como un inhibidor del factor estimulante de colonias del receptor tipo 1 (CSF- 1R), el factor de crecimiento derivado de las plaquetas de los receptores alfa y beta (PDGFR a y b) tirosin quinasas y c-Kit (receptor del factor de células madre) (7). Prácticamente todos los pacientes tratados con imatinib tienen al menos un evento adverso de cualquier grado; los que se describen, por lo general son leves y se documentan en fases avanzadas de la enfermedad. Los más frecuentes incluyen edema periorbitario con lagrimeo constante, diarrea, náuseas, erupción cutánea, reacciones cutáneas que comprometen manos y pies, fatiga, disnea, estomatitis y mucositis (7). Los hallazgos anormales de laboratorio más frecuentes son: anemia, granulocitopenia, hipofosfatemia y elevación de las enzimas hepáticas (7, 8). La toxicidad cardiaca es menos común, más grave y difícil de diagnosticar en las primeras etapas (9). Entre los efectos adversos cardiacos están: prolongación del intervalo QT, reducción asintomática de la fracción de eyección ventricular izquierda, clínica de insuficiencia cardíaca congestiva, síndromes coronarios agudos e infarto agudo del miocardio. Con el tratamiento con estos agentes también se han asociado la hipertensión y la muerte súbita (9). Kerkela y colaboradores realizaron un estudio en el que evaluaron la fracción de eyección del ventrículo izquierdo antes de iniciar tratamiento con imatinib y después de que desarrollaron síntomas de insuficiencia cardíaca. La fracción de eyección del ventrículo izquierdo había caído en 25% ± 8% con respecto a su valor pre-tratamiento. Los autores realizaron biopsias de miocardio en dos de cada diez pacientes que desarrollaron insuficiencia cardiaca congestiva y éstas mostraron espirales prominentes de la membrana en los miocitos, anormalidades en las mitocondrias con crestas borradas, gotas lipídicas dispersas y de vacuolas citosólicas, con acumulación de glucógeno y muerte celular por necrosis; estos hallazgos son característicos de miopatías inducidas por toxinas y de muerte celular por reducción de ATP. Concluyeron que el imatinib es cardiotóxico y puede conducir a una disfunción grave del ventrículo izquierdo y a un fracaso de la bomba cardiaca (10).
El derrame pericárdico y pleural por imatinib es una complicación rara, poco reportada, con baja incidencia, y se relaciona con la inhibición del factor de crecimiento derivado de plaquetas beta (PDGFR - b), que se encuentra distribuido ampliamente en muchos órganos, estando presente en fibroblastos, células del músculo liso y pericitos. Entre sus funciones está la regulación del proceso de angiogénesis a nivel tisular, y desempeña un papel importante de soporte en la fisiología de los fluidos, regulando la presión hidrostática en el espacio intersticial (11, 12).
Con base en lo anterior, se han desarrollado múltiples estudios de biología molecular en los cuales se ha concluido que el déficit del PDGFR-b genera un estado de anasarca, de diferentes magnitudes, secundario a la deficitaria producción de capilares que sean efectivos y eficientes para mantener un volumen circulante efectivo adecuado para los requerimientos metabólicos; a pesar de este déficit en la producción del factor en cuestión, la literatura refiere que con el uso de mesilato de imatinib, al no ser un inhibidor potente, no debería ser frecuente la incidencia de edema y de serositis. Como el enunciado anterior no se correlaciona con los hallazgos en la práctica clínica, se asume una etiología multifactorial para dichos efectos secundarios (11). Los inhibidores de la tironsina kinasa de segunda generación, como el dasatinib, tienen la mayor incidencia de derrame pleural y pericárdico; oscila entre 7% y 35%, comparado con imatinib y nilotinib con una incidencia de menos de 1% dada por la diferencia de inhibición del PDGFR-b (13, 14).
Entre los factores de riesgo para el desarrollo de derrames se encuentran: antecedente de enfermedad cardíaca, hipertensión, régimen de dosificación dos veces al día, historia previa de erupción de la piel mientras se estén tomando inhibidores de la tirosina kinasa, historia de enfermedad autoinmune e hipercolesterolemia (15). En casos reportados en la literatura, se ha identificado una posible cadena de eventos que culmina con la aparición del derrame pericárdico: inicialmente el paciente es asintomático, comienza la retención de líquidos sin alteraciones en el examen físico; posteriormente, el primer cambio objetivo de retención de líquidos es el aumento de peso. A medida que el tiempo transcurre, sin cambios de conducta por el aumento de peso, se da paso a la sintomatología, la cual se manifiesta con edema de miembros inferiores, aumento importante de peso, disnea progresiva (derrame pleural) y finalmente, de no ser tratado a tiempo, fallecimiento a causa de taponamiento cardiaco (derrame pericárdico no tratado) (16).
El tratamiento de la serositis debe individualizarse con base en la sintomatología y la severidad del cuadro, con soporte imaginológico, y de ser necesario dinámico. En caso de enfrentarse a un paciente asintomático, sólo se debe hacer seguimiento clínico e imaginológico, para que cuando refiera el primer síntoma, se le suspenda el medicamento y se le valore la regresión de las serositis (tiempo estimado de cuatro semanas). En casos más avanzados puede ser útil el tratamiento con ciclos cortos de corticoides, reportado como tratamiento efectivo, con tiempo de resolución de hallazgos imaginológicos en 72 horas. Finalmente, si todas las medidas empleadas fueron inefectivas, se procede a realizar estudio citoquímico con toracentesis o pericardiocentesis a fin de descartar compromiso neoplásico que se manifieste con la serositis (11, 17).
Conclusión
Los principales efectos adversos asociados al uso del imatinib son por lo general leves y se presentan en estadios avanzados de la enfermedad. Entre éstos inicialmente pueden destacarse los hematológicos, con una incidencia reportada no mayor de 40%, dosis dependiente; también se pueden ver afectados otros órganos, como la piel, el tracto gastrointestinal y el sistema cardio-respiratorio. La toxicidad cardiaca es menos común, es más grave y difícil de diagnosticar en las primeras etapas (9). El derrame pericárdico y pleural por imatinib es una complicación rara, poco reportada, con baja incidencia, secundaria a la inhibición PDGFR - b, por la relación de este último con la homeostasis hídrica tisular (18). En un reciente estudio, se demostró que sólo 1,7% de 1.276 pacientes tenían síntomas atribuibles a falla cardiaca sistólica pero no se reportó la asociación de esta sintomatología con evidencia objetiva de serositis pericárdica (17). Por ello, se debe vigilar a los pacientes con factores de riesgo para presentar este tipo de complicaciones con el uso del medicamento. Una vez se ocurre el efecto adverso, se individualiza el tratamiento. Finalmente, hacen falta estudios clínicos para determinar cual conducta terapéutica genera menor morbilidad y mortalidad para el paciente.
Bibliografía
1. Cuéllar F. Leucemias agudas del niño y del adulto. Fundamentos de Medicina Interna. Hematología. 6ª. Edición. Medellín: Corporación para Investigaciones Biológicas; 2004. p. 123-126. [ Links ]
2. Rodríguez M, Cardona AF, Enciso L, et al. Leucemia mieloide crónica en crisis blástica: bases moleculares y diagnóstico (parte I). Rev Colom Carcerol 2006;10 (4): 257-266. [ Links ]
3. Arora A, Eric M Scholar. Role of tyrosine kinase inhibitors in cancer therapy. J Pharmacol Exper Therap 2005; 315 (3): 971-979. [ Links ]
4. Ravandi F, Kebriaei P. Philadelphia -positive acute lymphoblastic leukemia. Hematol Oncol Clin North Am 2009; 23: 1043-1063. [ Links ]
5. Gómez MA, Morel IA, Ramírez LD, Gómez DS. Efectos adversos del mesilato de imatinib en el tratamiento de la leucemia mieloide crónica. Rev Pos Cátedra Med 2007; 174: 16-19. [ Links ]
6. Carpiuc KT, Stephens JM, Botteman MF, Feng W, Hay JW. A review of the clinical and economic outcomes of imatinib in Philadelphia chromosome-positive acute lymphoblastic leukemia. Expert Opin Pharmacother 2007; 8: 2775-87. [ Links ]
7. Joensuu H, Trent JC, Reichardt P. Practical management of tyrosine kinase inhibitor-associated side effects in GIST. Cancer Treat Rev 2011; 37 (1): 75-88. [ Links ]
8. Blanke CD, Rankin C, Demetri GD, et al. Phase III randomized, intergroup trial assessing imatinib mesylate at two dose levels in patients with unresectable or metastatic gastrointestinal stromal tumors expressing the kit receptor tyrosine kinase: S0033. J Clin Oncol 2008; 26: 626-32. [ Links ]
9. Orphanos GS, Ioannidis GN, Ardavanis AG. Cardiotoxicity induced by tyrosine kinase inhibitors. Acta Oncol 2009; 48 (7): 964-70. [ Links ]
10. Kerkela R, Grazette L, Yacobi R, Iliescu C, Patten R, Beahm C, et al. Cardiotoxicity of the cancer therapeutic agent imatinib mesylate. Nat Med 2006; 12: 908-16. [ Links ]
11. Kelly K, Swords R, Mahalingam D, Padmanabhan S, Giles FJ. Serosal inflammation (pleural and pericardial effusions) related to tyrosine kinase inhibitors. Target Oncol 2009; 4 (2): 99-105. [ Links ]
12. Motzer RJ, Hutson TE, Tomczak P, Michaelson MD, Bukowski RM, Rixe O, et al. Sunitinib versus interferon alfa in metastatic renal-cell carcinoma. N Engl J Med 2007; 356: 115-24. [ Links ]
13. van der Geer P, Hunter T, Lindberg RA. Receptor proteintyrosine kinases and their signal transduction pathways. Annu Rev Cell Biol 1994; 10: 251. [ Links ]
14. Talpaz M, Shah N, Kantarjian H, Donato N, Nicoll J, Paquette R, et al. Dasatinib in imatinib-resistant Philadelphia chromosome-positive leukemias. N Engl J Med 2006; 354: 2531-41. [ Links ]
15. Quintas-Cardama A, et al.Pleural effusion in patients with chronic myelogenous leukemia treated with dasatinib after imatinib failure. J Clin Oncol 2007; 25 (25): 3908-3914. [ Links ]
16. Pieters R, Carroll WL. Biology and treatment of acute lymphoblastic leukemia. Hematol Oncol Clin North Am 2010; 24: 1-18. [ Links ]
17. Ribeiro Marcolino MS, Bittencourt HNS, Barbosa MM, Nunes MCP, Xavier VF, Clementino NCD. An evaluation of the cardiotoxicity of imatinib mesylate, Leukemia Research 2008; 32: 1809-1814. [ Links ]
18. Atallah E, Durand JB, Kantarijan H, Cortes J. Congestive heart failure is a rare event in patient receiving imatinib therapy. Blood 2007; 110 (4). [ Links ]














