Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.29 no.2 Bogotá Apr./June 2014
Rendimiento diagnóstico y hallazgos con la cápsula endoscópica en pacientes con sangrado digestivo de origen oscuro en la Clínica Universitaria San Juan de Dios en Cartagena, Colombia
Fernando García del Risco MD. (1), Elizabeth Arrieta López MD. (2)
(1) Médico Gastroenterólogo Clínico, Profesor Asociado de la Facultad de Medicina, Universidad de Cartagena. Jefe servicio de Gastroenterología, Clínica Universitaria San Juan de Dios. Cartagena, Colombia.
(2) Médico residente de Medicina Interna, II año, Universidad del Sinú, Seccional Cartagena. Maestrante en Epidemiología Clínica, Universidad Nacional de Colombia. Clínica Universitaria San Juan de Dios. Cartagena, Colombia.
Fecha recibido: 25-11-13 Fecha aceptado: 08-05-14
Resumen
Introducción: La cápsula endoscópica (CE) es, actualmente, el estudio de primera elección en la exploración del sangrado digestivo oscuro (SDO), después de una esofagogastroduodenoscopia (EGD) y una ileocolonoscopia negativas. Objetivo: Evaluar el rendimiento diagnóstico y los hallazgos en el intestino delgado en 50 pacientes con sangrado digestivo de origen obscuro en nuestra institución.
Materiales y métodos: Estudio observacional descriptivo retrospectivo, en una cohorte de pacientes que consultaron por SDO a la Clínica Universitaria San Juan de Dios en la ciudad de Cartagena, del 1 enero del 2010 al 31 abril del 2013. El rendimiento diagnóstico de la CE fue definido por la presencia de lesiones altamente significativas (P2), poco significativas (P1) y normales (P0). Para el análisis de los resultados se utilizó el software STATA 11.0.
Resultados: Se incluyeron 50 pacientes con SDO. De estos, 34 casos con SDO evidente (68%) y 16 con SDO oculto (32%). El 62% (31) de sexo femenino, con una edad promedio de 60,14 años, DE±20,02 (20 a 87 años). La CE se realizó de manera ambulatoria en 26 casos (52%) e intrahospitalaria en 24 casos (48%). El rendimiento diagnóstico de la CE en el SDO (lesiones P2) fue de 58% (29/50). En SDO evidente 61,74%(21/34) y en SDO oculto 50% (8/16). La preparación fue adecuada en el 92% de los casos. La exploración completa del intestino delgado se logró en el 96%. Hubo una retención de la cápsula en dos pacientes. Las lesiones P2 encontradas en el intestino delgado fueron vasculares en 51,9%, tumorales en 20,6%, parasitarias en 13,7%, en lesiones ulcerosas e inflamatorias 6,9% y en divertículos 6,9%. Las lesiones P2 responsable del SDO por fuera del intestino delgado, al alcance de una EGD y colonoscopia, se encontraron en el 24,13%(7/29), una en el esófago, 2 en el estómago, una en el duodeno y 3 en el colon derecho.
Conclusión: La rentabilidad diagnóstica de la CE en nuestra serie fue del 58%. Las lesiones vasculares (angiodisplasias) fueron la primera causa de sangrado, hallazgo que es comparable con otras publicaciones a nivel nacional e internacional. Llama la atención, en nuestro estudio, como segunda causa los tumores y la infestación parasitaria en la población estudiada.
Palabras claves
Cápsula endoscópica, melena, hematoquecia, anemia, sangrado gastrointestinal oscuro.
INTRODUCCIÓN
La invención de la cápsula endoscópica (CE) en el 2001, revolucionó el estudio del intestino delgado (1). Este método no invasivo, permite la exploración de todo el intestino delgado en la mayoría de los pacientes, y la obtención de imágenes de alta resolución, por lo que es considerado, a la fecha, como el estudio de primera elección en pacientes con sangrado digestivo oscuro (SDO), después de una evaluación inicial negativa con endoscopia bidireccional (endoscopia digestiva alta y una ileocolonoscopia) y/o radiológica del intestino delgado (2). La CE tiene un rendimiento diagnóstico en la exploración del intestino delgado significativamente superior, con una sensibilidad del 89% y una especificidad del 95%, cuando se compara con métodos diagnósticos radiológicos y endoscópicos como la enteroscopia de empuje, la enteroscopia de doble balón (EDB) (3); esta última con una tasa de detección similar a la CE, pero con la desventaja que la EDB es un procedimiento endoscópico invasivo que requiere de mucho tiempo, del uso de anestesia general, no está exento de complicaciones y la exploración de todo el intestino delgado puede ser técnicamente difícil (4).
La CE es un procedimiento muy bien tolerado, mínimamente invasivo y fácil de realizar. La tasa de detección de lesiones potencialmente sangrantes, en pacientes con SDO, puede variar entre el 40% y el 80% (5). Las lesiones hemorrágicas significativas encontradas con CE, en pacientes con SDO, incluyen principalmente las lesiones vasculares (angiodisplasias), tumores, úlceras, divertículos y parásitos (5). La causa del SDO se encuentra al alcance de una endoscopia superior e inferior hasta en el 25% de los casos estudiados, por lo que se aconseja un second look, es decir, repetir la esofagogastroduodenoscopia (EGD) y/o la colonoscopia antes del estudio con CE (6).
Hasta la fecha, en la Costa Atlántica colombiana, no hay estudios publicados que permitan conocer las principales causas del SDO, lo cual nos motivó para la realización de este estudio.
Definiciones
- El SDO fue definido como la presencia de melena y/o hematoquecia persistentes o anemia con prueba de sangre oculta positiva, después de la EGD y colonoscopia negativas (8,9).
- SDO evidente: el SDO que se manifiesta con melena y/o o hematoquecia (9).
- SDO oculto: el SDO que se manifiesta con anemia por deficiencia de hierro o sangre oculta en heces persistentemente positiva (9).
- La anemia es definida como una concentración de hemoglobina <13 g/dL en hombres y <12 g/dL en mujeres, de más de 3 meses de evolución, sin sangrado proctológico o ginecológico obvio.
Preparación
- Adecuada: presencia de líquidos y residuos escasos, con poca interferencia en la visualización de la mucosa intestinal.
- Inadecuada: presencia de líquidos y residuos abundantes, con gran interferencia en la visualización de la mucosa intestinal.
Lesiones encontradas con la CE
Las lesiones encontradas con la CE se clasificaron, para el diagnóstico definitivo del paciente, según el grado de relevancia en:
- (P0): ausencia de lesiones (normal).
- (P1): lesiones poco significativas (erosiones, xantomas, hiperplasia nodular linfoide).
- (P2): lesiones altamente significativas (angiodisplasias, tumores, úlceras, parásitos tipo uncinarias, divertículos).
Rendimiento diagnóstico
Se definió el rendimiento diagnóstico con la identificación de lesiones P2 responsables del SDO.
Localización de las lesiones en el intestino delgado
La localización de las lesiones en los distintos segmentos del intestino delgado se logró con el software del dispositivo, que permite ubicar la CE de acuerdo a la posición de esta en un gráfico que aparece en el monitor. El duodeno se encuentra justo después de que la CE pasa el píloro y se mueve a lo largo de un asa de derecha a izquierda del dispositivo de localización en la parte superior. El yeyuno se localiza cuando la CE se encuentra en el lado izquierdo del dispositivo de localización o en el tercio proximal del tránsito intestinal dibujado en la pantalla. El íleon se localiza cuando la CE está en el lado derecho del dispositivo de localización o en el tercio distal del intestino delgado. La cápsula situada en el centro del abdomen o en el tercio medio del intestino delgado fue clasificada como lesión yeyunoileal.
MATERIALES Y MÉTODOS
Diseño del estudio
Estudio observacional descriptivo retrospectivo, de corte transversal, con CE del intestino delgado, en una cohorte de pacientes que consultaron a la Clínica Universitaria San Juan de Dios por SDO en la ciudad de Cartagena, del 1 Enero del 2010 al 31 abril del 2013. Se incluyeron pacientes adultos con SDO evidente u oculto, a quienes se les ordenó exploración del intestino delgado luego de una EGD y colonoscopias negativas. Se revisaron las historias, el estudio con CE y la evolución de los pacientes, luego del procedimiento.
Preparación y análisis del estudio
Todos los pacientes incluidos en el estudio se prepararon de acuerdo al protocolo establecido en nuestra institución, el cual consiste en una dieta líquida y la ingesta de 2 litros de PEG la noche anterior al estudio. El día del procedimiento a cada paciente le colocaron 8 sensores en la pared abdominal, conectados a una grabadora de datos, ubicada en un cinturón portado por el paciente durante todo el tiempo. Luego de la sincronización de la cápsula con la grabadora de datos, cada paciente ingirió la CE (PillCam© Given Imaging, Israel) en medio vaso de agua. El registrador de datos fue conectado a un computador y las imágenes fueron descargadas y procesadas en la estación de trabajo. El video resultante de las 58 000 imágenes fue estudiado de manera exhaustiva por un gastroenterólogo entrenado. La duración del estudio fue de 8 horas. La información obtenida fue registrada en una base de datos de Excel (Microsoft Office 2010).
Análisis estadístico
Se realizó un análisis estadístico descriptivo para cada variable, calculando media, con desviaciones estándar (±DE), para variables continuas y mediana, con rango intercuartílico (RIC), para variables de distribución no normal. La distribución de probabilidad de cada variable se midió mediante la prueba de Shapiro-Wilk. Las variables categóricas se agruparon en frecuencias absolutas y relativas, y medidas en porcentajes para su descripción. Las diferencias estadísticamente significativas se evaluaron a través de pruebas de hipótesis: las variables cuantitativas se estimaron mediante la prueba de la t de Student; y las diferencias correspondientes a las variables cualitativas se estimaron mediante la prueba de Chi cuadrado o la prueba de significancia exacta de Fisher, cuando la primera no resultase aplicable. En todos los contrastes de hipótesis se rechazará la hipótesis nula con un error de tipo I (valor de p) menor a 0,05. Los análisis se realizaron usando el software STATA 11.0. (Statistical Software: Release 11. College Station, TX: Stata Corp LP).
Aspectos éticos
El protocolo del estudio fue aprobado por el Comité de ética de la Clínica Universitaria San Juan de Dios. Se garantizó la confidencialidad de la información. En la historia clínica reposaba el consentimiento de autorización del estudio con CE firmado por todos los pacientes. La recolección de la información, en forma retrospectiva, de los registros de la historia clínica es considerada una investigación "sin riesgo", de acuerdo a la resolución 8430 de 1993, del Ministerio de Salud de Colombia.
RESULTADOS
Del 1 de enero del 2010 al 31 abril del 2013, se realizaron 59 estudios con CE en la Clínica Universitaria San Juan de Dios, en la ciudad de Cartagena, de los cuales se excluyeron 9 casos, pues el estudio se realizó por una indicación diferente al sangrado digestivo de origen oscuro (3 por dolor abdominal recurrente, 3 por diarrea crónica, 2 por control de enfermedad de Crohn, y uno por control de un linfoma de la cuarta porción del duodeno postratamiento). Se analizaron 50 pacientes, de los cuales el 55% (34 casos) tenían SDO evidente y 45% (16 casos) SDO oculto (figura 1). El 62% (31 pacientes) fueron de sexo femenino, con una edad promedio de 60,14 años (DE± 20,02). Los procedimientos se realizaron de forma ambulatoria en el 52% de los casos. La prevalencia global de anemia en la población estudiada fue de 35,19 %, con un valor promedio de hemoglobina de 8,5 g/dL (DE±2.4), con un valor mínimo de 2,8 g/dL y máximo de 10,8 g/dL (tabla 1). La hemoglobina promedio previa a la realización de la CE, fue de 7,0 g/dL (DE± 2) para SDO evidente y de 8,7 g/dL (5,0-12,6 g/dL) para SDO oculto (tabla 1). No se encontraron diferencias estadísticamente significativas en las características basales entre los pacientes con SDO visible y oculto. El principal motivo de consulta fue la melena 60%, seguido por la anemia en el 32% de los casos (figura 2). Todos los pacientes tenían estudios endoscópicos previos, la mayoría una sola EGD y colonoscopia (92% [n=46] y 96% [n=48], respectivamente), sin embargo al 7,41% (n=4) se le habían realizado 3 EGD y el 3,7% de los pacientes tenían 2 colonoscopias o más con un máximo de 4 colonoscopias.
Hospitalizaciones y estudios previos al estudio con CE
Cuatro pacientes habían sido hospitalizados antes del estudio con CE. Tres pacientes en una ocasión, y una paciente con tres hospitalizaciones previas al estudio.
A 12 pacientes les practicaron otros estudios para determinar la causa del SDO: tomografía axial computarizada (TAC) abdominal a 5, tránsito intestinal a 5, gammagrafía y angiografía a 1 paciente, respectivamente.
Tránsito de la CE e incidentes
La tolerancia a la preparación fue excelente. Ningún paciente refirió queja alguna durante la ingestión de la CE. El tránsito de la CE en esófago fue de 1,86 min (DE± 5.41), en estómago de 47,03 min (DE± 66,91), en intestino delgado de 3,29 horas (DE±1,46). El tiempo total de tránsito de la cápsula, desde la boca hasta la el colon, fue de 4,42 horas (DE±2,95) (tabla 2). En 2 pacientes (3,7%) no se pudo hacer la exploración completa del intestino delgado, en un caso por retención de la CE en el íleon, con obstrucción parcial intestinal, que requirió hospitalización y tratamiento médico con corticoides intravenosos (IV) por 3 días, con la expulsión de la cápsula el día 11; y otro por un tumor ileal con retención de la CE y expulsión espontánea el día 4 (tabla 3).
Hallazgos con CE
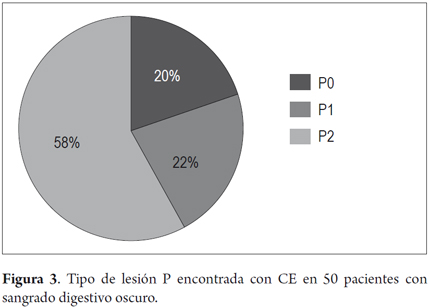
Se encontraron lesiones P2 responsables del SDO en 29 (58%) de los 50 pacientes estudiados (figura 3); en el 61,7% (n=21) de los pacientes con SDO evidente y en el 50% (n=8) con SDO oculto. De los pacientes restantes, el 20% (n=10) tuvieron un estudio con CE normal (P0), y 22% (n=11) tuvieron lesiones no significativas P1 (tabla 4). Las lesiones P2, responsables del SDO, más frecuentes en el intestino delgado fueron vasculares 51,9%, tumorales 20,6% y parasitarias 13,7%, (figura 4), siendo las lesiones vasculares la principal causa tanto en los pacientes con sangrado digestivo oscuro oculto, como evidente; sin embargo, la causa tumoral es la segunda en frecuencia en los pacientes con SDO visible, mientras que en los pacientes con SDO oscuro, los parásitos, las lesiones ulcerosas e inflamatorias y los divertículos, comparten la misma prevalencia en la población estudiada (12,5% cada una) (tabla 5). La CE permitió el diagnóstico de 7 tumores: dos linfomas ileales, un hemangioma cavernoso yeyunal, una linfangiomatosis ileal, un tumor carcinoides, una poliposis de intestino delgado y un tumor metastásico de ovario a íleon (figura 5). En 5 pacientes se diagnosticó uncinariasis en duodeno y yeyuno (figura 6).
Localización anatómica de las lesiones P2
En los 29 pacientes con lesiones P2, causantes del SDO, la localización anatómica de las lesiones fue: en el intestino delgado en el 75,8% de los casos (n=22), 9 en yeyuno (42,8%) y 12 en el íleon (57,14%). El 24,2% (n=7) de los pacientes con lesiones P2 estaban al alcance de una EGD y colonoscopia (figura 7), una angiodisplasia en esófago, 2 angiodisplasias en estómago, 1 angiodisplasia en duodeno y 3 angiodisplasias en el colon derecho (figura 8); sin embargo, los estudios endoscópicos realizados previamente fueron reportados como normales. La CE fue normal en 8 pacientes (33,46%).
Lesiones P2 y rentabilidad diagnóstica de la CE
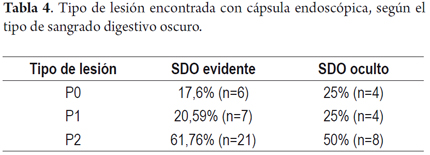
En los pacientes con SDO evidente se encontraron lesiones P0 en el 17,65%, P1 en el 20,59% y P2 en el 61,76% de los casos. En el grupo de SDO oculto se encontraron lesiones P0 en el 25%, P1 en el 25% y P2 en el 50% de los casos (tabla 5). No hubo diferencias estadísticamente significativas en cuanto a la rentabilidad diagnóstica de la CE entre los dos grupos, ni en el análisis global (p: 0,574), ni en la estratificación según el grado de la lesión (p: 0,723).
TRATAMIENTO
En los 50 pacientes estudiados, el tratamiento fue médico en 44 (hierro oral o intravenoso, tratamiento antiparasitario, tratamiento de enfermedad de Crohn), quirúrgico en 4, con resección del segmento del intestino afectado (un linfoma ileal, un hamartoma cavernoso yeyunal, una linfangiomatosis ileal y un tumor carcinoide) (tabla 5); y endoscópico en 2 pacientes (enteroscopia más dilatación con balón de una estenosis ileal en una enfermedad de Crohn estenosante y fulguración de una angiodisplasia duodenal con plasma de argón en el otro paciente) (ver tabla 3).
EVOLUCIÓN
Se logró el seguimiento, por vía telefónica, o control, por consulta externa, de 45 de los 50 pacientes estudiados con CE, desde los 3 meses, hasta 3 años y 3 meses. Cinco pacientes fallecieron durante el seguimiento: 4 por causas diferentes al SDO y un paciente por un linfoma ileal. De los 4 pacientes tratados quirúrgicamente: un linfoma ileal recibió tratamiento con quimioterapia y a los dos años de seguimiento, la paciente no ha resangrado. El linfoma cavernoso yeyunal, el tumor carcinoides y la linfangiomatosis ileal están asintomáticos a un año de seguimiento médico (tabla 6). Los 34 pacientes con tratamiento médico, con lesiones P0 y P1, ninguno ha resangrado, con seguimientos de 3 meses a tres años.
DISCUSIÓN
El SDO es responsable del 5% de todos los casos de hemorragia de las vías digestiva; las causas de esta alteración incluyen una larga y variada lista, siendo las más frecuentes las lesiones vasculares, inflamatorias, tumorales y parasitarias. La CE, desde su invención hace 12 años, se ha convertido en parte integral en la evaluación diagnóstica del SDO (7).
Este estudio realizado en nuestro centro con 50 pacientes, con SDO, nos permitió conocer la rentabilidad diagnóstica, etiología y desenlace de cada uno de ellos. La indicación más frecuente para el estudio con CE fue el SDO (84,7%). El rendimiento diagnóstico fue del 58%, muy similar al encontrado a nivel nacional por Juliao y colaboradores (57%) (8), y Benavente en Perú (58,5%) (9). Un metanálisis publicado por Triester mostró un rendimiento diagnóstico para la CE del 61% a 63% (10). Una revisión sistemática de Liao y su equipo de trabajo, de 227 artículos publicados, encontró un rendimiento diagnóstico de 60,5% (5). Mientras que en Tailandia, el estudio de Pongprasobchai, en 103 pacientes con SDO, encontró un rendimiento diagnóstico para la CE de apenas del 36%, atribuido a la poca prevalencia de las lesiones vasculares (angiodisplasia) en los países asiáticos (11).
El motivo de consulta más frecuente de nuestros pacientes fue la melena (53,7%), en segundo lugar la anemia (35,19%) y la hematoquecia en el 12,96%, en concordancia con otros estudios (2). Los pacientes con melenas tuvieron más hallazgos anormales en la CE (p: 0,038). Este hallazgo no fue estadísticamente significativo.
Las características demográficas de nuestra población fueron similares a las encontradas en otras series (8-11). La edad promedio fue de 60 años, con un predominio del sexo femenino en ambos grupos (SDO evidente y SDO oculto). La edad promedio de los pacientes con hallazgos significativos (P2) con SDO evidente (57,5 años) fue menor cuando se comparó con el grupo de SDO oculto (62,6 años), esta diferencia etaria no fue estadísticamente significativa (p: 0,059).
La principal causa de lesiones P2 responsables del SDO en nuestro estudio fueron las vasculares (51,9%), muy similares a las encontradas por Juliao y colaboradores (47,1%) (8), Galeano y su equipo (62,5%) (12) y estudios internacionales (51% al 79%) (2,10). Es de anotar que uno de los dos primeros casos de SDO por lesiones vasculares (angiodisplasias) publicados en nuestro país, realizado por la Dra. Galeano, correspondió a una paciente remitida de nuestra institución en Cartagena (13). Estudios en Tailandia revelaron una baja prevalencia de lesiones vasculares: 27% en Indonesia (11), 31% en la India (14) y 23% y 24% en un estudio en Japón con EDB (15). Esos trabajos mostraron que las úlceras de intestino delgado eran la principal causa de SDO (41%-53%) por encima de las lesiones vasculares (23%-24%), a diferencia de lo encontrado en países occidentales. Las úlceras del intestino delgado son la causa más frecuente de SDO en los países asiáticos (11).
La segunda causa de lesiones P2 responsables del SDO, en nuestro estudio, fueron los tumores (20,6%). Con una localización anatómica predominante en el íleon (5/7) y en mujeres (4/7). Llama la atención la alta frecuencia de tumores, cuando se comparan nuestros hallazgos con otros estudios a nivel nacional como el de Juliao y Galeano y su equipo de trabajo, quienes encontraron tumores solo en el 8,9% y 15,4% de los casos (8,12). En el estudio coreano, de Cheung, de 1332 casos con CE en 14 centros, se encontraron solo 57 tumores en intestino delgado (4,3%), 30 tumores malignos (57%), 3 adenocarcinomas, 20 tumores estromales, 8 linfomas y dos tumores metastásicos (16).
Nosotros encontramos 4 tumores malignos (57%): 2 linfomas, 1 tumor estromal, y 1 tumor metastásico de ovario a íleon y tumores benignos infrecuentes (un hemangioma cavernoso de yeyuno y una linfangiomatosis ileal). Los tumores que más metástasis hacen en el intestino delgado son los de: melanoma, riñón, pulmón, testículo, estómago, ovario, hígado y útero (16-19). La alta frecuencia de tumores en nuestro estudio requiere confirmación con un seguimiento más estricto y con un mayor número de casos.
La tercera causa fue las parasitosis (13,7%). En 5 pacientes, el diagnóstico fue de uncinariasis en duodeno y yeyuno, muy parecido al encontrado en el estudio de Galeano y colaboradores (10,9%). Contrasta con el estudio de Juliao y su equipo de trabajo (8), quienes; en su estudio, no encontraron ningún caso de parasitosis. Estudios en la India, con condiciones socioeconómicas muy parecidas a la nuestra, en 53 pacientes, con SDO estudiados con CE y EDB, encontraron como causa infecciosa al 12% de los casos: 6% uncinariasis y 6% tuberculosis intestinal (20). La uncinariasis puede ser una causa de SDO evidente, como ha sido reportado por Chen y colaboradores (21). La alta frecuencia de uncinariasis en nuestro estudio se puede explicar por la procedencia del área rural en 4 de los 5 de pacientes, donde las condiciones sanitarias son precarias.
La localización anatómica de las lesiones sangrantes significativa (P2), en 9 de los 34 pacientes (24,2%), se encontró en el estómago, duodeno proximal y colon, lo que pudo evitar la realización de la CE. El estudio francés de Lepileur y colaboradores, con 911 pacientes, encontró una prevalencia de lesiones con CE, al alcance de endoscopia alta y colonoscopia, en el 12,6% (22); el estudio canadiense de Shahidi y su equipo de investigadores en el 17,8% (23) y Bar Meir y sus colegas, en una serie de 20 pacientes con SDO oculto, una segunda CE mostró lesiones en el 35% (7/20) de los pacientes, por lo que se recomienda un second look antes de la CE (24). Para evitar la no visualización de lesiones al alcance de una EGD y colonoscopia, es importante que el endoscopista esté familiarizado con lesiones que pueden pasar desapercibidas (Dieulafoy, angiectasias, uncinarias, lesiones sangrantes inusuales o raras), tener presente que algunas lesiones sangran en forma lenta e intermitente y que la presencia de sangre, la anemia, la deshidratación, el uso de sedantes y una mala preparación del colon llevan a una pobre visualización de la mucosa (25).
La preparación en nuestro estudio fue adecuada en el 92%. En el estudio de Juliao y colaboradores (8) fue del 83%, y en otras series la preparación adecuada varía de un estudio a otro, del 69% al 95% (26,27). No hay una preparación única estandarizada; sin embargo, la dieta previa al estudio es importante. Nosotros ordenamos una dieta líquida 24 horas antes del estudio y el uso de 2 litros de PEG. Este esquema de preparación fue de mucha utilidad en nuestra serie. No se usaron procinéticos y se recomendó la movilización del paciente durante el estudio, mientras fuera posible. La exploración del intestino delgado fue satisfactoria en el 96%.
El tiempo de tránsito de la CE, desde la boca hasta el colon, fue de 4,42 horas (DE±2,95) (282 minutos), muy similar al estudio de Westerhof y colaboradores, en 691 pacientes, en donde se registró un tiempo de tránsito de la CE, desde la boca hasta el colon, de 246 minutos,(90-342) (28).
La retención de la CE ocurrió en dos pacientes (4%), uno con enfermedad de Crohn y otro con un linfoma ileal. Este porcentaje de retención de la CE está acorde con lo descrito en grandes series, que demuestran que los pacientes con enfermedad de Crohn y tumores son los que tienen mayor riesgo de retención de la CE. Hoog y su equipo, en Estocolmo, en 2300 pacientes estudiados, encontraron que el riesgo relativo de retención de la CE en pacientes con sospecha de enfermedad de Crohn fue de 0,76 (IC 0,18-3,08), en pacientes con enfermedad de Crohn conocida fue de 9,39 (IC 3,32- 26,54), y en casos de tumores del intestino delgado de 3,88 (IC 1,18- 12,81) (29). La retención de la CE ocurre en promedio en el 0,7% de los todos los estudios con CE y varía según el diagnóstico que motivó el examen. En la población general el riesgo de retención de cápsula varía de 0,4% a 2,5%, y aumenta a 13% en pacientes con enfermedad Crohn conocida y hasta el 21% en pacientes con sospecha de obstrucción intestinal (30,31).
La tasa de recurrencia de SDO en nuestro estudio, durante el seguimiento, fue baja (25%), más frecuente con CE positivas (23%), a 24 meses de seguimiento. El estudio de Juliao y colaboradores (8) encontró una tasa de recurrencia de sangrado más alta del 45% a 14 meses de seguimiento. Se pensó que algunas de las causas de SDO en nuestro estudio con lesiones P2 como los tumores y las parasitosis que corresponden al 24%, el tratamiento de estas patologías resuelven el sangrado en forma definitiva lo cual podría explicar esta diferencia. Park y su equipo, en un estudio coreano, encontraron una tasa de resangrado en el 35,3% de 51 pacientes, a 31,7 meses de seguimiento (32).
El tratamiento fue médico en el 88% de nuestros pacientes, con hierro parenteral u oral y medidas conservadoras, quirúrgico en el 8% y endoscópico en el 4%. En el estudio de Lepileur y colaboradores, el seguimiento de 356 pacientes con SDO estudiados con CE, el manejo fue médico en el 30% y quirúrgico, endoscópico (EDB) y radiológico intervencionista en el 70% de los casos (22). Esta diferencia tan marcada en el abordaje con nuestros pacientes se debe a varias razones: la falta de enteroscopistas intervencionista en la ciudad, problemas de índole administrativo con retardo en la autorización de los estudios por las EPS, incluyendo la CE, las EDB y la remisión a sitios especializados. Uno de nuestros pacientes con un tumor yeyunal sangrante estuvo hospitalizado durante un mes, requirió más de 15 transfusiones, hasta la autorización del estudio con CE. En el estudio de Juliao y colaboradores (8), el tratamiento fue médico en el 76%, muy parecido al presente estudio.
CONCLUSIÓN
En nuestra serie, el rendimiento diagnóstico de la CE en el estudio del SDO fue del 58%, comparable a lo reportado en otros estudios nacionales e internacionales. Llama la atención la alta frecuencia de tumores y parásitos, hallazgo a confirmar con estudios prospectivos y un mayor número de casos.
Declaración de conflicto de interés
Los autores declaran no tener, de manera directa o indirecta, conflicto de interés de tipo académico, científico, financiero o personal para la publicación de este manuscrito.
REFERENCIAS
1. Iddan G, Meron G, Glukhovsky A, Swain P. Wireless capsule endoscopy. Nature. 2000;405(6785):417. [ Links ]
2. Mergener K, Ponchon T, Gralnek I, Pennazio M, Gay G, Selby W, et al. Literature review and recommendations for clinical application of small-bowel capsule endoscopy, based on a panel discussion by international experts. Consensus statements for small-bowel capsule endoscopy, 2006/2007. Endoscopy. 2007;39(10):895-909. [ Links ]
3. Keum B, Chun HJ. Capsule endoscopy and double balloon enteroscopy for obscure gastrointestinal bleeding: which is better? J Gastroenterol Hepatol. 2011;26(5):794-5. [ Links ]
4. Xin L, Liao Z, Jiang Y-P, Li Z-S. Indications, detectability, positive findings, total enteroscopy, and complications of diagnostic double-balloon endoscopy: a systematic review of data over the first decade of use. Gastrointest Endosc. 2011;74(3):563-70. [ Links ]
5. Liao Z, Gao R, Xu C, Li Z-S. Indications and detection, completion, and retention rates of small-bowel capsule endoscopy: a systematic review. Gastrointest Endosc. 2010;71(2):280-6. [ Links ]
6. Viazis N, Papaxoinis K, Vlachogiannakos J, Efthymiou A, Theodoropoulos I, Karamanolis DG. Is there a role for second-look capsule endoscopy in patients with obscure GI bleeding after a nondiagnostic first test? Gastrointest Endosc. 2009;69(4):850-6. [ Links ]
7. Teshima CW. Small bowel endoscopy for obscure GI bleeding. Best Pract Res Clin Gastroenterol. 2012;26(3):247-61. [ Links ]
8. Juliao Baños F, Muñoz Ortíz E, Delgado Y, Enrique C. Rendimiento diagnóstico y hallazgos de cápsula endoscópica en pacientes con sangrado digestivo de origen oscuro en el Hospital Pablo Tobón Uribe en Medellín - Colombia. Rev Colomb Gastroenterol. 2013;28(2):114-23. [ Links ]
9. Benavente Montoya M, Frisancho Velarde O. [Diagnostic yield of the endoscopic capsule and their impact in the clinical outcome]. Rev Gastroenterol Perú Órgano Of Soc Gastroenterol Perú. 2007;27(4):349-60. [ Links ]
10. Triester SL, Leighton JA, Leontiadis GI, Fleischer DE, Hara AK, Heigh RI, et al. A meta-analysis of the yield of capsule endoscopy compared to other diagnostic modalities in patients with obscure gastrointestinal bleeding. Am J Gastroenterol. 2005;100(11):2407-18. [ Links ]
11. Pongprasobchai S, Chitsaeng S, Tanwandee T, Manatsathit S, Kachintorn U. Yield, etiologies and outcomes of capsule endoscopy in Thai patients with obscure gastrointestinal bleeding. World J Gastrointest Endosc. 2013;5(3):122-7. [ Links ]
12. Galiano MT, Sánchez F, Pineda LF. Experiencia clínica del uso de la videocápsula endoscópica en el diagnóstico de patología del intestino delgado. Rev Col Gastroenterol. 2009;24(1):17-25. [ Links ]
13. Galiano MT, Cepeda R, García F. Angiodisplasias de intestino delgado, presentación de dos casos. Rev Col Gastroenterol. 2004;19:269-76. [ Links ]
14. Goenka MK, Majumder S, Kumar S, Sethy PK, Goenka U. Single center experience of capsule endoscopy in patients with obscure gastrointestinal bleeding. World J Gastroenterol WJG. 2011;17(6):774-8. [ Links ]
15. Ohmiya N, Yano T, Yamamoto H, Arakawa D, Nakamura M, Honda W, et al. Diagnosis and treatment of obscure GI bleeding at double balloon endoscopy. Gastrointest Endosc. 2007;66(3 Suppl):S72-77. [ Links ]
16. Cheung DY, Lee I-S, Chang DK, Kim JO, Cheon JH, Jang BI, et al. Capsule endoscopy in small bowel tumors: a multicenter Korean study. J Gastroenterol Hepatol. 2010;25(6):1079-86. [ Links ]
17. Imaoka H, Higaki N, Kumagi T, Miyaike J, Ohmoto M, Yamauchi K, et al. Characteristics of small bowel tumors detected by double balloon endoscopy. Dig Dis Sci. 2011;56(8):2366-71. [ Links ]
18. Lee B-I, Choi H, Choi K-Y, Byeon J-S, Jang H-J, Eun C-S, et al. Clinical characteristics of small bowel tumors diagnosed by double-balloon endoscopy: KASID multi-center study. Dig Dis Sci. 2011;56(10):2920-7. [ Links ]
19. Ludwig E, Kurtz RC. Tumors of the Small Intestine. In Feldman M, Friedman LS, Brandt LJ (eds). Sleisenger and Fordtrans Gastrointestinal and Liver Disease. 9th edition. Pathophysiology/Diagnosis/Management. Philadelphia: Saunders Elsevier. 2010;2145-53. [ Links ]
20. Das K, Sarkar R, Dasgupta J, Ray S, Ghatak S, Das K, et al. Obscure GI bleeding in the tropics: impact of introduction of double-balloon and capsule endoscopies on outcome. Gastrointest Endosc. 2010;72(2):292-300. [ Links ]
21. Chen J-M, Zhang X-M, Wang L-J, Chen Y, Du Q, Cai J-T. Overt gastrointestinal bleeding because of hookworm infection. Asian Pac J Trop Med. 2012;5(4):331-2. [ Links ]
22. Lepileur L, Dray X, Antonietti M, Iwanicki-Caron I, Grigioni S, Chaput U, et al. Factors associated with diagnosis of obscure gastrointestinal bleeding by video capsule enteroscopy. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc. 2012;10(12):1376-80. [ Links ]
23. Shahidi NC, Ou G, Svarta S, Law JK, Kwok R, Tong J, et al. Factors associated with positive findings from capsule endoscopy in patients with obscure gastrointestinal bleeding. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc. 2012;10(12):1381-5. [ Links ]
24. Bar-Meir S, Eliakim R, Nadler M, Barkay O, Fireman Z, Scapa E, et al. Second capsule endoscopy for patients with severe iron deficiency anemia. Gastrointest Endosc. 2004;60(5):711-3. [ Links ]
25. Pennazio M. Introduction to small-bowel bleeding. Techniques in Gastrointestinal Endoscopy 2012; 14:94-99. [ Links ]
26. Koornstra JJ. Bowel preparation before small bowel capsule endoscopy: what is the optimal approach? Eur J Gastroenterol Hepatol. 2009;21(10):1107-9. [ Links ]
27. Rokkas T, Papaxoinis K, Triantafyllou K, Pistiolas D, Ladas SD. Does purgative preparation influence the diagnostic yield of small bowel video capsule endoscopy?: A meta-analysis. Am J Gastroenterol. 2009;104(1):219-27. [ Links ]
28. Westerhof J, Koornstra JJ, Hoedemaker RA, Sluiter WJ, Kleibeuker JH, Weersma RK. Diagnostic yield of small bowel capsule endoscopy depends on the small bowel transit time. World J Gastroenterol WJG. 2012;18(13):1502-7. [ Links ]
29. Höög CM, Bark L-Å, Arkani J, Gorsetman J, Broström O, Sjöqvist U. Capsule retentions and incomplete capsule endoscopy examinations: an analysis of 2300 examinations. Gastroenterol Res Pract. 2012;2012:518718. [ Links ]
30. Cave D, Legnani P, de Franchis R, Lewis BS, ICCE. ICCE consensus for capsule retention. Endoscopy. 2005;37(10):1065-7. [ Links ]
31. Li F, Gurudu SR, De Petris G, Sharma VK, Shiff AD, Heigh RI, et al. Retention of the capsule endoscope: a single-center experience of 1000 capsule endoscopy procedures. Gastrointest Endosc. 2008;68(1):174-80. [ Links ]
32. Park JJ, Cheon JH, Kim HM, Park HS, Moon CM, Lee JH, et al. Negative capsule endoscopy without subsequent enteroscopy does not predict lower long-term rebleeding rates in patients with obscure GI bleeding. Gastrointest Endosc. 2010;71(6):990-7. [ Links ]











 text in
text in