Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.30 supl.1 Bogotá Dec. 2015
Guía de práctica clínica para el diagnóstico y tratamiento de la infección por Helicobacter pylori en adultos
Clinical Practice Guideline for the Diagnosis and Management of Adult Patients with Helicobacter pylori Infection
William Otero R. MD1, Alba Alicia Trespalacios R. Bact MSc Phd3, Lina Otero P. MD2, María Teresa Vallejo O. MD4, Marcela Torres Amaya QF5, Rodrigo Pardo MD6, Luis Sabbagh MD7
1 Profesor titular de medicina, Coordinador de Gastroenterología, Universidad Nacional de Colombia. Ex-presidente Asociación Colombiana de Gastroenterología, Ex-presidente Asociación Colombiana de Endoscopia Digestiva. Miembro honorario Sociedad Dominicana de Gastroenterología. Miembro Honorario Sociedad Venezolana de Endoscopia Digestiva, Gastroenterólogo, Clínica Fundadores. Bogotá, Colombia.
2 Profesora titular, facultad de Ciencias, Universidad Javeriana. Bogotá-Colombia. Directora de posgrado Facultad de Ciencias Pontificia Universidad Javeriana, Bogotá Colombia.
3 Especialista en medicina interna, especialista en gastroenterología. Asociación Colombiana de Gastroenterología. Bogotá-Colombia.
4 Médica cirujana, magíster en epidemiología Clínica, Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia. Bogotá-Colombia.
5 Química farmaceuta, magíster en epidemiología clínica, doctorado en Salud Pública (e), gerente editorial del Grupo Cochrane de Infecciones Transmisión Sexual. Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia. Bogotá-Colombia.
6 Médico internista, epidemiólogo, director del Instituto de Investigaciones Clínicas, Universidad Nacional de Colombia. Bogotá-Colombia.
7 Presidente de la Organización Panamericana de Gastroenterología, presidente de la Asociación Colombiana de Gastroenterología, expresidente de la Asociación Colombiana de Endoscopia Digestiva, director del posgrado en gastroenterología, Fundación Universitaria Sánitas. Bogotá-Colombia.
Resumen
Objetivo: brindar una guía de práctica clínica basada en la evidencia más reciente para el diagnóstico y tratamiento de la infección por Helicobacter pylori teniendo en cuenta la efectividad y seguridad de las intervenciones dirigidas a pacientes, personal asistencial, administrativo y entes gubernamentales de cualquier servicio de atención en Colombia.
Materiales y métodos: esta guía fue desarrollada por un equipo multidisciplinario con apoyo de la Asociación Colombiana de Gastroenterología, el Grupo Cochrane ITS y el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia. Se desarrollaron preguntas clínicas relevantes y se realizó la búsqueda de guías nacionales e internacionales en bases de datos especializadas. Las guías existentes fueron evaluadas en términos de calidad y aplicabilidad; una de ellas cumplió los criterios de adaptación, por lo que se decidió adaptar 4 preguntas clínicas y construir 10 de novo. El Grupo Cochrane realizó la búsqueda sistemática de la literatura. Las tablas de evidencia y recomendaciones fueron realizadas con base en la metodología GRADE. Las recomendaciones de la guía fueron socializadas en una reunión de expertos con entes gubernamentales y pacientes.
Resultados: se desarrolló una guía de práctica clínica basada en la evidencia para el diagnóstico y tratamiento de la infección de Helicobacter pylori en Colombia.
Conclusiones: la erradicación de H. pylori, curará las ulceras pépticas asociadas al mismo, la gastritis crónica sin atrofia o metaplasia intestinal y contribuirá a disminuir el riesgo de cáncer gástrico, que es la primera causa de muerte por cáncer en Colombia.
Palabras clave
Helicobacter pylori, diagnóstico, tratamiento.
Abstract
Objective: To provide a clinical practice guideline with the latest evidence for diagnosis and treatment of Helicobacter pylori infection for patients, caregivers, administrative and government bodies at all levels of care in Colombia.
Materials and Methods: This guide was developed by a multidisciplinary team with the support of the Colombian Association of Gastroenterology, Cochrane STI Group and Clinical Research Institute of the Universidad Nacional de Colombia. Relevant clinical questions were developed and the search for national and international guidelines in databases was performed. Existing guidelines were evaluated quality and applicability. One guideline met the criteria for adaptation, so the group decided to adapt 4 clinical questions and to develop 10 de novo clinical questions. Systematic literature searches were conducted by the Cochrane Group. The tables of evidence and recommendations were made based on the GRADE methodology. The recommendations of the guide were socialized in a meeting of experts with government agencies and patients.
Results: An evidence-based Clinical Practice Guidelines for the diagnosis and treatment of Helicobacter pylori infection was developed for the Colombian context.
Conclusions: The opportune detection and appropriate management of Helicobacter pylori would contribute to the burden of the disease in Colombia and its associated diseases.
Keywords
Helicobacter pylori, diagnosis, treatment.
PROPÓSITO Y ALCANCE
Esta guía de práctica clínica (GPC) está dirigida a los profesionales de la salud que tratan directamente a los pacientes infectados por Helicobacter pylori en cualquier servicio de atención del país; aborda aspectos relacionados con el diagnóstico, tratamiento y seguimiento de esta condición con el propósito de otorgar a los profesionales de la salud la más reciente evidencia respecto al diagnóstico, efectividad y seguridad de las diversas opciones terapéuticas, así como establecer pautas de seguimiento. La población objetivo de esta guía son los pacientes mayores de 18 años con sospecha diagnóstica o infección confirmada por Helicobacter pylori que sean tratados en cualquier nivel de atención. La guía no incluyó el manejo de pacientes con eventos adversos al tratamiento o pacientes gestantes o en lactancia.
Con el objetivo de brindar recomendaciones para el mejor manejo de la infección de H. pylori en Colombia, esta guía está dirigida a todo el personal en salud asistencial y administrativo, así como para aquellos que toman decisiones en salud, aseguradoras, pagadores del gasto en salud y a quienes generan políticas en salud.
JUSTIFICACIÓN
El Helicobacter pylori (H. pylori) afecta al 50% de la población mundial (1) y por lo menos al 80% de la población colombiana (2-4). Es el principal agente etiológico de gastritis crónica, úlceras pépticas y cáncer gástrico (5); en Colombia, estecáncer representa la primera causa de muertepor esta enfermedad en los hombres y la tercera en las mujeres (6). Diversos estudios colombianos han encontrado una alta resistencia de H. pylori a los antibióticos usualmente utilizados para erradicarlo (7), lo que probablemente explica que en la actualidad las tasas de erradicación con las terapias utilizadas estén por debajo del 90% (por intención de tratar [ITT]), que es considerado el valor mínimo aceptable para una terapia empírica (8,9). Con la terapia triple estándar, la eficacia alcanzada es de 62%-74% (10-12), con la terapia triple con levofloxacina de 75%-84% (11,12) y con la terapia secuencial de 62% (10). Más recientemente y utilizando terapias con duración de 2 semanas y varios antibióticos, se ha logrado superar el impacto de la resistencia antimicrobiana con una tasa de erradicación superior al 90% (13).
Una encuesta realizada en nuestro país encontró que los médicos no siguen las recomendaciones de los consensos o guías internacionales sino que, de manera intuitiva, prescriben diversos regímenes, que en su mayoría no han sido previamente investigados (14), aunque es posible que esta conducta esté relacionada con la dificultad para tener acceso a las guías y consensos internacionales. Al tener en cuenta estos antecedentes, la Asociación Colombiana de Gastroenterología consideró pertinente elaborar la presente guía de práctica clínica sobre H. pylori con el fin de consolidar la información internacional con respecto al diagnóstico, esquemas de tratamiento de primera línea, de segunda línea, esquemas clásicos, esquemas nuevos, dosis, optimización de los tratamientos, utilidad de los probióticos, ventajas del cultivo pretratamiento, necesidad del cultivo postratamiento fallido y verificación de la erradicación. El objetivo final es sintetizar la información más relevante, destacar los aspectos prácticos importantes para el manejo de H. pylori para que sean de utilidad a la comunidad médica nacional. Una amplia difusión de esta guía es uno de los compromisos adicionales de nuestra Asociación Colombiana de Gastroenterología.
MATERIALES Y MÉTODOS
El grupo desarrollador de la guía (GDG) diseñó una metodología rápida para la elaboración de esta guía. Para mayor información, la versión larga de la misma se encuentra en http://www.gastrocol.com/. El GDG contó con la participación de expertos temáticos en gastroenterología, medicina interna, bacteriología, química farmacéutica, salud pública y diseño de políticas, así como expertos epidemiólogos. De igual forma, el GDG recibió apoyo por parte de la Asociación Colombiana de Gastroenterología, el Instituto de Investigaciones Clínicas de la Universidad Nacional de Colombia y el Grupo Cochrane STI; este último realizó la búsqueda sistemática de la literatura y la consecución de los artículos de estudios primarios.
El GDG realizó una búsqueda sistemática de la literatura con el objeto de identificar todas las GPC nacionales e internacionales que abordaran el manejo de pacientes con infección por H. pylori. La búsqueda se realizó en TRIP database, Medline, EMBASE, Biblioteca Cochrane, Lilacs y literatura gris. Se evaluó la calidad de las GPC recuperadas con el instrumento AGREE II (13). Una vez se obtuvo la calidad global de cada guía, se construyó una matriz de decisión que examinó el tipo de guía, fecha de publicación, concordancia de los objetivos y alcance de la GPC (14). Con base en los resultados de la matriz de decisión, se consideró que 4 preguntas de la Guidelines for the diagnosis and treatment of Helicobacter pylori infection in Korea, 2013 eran susceptibles de ser adaptadas al contexto colombiano. Adicionalmente se realizaron diez preguntas de novo.
Todas las preguntas a desarrollar se estructuraron en formato PICO (población, intervención, comparación y desenlaces). El primer paso fue la búsqueda metódica de revisiones sistemáticas publicadas de las bases de datos especializadas hasta junio del 2015. Las revisiones sistemáticas (RS) identificadas fueron evaluadas con la herramienta AMSTAR (15). La síntesis de los estudios seleccionados se realizó a través de la construcción de los perfiles de evidencia en www.guidleinedevelopment.org y los niveles de evidencia fueron graduados según la clasificación GRADE (alta, moderada, baja y muy baja) (16,17).
NIVEL DE EVIDENCIA
Calidad global de la evidencia GRADE

La graduación de la fuerza y dirección de cada recomendación se determinó con base en el nivel de evidencia y otras consideraciones adicionales que fueron revisadas en pleno por el GDG, el ente gestor y los grupos de interés. Este ejercicio se desarrolló mediante la construcción de una mesa de trabajo que generó la fuerza de la recomendación de acuerdo con:

Las recomendaciones de la guía fueron socializadas en una reunión de expertos, entes gubernamentales y pacientes.
RECOMENDACIONES GENERALES
Diagnóstico
Pregunta 1: ¿cuál es la utilidad de las pruebas invasivas y no invasivas en el diagnóstico y/o verificación de erradicación de Helicobacter pylori?

La revisión sistemática (RS) de Ling y colaboradores (18) evaluó la exactitud diagnóstica del test de aliento de urea con 13C (13C TAU) comparado con endoscopia o serología en pacientes con dispepsia sin signos de alarma o pacientes con infección por H. pylori. Los autores encontraron que la sensibilidad de 13C TAU fue del 95% (IC 95% con rango de 90,1-97,5) con especificidad del 91,6% (IC 95% con rango de 81,3-96,4) y LR+ y LR negativo de 11,3 (IC 95% con rango de 4,8-26,6) y 0,05 (IC 95% con rango de 0,03-0,11) respectivamente. Para la verificación de la erradicación a las 6 semanas y 6 meses, la sensibilidad fue 98,9% y la especificidad fue 99,6% (p >0,05). Calidad de la evidencia: muy baja.
Adicionalmente, la RS realizada para la GPC sobre el diagnóstico y tratamiento de la infección por H. pylori en Corea evaluó la utilidad de los métodos no invasivos en el diagnóstico de la infección por H. pylori y reportó que la prueba de aliento de urea presentó una alta frecuencia de falsos negativos en pacientes que consumieron antibióticos o inhibidores de la bomba de protones (IBP) previamente o durante la prueba (11). Calidad de la evidencia: baja.
De manera consistente con los resultados anteriores, el tercer consenso brasilero de Helicobacter pylori apoya el uso del test de aliento con úrea marcada y la prueba de antígeno fecal con la recomendación de suspender los medicamentos antisecretores y antibióticos al menos 2 semanas antes del examen. En lo referente a las pruebas invasivas, el consenso determinó que en los pacientes dispépticos con indicación de endoscopia, se deben tomar en esta muestras del antro y cuerpo gástrico para realizar pruebas de identificación de H. pylori mediante histología o test de ureasa (10). Calidad de la evidencia: muy baja.
Tratamiento
Pregunta 2: ¿cuál es la efectividad y seguridad de la terapia de erradicación de Helicobacter pylori guiada por susceptibilidad determinada por cultivo en comparación con la terapia empírica?

La revisión de López y colaboradores (19) evaluó la efectividad y seguridad de la terapia guiada por susceptibilidad antibiótica en comparación con el tratamiento empírico en pacientes con infección por H. pylori que requirieran tratamiento de primera o segunda línea. El estudio compiló 10 ensayos clínicos y 3 estudios no aleatorizados, los cuales reportaron que en pacientes que fueron tratados por primera vez, el tratamiento guiado por susceptibilidad presentó una mayor frecuencia de erradicación en comparación con el tratamiento empírico (89,2% versus 77,3%, RR: 1,16 IC 95% con rango de 1,10 a 1,23), con frecuencia global de eventos adversos (EA) entre el 6% al 38%. Para el tratamiento de segunda línea, no fueron reportadas diferencias estadísticamente significativas entre las 2 aproximaciones terapéuticas (tratamiento guiado: 81,6%, tratamiento empírico: 60,5%, IC 95% 1,11, IC 95% con rango de 0,82 a 1,51) y la frecuencia global de EA estuvo entre el 26% al 65%. Calidad de la evidencia: baja.
Pregunta 3: ¿cuál debe ser la duración del tratamiento de erradicación de Helicobacter pylori?

Una RS de la literatura evaluó la efectividad y seguridad de 7, 10 y 14 días de tratamiento de erradicación en pacientes con infección confirmada por H. pylori. La revisión encontró diferencias estadísticamente significativas a favor de la terapia de 14 días sobre 7 días en el subgrupo de terapias triples (RR 0,66, IC 95% con rango de 0,60 a 0,74, EA RR 1,20 IC 95% con rango de 1,06 a 1,37), terapias cuádruples de antagonistas del receptor H2 de histamina (ARH2) + bismuto (RR 0,49, IC 95% con rango de 0,36 a 0,67); a favor de 14 días sobre 10 días en el subgrupo de terapia triple (RR 0,72, IC 95% con rango de 0,58 a 0,9) y a favor de 10 días sobre 7 días en el subgrupo de terapia triple (RR 0,80, IC 95% con rango de 0,72 a 0,89) (20). Calidad de la evidencia: baja.
Pregunta 4: ¿cuál es el esquema de tratamiento de primera línea en la erradicación de Helicobacter pylori?

Terapia secuencial: una RS evaluó la efectividad y seguridad de la terapia secuencial en comparación con la terapia triple estándar en pacientes con infección por H. pylori sin tratamiento previo. La revisión encontró una mayor erradicación en el grupo que recibió terapia secuencial (84,1% versus 75,1%, RR 1,13, IC 95% con rango de 1,09 a 1,17) sin encontrar diferencias en la frecuencia de eventos adversos (19% versus 18,2%, RR 1,01, IC 95% con rango de 0,91 a 1,13) (21). Calidad de la evidencia: moderada.
Terapia triple estándar: una RS evaluó la efectividad y seguridad de la terapia triple estándar en comparación con terapias duales, triples o cuádruples en pacientes con infección por H. pylori. La revisión no reportó diferencias estadísticamente significativas al comparar la erradicación de terapia triple con la terapia dual, con terapia cuádruple, con otras terapias triples ni en la frecuencia de eventos adversos (p >0,05) (22). Calidad de la evidencia: muy baja.
Terapia triple con levofloxacina: una RS que comparó la efectividad y seguridad de la terapia triple basada en levofloxacina con la terapia triple estándar en pacientes con infección por H. pylori sin tratamiento previo no encontró diferencias significativas en la erradicación del microorganismo (81,5% versus 77,2%, OR 1,28, IC 95% con rango de 0,88 a 1,85) ni en la frecuencia de EA (OR 0,87, IC 95% con rango de 0,59 a 1,29) (23). Calidad de la evidencia: muy baja. La adición de sales de bismuto a una triple terapia de 14 días puede lograr una eficacia del 91% (38).
Terapia triple con moxifloxacina: la revisión de Zhang y colaboradores no encontró diferencias estadísticamente significativas en la erradicación de H. pylori en los pacientes con infección por esta bacteria sin tratamiento previo que recibieron terapia triple o cuádruple con moxifloxacina en comparación con terapias cuádruple con o sin bismuto (84,2% versus 73,4%, OR 1,80, IC 95% con rango de 0,71 a 4,55), aunque encontró una menor frecuencia de EA en el grupo que recibió moxifloxacina (OR 0,45, IC 95% con rango de 0,26 a 0,77) (24). Calidad de la evidencia: muy baja.
Inhibidores de la bomba de protones (IBP): una RS evaluó la efectividad de los inhibidores de protones de primera y segunda generación en pacientes con infección por H. pylori sin tratamiento previo. La revisión reportó una mayor erradicación en los pacientes que recibieron esomeprazol en comparación con los IBP de primera generación (82,3% versus 77,6%, OR 1,32, IC 95% con rango de 1,01 a 1,73), sin encontrar diferencias entre ambos IBP de segunda generación (rabeprazol 76,7%, esomeprazol 78,7%, OR 0,90, IC 95% con rango de 0,70 a 1,1). La revisión no incluyó desenlaces adicionales (25). Calidad de la evidencia: muy baja.
Pregunta 5: ¿cuál es el esquema de tratamiento de segunda línea?

Terapia triple con moxifloxacina: la revisión de Zhang y colaboradores (24) que evaluó la efectividad y seguridad de la terapia basada en el uso de moxifloxacina en terapias triples o cuádruples en comparación con terapias cuádruples con o sin bismuto en pacientes con infección por H. pylori encontró diferencias en el subgrupo de segunda línea a favor de la moxifloxacina (erradicación: 73,3% versus 60,2%, OR 1,78, IC 95% con rango de 1,16 a 2,73; eventos adversos: OR 0,45, IC 95% con rango de 0,26 a 0,77). Calidad de la evidencia: muy baja.
Terapia cuádruple con bismuto: una RS (26) evaluó la efectividad y seguridad de la terapia cuádruple de bismuto + IBP + 2 antibióticos en comparación con la terapia triple estándar en pacientes con infección por H. pylori. La revisión no encontró diferencias entre los grupos en la erradicación de la bacteria (77,6% versus 68,9%, DR 0, IC 95% con rango de -1,2% a 13%) ni en EA. Calidad de la evidencia: baja.
Levofloxacina – amoxicilina: una RS evaluó la efectividad y tolerabilidad de la terapia triple basada en levofloxacina y amoxicilina en comparación con la terapia cuádruple en pacientes con infección por H. pylori provenientes de Europa y Asia. La revisión no reportó diferencias en la erradicación (76,5% versus 67,4%, OR 1,59, IC 95% con rango de 0,98 a 2,58), con una menor frecuencia de eventos adversos en el grupo de levofloxacina–amoxicilina (RR 0,39, IC 95% con rango de 0,18 a 0,86) (27). Calidad de la evidencia: muy baja.
Pregunta 6: ¿cuál es la efectividad y la seguridad de las terapias coadyuvantes en el tratamiento?

Probióticos: la revisión sistemática de Zheng y colaboradores (28) evaluó la efectividad y seguridad de la suplementación del tratamiento de erradicación con probióticos que contuvieran especies del género Lactobacillus en pacientes con infección por H. pylori. Los autores encontraron diferencias en la erradicación a favor del grupo que recibió probióticos (RR 1,14, IC 95% con rango de 1,06 a 1,22), sin diferencias significativas en la frecuencia de EA (p >0,05). Calidad de la evidencia: moderada.
Rebamipida: una RS evaluó la efectividad de la suplementación con rebamipida en el tratamiento de erradicación en pacientes con infección por H. pylori. La revisión encontró diferencias en la erradicación (OR 1,59, IC 95% con rango de 1,14 a 2,22) (29). Calidad de la evidencia: muy baja.
Terapia periodontal: una revisión sistemática (30) evaluó la efectividad del tratamiento periodontal (cepillado, limpieza interdental, raspado y alisado radicular, y uso de clorhexidina) más la terapia de erradicación en pacientes con infección por H. pylori. La revisión encontró que el tratamiento periodontal disminuye la persistencia de H. pylori en comparación con la terapia de erradicación sola (31,6% versus 77,5%, RR 0,37, IC 95% con rango de 0,21 a 0,64), sin reportar desenlaces de seguridad. Calidad de la evidencia: baja.
Consideraciones especiales del tratamiento
Tratamiento en sospecha de resistencia antimicrobiana

Se encontraron 3 RS que evaluaron la efectividad y seguridad de diversos tratamientos en poblaciones con resistencia antimicrobiana con infección por H. pylori. Las revisiones encontraron que en el grupo con resistencia a la claritromicina, la terapia secuencial presentó una mayor erradicación sobre la terapia triple estándar (80,9% versus 40,7%, RR 1,98, IC 95% con rango de 1,50 a 2,62) (21)ÿ sin diferencias en comparación con la terapia cuádruple con bismuto (58,3% versus 85,7%, DR -0,274, IC 95% con rango de -0,599 a 0,184) (31). En el subgrupo con resistencia a nitroimidazoles, la terapia triple por 14 días fue superior a la terapia secuencial (terapia secuencial 72,7%, terapia triple 89,1%, DR -0,164, IC 95% con rango de -0,328 a -0,0014), sin diferencias significativas en la comparación de terapia secuencial versus terapia cuádruple basada en bismuto (p >0,05) (31). En el subgrupo con resistencia a claritromicina y metronidazol no se encontraron diferencias entre las comparaciones de terapia secuencial versus terapia triple y terapia secuencial versus terapia cuádruple (31). Adicionalmente, otra de las revisiones evaluó la eficacia del tratamiento cuádruple versus la terapia triple estándar ajustando la frecuencia de resistencia a la claritromicina mediante metarregresión, la cual no influencia la resistencia a este medicamento en la eficacia del régimen terapéutico (r = 0,17) (26). Calidad de la evidencia: baja.
Dosis de claritromicina
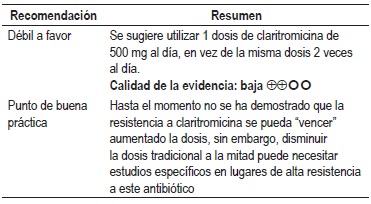
La revisión de Harb y colaboradores que evaluó la efectividad y seguridad de la dosis de claritromicina en pacientes con infección por H. pylori que recibieran esquemas que incluyeran este medicamento encontró que el grupo que recibió la mitad de la dosis de presentó una menor frecuencia de EA (RR 0,67, IC 95% con rango de 0,60 a 0,75) en comparación de la dosis completa, sin encontrar diferencias significativas en la erradicación (mitad de dosis: 82,5%, dosis estándar: 83,4%, RR 0,98, IC 95% con rango de 0,95 a 1,02) (32). Calidad de la evidencia: baja.
Tratamiento en comorbilidades específicas
Pregunta 8: ¿cuál es la efectividad y seguridad del tratamiento de erradicación de Helicobacter pylori para la prevención de lesiones gástricas malignas y premalignas?

Incidencia de cáncer gástrico: una revisión sistemática (33) evaluó el efecto del tratamiento de erradicación de H. pylori en el pronóstico histológico de lesiones gástricas en pacientes adultos. La revisión encontró que el tratamiento para la erradicación de H. pylori redujo la incidencia total de cáncer gástrico (RR 0,70, IC 95% con rango de 0,49 a 0,99), cáncer gástrico metacrónico (RR 0,52, IC 95% con rango de 0,31 a 0,87), atrofia (RR 0,25, IC 95% con rango de 0,08 a 0,81), progresión histológica de la atrofia gástrica (RR 0,82, IC 95% con rango de 0,68 a 0,99), sin encontrar cambios en la incidencia de cáncer gástrico una vez instaurada la metaplasia intestinal (RR 0,88, IC 95% con rango de 0,59 a 1,31). Calidad de la evidencia: moderada.
Incidencia de cáncer gástrico en pacientes sanos y asintomáticos: la revisión de Wong y colaboradores (34) encontró una reducción global de la incidencia de cáncer gástrico en los pacientes que recibieron tratamiento de erradicación (RR 0,66, IC 95% con rango de 0,46 a 0,95), sin encontrar diferencias en los subgrupos con lesiones precursoras o preneoplásicas. Calidad de la evidencia: muy baja.
Pregunta 9: ¿cuál es el efecto de la erradicación de Helicobacter pylori en los síntomas de la enfermedad por reflujo gastroesofágico?

Una RS de 2012 evaluó con 10 ensayos clínicos la mejoría de los síntomas de enfermedad por reflujo gastroesofágico (ERGE) y esofagitis esofágica en pacientes tratados para la erradicación del H. pylori. No se encontró diferencia significativa para la ERGE sintomática (OR 0,81, IC 95% con rango de 0,56-1,17, p = 0,27) o evidencia endoscópica de la esofagitis por reflujo (OR 1,13; IC 95% con rango de 0,72 - 1,78; p = 0,59) entre los 2 grupos. Calidad de la evidencia: baja (35).
Pregunta 10: ¿cuál es el efecto de la erradicación de Helicobacter pylori en los pacientes con dispepsia?

Una RS de 2014 evaluó los efectos a largo plazo de la erradicación de H. pylori. Se incluyeron 14 ensayos clínicos controlados (ECC) de Europa, Asia del este, Oceanía, Norteamérica y Suramérica, y se evaluaron los esquemas para la erradicación de H. pylori comparados con placebo y procinéticos solos. El análisis de los 2993 pacientes mostró que aquellos que recibieron terapia de erradicación presentaron una mayor probabilidad de mejoría en los síntomas de dispepsia comparado con el grupo control (OR 1,38, IC 95% con rango de 1,18-1,62); en el análisis por subgrupos, los pacientes de las Américas mostraron una mejoría mayor (OR 1,43, IC 95% con rango de 1,12 - 1,83, 1238 pacientes). La RS no identificó desenlaces de calidad de vida o eventos adversos. Calidad de la evidencia: moderada (36).
Pregunta 11: ¿cuál es el efecto de la erradicación de Helicobacter pylori en los pacientes con antecedente de úlcera péptica?

La RS desarrollada para la GPC Coreana sobre el diagnóstico y tratamiento de la infección de Helicobacter pylori, 2013, evaluó el beneficio de erradicar esta bacteria en pacientes con antecedente de úlcera péptica. Se encontró que su erradicación es un tratamiento eficaz para la prevención de úlceras pépticas y la recurrencia de las mismas, la cual usualmente oscila entre 60% y 100%, sin embargo, con la erradicación de H. pylori esta tasa de recurrencia se reduce a menos del 5%. Calidad de la evidencia: baja.
Pregunta 12: ¿cuál es el efecto de la erradicación de Helicobacter pylori en los pacientes que van a tomar de manera crónica antiinflamatorios no esteroideos (AINES)?
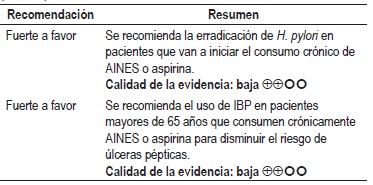
La RS desarrollada para la GPC Coreana sobre el diagnóstico y tratamiento de la infección por H. pylori recomienda el tratamiento de erradicación en los pacientes que consumen de manera crónica AINES debido a que la erradicación reduce el riesgo de úlcera péptica. De manera consistente, el tercer consenso brasilero de Helicobacter pylori soporta dicha recomendación teniendo en cuenta que el uso de AINES aumenta 4,89 veces el riesgo de úlcera péptica y la presencia de H. pylori concomitante aumenta 6,13 veces el riesgo de sangrado gastrointestinal. Calidad de la evidencia: baja.
Pregunta 13: ¿cuál es la utilidad de la erradicación de Helicobacter pylori en pacientes con linfoma MALT de alto y bajo grado?

La RS desarrollada para la GPC Coreana sobre el diagnóstico y tratamiento de la infección por H. pylori recomienda el tratamiento de erradicación en los pacientes que presentan linfoma MALT confinado a la mucosa y submucosa, dado que la frecuencia de favorabilidad del tratamiento se encuentra entre el 60% al 80%(11, 37). Adicionalmente, para los pacientes en los que no se obtenga remisión de la enfermedad con la erradicación de H. pylori, la guía recomienda el uso de otros tratamientos (resección quirúrgica, quimioterapia, radioterapia) (11). Calidad de la evidencia: baja.
Pregunta 14: ¿cuál es el efecto de la erradicación de Helicobacter pylori en los pacientes con anemia ferropénica?
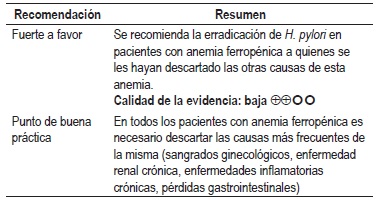
La revisión sistemática desarrollada para la GPC Coreana sobre el diagnóstico y tratamiento de la infección de Helicobacter pylori, 2013, y el tercer consenso brasilero de Helicobacter pylori apoyan la erradicación de esta bacteria en pacientes con anemia ferropénica en quienes no ha podido ser determinada la etiología, debido a la asociación sugerida entre esta patología y la infección por H. pylori (10, 11).
ALGORITMO 1. DIAGNÓSTICO

ALGORITMO 2. VERIFICACIÓN DE LA ERRADICACIÓN DE LA INFECCIÓN DESPUÉS DEL PRIMER TRATAMIENTO

ALGORITMO 3. TRATAMIENTO INICIAL DE LA INFECCIÓNPOR HELICOBACTER PYLORI

DECLARACIÓN DE CONFLICTOS DE INTERÉS
Los autores declaran no tener conflictos de interés, no estar involucrados como investigadores en ensayos clínicos en curso sobre el tema, y no haber recibido donaciones o beneficios por parte de los grupos interesados en las recomendaciones. El doctor William Otero, declara haber sido conferencista de los siguientes laboratorios: Abbott-Lafrancol, Biotoscana, Janssen, Tecnofarma y Procaps.
FUENTE DE FINANCIACIÓN
La presente guía fue desarrollada mediante un convenio de extensión entre la Asociación Colombiana de Gastroenterología y la facultad de Medicina de la Universidad Nacional.
REFERENCIAS
1. IARC. Schistosomes, liver flukes and Helicobacter pylori. IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Lyon, 7-14 June 1994. IARC Monogr Eval Carcinog Risks Hum. 1994;61:1-241. [ Links ]
2. Tonkic A, Tonkic M, Lehours P, Megraud F. Epidemiology and diagnosis of Helicobacter pylori infection. Helicobacter. 2012 Sep;17 Suppl 1:1-8. [ Links ]
3. Malfertheiner P, Megraud F, OMorain CA, Atherton J, Axon AT, Bazzoli F, et al. Management of Helicobacter pylori infection--the Maastricht IV/ Florence Consensus Report. Gut. 2012 May;61(5):646-64. [ Links ]
4. Herrero R, Park JY, Forman D. The fight against gastric cancer - the IARC Working Group report. Best Pract Res Clin Gastroenterol. 2014 Dec;28(6):1107-14. [ Links ]
5. Graham DY. Helicobacter pylori update: Gastric cancer, reliable therapy, and possible benefits. Gastroenterology. 2015 Apr;148(4):719-31 e3. [ Links ]
6. Graham DY. History of Helicobacter pylori, duodenal ulcer, gastric ulcer and gastric cancer. World J Gastroenterol. 2014 May 14;20(18):5191-204. [ Links ]
7. Camargo MC, Garcia A, Riquelme A, Otero W, Camargo CA, Hernandez-Garcia T, et al. The problem of Helicobacter pylori resistance to antibiotics: A systematic review in Latin America. Am J Gastroenterol. 2014 Apr;109(4):485-95. [ Links ]
8. Hopkins RJ. In search of the Holy Grail of Heliocobacter pylori remedies. Helicobacter. 2001 Jun;6(2):81-3. [ Links ]
9. Graham DY, Lu H, Yamaoka Y. A report card to grade Helicobacter pylori therapy. Helicobacter. 2007 Aug;12(4):275-8. [ Links ]
10. Coelho LG, Maguinilk I, Zaterka S, Parente JM, do Carmo Friche Passos M, Moraes-Filho JP. 3rd Brazilian Consensus on Helicobacter pylori. Arq Gastroenterol. 2013 Apr;50(2). [ Links ]
11. Kim SG, Jung HK, Lee HL, Jang JY, Lee H, Kim CG, et al. Guidelines for the diagnosis and treatment of Helicobacter pylori infection in Korea, 2013 revised edition. J Gastroenterol Hepatol. 2013;29(7):1371-86. [ Links ]
12. Gómez M, Otero W, Gutiérrez Ó. Tratamiento de la infección por Helicobacter pylori. Encuesta en un grupo de médicos generales y especialistas en Colombia. Rev Col Gastroenterol. 2007;22(1):7-16. [ Links ]
13. AGREE C. Instrumento AGREE II Instrumento para la evaluación de Guías de Práctica Clínica. Guiasalud; 2009 [updated 2009; cited 2015]; Available from: http://www.guiasalud.es/contenidos/documentos/Guias_Practica_Clinica/Spanish-AGREE-II.pdf. [ Links ]
14. Social MdlP, Colciencias, Bogotá CdEeIeSdlFSFd, Harvard EdSPdlUd. Guía Metodológica para el desarrollo de Guías de Atención Integral en el Sistema General de Seguridad Social en Salud Colombiano. 2010 [cited 2015. Available from: https://www.minsalud.gov.co/salud/Documents/Gu%C3%ADa%20Metodol%C3%B3gica%20para%20la%20elaboraci%C3%B3n%20de%20gu%C3%ADas.pdf. [ Links ]
15. Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: A measurement tool to assess the methodological quality of systematic reviews. BMC Med Res Methodol. 2007;7:10. [ Links ]
16. Brozek JL, Akl EA, Alonso-Coello P, Lang D, Jaeschke R, Williams JW, et al. Grading quality of evidence and strength of recommendations in clinical practice guidelines. Part 1 of 3. An overview of the GRADE approach and grading quality of evidence about interventions. Allergy. 2009 May;64(5):669-77. [ Links ]
17. Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, et al. GRADE: An emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008 Apr 26;336(7650):924-6. [ Links ]
18. Ling D. Carbon-13 urea breath test for Helicobacter pylori infection in patients with uninvestigated ulcer-like dyspepsia: An evidence-based analysis. Ont Health Technol Assess Ser. 2013;13(19):1-30. [ Links ]
19. Lopez-Gongora S, Puig I, Calvet X, Villoria A, Baylina M, Munoz N, et al. Systematic review and meta-analysis: Susceptibility-guided versus empirical antibiotic treatment for Helicobacter pylori infection. J Antimicrob Chemother. 2015 Jun 14. [ Links ]
20. Yuan Y, Ford AC, Khan KJ, Gisbert JP, Forman D, Leontiadis GI, et al. Optimum duration of regimens for Helicobacter pylori eradication. Cochrane Database Syst Rev. 2013;12:CD008337. [ Links ]
21. Feng L, Wen MY, Zhu YJ, Men RT, Yang L. Sequential Therapy or Standard Triple Therapy for Helicobacter pylori Infection: An Updated Systematic Review. Am J Ther. Jan 7. [ Links ]
22. Wang B, Lv ZF, Wang YH, Wang H, Liu XQ, Xie Y, et al. Standard triple therapy for Helicobacter pylori infection in China: A meta-analysis. World J Gastroenterol. 2014 Oct 28;20(40):14973-85. [ Links ]
23. Ye CL, Liao GP, He S, Pan YN, Kang YB, Zhang ZY. Levofloxacin and proton pump inhibitor-based triple therapy versus standard triple first-line therapy for Helicobacter pylori eradication. Pharmacoepidemiol Drug Saf. 2014 May;23(5):443-55. [ Links ]
24. Zhang G, Zou J, Liu F, Bao Z, Dong F, Huang Y, et al. The efficacy of moxifloxacin-based triple therapy in treatment of Helicobacter pylori infection: A systematic review and meta-analysis of randomized clinical trials. Braz J Med Biol Res. 2013 Jul;46(7):607-13. [ Links ]
25. McNicholl AG, Linares PM, Nyssen OP, Calvet X, Gisbert JP. Meta-analysis: esomeprazole or rabeprazole versus first-generation pump inhibitors in the treatment of Helicobacter pylori infection. Aliment Pharmacol Ther. 2012 Sep;36(5):414-25. [ Links ]
26. Venerito M, Krieger T, Ecker T, Leandro G, Malfertheiner P. Meta-analysis of bismuth quadruple therapy versus clarithromycin triple therapy for empiric primary treatment of Helicobacter pylori infection. Digestion. 2013;88(1):33-45. [ Links ]
27. Di Caro S, Fini L, Daoud Y, Grizzi F, Gasbarrini A, De Lorenzo A, et al. Levofloxacin/amoxicillin-based schemes versus quadruple therapy for Helicobacter pylori eradication in second-line. World J Gastroenterol. 2012 Oct 28;18(40):5669-78. [ Links ]
28. Zheng X, Lyu L, Mei Z. Lactobacillus-containing probiotic supplementation increases Helicobacter pylori eradication rate: Evidence from a meta-analysis. Rev Esp Enferm Dig. 2013 Sep;105(8):445-53. [ Links ]
29. Nishizawa T, Nishizawa Y, Yahagi N, Kanai T, Takahashi M, Suzuki H. Effect of supplementation with rebamipide for Helicobacter pylori eradication therapy: A systematic review and meta-analysis. J Gastroenterol Hepatol. 2014 Dec;29 Suppl 4:20-4. [ Links ]
30. Bouziane A, Ahid S, Abouqal R, Ennibi O. Effect of periodontal therapy on prevention of gastric Helicobacter pylori recurrence: A systematic review and meta-analysis. J Clin Periodontol. 2012 Dec;39(12):1166-73. [ Links ]
31. Gatta L, Vakil N, Vaira D, Scarpignato C. Global eradication rates for Helicobacter pylori infection: Systematic review and meta-analysis of sequential therapy. BMJ. 2013;347:f4587. [ Links ]
32. Harb AH, Chalhoub JM, Abou Mrad R, Sharara AI. Systematic review and meta-analysis: Full- versus half-dose anti-microbials in clarithromycin-based regimens for Helicobacter pylori eradication. Aliment Pharmacol Ther. 2015 Jul;42(2):131-41. [ Links ]
33. Chen HN, Wang Z, Li X, Zhou ZG. Helicobacter pylori eradication cannot reduce the risk of gastric cancer in patients with intestinal metaplasia and dysplasia: Evidence from a meta-analysis. Gastric Cancer. 2015 Jan 22. [ Links ]
34. Wong BC, Lam SK, Wong WM, Chen JS, Zheng TT, Feng RE, et al. Helicobacter pylori eradication to prevent gastric cancer in a high-risk region of China: A randomized controlled trial. JAMA. 2004 Jan 14;291(2):187-94. [ Links ]
35. Zhao B, Zhao J, Cheng WF, Shi WJ, Liu W, Pan XL, et al. Efficacy of Helicobacter pylori eradication therapy on functional dyspepsia: A meta-analysis of randomized controlled studies with 12-month follow-up. J Clin Gastroenterol. 2014 Mar;48(3):241-7. [ Links ]
36. Gisbert JP, Calvet X, Ferrandiz J, Mascort J, Alonso-Coello P, Marzo M. [Clinical practice guideline on the management of patients with dyspepsia. Update 2012]. Gastroenterol Hepatol. 2012 Dec;35(10):725 e1-38. [ Links ]
37. Wotherspoon AC, Doglioni C, Diss TC, Pan L, Moschini A, de Boni M, et al. Regression of primary low-grade B-cell gastric lymphoma of mucosa-associated lymphoid tissue type after eradication of Helicobacter pylori. Lancet. 1993 Sep 4;342(8871):575-7. [ Links ]
38. Gisbert JP, Romano M, Gravina AG, et al. Helicobacter pylori second-line rescue therapy with levofloxacin-and bismuth-containing quadruple therapy, after failure of standard triple or non-bismuth quadruple treatments. Aliment Pharmacol Ther. 2015; early Rel. Doi:10.111/apt.13128 [ Links ]













