Introducción
El trasplante de hígado (TH) es actualmente el tratamiento de elección para pacientes con insuficiencia hepática crónica, insuficiencia hepática aguda con indicadores de mal pronóstico, tumores hepáticos primarios seleccionados y para algunos pacientes con errores innatos en el metabolismo 1,2.
Los pacientes con disfunción hepática crónica cursan con regulación de la glucemia alterada, secundaria a hiperinsulinemia y resistencia a la insulina, mecanismos responsables de la diabetes hepatógena 3. Cuando los pacientes presentan insuficiencia hepática agudamente descompensada, cursan frecuentemente con hipoglucemia e hiperglucagonemia 4,5.
En el informe sobre TH de 2012 (Organ Procurement and Transplantation Network/Scientific Registry of Transplant Recipients [OPTN/SRTR]), cerca del 25% de los pacientes trasplantados tenía diabetes mellitus (DM) preexistente 6 y el 80% de los pacientes en lista de espera cursaban con resistencia a la insulina y alteraciones en el metabolismo de la glucosa 7.
La hiperglucemia se asocia con un incremento de la morbimortalidad, tasas más altas de infección, disfunción renal, disfunción del injerto, lesión hepática isquémica-reperfusión y complicaciones vasculares en pacientes trasplantados; a pesar de lo cual aún no hay evidencia contundente que permita establecer una guía de control glucémico 8. Actualmente, existen 2 recomendaciones con respecto al nivel de glucemia óptimo: el primero propone como meta un nivel de glucosa máximo de 180 mg/dL 9 y el segundo es la aceptación de niveles de glucosa hasta de 150 mg/dL 10. La Asociación Americana de Endocrinólogos Clínicos y la Asociación Americana de Diabetes (ADA) recomiendan iniciar infusión de insulina en pacientes críticamente enfermos con el objetivo de mantener niveles de glucemia <180 mg/dL 11.
Adicionalmente, en el TH se ha documentado una incidencia de diabetes postrasplante del 7% al 30%, que se asocia con diversos factores de riesgo como índice de masa corporal (IMC) pretrasplante >25 kg/m2; edad >40 años; afroamericanos e hispánicos; algunas asociaciones genéticas como polimorfismos en IRS-1, HNF-4, TCF7L2, KCNJ11-Kir6.2; inductores inflamatorios como la hepatitis B (VHB); incompatibilidad del complejo mayor de histocompatibilidad (HLA); episodios de rechazo; infección por citomegalovirus y el uso de inmunosupresores, en especial los inhibidores de la calcineurina, glucocorticoides y los inhibidores de mTOR 12.
Basados en publicaciones previas 13, el diagnóstico de diabetes postrasplante se puede establecer con cualquiera de los criterios de la ADA o de la Organización Mundial de la Salud (OMS) para el diagnóstico de DM (Tabla 1), una vez el paciente ha sido dado de alta y se haya titulado la inmunosupresión a dosis de mantenimiento. Sin embargo, la hemoglobina glucosilada (HbA1c) antes del primer año postrasplante no debe ser usada como criterio único dada su falta de exactitud diagnóstica en este período.
Tabla 1 Criterios de diagnóstico de diabetes en pacientes postrasplante

Tomado de: Shivaswamy V et al. Endocrine Reviews. 2016;37(1):37-61.
El objetivo principal de esta investigación fue determinar los valores de glucemia en cada una de las fases de la cirugía del TH y su relación con la presencia o no de diabetes pretrasplante, la aparición de infecciones, el rechazo del trasplante y la mortalidad postoperatoria.
Materiales y métodos
Diseño de estudio
Se realizó un estudio de cohorte retrospectivo con 73 pacientes adultos sometidos a TH de donantes cadavéricos en el Hospital San Vicente Fundación Rionegro entre octubre de 2013 y diciembre de 2015. Se excluyeron los pacientes que fallecieron durante la inducción anestésica (n = 3). El protocolo de investigación fue aprobado por la Unidad de Investigaciones y el Comité de Ética de la Investigación del Hospital San Vicente Fundación.
Protocolo del TH
El Hospital San Vicente Fundación es un referente nacional y regional para el desarrollo de trasplantes. En promedio, se realizan 26 TH al año de donantes cadavéricos.
Los TH se realizaron con hígados completos de donantes mediante técnica de piggyback sin derivación venovenosa. Se realizó anastomosis portoportal terminoterminal, y la anastomosis arterial se realizó después de la reperfusión del órgano; en su mayoría se usó histidina-triptofano-ketoglutarato (HTK) como solución de preservación; en casos aislados independientes, se usó la solución de la Universidad de Wisconsin.
Se monitorizó la glucemia central en todos los pacientes antes de entrar a salas de cirugía, el manejo anestésico se realizó según los protocolos del hospital, las transfusiones en el intraoperatorio se realizaron con base en los niveles de hematócrito y el uso de vasoactivos se indicó bajo parámetros hemodinámicos de los pacientes.
De forma intraoperatoria, se midieron los niveles de glucosa capilar con tiras de glucometría durante 3 fases: fase de hepatectomía, fase anhepática y fase posterior a la reperfusión del órgano. Con los datos obtenidos se definió el aporte de carbohidratos con dextrosa en agua destilada (DAD) al 10% o el inicio de infusión de insulina regular, cuya meta es mantener la glucemia intraoperatoria <180 mg/dL. Durante la fase anhepática se administró la infusión de 500 mg de metilprednisolona como protocolo de inmunosupresión.
Variables de estudio y fuentes de información
Los datos se obtuvieron del sistema de historia electrónica SAP, el cual permite el almacenamiento de la información de las historias clínicas de los pacientes del hospital. La información fue extraída de la historia clínica por los investigadores en un formato prediseñado con una estandarización previa.
Se tomaron variables demográficas (edad, género y año de trasplante) y variables clínicas: antecedente de diabetes pretrasplante, niveles de glucemias en fase inicial, en la fase anhepática y al final de la cirugía de trasplante, y clasificaciones Model for end-stage liver disease (MELD) y Child-Pugh. La escala MELD pretrasplante se calculó con la siguiente fórmula: R = 9,57 X loge [creatinina en mg/dL] + 3,78 x loge [bilirrubina en mg/dL] + 11,20 x loge [ratio internacional normalizado -INR-] + 6,43, tal como lo recomiendan Kamath y colaboradores 14.
Se tomaron datos adicionales de las historias clínicas con respecto a la infección en el período postoperatorio, órganos afectados y microorganismos identificados mediante cultivos. Se evaluó si se cumplían los criterios para el diagnóstico de diabetes postrasplante, si presentó rechazo del injerto y mortalidad global por cualquier causa.
Análisis estadístico
El procesamiento de los datos se realizó con el programa SPSS (IBM Corp. Released 2012. IBM SPSS Statistics for Windows, Version 21.0. Armonk, Nueva York: IBM Corp.). Para el análisis descriptivo univariado, las variables categóricas se expresaron en frecuencias absolutas y relativas. A las variables cuantitativas se les evaluó la normalidad en su distribución; para aquellas variables que se distribuían de forma normal se utilizaron medidas de tendencia central y dispersión como la media aritmética y desviación estándar; y las variables que no cumplían la condición de normalidad se describieron por medio de la mediana y rango intercuartílico (RIQ).
Se buscaron diferencias entre infección temprana, rechazo del trasplante y mortalidad en los primeros 30 días de trasplante entre pacientes con y sin diabetes antes del trasplante. Para la comparación de las variables cualitativas, se realizó la prueba de chi cuadrado (χ2) de Pearson. Para las variables cuantitativas se utilizó la prueba U Mann-Whitney de muestras independientes. En caso de medidas repetidas, se utilizó la prueba de Friedman. Se consideraron diferencias significativas aquellas con un valor de p <0,05.
Resultados
Se estudió un total de 73 pacientes sometidos a TH entre octubre de 2013 y diciembre de 2015. 12 trasplantes (16,4%) se realizaron en el año 2013, 31 (42,5%) en el año 2014 y 30 (42,1%) en el año 2015. El 54,8% (n = 40) eran de sexo masculino; la mediana de edad fue de 59 años (RIQ: 52-63,5) con una edad mínima de 33 años y una máxima de 71 años. Del total de pacientes trasplantados, el 90,4% correspondió a TH y los restantes a trasplante combinado de hígado y riñón.
La mediana de puntaje MELD fue 22 (RIQ: 16-24); con respecto a la clasificación Child-Pugh, la mayoría de los pacientes (41,1%, n = 30) estaba en la categoría C de esta clasificación, seguida del 28,8% (n = 21) para clasificación B.
Del total de pacientes estudiados, 24 (32,9%) tenían antecedente de DM al momento del TH. No se encontraron diferencias en el puntaje MELD (p = 0,104, U Mann-Whitney de muestras independientes) ni en la clasificación Child-Pugh entre los pacientes diabéticos y no diabéticos antes del trasplante (Tabla 2).
Tabla 2 Características demográficas y severidad del compromiso hepático
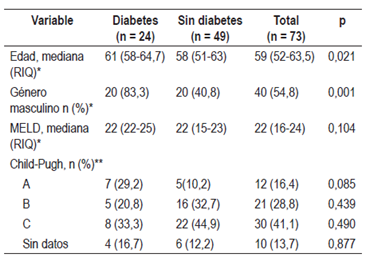
*U Mann-Whitney de muestras independientes. **χ2 de Pearson. Significancia: p <0,05.
Se evaluaron las glucemias en fase inicial del trasplante, fase anhepática y al final de la cirugía de trasplante, y se encontró un incremento significativo en los niveles de glucemia tanto en los pacientes con diabetes establecida antes del trasplante como en los no diabéticos (p <0,000, prueba de Friedman). En los pacientes diabéticos, la glucemia en la fase inicial fue de 127 mg/dL (RIQ: 111-167) y en la final de 212 mg/dL (RIQ: 169-264) (p = 0,001, prueba de Friedman); mientras que en los pacientes no diabéticos, la glucemia inicial fue de 105 mg/dL (RIQ: 88-122) en comparación con una glucemia final de 190 mg/dL (RIQ: 149-236) (p <0,000, prueba de Friedman) (Tabla 3).
Tabla 3 Niveles de glucemia según la fase del trasplante y antecedente de diabetes pretrasplante

*Mediana (RIQ). **Prueba de Friedman, significancia: p <0,05.
La variación de las glucemias durante las fases del trasplante fue de mayor magnitud en los pacientes no diabéticos en comparación con los no diabéticos. Cuando se compararon los niveles de glucemia en la fase final con respecto a la inicial en los pacientes diabéticos (84,5 mg/dL) frente a los no diabéticos (85 mg/dL), no se encontró diferencia estadísticamente significativa (p = 0,690).
En el análisis estratificado de glucemia, en las 3 fases de TH en pacientes diabéticos frente a los no diabéticos, la mayor proporción de los pacientes presentó glucemias en la fase inicial entre 71 y 140 mg/dL (82,2%) y en la fase final >180 mg/dL (61,6%). No se encontró diferencia estadísticamente significativa entre los grupos (Tabla 4).
Tabla 4 Estratificación de niveles de glucemia según la fase del trasplante y antecedente de diabetes pretrasplante

*χ2 de Pearson, significancia: p <0,05.
Se evaluó la aparición de infecciones luego del trasplante y se encontró una mayor proporción en pacientes diabéticos (50%), en comparación con los no diabéticos (44,9%). Al evaluar la presencia de infección postrasplante según los rangos de glucemia en los pacientes diabéticos y no diabéticos en la fase inicial, no se encontraron diferencias significativas (Tabla 5), ni tampoco en relación con los niveles de glucemia en cada una de las fases del trasplante, tanto en pacientes diabéticos como no diabéticos (Tabla 6).
Tabla 5 Presencia o no de infección según presencia o no de diabetes, de acuerdo con los niveles de glucemia en la fase inicial del trasplante

*χ2 de Pearson, significancia: p <0,05.
Tabla 6 Relación de niveles de glucemia e infección en pacientes con TH

*Mediana (RIQ). **Prueba U Mann-Whitney, significancia: p <0,05.
Con respecto al tipo de infección, la mayoría fue más frecuente en los pacientes diabéticos, pero llama la atención el hallazgo de infección del tracto urinario más frecuente en pacientes no diabéticos (16,3%) frente a los diabéticos (8,3%) (Tabla 7).
Tabla 7 Infección postquirúrgica según antecedentes de diabetes pretrasplante

*Estadística de Fisher. **Significancia: p <0,05. ISO: infección del sitio operatorio; ITU: infección del tracto urinario.
La proporción global de rechazo del injerto fue del 11%, más frecuentemente en los pacientes diabéticos (14,3%) en comparación con los no diabéticos (4,2%) (p = 0,258, estadística de Fisher). La mortalidad global fue de 34,2%, más frecuentemente en los pacientes diabéticos (45,8%) en comparación con los no diabéticos (28,6%) (p = 0,191, estadística de Fisher).
Durante el seguimiento ambulatorio de los pacientes, 11 (15,1%) cumplieron los criterios para diabetes postrasplante. Sin embargo, es importante para el análisis que en el 16,4% de las historias clínicas revisadas no se encontró ningún registro del seguimiento glucémico.
Discusión
La resistencia a la insulina 15 y la hiperglucemia 16 se asocian fuertemente con el incremento de la morbimortalidad perioperatoria en cirugías abdominales mayores incluido el TH 17. Sin embargo, hay factores que teóricamente sugieren mayor impacto metabólico perioperatorio en estos pacientes: la fisiopatología en la enfermedad hepática, que cursa con hiperinsulinemia e hiperglucagonemia 18; los cambios metabólicos que sufre el hígado nativo y el donado; la infusión de dosis altas de glucocorticoides y el estrés quirúrgico 19.
Al analizar el puntaje de nuestros pacientes medido por las escalas MELD y Child-Pugh, los hallazgos fueron similares a los informados en otros estudios 20. En nuestra institución, los pacientes trasplantados fueron quienes estaban más gravemente enfermos de acuerdo con la escala de Child-Pugh. Estudios previos han reportado una relación entre el puntaje de gravedad de la enfermedad y los niveles de glucemia antes de la cirugía 21.
La diabetes hepatógena se presenta en el 30%-60% de los pacientes con cirrosis 3. En nuestro estudio, los pacientes con diabetes antes del trasplante tenían niveles de glucosa más elevados con respecto a los no diabéticos. Así mismo, se encontró un incremento de la glucemia durante el procedimiento quirúrgico, lo que es esperable por el trauma quirúrgico y los bolos de glucocorticoides. Cabe anotar que en el postoperatorio hubo una disminución progresiva de la glucemia y alcanzó un adecuado control glucémico tanto en diabéticos como en no diabéticos, hallazgo explicable por el tratamiento intraoperatorio y postoperatorio por parte del anestesiólogo.
Los estudios previos han demostrado que la glucemia elevada se asocia con mayor incidencia de complicaciones postoperatorias incluidas la infección del sitio operatorio, retraso en la cicatrización y mayor mortalidad 22,23. En nuestro análisis no se encontró una asociación entre las glucemias elevadas durante el trasplante y el desarrollo de infecciones, hallazgo similar al encontrado por otros autores 24. Estos resultados se pueden deber al tamaño de muestra pequeño.
Antes del trasplante, los pacientes con diabetes tenían glucemias más elevadas. Durante el procedimiento y al final del mismo se lograron glucemias similares, lo cual podría explicar que la tasa de complicaciones encontrada al final del estudio en ambos grupos no fuera estadísticamente diferente.
A pesar del efecto proinflamatorio descrito en la diabetes hepatogénica, que estimula las vías de señalización intracelular [cinasa Janus/transductor de señal y activador de la transcripción (JAK/STAT), fosfato de dinucleótido de nicotinamida y adenina (NADPH) oxidasa, proteína cinasa activada por mitógenos (MAPK), cinasa reguladora de señales extracelulares (ERK) y cinasa c-Jun N-terminal (JNK)] con la activación de factores de transcripción que permiten el incremento de la expresión de citocinas y factores de crecimiento, y la potenciación de la respuesta inmunológica al cuerpo extraño 25; en nuestro análisis se encontró que dicha respuesta fue más frecuente en los pacientes no diabéticos previos al trasplante.
Adicionalmente, no se encontró relación entre los niveles de glucemia en cada una de las fases y la presencia de rechazos, por lo que tampoco requirieron modificaciones en el manejo inmunosupresor para evitarlos, tal como lo recomiendan varios autores 26.
Un hallazgo bastante interesante fue la mayor tasa de mortalidad de origen cardiovascular en los pacientes diabéticos previos al trasplante en comparación con aquellos que no tenían dicho antecedente, lo que también ha sido demostrado en múltiples estudios previos en los que se considera la diabetes como un factor de riesgo para el compromiso micro y macrovascular, la cual se pone a prueba en un estado de estrés metabólico tan alto como lo es el TH 27.
Al analizar los datos de diabetes postrasplante, se encontraron bastantes problemas en la consecución de los datos; sin embargo, el 15,1% de los pacientes diagnosticados con diabetes postrasplante corresponde al reportado en la literatura mundial 28, que sigue las recomendaciones de la ADA y la OMS 29.
A pesar de ser un estudio retrospectivo con una limitante importante en la consecución de los datos, se encontraron datos llamativos que invitan a los grupos de TH a analizar sus estadísticas con base en los niveles de glucemia y en el desarrollo de diabetes postrasplante.
Conclusiones
Después del análisis retrospectivo en un hospital del cuarto nivel en Colombia, se identificó un buen control glucémico en las diferentes fases del TH en los pacientes con DM preexistente, posiblemente por el esquema de tratamiento utilizado por la institución, lo cual permite adecuados niveles de glucosa durante las diferentes fases de la cirugía.
No se evidenció una relación entre los niveles de glucemia con el incremento en la mortalidad ni la incidencia de infecciones al comparar el grupo de pacientes con diabetes preexistente con el grupo de no diabéticos; se considera que esto es consecuencia de un adecuado control glucémico en los pacientes analizados.
A pesar de lo anterior, en el grupo de pacientes con DM hubo mayor mortalidad global, atribuible en su mayor parte a la enfermedad cardiovascular.
Con respecto a la tasa de rechazo del injerto, no se encontraron diferencias estadísticamente significativas entre los grupos. Se requieren estudios adicionales con mayor número de pacientes y a más largo plazo para evaluar este aspecto.
Por último, el hallazgo de la incidencia de DM postrasplante en nuestro análisis fue similar al de otras cohortes, incluso puede existir subregistro por falta de datos en algunas de las historias clínicas; esto plantea la necesidad de su búsqueda activa en los pacientes.











 text in
text in 


