Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Agronomía Colombiana
Print version ISSN 0120-9965
Agron. colomb. vol.26 no.1 Bogotá Jan./June 2008
FITOMEJORAMIENTO, RECURSOS GENÉTICOS Y BIOLOGÍA MOLECULAR
Teresa Mosquera1, Cristhian Fernández2, Lizeth Martínez3, Andrea Acuña3 y David Cuéllar4
1 Profesora asociada, Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. tmosquerav@unal.edu.co
2 Programa de Maestría en Ciencias Agrarias, Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. jhcristhian@gmail.com
3 Estudiantes, Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. licethmartinez@gmail.com; andreacunag@gmail.com
4 Profesor especial, Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. dcuellarg@unal.edu.co
Fecha de recepción: agosto 2 de 2007. Aceptado para publicación: abril 9 de 2008
RESUMEN
Este artículo presenta una revisión de la resistencia en papa a patógenos, en cuanto a genes mapeados y clonados, y loci de rasgos cuantitativos (QTL) mapeados, en la que se resaltan las relaciones entre resistencia cuantitativa y cualitativa en el caso P. infestans. El conocimiento logrado ha permitido generar un mapa funcional sobre el cual se localizan QTL para resistencia a patógenos. Se han mapeado 20 genes R de resistencia a virus, hongos, nematodos y oomicetos, utilizando marcadores moleculares. La mayoría de estos genes R fueron introducidos de especies silvestres. Catorce de ellos se encuentran en hot spots para resistencia y confieren resistencia a varios patógenos. A la fecha se han identificado cinco clusters de resistencia. La resistencia monogénica envuelve dos procesos básicos: percepción del ataque del patógeno, seguida de una respuesta para limitar la enfermedad. La percepción implica receptores específicos para cepas patogénicas, que son decodificadas por genes de resistencia. En una planta se encuentra un gran repertorio de genes de resistencia R, ubicados en diferentes sitios del genoma. Estos genes expresan diferentes proteínas que pueden ser agrupadas en varias familias. La mayoría de proteínas R contienen repeticiones en grupos, ricas en leucina (LRR). Se plantea la colocalización de genes R y QTL en diferentes cromosomas. Una hipótesis señala que los QTL son variantes alélicas con efecto menos extremo que los genes R y una segunda hipótesis plantea que los QTL de resistencia mapean en regiones del genoma que contienen genes de función conocida involucrados en la respuesta general al ataque de patógenos.
Palabras clave: resistencia cuantitativa, resistencia cualitativa, genes de resistencia, QTL, genes mayores.
ABSTRACT
This review is about the genetics of the Solanum tuberosum pathogen resistance, underlying the relationship between quantitative and qualitative resistance in the P. infestans case. The knowledge obtained permits to generate a functional map localizing chromosomal regions for the pathogen resistance loci. Twenty R genes of resistance for viruses, fungi, nematodes and oomycetes using molecular markers were mapped. Most of these R genes were introduced from wild species. From them, fourteen are localized in hot spots and they confer resistance to several pathogens. To date five clusters of resistance have been identified. Monogenic resistance includes two basic processes: perception of a pathogen attack followed by a response to limit the disease. The perception implies specific receptors for pathogenic strains decodified by resistance genes. There is a large amount of R genes situated in one plant and localized in different places of the genome. These genes express different proteins. Most of the R proteins contain tandem repeats, leucine rich (LRR). The co-localization of R genes and QTL in different chromosomes have been found. One hypothesis points out that QTL are allelic variants with less extreme effect than R genes. A second hypothesis points out that resistance QTL are mapped in the regions of genome that contain known functions genes involved in a general response for the pathogen attack.
Key words: quantitative resistance, qualitative resistance, resistance genes, QTL, major genes.
Introducción
El cultivo de la papa es atacado por varios patógenos, entre los que se encuentran virus, hongos, bacterias, nematodos y el oomiceto Phytophthora infestans que causa la enfermedad más severa en el mundo. El valor de las pérdidas de la producción global anual y los costos de protección del cultivo se estiman en cinco billones de dólares (Duncan, 1999; Turkensteen y Flier, 2002).
Centros de investigación y de mejoramiento de cultivos están introduciendo en sus rutinas la selección asistida por marcadores, ya que la mayoría de los rasgos importantes en los cultivos tales como producción, calidad y algunas formas de resistencia a enfermedades son controlados por genes que pueden asociarse a marcadores moleculares (Collard et al., 2005). En los últimos 15 años, gracias al advenimiento de los marcadores moleculares, se ha ampliado el conocimiento de la resistencia en papa. Con la información aportada a partir de tales estudios se ha podido generar un mapa funcional que contiene las regiones cromosomales para estos loci (Gebhardt y Valkonen, 2001) (figura 1).
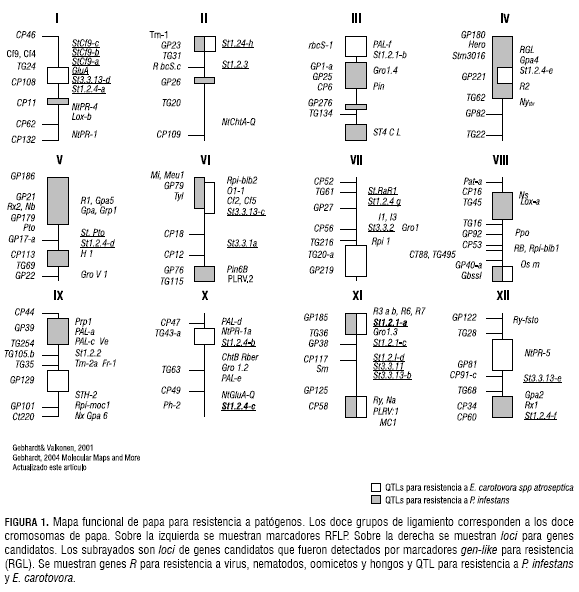
Este artículo presenta una revisión del estado del arte de la resistencia en papa a patógenos, en cuanto a genes mapeados y clonados y QTL mapeados, en la que se destacan las relaciones entre resistencia cuantitativa y cualitativa en el caso P. infestans.
En papa se han encontrado dos tipos de resistencia genética a patógenos: la de hipersensibilidad —denominada también cualitativa o monogénica— y la resistencia cuantitativa, de campo o poligénica (Bormann, 2004). La resistencia monogénica involucra dos procesos básicos: percepción del ataque del patógeno y una respuesta para limitar la enfermedad. La percepción implica receptores específicos para cepas patogénicas, que son decodificadas por genes de resistencia. En una planta se encuentra un gran repertorio de genes de resistencia ubicados en diferentes sitios del genoma (Gebhard y Valkonen, 2001). A la fecha se han clonado varios genes R. Estos genes expresan diferentes proteínas que pueden ser agrupadas en varias familias. La mayoría de proteínas R contiene repeticiones en grupos, ricas en leucina (LRR), las cuales pueden tener un papel importante en el reconocimiento específico. La familia más grande de proteínas R (NB-LRR) posee adicionalmente al LRR un sitio de unión a nucleótido (NB).
La generación de genes R de resistencia cualitativa polimórfica involucra duplicación de genes, seguida de divergencia en la secuencia de ADN por mutación puntual y por deleción y duplicación de repeticiones de ADN intragénico. La recombinación de estos genes asegura variación para generar diversidad en la secuencia de genes. La presión del patógeno selecciona especificidad funcional de la resistencia y da como consecuencia diversidad de genes R (Ellis et al., 2000). Por ejemplo, la clonación del gen RPP13 de Arabidopsis thaliana de resistencia a Peronospora parasítica, reportado por Bittner et al. (2000), muestra tres especificidades identificadas en un locus, el cual parece ser un gen simple con múltiples alelos, muy variables, que están sujetos a selección diversificadora. Este es un mecanismo que, evolutivamente, conduce a que genes de resistencia se presenten concentrados en regiones de los cromosomas.
La resistencia cuantitativa, a diferencia de la cualitativa, es controlada por loci de rasgos cuantitativos (QTL) o por varios genes (Agrios, 2005; Collard et al., 2005) y comprende reacciones diferentes que incluyen: velocidad de penetración, restricciones a la penetración, restricciones a la tasa de invasión del tejido celular y velocidad de esporulación del patógeno en la planta. Estos genes actúan juntos para la defensa de la planta y la actuación de un gen puede ser insuficiente si se expresa solo. Cada planta tiene un cierto nivel de resistencia cuantitativa que responde a diferentes patógenos (no específicos). Este tipo de resistencia no es absoluta, sino que atenúa o detiene el progreso de la enfermedad y puede ser afectada por cambios en el ambiente (Agrios, 2005). Gebhardt y Valkonen (2001) sugirieron que genes similares a los R pueden contribuir a la resistencia cuantitativa. En papa se ha encontrado que 18 QTL contribuyen a resistencia cuantitativa, aunque en cada caso sólo actúan entre uno y cuatro QTL.
Recientemente, se está utilizando con éxito el mapeo por asociación, para precisar la ubicación de QTL, el cual no utiliza poblaciones segregantes, sino colecciones de germoplasma, y emplea el concepto de ligamiento en desequilibrio. También los progresos técnicos en el área de la biología molecular y la genómica han hecho posible la clonación de QTL, lo que permite conocer tanto las secuencias codificantes como no codificantes de ADN de dichos QTL (Salvi y Tuberosa, 2005).
Genes que confieren resistencia cualitativa en papa
En papa se han mapeado 20 genes de resistencia a virus, nematodos y oomicetos (tablas 1 y 2), utilizando marcadores moleculares. La mayoría de estos genes R fueron introducidos de especies silvestres. Otros genes de resistencia al nematodo de la agalla de la raíz, Globodera pallida, patotipos Pa2 y Pa3, de S. spegazinii han sido mapeados (Kreike et al., 1994; Rouppe van der Voort et al., 1997; 2000) y el gen R MC1, que confiere resistencia a Meloidogyne chitwoodi, se localizó en el cromosoma XI (Brown et al., 1996). De los 20 genes R mapeados, catorce se encuentran en hot spots para resistencia. Gebhardt y Valkonen (2001) observaron que muchos genes R están organizados en clusters de genes de resistencia y que confieren resistencia a varios patógenos. A la fecha se han identificado cinco clusters de resistencia:
• Los genes R1 (P. infestans), Rx2 y Nb (PVX), en la región proximal en el cromosoma V.
• Los genes H1 y GroV1 (G. rostochiensis), en el brazo largo del cromosoma V.
• Los genes R3, R6, y R7 (P. infestans), en el brazo corto posición distal del cromosoma XI.
• Los genes Ryadg (PVY), Naadg (PVA), RMcl (M. chitwoodi) y Sen1 (Synchytrium endobioticum), en el brazo corto posición distal de cromosoma XI.
• Los genes Rx1 (PVX) y Gpa2 (G. pallida) (Gebhardt y Valkonen, 2001), en el brazo largo posición distal del cromosoma XII.

Para la resistencia cualitativa a P. infestans, se han identificado once genes que provienen de la especie silvestre S. demissum, los cuales inducen respuesta hipersensible (HR) a la infección con razas específicas de P. infestans (Malcolmson y Black, 1966). Estos genes se han mapeado: R1, en el cromosoma V (Leonard-Schippers et al., 1992); R2, en el cromosoma IV (Li et al., 1998); R3, R3b, R5, R6 y R7, R8, R9, R10 y R11, agrupados en el cromosoma XI (El- Kharbotly et al., 1994; El-Kharbotly et al., 1996; Huang et al., 2004; Huang, 2005). Recientemente, han sido reportados otros genes R que confieren resistencia a P. infestans y cuya resistencia es derivada de fuentes diferentes a S. demissum (tabla 2).

Los genes que han sido clonados a la fecha y que confieren resistencia a diferentes patógenos en S. tuberosum se presentan en la tabla 3. El primer gen clonado y caracterizado que confiere resistencia raza específica a P. infestans es el gen R1 (Ballvora et al., 2002). Este gen, es un gen mayor miembro de la superfamilia de genes de resistencia, caracterizados por una coiled coil (CC), un nucleótido de unión (NB) y un dominio de repeticiones ricas en leucina (LRR) (Ballvora et al., 2002; Chrisholm et al., 2006; Ballvora et al., 2007). Este gen codifica para una proteína de 1293 aminoácidos. En contraste con el alelo r1, susceptible, el R1 tiene una inserción grande de un gen funcional R (Ballvora et al., 2002). Adicionalmente, se han encontrado interacciones entre locus y entre alelos marcadores ligados al cluster de genes tipo NB-LRR. Se destacan las interacciones observadas entre marcadores del locus R1 para resistencia a P. infestans en el cromosoma V y otros siete loci en diferentes cromosomas, entre los cuales está el locus Gro1 de resistencia a nematodos en el cromosoma VII (Paal et al., 2004). El locus Gro1 ocupa una posición similar a la del locus Rpi1 para resistencia a P. infestans (Kuhl et al., 2001).

Si la familia de genes tipo NB-LRR es causal de QTL para resistencia, las interacciones fenotípicas observadas entre los loci pueden indicar interacción física entre dos o más proteínas tipo NB-LRR. La especificidad y la cinética de reconocimiento del patógeno, la transducción de señales y las respuestas de defensa pueden ser determinadas de manera cuantitativa por la composición de la subunidad de tales complejos de reconocimiento. La respuesta de resistencia cualitativa sería nada más que una reacción extremadamente rápida disparada por un complejo de reconocimiento, incluyendo un gen R (Robertson et al., 1985). Los complejos de reconocimiento se han propuesto para explicar la imposibilidad de encontrar in vitro una interacción específica entre un único gen R que tenga un dominio LRR y el correspondiente producto del gen de virulencia (McDowell y Woffenden, 2003). A nivel molecular, no ha sido identificada aún ninguna interacción entre pares de genes de resistencia en plantas tipo NB-LRR (Bormann et al., 2004).
QTL que confieren resistencia cuantitativa en papa
Se han realizado esfuerzos en diferentes especies, tendientes a la clonación de QTL, que han hecho posible que QTL puedan ser analizados cuidadosamente a nivel molecular (Salvi y Tuberosa, 2005). Para avanzar en este sentido, Ballvora et al. (2007) reportan la secuencia genómica parcial para la región comprendida entre los marcadores GP21 y GP179 (figura 2) sobre el cromosoma V, región reportada por localizar el QTL de mayor reproducibilidad para resistencia a P. infestans y localizar con genes R (Gebhardt y Valkonen, 2001; Ghislain et al., 2001; Bormann et al., 2004). La anotación funcional de esta secuencia identificó 48 ORF (fragmentos abiertos de lectura) en un contig y 22 en el otro. Diez ORF fueron clasificados como resistance like genes; once, como genes que contienen proteínas F-box; trece, como elementos transponibles y tres, como factores de transcripción. Las proteínas F-box se encontraron para el gen R1, pero ninguna de ellas se encontró en el r1. Estas proteínas están involucradas en varias vías de señalización en A. thaliana y, recientemente, se han sugerido dichas proteínas como receptores para varias hormonas de plantas (Kepinski y Leyser, 2005). Además, se identificó un dominio F-box en la proteína STG1 que juega un papel importante como chaperona en la estabilización de proteínas R (Shirazu y Schulze-Lefert, 2000; Schulze-Lefert, 2004).

En relación a la determinación de loci para rasgos cuantitativos para resistencia a P. infestans, se han realizado varios estudios con poblaciones diploides (Collins et al., 1999; Ewing et al., 2000; Ghislain et al., 2001; Leonardo-Schippers et al., 1994; Oberhagemann et al., 1999; Sandbrink et al., 2000; Trognitz et al., 2002; Visker et al., 2003b; Mosquera, 2007) y uno con una población tetraploide (Meyer et al., 1998). Estos estudios sobre resistencia cuantitativa a P. infestans han identificado QTL en los doce cromosomas de la papa. El QTL del cromosoma V tiene el mayor efecto y es el más reproducible (Gebhardt y Valkonen, 2001; Ghislain et al., 2001; Bormann et al., 2004). Un locus mayor, Gpa, fue mapeado para el cromosoma V y dos loci menores fueron mapeados en los cromosomas IV y VII (Barone et al., 1990). Dos QTL involucrados en resistencia a Globodera rostochiensis, patotipo R01, fueron mapeados para los cromosomas X y XI del genoma de papa (Gebhardt y Valkonen, 2001). En la tabla 4, se presentan los QTL mapeados en papa para resistencia a P. infestans. Gebhard y Valkonen (2001) resaltan que la resistencia cuantitativa contra P. infestans y E. carotovora es controlada por QTL de efecto pequeño a lo largo de los doce cromosomas, mientras que la resistencia cuantitativa a nematodos parece estar controlada por pocos QTL con efectos grandes.

Otros candidatos para participar en el control de resistencia cuantitativa a P. infestans lo constituyen los genes funcionales en la respuesta de defensa (Leonards-Schippers et al., 1994; Trognitz et al., 2002), tales como glutation S-transferasa (Hahn y Strittmatter, 1994) que codifica en el locus Prp1, en la posición distal del brazo corto del cromosoma IX, genes para fenilalanina amonio liasa (Hahlbrock y Scheel, 1989), que mapean en la misma región, como el Prp1 (Gebhardt et al., 1991), y genes como osmotina, localizados en la posición distal del brazo largo del cromosoma VIII y en la posición proximal del cromosoma XI (Castillo-Ruiz, 2002). El reconocimiento de patógenos y las respuestas de defensa están conectados por redes de transducción de señales (McDowell y Woffenden, 2003). La variación alélica en una parte de la red puede tener efectos diferenciales sobre la variación alélica que afecta otras partes. Esta explicación se puede considerar como un modelo molecular de la interacción observada entre los QTL de resistencia no ligados.
Relaciones genéticas entre resistencia cuantitativa y cualitativa en papa
El empleo de genes R, contra P. infestans ha sido abandonado por los fitomejoradores a favor del empleo de genes de resistencia cuantitativa. La comprensión de las bases genéticas de la resistencia cuantitativa abre la posibilidad de explotar información sobre la ubicación de factores genéticos positivos y negativos que afectan la resistencia, útil para la selección asistida con marcadores moleculares (Collins et al., 1999; Mosquera, 2007).
Varios QTL que determinan resistencia a diferentes patógenos han sido ubicados en regiones en donde se presentan genes R, genes PR y genes de defensa, de donde se presume que las mismas clases de genes podrían estar involucradas en ambos tipos de resistencia, cualitativa y cuantitativa y que, posiblemente, la variación en algunos alelos cause varios grados de resistencia (Gerbhardt y Valkonen, 2001). Estos autores, basándose en el estudio de un cluster genético con genes R, plantearon que los QTL para resistencia tienen una base molecular similar a los genes R. El mapeo de genes de papa con secuencia similar a genes R clonados de otras plantas y otros relacionados con defensa revelan ligamiento entre genes candidatos, genes R y QTL para resistencia. Un ejemplo bien conocido de colocalización lo constituye la parte distal del cromosoma V, región de gran actividad genética que se conoce como hot spot del cromosoma V (figura 2). En este hot spot se localiza un cluster de QTL para resistencia a P. infestans y a nematodos y colocalizan genes R para resistencia a P. infestans, nematodos y virus (Bendahmane et al., 2000; De Jong et al., 1997; Ritter et al., 1991; Gebhardt et al., 1993; Ballvora et al., 2002).
Se han dado dos explicaciones para la localización de genes que actúan sobre la resistencia de campo. La primera, la colocalización de QTL de resistencia con genes R mapeados, ha conducido a la propuesta que los QTL son variantes alélicas menos extremas que los genes R (Leonards-Schippers et al., 1994). La segunda, algunos QTL de resistencia mapean en regiones del genoma que contienen genes de función conocida involucrados en la respuesta general al ataque de patógenos o al estrés (Collins et al., 1999).
Un estudio de mapeo comparativo entre genes de resistencia a enfermedades de la familia Solanaceae (pimiento, papa y tomate) reveló que los genes R tienden a estar agrupados (Grube et al., 2000). Los clusters de genes de resistencia a enfermedades parecen estar en posiciones cromosomales coincidentes con QTL para resistencia a tizón tardío, detectados en tomate, lb1a, lb3, lb4, lb5b, lb11b (Brouwer et al., 2004). Los QTL lb4 y lb11b también parecen colocalizar con clusters en papa que contienen loci R, conocidos por conferir resistencia a aislamientos específicos de P. infestans (Grube et al., 2000; Gebhardt y Valkonen, 2001). Por otra parte, en un estudio de QTL para resistencia parcial a Xanthomonas oryzae pv. oryzae en arroz, se encontró que genes R derrotados actúan como QTL, confiriendo resistencia parcial (Li et al., 1999). Estudios más detallados sugieren que los genes R tipo NB-LRR podrían explicar las bases moleculares de la resistencia cuantitativa.
Perspectivas
El conocimiento referido a genes y QTL que controlan resistencia a diferentes patógenos, en S. tuberosum ha avanzado sensiblemente en los últimos 15 años. Se ha avanzado en el mapeo de genes, de QTL y en la clonación de algunos genes de resistencia, no obstante, la comprensión a nivel molecular de cómo actúan y se interrelacionan los diferentes genes para responder al ataque de los patógenos aún no es clara. Los modelos para rasgos cuantitativos describen fenómenos complejos relacionados con una totalidad, mientras que los genes allí contenidos no se conocen o permanecen en lo que ha sido definido como una niebla estadística (Mauricio, 2001). Tampoco son claras las fronteras entre la resistencia cualitativa y cuantitativa, aunque se plantean hipótesis plausibles que las relacionan.
La investigación sobre la genética de la variación en papa continúa de tal manera que incrementará el conocimiento de las colecciones de germoplasma, lo cual facilitará su uso en programas de mejoramiento y de ingeniería genética. Por ejemplo, grupos de investigación buscan nuevas fuentes de resistencia genética a patógenos, y es así como en el cromosoma IV de varias especies de papa se reportan QTL para resistencia a P. infestans con efecto mayor que podrían contener genes novedosos (Lokossou et al., 2007).
Literatura citada
Agrios, G. 2005. Plant pathology. 5th edition. Elsevier Academic Press, Nueva York. 922 p. [ Links ]
Ballvora, A., M.R. Ercolano, J. Weiss, K. Meksem, C.A. Bormann, P. Oberhagemann, F. Salamini y C. Gerbhardt. 2002. The R1 Gene for potato resistance to late blight (Phytophthora infestans) belongs to the leucine Zipper/NBS/LRR class of plant resistance genes. Plant J. 30, 261-371. [ Links ]
Ballvora, A., A. Jöcker, P. Viehöver, H. Ishihara, J. Paal, K. Meksem, R. Bruggmann, H. Schoof, B. Weisshaar y C. Gerbhardt. 2007. Comparative sequence analysis of Solanum and Arabidopsis in a hot spot for pathogen resistance on potato chromosome V reveals a patchwork of conserved and rapidly evolving genome segments. BMC Genomics 8, 112 doi: 10.1186/1471- 2164-8-112. [ Links ]
Barone, A., E. Ritter, U. Schachtschabel, T. Debener, F. Salamini y C. Gebhardt. 1990. Localization by restriction fragment length polymorphism mapping in potato of a major dominant gene conferring resistance to the potato cyst nematode Globodera rostochiensis. Mol. Gen. Genet. 224, 177-182. [ Links ]
Bendahmane A., K. Kanyuca y D.C. Baulcombe. 1999. The Rx gene from potato controls separate virus resistance and cell death responses. Plant Cell 11, 781-791. [ Links ]
Bendahmane A., M. Querci, K. Kanyuca y D.C. Baulcombe. 2000. Agrobacterium transient expression system as a tool for the isolation of disease resistance genes: application to the Rx2 locus in potato. Plant J. 21, 73-81. [ Links ]
Bittner-Eddy P.D., I.R. Crute, E.B. Holub y J.L. Beynon. 2000. RPP13 is a simple locus in Arabidopsis thaliana for alleles that specify downy mildew resistance to different avirulence determinants in Peronospora parasitica. Plant J. 21, 177-188. [ Links ]
Bormann, C.A., A.M. Rickert, R.A. Castillo, J. Paal, J. Lübeck, J. Strahwald, K. Buhr y C. Gebhardt. 2004. Tagging quantitative trait loci for maturity-corrected late blight resistance in tetraploid potato with PCR-based candidate gene markers. Mol. Plant Microbe Interactions 17(10), 1126-1138. [ Links ]
Brigneti, G., J. Garcia-Mas y D. C. Baulcombe. 1997. Molecular mapping of the potato virus Y resistance gene Rysto. Theor. Appl. Genet. 94(2), 198-203. [ Links ]
Castillo-Ruiz, R.A. 2002. A potato large insert library for isolation of candidate loci for late blight resistance and studies on their genome organization. Ph.D. thesis. University of Cologne, Germany. [ Links ]
Collard, B.C.Y., M.Z.Z. Jahufer, J.B. Brouwer & E.C.K. Pang. 2005. An introduction to markers, quantitative trait loci (QTL) mapping and marker assisted selection for crop improvement: The basic concepts. Euphytica 142, 169-196. [ Links ]
Collins, A., D. Milbourne, L. Ramsay, R. Meyer, C., Chatot-Balandras, P. Oberhagemann, W. de Jong, C. Gebhardt, E. Bonnel y R. Waugh. 1999. QTL for field resistance to late blight in potato is strongly correlated with maturity and vigour. Mol. Breeding 5, 387-398. [ Links ]
Chrisholm, S.T., G. Coaker, B. Day y B.J. Staskawicz. 2006. Host Microbe Interactions: Shaping the evolution of the plant immune response. Cell 124, 803-814. [ Links ]
De Jong, W., A. Forsyth, D. Leister, C. Gebhardt y D.C. Baulcombe. 1997. A potato hypersensitive resistance gene against potato virus X maps to a resistance gene cluster on chromosome 5. Theor Appl. Genet. 95(1-2), 246-252. [ Links ]
Duncan, J.M. 1999. Phytophthora - an abiding threat to our crops. Microbiol Today 26, 114-116. [ Links ]
Ellis, J., P. Dodds y T. Prior. 2000. Structure, function and evolution of plant disease resistance genes. Biotic Interactions 3, 278-284. [ Links ]
El-Kharbotly, A., C. Leonards-Schippers, D.J. Huigen, E. Jacobsen, A. Pereira, W.J. Stiekema, F. Salamini y C. Gebhardt. 1994. Segregation analysis and RFLP mapping of R1 and R3 alleles conferring race-specific resistance to Phytophthora infestans in progeny of dihaploid potato parents. Mol. Gen. Genet. 242, 749-754. [ Links ]
El-Kharbotly, A., C. Palomino-Sánchez, F. Salamini, E. Jacobsen y C. Gebhardt. 1996a. R6 and R7 alleles of potato conferring race-specific resistance to Phytophthora infestans (Mont.) de Bary identified genetic loci clustering with the R3 locus on chromosome XI. Theor. Appl. Genet. 92, 880-884. [ Links ]
Ewing, E.E., I. Simko, C.D. Smart, M.W. Bonierbale, E.S.G.G. Mizubuti, D. May y W.E. Fry. 2000. Genetic mapping from field tests of qualitative and quantitative resistance to Phytophthora infestans in a population derived from Solanum tuberosum and Solanum berthaultii. Mol. Breeding 6, 25-36. [ Links ]
Gebhardt, C., E. Ritter, A. Barone, T. Debener, B. Walkemeier, U. Schachtschabel, H. Kaufmann, R.D. Thompson, M.W. Bonierbale, M.W. Ganal, S.D. Tanksley y F. Salamini. 1991. RFLP maps of potato and their alignment with the homologues tomato genome. Theor. Appl. Genet. 83, 49-57. [ Links ]
Gebhardt, C., D. Mugniery, E. Ritter, F. Salamini y E. Bonnel. 1993. Identification of RFLP markers closely linked to the H1 gene conferring resistance to Globodera rostochiensis in potato. Theor. Appl. Genet. 85, 541-544. [ Links ]
Gebhardt, C. y J.P.T. Valkonen. 2001. Organization of genes controlling disease resistance in the potato genome. Annu. Rev. Phytopathol. 39, 79-102. [ Links ]
Gebhardt, C. 2004. Potato genetics: molecular maps and more. pp. 215-226. En: Lörz, H. y G. Wenzel (eds.). Biotechnology in agriculture and forestry. Vol 55. Molecular Marker System. Springer-Verlag, Berlin, Heidelberg. 476 p. [ Links ]
Ghislain, O.M., B. Trognitz, M.D. Herrera, J. Solis, G. Casallo, C. Vásquez, O. Hurtado, R. Castillo, L. Portal y M. Orrillo. 2001. Genetic loci associated with field resistance to late blight in offspring of Solanum phureja and S. tuberosum grown under short-day conditions. Theor. Appl. Genet. 103, 433-442. [ Links ]
Grube, R.C., E.R. Radwanski y M. Jahn. 2000. Comparative genetics of disease resistance within the Solanaceae. Genetics 155, 873-887 [ Links ]
Hahlbrock, K. y D. Scheel. 1989. Physiology and molecular biology of phenylpropanoid metabolism. Annu. Rev. Plant Physiol. 40, 347-369. [ Links ]
Hahn, K. y G. Strittmatter. 1994. Pathogen-defense gen Prp-1 from potato encodes and auxine-responsive glutathione S-transferase. Eur. J. Biochem. 226, 619-626. [ Links ]
Hämäläinen, J.H., K.N. Watanabe, J.P.T. Valkonen, A. Arihara, R.L. Plaisted, E. Pehu, L. Miller y S.A. Slack. 1997. Mapping and marker-assisted selection for a gene for extreme resistance to potato virus Y. Theor. Appl. Genet. 94, 192-197. [ Links ]
Hämäläinen, J.H., V.A. Sorri, K.N. Watanabe, C. Gebhardt y J.P.T. Valkonen. 1998. Molecular examination of a chromosome region that controls resistance to potato Y and A potyviruses in potato. Theor. Appl. Genet. 96, 1036-1043. [ Links ]
Hämäläinen, J.H., T. Kekarainen, C. Gebhardt, K.N. Watanabe y J.P.T. Valkonen. 2000. Recessive and dominant genes interfere with the vascular transport of Potato virus A in diploid potatoes. Mol. Plant Microbe Interactions 13(4), 402-412. [ Links ]
Huang, S., V.G.A.A. Vleeshouwers, J.S. Werij, R.C.B. Hutten, H.J. van Eck, R.G.F. Visser y E. Jacobsen. 2004. The R3 resistance to Phytophthora infestans in potato is conferred by two closely linked R3 genes with distinct specificities. Molecular Plant Microbe Interactions 17, 428-435. [ Links ]
Huang, S. 2005. The discovery and characterization of the major late blight resistance complex in potato: genomic structure, functional diversity and implications. Ph.D. thesis, Wageningen University, Wageningen. [ Links ]
Kepinski, S. y O. Leyser. 2005. The A. thaliana F-box protein TIR1 is an auxin receptor. Nature 435, 446-451. [ Links ]
Kover, P.X. y A.L. Caicedo. 2001. The genetic architecture of disease resistance in plants and the maintenance of recombination by parasites. Mol. Ecol. 10, 1-16. [ Links ]
Kreike, C.M., J.R.A. De Koning, J.H. Vinke, J.W. Van Ooijen y W.J. Stiekema. 1994. quantitatively-inherited resistance to Globodera pallida is dominated by one major locus in Solanum spegazzinii. Theor. Appl. Genet. 88, 764-769. [ Links ]
Kuhl, J.C., R.E.Jr. Hanneman y M.J. Havey. 2001. Characterization and mapping of Rpi1, a late blight resistance locus from diploid (1EBN) Mexican Solanum pinnatisectum. Mol. Genet. Genomics 265, 977-985. [ Links ]
Leonards-Schippers, C., W. Gieffers, F. Salamini y C. Gebhardt, 1992. The R1 gene conferring race-specific resistance to Phytophthora infestans in potato is located on chromosome V. Molecular and General Genetics 233, 278-283. [ Links ]
Leonards-Schippers, C., W. Gieffers, R. Schaffer-Pregl, E. Ritter, S. J. Knapp, F. Salamini y C. Gebhardt. 1994. Quantitative resistance to Phytophthora infestans in potato: a case study for QTL mapping in allogamous plant species. Genetics 137, 67-77. [ Links ]
Li, Z.K., L.J. Luo, H.W. Mei, A.H. Paterson, X.H. Zhao, D.B. Zhong, Y.P. Wang, X.Q. Yu, L. Zhu, R. Tabien, J.W. Stansel y C.S. Ying. 1999. A defeated rice resistance gene acts as a QTL against a virulent strain of Xanthomonas oryzae pv oryzae. Mol. Gen. Genet. 261, 58-63. [ Links ]
Lokossou, A., G. van H. Arkel, A. Adillah, T.-H. Park, R. Hutten, H. Van Eck, R. Visser, E. Jacobsen y E. Vossen. 2007. Cloning of Rpi-blb3 and other functional alleles from a major late blight resistance locus on chromosome IV of potato. Proc. 4th Solanaceae Genome Workshop 2007. September 9-13 Jeju, Island Korea. pp. 77. [ Links ]
Malcolmson, J.F. y W. Black. 1966. New R genes in S. demissum Lindl. and their complementary races of Phytophthora infestans (Mont.) de Bary. Euphytica 15, 199-203. [ Links ]
McDowell, J. M. ynd B.J. Woffenden. 2003. Plant disease resistance genes: Recent insights and potential applications. Trends Biotechnol. 21, 178-183 [ Links ]
Marczewski, W., D. Strzelczyk-Zyta, J. Hennig, K. Witek y C. Gebhardt. 2006. Potato chromosomes IX and XI carry genes for resistance to potato virus M. Theor. Appl. Genet. 112 (7), 1232-1238. [ Links ]
Mauricio, R. 2001. Mapping quantitative trait loci in plants: uses and caveats for evolutionary biology. Nat. Rev. Genet. 2, 370-381 [ Links ]
Meyer, R.C.D., C.A. Milbourne, J.E. Hacket, J.W. Bradshaw, Nichol y R. Waugh. 1998. Linkage analysis in tetraploid potato and association of markers with quantitative resistance to late blight (Phytophthora infestans). Mol. Gen. Genet. 259, 150-160. [ Links ]
Milbourne, D., R.C. Meyer, A.J. Collins, L.D. Ramsa y C. Gebhardt. 1998. Isolation, characterization and mapping of simple sequence repeat loci in potato. Mol. Gen. Genet. 259, 233-45. [ Links ]
Mosquera, T. 2006. Análisis genético y molecular de la resistencia cuantitativa a tizón tardío (Phytophthora infestans) en Solanum phureja. Tesis doctoral. Facultad de Agronomía, Universidad Nacional de Colombia, Bogotá. [ Links ]
Naess, S.K., J.M. Bradeen, S.M. Wielgus, G.T. Haberlach y J.M. McGrath, 2000. Resistance to late blight in Solanum bulbocastanum is mapped to chromosome 8. Theor. Appl. Genet. 101, 697-704. [ Links ]
Oberhagemann, P., C. Chatot-Balandras, R. Schäfer-Pregl, D. Wegener, C. Palomino, F. Salamini, E. Bonnel y C. Gebhardt. 1999. A genetic analysis of quantitative resistance to late blight in potato: towards marker-assisted selection. Mol. Breeding 5, 399-415. [ Links ]
Paal, J., H. Henselewski, J. Muth, K. Meksem, C.M. Menendez, F. Salamini, A. Ballvora & C. Gebhardt. 2004. Molecular cloning of potato Gro1-4 gene conferring resistance to pathotype Ro1 of the root cyst nematode Globodera rostochiensis, based on a candidate gene approach. Plant J. 38, 285-297. [ Links ]
Park, T-H., G.A.A. Vivianne, J.-B. Vleeshouwers, C.B. Hutten y G.F. Richard. 2005. Identification, characterization and high resolution mapping of resistance genes to Phytophthora infestans in potato. Dissection of foliage and tuber late blight resistance en mapping population of potato. Ch. 3. Ph.D. thesis. Wageningen. 122 p. [ Links ]
Rauscher, G.M., C.D. Smart, I. Simko, M. Bonierbale, H. Mayton, A. Greenland y W.E. Fry, 2006. Characterization and mapping of RPi-ber, a novel potato late blight resistance gene from Solanum berthaultii. Theor. Appl. Genet. 112, 674-687. [ Links ]
Ritter, E., T. Debener, A. Barone, F. Salamini y C. Gebhardt, 1991. RFLP mapping on potato chromosomes of two genes controlling extreme resistance to potato virus X (PVX). Mol. Gen. Genet. 227, 81-85. [ Links ]
Robertson, D.S. 1985. A possible technique for isolating genomic DNA for quantitative traits in plants. J. Theor. Biol. 117, 1-10. [ Links ]
Rouppe van der Voort J., P. Wolters, R. Folkertsma, R. Hutten y P. Van Zandvoort. 1997. Mapping of the Cyst nematode resistance locus Gpa2 in potato using a strategy based on comigrating AFLP markers. Theor. Appl. Genet. 95, 874-880. [ Links ]
Salvi, S. y R. Tuberosa. 2005. To clone or not to clone plant QTLs: present and future challenges. Trends Plant Sci. 10(6), 297-304. [ Links ]
Sandbrink, J.M., L.T. Colon, P.J.C.C. Wolters & W.J. Stiekema. 2000. Two related genotypes of Solanum microdontum carry different segregating alleles for field resistance to Phytophthora infestans. Mol. Breeding 6, 215-225. [ Links ]
Shirazu, K. y P. Schulze-Lefert. 2000. Regulators of cell death in disease resistance. Plant Mol. Biol. 44, 371-385. [ Links ]
Schulze-Lefert, P. 2004. Plant immunity: The origami of receptor activation. Curr. Biol. 14, R22-R24. [ Links ]
Song, J., J.M. Braaden, S.K. Naess, J.A. Raasch, S.M. Wielgus, G. T. Haberlach, J. Liu, H. Kuang, S. Austin-Phillips, C.R. Buell, J.P. Helgeson y J. Jiang. 2003. Gene RB cloned from Solanum bulbocastanum confers broad resistance to potato late blight. Proc. Natl. Acad. Sci. United States of America 100, 9128-9133. [ Links ]
Tommiska, T.J., J.H. Hämäläinen, K.N. Watanabe y J.P.T. Valkonen. 1998. Mapping of the gene Nxphu that controls hypersensitive resistance to potato virus X in Solanum phureja IvP35. Theor. Appl. Genet. 96, 840-843. [ Links ]
Trognitz, F., P. Manosalva, R. Gysin, D. Nino-Liu, R. Simon, M.D. Herrera, B. Trognitz, O.M. Ghislain y N. Estrada, 2002. Plant defense genes associated with quantitative resistance to potato late blight in Solanum phureja x dihaploid S. tuberosum hybrids. Mol. Plant Microbe Interactions 15, 587-597. [ Links ]
Turkensteen, L.J. y W.G. Flier. 2002. Late blight: Its global status in 2002 and beyond. pp.1-9. Proc. Global Initiative on Late Blight Conf., 11-13 July 2002. Hamburg. [ Links ]
Van der Vossem, E.A.G., J.N.A.M. Rouppe van der Voort, K. Kanyuca, A. Bendahmane, H. Sandbrink, D.C. Baulcombe, J. Bakker, W.J. Stiekema y R.M. Klein-Lankhorst. 2000. Homologues of a single resistance gene cluster in potato confer resistance to distinct pathogens: a virus and a nematode. Plant J. 23, 567-576. [ Links ]
Van der Vossem, E.A.G., A. Sikkema, B.L. Hekkert, J. Gros, P. Stevens, M. Muskens, D. Wouters, A. Pereira, W.J. Stiekema y S. Allefs. 2003. An ancient R gene from the wild potato species Solanum bulbocastanum confers broad-spectrum resistance to Phytophthora infestans in cultivated potato and tomato. Plant J. 36, 867-882. [ Links ]
Van der Vossen, E.A.G., M. Muskens, A. Sikkema, J. Gros, D. Wouters, A. Pereira y S. Allefs. 2004. The Rpi-blb2 gene from Solanum bulbocastanum is allelic to the Mi1 gene from tomato and confers broad spectrum resistance to Phytophthora infestans in cultivated potato and tomato pp. 21. 1st Solanaceae Genome Workshop, Sept. 19-21 2004. Wageningen. [ Links ]
Visker, M.H.P.W., L.C.P. Keizer, H.J. van Eck, E. Jacobsen, L.T. Colon y P.C. Struik. 2003. Can the QTL for late blight resistance on potato chromosome 5 be attributed to foliage maturity type? Theor. Appl. Genet. 106, 317-325. [ Links ]














