Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Medicas UIS
Print version ISSN 0121-0319
Medicas UIS vol.28 no.1 Bicaramanga Jan./Apr. 2015
Genes del Mycobacterium tuberculosis
involucrados en la patogenicidad y resistencia a
antibióticos durante la tuberculosis pulmonar y
extrapulmonar
Dilia Fontalvo Rivera*
Doris Gómez Camargo**
*Médica Pediatra. Estudiante de doctorado en Medicina Tropical. Universidad de Cartagena. Cartagena. Bolívar. Colombia.
** Bacterióloga. Magister en Microbiología. Doctorado en Bioquímica y Biología molecular. Docente Investigadora Universidad de Cartagena. Directora regional Doctorado Medicina Tropical. Facultad de Medicina. Universidad de Cartagena. Cartagena. Bolívar. Colombia.
Correspondencia: Dra. Dilia Fontalvo. Dirección: Urbanización Sevilla Real Manzana Andalucía Casa 2. Cartagena. Bolívar. Colombia. Correo electrónico: diliafontalvor@gmail.com - dfontalvor@unicartagena.edu.co.
Artículo recibido el 11 de julio de 2014 y aceptado para publicación el 15 de diciembre de 2014.
RESUMEN
Introducción: la tuberculosis sigue siendo un problema en salud pública, causada por el complejo Mycobacterium tuberculosis, por tanto es importante conocer las características genéticas de la bacteria. Objetivo: realizar una revisión bibliográfica sobre los principales componentes del genoma del Mycobacterium tuberculosis, a fin de comprender los mecanismos de patogénesis y la resistencia a medicamentos. Metodología de búsqueda: búsqueda de literatura en español e inglés a través Medline, PubMed, SciELO, UniProt, TubercuList. De 118 publicaciones revisadas solo 93 fueron seleccionados. Resultados: el genoma del Mycobacterium tuberculosis H37Rv comprende 4 411 529 pares de bases. Gran parte de su capacidad de codificación está destinada a la producción de enzimas envueltas en la lipogénesis y lipólisis. Conclusión: las dificultades para manipular las micobacterias genéticamente han hecho de ellas un modelo difícil de caracterizar genéticamente. El desarrollo de herramientas para la manipulación genética han facilitado el entendimiento de la organización del genoma, expresión de sus genes y determinación fenotípica que influyen en su patogenicidad y resistencia a fármacos. MÉD.UIS. 2015;28(1):39-51.
Palabras Clave: Mycobacterium tuberculosis. Genes. Genoma. Metabolismo. Resistencia a medicamentos.
Mycobacterium tuberculosis genes involved in pathogenicity and resistance to antibiotics
for pulmonary and extrapulmonary tuberculosis
ABSTRACT
Introduction: tuberculosis is a public health problem caused by the Mycobacterium tuberculosis complex, so it is important to know the genetic characteristics of the bacteria. Objetive: to execute a literature review of the main components of the genome of Mycobacterium tuberculosis to understand the mechanisms in the pathogenesis and drug resistance. Methodology: a literature review in Spanish and English using Medline, PubMed, Scielo, Uniprot, Tuberlist. Results: the complete genome sequence of Mycobacterium tuberculosis, H37Rv comprises 4,411,529 base pairs. A very large portion of its coding capacity is devoted to the production of enzymes involved in lipogenesis and lipolysis. Conclusion: difficulties to manipulate genetically mycobacteria have made them a difficult model to characterize genetically. The developments of tools for genetic manipulation have been facilitating the understanding of genome organization, expression of their genes and phenotypic determination that influence in the pathogenicity and drug resistance. MÉD.UIS. 2015;28(1):39-51.
Keywords: Mycobacterium tuberculosis. Genes. Genome. Metabolism. Drug resistance.
¿Cómo citar este artículo?: Fontalvo D, Gómez D. Genes del Mycobacterium tuberculosis
involucrados en la patogenicidad y resistencia a antibióticos durante la tuberculosis pulmonar y
extrapulmonar. MÉD.UIS. 2015;28(1):39-51.
INTRODUCCIÓN
La Tuberculosis (TB) sigue siendo un problema de salud pública. La Organización Mundial de la Salud (OMS) para el 2012 reportó 8,6 millones de casos de TB en el mundo, de los cuales 1,3 millones fallecieron por esta causa. Su principal agente etiológico en el humano es el Mycobacterium tuberculosis (M. tuberculosis) bacteria aeróbica facultativa, ácidoalcohol resistente por su resistencia a la decoloración de la fucsina básica. Dentro de las características del M. tuberculosis, están el crecimiento lento, estado de latencia, envoltura celular compleja, patogénesis intracelular y homogeneidad genética1. La pared celular es rica en peptidoglucano, glicolípidos y polisacáridos que junto con otros componentes como los ácidos micólicos, ácido micoserósido, fenoltiocerol, lipoarabinomanano y arabinogalactano contribuyen a la longevidad, a la respuesta inflamatoria y a la patogénesis de la micobacteria2,3.
El tiempo de generación del M. tuberculosis en medio sintético o en animales infectados es aproximadamente de 24 horas. Esto contribuye a la cronicidad de la enfermedad, la necesidad de tratamientos prolongados y representa un obstáculo para su aislamiento cuando se tiene como objeto de investigación. Las bases moleculares de latencia y reactivación permanecen oscuras pero se presume que pueda ser una condición genética y que envuelve mecanismos de señalización programadas4,5. Es por esto, que es importante conocer el genoma y la replicación cromosómica, especialmente su iniciación y regulación. El codón de iniciación para el gen dnaA, un sello distintivo para el origen de la replicación, oriC, fue elegido como el punto de partida para la numeración. Se trata de un genoma rico en DNA repetitivo, especialmente en forma de secuencias de inserción, como la IS6110, de la que se han hallado 16 copias. También son fuentes de repetición las nuevas familias multigénicas y genes housekeeping duplicados. Pese a que la tasa de duplicación es similar a la de otros microorganismos (el 51% de sus secuencias codificantes han surgido a partir de un proceso de duplicación), como Escherichia coli o Bacillus subtilis, difiere respecto a ellos en el hecho de que el grado de conservación es considerablemente superior, es decir, al proceso de duplicación no le ha seguido un fenómeno de divergencia, lo cual constituye una evidencia más que confirma la hipótesis de que M. tuberculosis ha surgido de un proceso de especiación relativamente reciente, o bien que se halla ante un bottleneck3,6,7.
El objetivo de este artículo es presentar una revisión bibliográfica de la literatura científica actualizada sobre los principales componentes del genoma del M. tuberculosis a fin de comprender los mecanismos de patogénesis y resistencia a medicamentos de esta micobacteria.
METODOLOGÍA
Se realizó una búsqueda de artículos de investigación, monografías, revisiones y libros en español e inglés publicados después de 1994, que cumplían como criterios de inclusión el estudio de las características del genoma del M. tuberculosis, que estuvieran relacionadas con su patogénesis y la resistencia a fármacos antifímicos. Se excluyeron aquellos que carecían de soporte científico. Se realizó búsqueda electrónica en las bases de datos de Medline, PubMed, Scielo, UniProt, TubercuList, mediante descriptores MESH presentes en el título, el resumen o las palabras claves, usando la siguiente estructura: "[("genome" OR "genome"]) AND ("Mycobacterium tuberculosis" OR ("Mycobacterium" AND "tuberculosis" OR "Mycobacterium tuberculosis" ["All Fields"]). Se encontraron 118 publicaciones, de las cuales 93 cumplieron con los criterios de inclusión.
ORGANIZACIÓN Y SECUENCIA DEL GENOMA
La secuenciación del genoma completo del M. tuberculosis H37Rv fue publicada en 1998 identificando 3974 genes (actualmente 4011). El genoma comprende 4 411 529 pares de bases (pb) con un contenido de Guanina+Citosina (G/C) de 65,6%, esto representa la segunda secuencia bacteriana más grande disponible después de la Escherichia coli3,6. El hecho de que la proporción G/C sea elevada a lo largo de todo el genoma, de una forma homogénea, no concentrada en regiones puntuales, denota que se trata de un genoma que no ha recibido el impacto de la transferencia horizontal de islas de patogenia. No obstante, se observan regiones con una proporción en G/C superior a la media y que son secuencias pertenecientes a una gran familia de genes que incluyen PGRSs (polymorphic G+C-rich secuences).
SECUENCIAS DE INSERCIÓN Y PROFAGOS
La Secuencias de Inserción (IS del inglés Insertion Sequence), son pequeños (< 2,5 kilobases) segmentos de ADN que puede insertarse en una molécula blanco8. Antes de que se completara la secuencia del M. tuberculosis H37Rv, se describieron cuatro elementos de IS en la micobacteria llamadas IS61109, IS108110, IS154711 y el elemento IS-like12. La mayoría de las secuencias de inserción del M. tuberculosis H37Rv, se han insertado en regiones intergénicas o no codificantes, a menudo cerca de las regiones del ARN de transferencia (ARNt).
En el genoma del H37Rv contiene 16 copias de secuencias de inserción IS6110, que ha sido utilizado en gran medida en el estudio de la epidemiología molecular de la TB y se han hallado seis copias de IS1081, el elemento más estable3. Se han identificado nuevos elementos de inserción entre ellos las familias, IS3, IS5, IS21, IS30, IS110,IS256 y el ISL38. Otra familia encontrada es la de REP13E12 que está localizada a lo largo del genoma del M. tuberculosis y está presente solo en los miembros de este complejo3,13-5 (Ver Figura 1).
Se han encontrado al menos dos profagos en el genoma y su presencia puede explicar el por qué el M. tuberculosis muestra niveles persistentemente bajos de lisis en los cultivos. Los profagos phiRv1 y phiRv2, ambos tiene 10kb en longitud y están similarmente organizados. El sitio de inserción de phiRv1 corresponde a parte de una secuencia repetida de la familia 13E12 que parece estar integrado al operon de biotina3,15,16.
FUNCIÓN PROTEICA
Se han atribuido funciones precisas en aproximadamente 40% de las proteínas, con funcionalidades similares en un 44% y el restante 16% no parecían proteínas conocidas y pueden estar relacionadas con funciones específicas de las micobacterias. Fueron identificados 3924 marcos de lectura abierto ORFs (open reading frames) en el genoma. Algunos de estos genes parecen tener mutaciones con cambio o desplazamiento. Tres genes (dnaB, recA y Rv1461) han sido invadidos por las secuencias que codifican inteinas. En cuanto a la composición aminoacídica, predominan aminoácidos del tipo alanina, glicina, prolina, arginina y triptófano, puesto que son los codificados por codones ricos en G/C3.
ASPECTOS INMUNOLÓGICOS Y PATOGENICIDAD
En vista de la alta carga de TB, la vacunación se convierte en una acción prioritaria en salud pública. Con el conocimiento de los componentes estructurales y del genoma del M. tuberculosis se han abordado varias áreas del desarrollo de vacunas que han sido prometedoras, incluyendo la vacunación con ADN, el uso de proteínas secretorias y de componentes inmunógenos de la envoltura del M. tuberculosis y las recombinantes con la BCGBovis17- 21. Por otra parte, se encontró en el genoma dos grandes familias ricas en glicina, la PE (por las regla nemotécnica internacional de los aminoácidos P: Prolina y E: Ácido Glutámico) y PPE (Prolina- Prolina-Ácido Glutámico), que revisten importancia inmunológica, por presentar abundantes antígenos potencialmente polimórficos3.
FAMILIA MULTIGENES PROLINA - ÁCIDO GLUTÁMICO (PE) Y PROLINA-PROLINA-ÁCIDO GLUTÁMICO (PPE)
Constituyen dos nuevas familias de proteínas que ocupan aproximadamente el 10% del genoma, considerados como la mayor fuente de variabilidad genética del M. tuberculosis. Las PE (motivos ProlinaÁcido Glutámico a nivel del extremo N-terminal) y las PPE (Prolina-Prolina-Ácido Glutámico), se caracterizan por ser ricas en prolina y ácido glutámico, y por su repetidos en tándem (MPTRs) respectivamente, que hacen pensar en ellas como potenciales antígenos3,21-4. El elevado grado de polimorfismo repetitivo de secuencias (PGRSs) y polimorfismos mayores (10-15 pb-minisatélites) de la familia PE se compone de 99 miembros que en el extremo N-terminal contiene un dominio altamente conservado compuesto por 110 residuos aminoacídicos que se disponen dando lugar a una estructura globular, mientras que el extremo C-terminal varía en secuencia, longitud y número de repeticiones. Estudios filogenéticos han llevado a subdividir la familia PE, en dos subfamilias, la de PE de 34 miembros y la más numerosa de 65 miembros, el de las Polymorphic GC Rich Repetitive Sequence (PGRS), cuyo contenido en glicina supera el 50% y se distribuye en forma de repeticiones en tándem del motivo glicina-glicina-alanina (Gly-Gly-Ala) o de glicina-glicina-asparagina (Gly-Gly-Asn) en el extremo carboxilo terminal, mientras que el dominio amino terminal está conservado3,21,24,25.
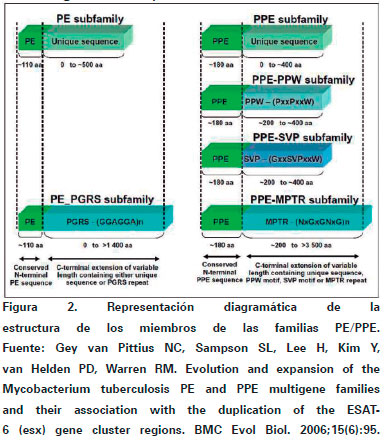
La familia PPE compuesta por 69 miembros, se divide en cuatro subfamilias con base en los motivos de aminoácidos que presentan en el dominio C-terminal de su secuencia de aminoácidos. También tienen un dominio conservado en el extremo N-terminal que está compuesto por 180 residuos de aminoácidos, seguidos de segmentos C-terminal que varía marcadamente en composición y longitud. Estas proteínas se dividen en cuatro subfamilias, la PPESVP, con 24 miembros, se caracteriza por el motivo Gly-X-X-Ser-Val-Prol-X-X-Trp (Gly: glicina-X: cualquier otro aminoácido-Ser: serina-Val: valina- Prol: prolina- Trp: triptofano), entre la posición 300-350 en la secuencia de aminoácidos. La segunda subfamilia con 23 miembros es la de secuencia mayor de repetición en tándem o MPTR (major polymorphic tándem repeat), caracterizado por múltiples copias en tándem de Asn-X-Gly-X-Gly-Asn-X-Gly (Asn: asparagina). La tercera subfamilia, llamada PPE-PPW, está compuesta por 10 miembros, está caracterizada por una región conservada de 44 aminoácidos en el extremo C-terminal de Gly-Phe-X-Gly-Thr (Phe: fenilalanina-Thr: treonina) y Prol-X-X-Trp. La última subfamilia compuesta por 12 miembros, consiste en proteínas con bajo porcentaje de homología en el extremo C-terminal3,21-3,26,27 (Ver Figura 2). Se ha encontrado una proteína PE_PGRS33 codificada por el gen Rv1818c de M. tuberculosis compuesta por 498 aminoácidos con un 41% de glicina y 20% de alanina y está involucrada en la interacción de las moléculas de superficie celular de la micobacteria con los macrófagos del huésped3,24-7.
REGULACIÓN DE LOS GENES Y SEÑALES DE TRADUCCIÓN
La regulación de los genes en procariotas es llevada por la RNA Polimerasa (RNAP). La purificación y caracterización bioquímica de esta enzima ha permitido identificar dos componentes principales: el núcleo de la RNAP y el Factor Sigma (FS)29. El núcleo es un complejo multiproteíco constituido por las subunidades α, β, β'y σ. El FS se asocia transitoriamente con el núcleo de la RNAP y es responsable del reconocimiento del promotor. En la codificación de los factores sigmas se han identificado 13 marcos de lectura en la secuencia del genoma del M. tuberculosis H37Rv (Ver Figura 3) y más de 100 proteínas reguladoras que median la expresión de los genes y el inicio de la transcripción3,28,29. El FS contiene muchos, sino todos, los determinantes de reconocimiento de promotores específicos para la RNA polimerasa. El FS ha sido dividido en dos principales familias: sigma 70 (α70) y sigma 54 (α54)3,27,28,30,31. Los miembros de la familia α54 son relativamente raros y no se han encontrado en las micobacterias, en contraste a la α70 que está en el genoma de todas las bacterias. La familia α70 contiene hasta cuatro regiones conservadas (regiones 1, 2, 3 y 4) y han sido divididas en cuatro subregiones (1-4) basados en su relación filogenética y estructura molecular. La región 1, se divide en 1.1 y 1.2, comprende esencialmente factores α Housekeeping que contiene todos los cuatro grupos conservados. La región 2 está compuesta por cuatro subregiones y tiene los factores más estrechamente relacionados. La subregión 2.4 se requiere para el reconocimiento de promotores de la región - 10 de la transcripción, mientras que el 2.3 está envuelto en la fusión de las burbujas de transcripción a partir del nucleótido número 10 del ADN molde32,33. La región 3, comprende las subregiones 3.0, 3.1 y 3.2. El grupo cuatro tiene factores α que incluye factores que contienen regiones 4.1 y 4.2. Esta última es responsable del reconocimiento del promotor -35 (Ver Figura 3).
El M. tuberculosis codifica un repertorio de 13 FS, de los cuales αA, αB y αF son representativos de los grupos 1,2 y 3 de la familia α70 los restantes 10 FS son parte del grupo cuatro (Ver Figura 3). El factor αA es indispensable para el crecimiento del M. tuberculosis. La sobreexpresión parece ser responsable del crecimiento intracelular y el incremento en la resistencia a los superóxidos. En el H37Rv, este factor se mantiene en niveles casi constantes, sin embargo, se han observado bajas cantidades en las fases con disminución en la aireación y la fase de crecimiento estacionario29,34. El factor αB también está relacionado con el crecimiento de la micobacteria y la respuesta al estrés. Los mutantes para este factor son más sensibles a varios estresores, entre ellos, el de tipo osmótico, oxidativo y el choque térmico35. El factor αF parece jugar un papel clave en la fase estacionaria de crecimiento y se ha detectado su incremento en la depleción de nutrientes en el M. tuberculosis36,37. Los mutantes del gen para el factor αF, han mostrado ser más permeables a solutos hidrofóbicos, sugiriendo que αF regula componentes de la envoltura celular en la cual se ha relacionado más con los sulfolípidos y estos hallazgos podrían explicar por qué los mutantes del factor αF, son más sensibles a la rifampicina38.
METABOLISMO GENERAL, REGULACIÓN Y RESISTENCIA MEDICAMENTOSA
Metabolismo en estado de latencia y estado de anaerobiosis
M. tuberculosis es un aerobio facultativo, del que se conocen varias rutas metabólicas de anaerobiosis, disponibles para que al estar en fase de latencia, pueda habitar en un microambiente con escasa o nula concentración de oxígeno. Cuando se somete in vitro a bajas concentraciones de oxígeno, según el modelo de estudio de Wayne y Hayes39, el M. tuberculosis presentaba una adaptación a estas condiciones de hipoxia, en dos fases que han sido denominadas, Persistencia No Replicativa 1 y 2 (NRP1 Y NRP2). La primera comienza cuando la concentración de oxígeno en el medio y en el ambiente es de 1% y 72% respectivamente y se caracteriza por la detección súbita de ADN pero no de ARN. Las bacterias en esta fase se hacen resistentes a isonizaida, rifampicina y ciprofloxacina. En el estadio NRP2, la concentración de oxígeno en el medio y en el aire es de 0,06% y 15% respectivamente, se caracteriza por la disminución inicial en la concentración global de ATP y se detiene el aumento del volumen celular39,40. En el estudio de la expresión genética del M. tuberculosis H37Rv, en estado de hipoxia y latencia, se ha encontrado que el sistema de transcripción de dos componentes dormancy survival regulator (dos/RS)41, es el principal mediador de la respuesta a la hipoxia y controla la sobreexpresión de 52 genes y la represión de 19 genes.
El M. tuberculosis adapta su metabolismo al ambiente anaeróbico activando las vías de respiración del nitrato, así como la vía del glioxilato a través de la estimulación de las enzimas isocitrato liasa y glioxilato deshidrogenasa (Ver figura 4)42. Esta vía, permite al M. tuberculosis sintetizar carbohidratos a partir de ácidos grasos.
METABOLISMO DE LOS LÍPIDOS
Aproximadamente el 8% del genoma está dedicado al metabolismo lipídico. M. tuberculosis utiliza preferentemente carbohidratos cuando crece in vitro y ácidos grasos cuando infecta a su hospedero. Actualmente, se describen más de 200 genes involucrados en el metabolismo de los lípidos y ácidos grasos, entre los cuales están incluidos entre otros, la metil malonil CoA epimerasa (mce-1, mce-2, mce-3, mce-4), enoyl-acyl carrier protein reductasa (inhA), acyl-CoA synthasa (fad), pantoate-β-alanine ligase/ pantoate aspartate 1-decarboxilase (panC/ panD)3,43.
En el metabolismo de los ácidos grasos insaturados, se produce el propionil- CoA, que debe metabolizarse adicionalmente antes de que sus átomos de carbono puedan entrar en el ciclo de la acetil-CoA. Luego del paso de propionil- CoA a D-malonil-CoA, actúa la enzima metilmalonil CoA epimerasa que lo metaboliza a L-metil malonil-CoA que finalmente llega a succinil CoA, para seguir la ruta de la Acetil- CoA (Ver Figura 5)43.
Degradación de los ácidos grasos
La degradación de los lípidos de las células del huésped es vital en la forma intracelular del M. tuberculosis. A través de una amplia familia de enzimas b-oxidativas, codificadas por múltiples copias en el genoma, las membranas celulares del huésped proveen precursores para muchos procesos metabólicos así como para potenciales precursores para constituyentes de la pared celular micobacteriana. Esas enzimas producen acetil CoA, el cual puede ser convertido en diferentes metabolitos y ser fuente energética para el M. tuberculosis (Ver Figura 6a)43.
Al menos dos tipos discretos de enzimas, la sintetasa de ácidos grasos tipo I y tipo II, están involucradas en la biosíntesis de ácidos grasos en las micobacterias. Los genes que sintetizan ácido micólico incluyen la sintetasa de ácidos grasos tipo I conocido como fas (fatty acid syntethasa) y un sistema de tipo II, que consiste en componentes de enzimas disociables que actúa sobre una proteína portadora de acilo conocida como ACP (acyl-carrier protein). Fas II es incapaz de sintetizar ácidos grasos de novo, pero elonga palmitoil -ACP a los ácidos grasos en 24 a 56 carbonos. Algunos componentes de fas II pueden ser blanco importante de los medicamentos antituberculosos como la isoniazida, incluyendo la enoyl -ACP reductasa (InhA), cetoacil-ACP sintetasa (KasA) y la ACP-AcpM. El estudio del genoma muestra que hay tres potenciales cetoacil sintetasa: KasA y KasB que están altamente relacionadas, agrupadas en sus genes en acpM, mientras que KasC es de homología distante del sistema de las cetoacilsintetasa III (Ver Figura 6b)5,41,43.
El M. tuberculosis sintetiza policétidos por varias vías. Un sistema modular tipo I similar al de la síntesis de la eritromicina es codificado por un gran operon, el ppsABCDE, que funciona en la síntesis de fenoltiocerol. El grupo de genes pps, se produce inmediatamente aguas arriba, es decir, ubicado a la izquierda del extremo 5' del punto de inicio de la transcripción del mas, codifica la enzima multifuncional sintetasa de ácido micoserósido, dado que sus productos tiocerol y ácido micocerósido, forman la molécula más abundante de la pared celular, el dimicocerosato de tiocerol3 (Ver Figura 6c).
GENES IMPLICADOS EN LA RESISTENCIA A FÁRMACOS
Resistencia a Rifampicina
La rifampicina actúa como bactericida interfiriendo con la síntesis de ARN mensajero al unirse a la ARN polimerasa, que está compuesta por cuatro subunidades diferentes codificadas por los genes rpoA, rpoB, rpoC y rpoD1. Las micobacterias desarrollan resistencia a rifampicina mediante mutaciones en una región definida de la subunidad β de la ARN polimerasa, que es codificada por el gen rpoB. Estudios comparativos de secuencias de rpoB, mostraron seis regiones altamente conservadas (regiones I a VI) y en las cuales se han encontrado la mayoría de las mutaciones en el gen relacionadas con la resistencia a la rifampicina44,45. Esta está determinada por mutaciones que incluyen deleciones, inserciones y sustituciones que están concentradas en una pequeña zona de un gen rpoB de M. tuberculosis, las cuales generalmente se localizan en un corto segmento que incluye los codones 507 a 533. Las más frecuentes son las mutaciones en codones para asparagina 516, histidina 526 y serina 531 (Ver Figura 7)3, 46-54.
GENES DE RESISTENCIA A ISONIAZIDA
La isoniazida, forma hidrácida del ácido nicotínico, es una prodroga de gran actividad sobre M. tuberculosis con una Concentración Inhibitoria Mínima (CIM) de 0,05 μg/ml, que al ser captada por la bacteria, es activada por el sistema catalasa-peroxidasa a la forma activa, el ácido nicotínico, de manera que la ausencia de actividad catalasa, debido a mutaciones en el gen katG, codificante de esta enzima, es uno de los mecanismos de resistencia a la isoniazida. El mecanismo de acción es la inhibición específica de la síntesis de ácidos micólicos, sin afectar la de otros ácidos grasos52.
KatG es una proteína de 80 KDa, compuesta por 740 aminoácidos, es codificada por el gen katG, que se encuentra en una región relativamente inestable, haciéndolo susceptible de sufrir inserciones, deleciones y mutaciones. Las mutaciones se concentran en una región codificante del gen katG, que comprende mayormente los codones 300 al 507, siendo las más frecuentes las sustituciones de la serina 315 por treonina y el residuo de arginina 463 por leucina. Estas mutaciones explican aproximadamente el 42-58% de los casos clínicos resistentes a isoniazida (Ver Figura 8)55-7.
Gen inhA
La enzima enoil ACP reductasa codificada por gen inhA, está involucrada en los pasos de elongación de ácidos grasos del M. tuberculosis y se ha identificado como blanco de acción de la isoniazida. La isoniazida activada interfiere con la síntesis de ácido micólico por inhibición de la NADH dependiente de la enoil ACP reductasa. La mutación del gen inhA, que la codifica explica aproximadamente el 25% de los casos de resistencia a isoniazida. Las mutaciones en el gen inhA, no solo causa resistencia a la isoniazida, sino también a la ethionamida. Se han encontrado dos genes que participan en esta resistencia combinada de ethionamida - isoniazida, designado como mabA e inhA para referirse a la ethionamida e isoniazida respectivamente. La principal sustitución se da en la posición 94 de la Ser por la A58-60.
Gen oxyR
En M. tuberculosis, el oxyR, el gen regulador central en la respuesta al estrés oxidativo y de nitratos, está sorprendentemente inactivo y está representado en el genoma de la micobacteria, como un pseudogen, situado entre los marcos de lectura abierto, Rv2427c y Rv2428. Es conocido que el gen oxyR regula algunos genes envueltos en la respuesta al estrés oxidativo, incluyendo, ahpC, katG, gorA, fur, dps y oxyS.
Los genes oxyR y ahpC están estrechamente relacionados, con transcripción inversa. Sorprendentemente, el gen oxyR, fue inactivado naturalmente, por acumulación de múltiples alteraciones genéticas, incluyendo mutación con cambio, mutaciones puntuales y deleciones61-3.
Gen ahpC
La enzima Alkil hidroperoxidasa tipo C (AhpC) es capaz de detoxificar peróxidos orgánicos y probablemente, también peróxido de hidrógeno. Esta enzima se ha inactivado en M. tuberculosis H37Rv por recombinación homóloga utilizando un plásmido con el gen inactivado. La mutante obtenida fue tan virulenta como la cepa original en ratones BALB/c infectados por vía intravenosa. Estos resultados sugieren que este gen no juega un papel importante en el inicio de la infección. Sin embargo, el hallazgo de niveles elevados de expresión de AhpC en cultivos estáticos de M. tuberculosis obliga a definir en el futuro el papel de esta enzima en niveles posteriores de infección64-6.
La peroxiredoxina AhpC de M. tuberculosis ha sido expresada, purificada y bien caracterizada, de manera que se ha descubierto que difiere de otras proteínas Ahp de la familia a nivel de tres residuos de cisteína que, mediante estudios de mutagénesis, se sabe que son esenciales para la actividad catalítica. La expresión de AhpC está asociada con la resistencia a isoniazida y muchas de las cepas resistentes a este antifímico poseen una mutación a nivel de la región promotora (mutación promoter-up)64,67.
Gen fur
Se encuentra localizado a 471pb corriente arriba del sitio de inicio del codón del gen katG. El análisis de las cadenas de M. tuberculosis revelan que esta región contiene un marco de lectura abierto que codifica para el furA, un homólogo de FUR, un regulador de la captación del hierro encontrado en bacterias entéricas con la E. coli y S. typhimurium y el cual se ha encontrado envuelto en la detoxificación de radicales de oxígeno62,68.
GENES RESISTENCIA ESTREPTOMICINA (S): rrs y rpsL
La S es un aminoglucósido bactericida que actúa sobre los ribosomas inhibiendo la síntesis de proteínas, al unirse a la fracción 16s rRNA. Cerca de 65-75% de las cepas resistentes a la S son explicadas por las mutaciones identificadas en los genes rrs y rpsL, que codifica la proteína ribosomal S12. Las mutaciones puntuales del gen rrs, se encuentran en dos regiones, en torno a los nucleótidos52 0 y 915. La región 530 del 16S del rRNA es altamente conservada y esta adyacente a la región 915 en los modelos de estructura secundaria. La mayoría de las mutaciones puntuales que producen resistencia a la S ocurren en el gen rpsL. La más común es el codón 43 donde se da el cambio de AAG por AGG, como resultado de una sustitución de Lisina (Lys) por Arginina (Arg), menos frecuentemente un AAG por ACG, por una sustitución de Lys por Treonina (Tre). Las mutaciones también pueden ocurrir en el codón 88 y resulta en la sustitución de Lys por Arg ( AAG por AGG) o Lys por Glic ( AAG por CAG)69-71.
GENES RESISTENCIA A PIRAZINAMIDA: pncA
La pirazinamida es un análogo estructural de la nicotinamida. La acción bactericida intracelular de la pirazinamida es debida a la acumulación de su derivado activo, ácido pirazinoico, al degradarse por el efecto de la pirazinamidasa de las cepas sensibles. Actúa en un pH ácido sobre poblaciones de micobacterias que están en estado latente en el interior de los fagosomas. En los bacilos resistentes se han identificado interrupciones en el gen pncA, codificante de la enzima pirazinamidasa, por lo cual no se podría activar el antibiótico. Se han identificado entre otras sustituciones en las posiciones Cys63Prol, Gln138Prol y Asp63His y deleción de un nucleótido de guanina en las posiciones 162 y 28872.
GENES RESISTENCIA A ETAMBUTOL: embCAB
Es un compuesto sintético que actúa como bacteriostático, cuyo mecanismo de acción es inhibir la transferencia de ácidos micólicos presentes en la pared micobacteriana y la inhibición de la síntesis de arabinogalactano y lipoarabinomanano, al actuar sobre la arabinosil transferasa que media la polimerización de la arabinosa en el arabinogalactano. Las alteraciones génicas identificadas hasta ahora se concentran en un operon designado como embCAB, que incluye tres genes codificantes para arabinosiltransferasas. Las mutaciones en la región emb se asocian a altos niveles de resistencia y se han identificado en aproximadamente el 65% de los aislamientos clínicos resistentes a etambutol. Los estudios realizados sobre las mutaciones en el gen embCAB han encontrado alteraciones en su mayoría en el codón 306 con sustituciones de metionina por valina (Met306Leu), otros hallados son sustituciones de Fenilalanina por Valina (Fen330Val) y la de Treonina por Isoleucina (Treo630Iso). Para obtener la genética molecular de síntesis de arabinano, Belanger y cols, identificaron dos loci en el gen embAB en M. avium que codifica la arabinosiltransferasa. Trabajando en paralelo, Telenti y cols, secuención genes codificantes para el emb en M. smegmatis. Tres genes organizados como un operon fueron identificados y designados como embCAB. La gran mayoría (89%) de las cadenas tienen una mutación en el codón 306, sin embargo también se han identificado en otros tres: Fen285Leu, Fen330Val y Tre630Ile73,74 (Ver Figura 9).
GENES DE RESISTENCIA A FLUOROQUINOLONAS (FQ): gyrA, gyrB
Se encuentra en este grupo la ciprofloxacina, ofloxacina, moxifloxacina y gatifloxacina, como fármacos utilizados en caso de resistencia a los medicamentos de primera línea. La actividad de las fluoroquinolonas tiene lugar a nivel de la DNA girasa una topoisomerasa de tipo II que está compuesta por las subunidades A y B que están codificadas por los genes gyrA y gyrB respectivamente, interfiriendo así con la replicación del ADN. Un sitio de acción secundario es la topoisomerasa IV codificada por los genes parC y parE75.
Las mutaciones asociadas con altos niveles de resistencia a las FQ se encuentran agrupadas en una región de 40 aminoácidos en el gen gyrA conocida como Región Determinante de Resistencia a la Quinolona (QRDR, por la sigla del inglés de quinolone resistance determining region)76. Se han descrito polimorfismos en los codones 90, 91, 94 y 95. Las mutaciones en los tres primeros codones se asocian con resistencia a la ciprofloxacina, mientras que las cepas sensibles a este antibiótico se han visto que carecen estas mutaciones75.
En estudios realizados en pacientes con tuberculosis multidrogoresistente con resistencia a FQ en Nueva York, encontraron otras sustituciones de aminoácidos relacionados con resistencia, hallando mutaciones en los codones 90 (Ala>Val) y en el 94 (Asp>Ala, Asn, Gly, His, Tir) en el gen gyrA75-77. Las mutaciones N538D, E540V y R485C + T539N, han conferido resistencia a las cuatro FQ, ciprofloxacina, ofloxacina, levofloxacina y moxifloxacina. Las mutaciones D500H y D500N se asocian a resistencia a levofloxacina y ofloxacina, mientras que las mutaciones N538K y E540D, lo hacen con solo moxifloxacina78 (Ver Figura 10).
GENES DE RESISTENCIA A AMINOGLUCÓSIDOS: KANAMICINA, AMIKACINA, VIOMICINA Y CAPREOMICINA: rrs, tlyA
Los aminoglucósidos impiden la síntesis de proteínas por inhibición de la función normal de los ribosomas. El mecanismo molecular más común de resistencia en kanamicina y amikacina se ha asociado con una mutación en el gen rrs que codifica para la subunidad 16S del rARN. Las mutaciones en el gen tlyA que codifica la 2'-O-metiltransferasa que modifica el nucleótido C1409 en la hélice 44 de ARNr 16S y el nucléotido C1920 en la hélice 69 del ARNr 23S (subunidad 50S), está implicado en la resistencia a la capreomicina y viomicina79. Se han reportado mutaciones en el gen GidB (glucosa-inhibitol división protein B) , que podrían explicar el 27% de las resistencia de la estreptomicina79.
GENES INVOLUCRADOS EN LAS BOMBAS DE EFLUJO COMO MECANISMOS DE RESISTENCIA
El resistoma intrínseco se constituye en un fenotipo antiguo que ha evolucionado en la bacteria y que le confiere propiedades de resistencia intrínseca y no adquiridas sin exposición previa a antibióticos80-2. Esta resistencia intrínseca usualmente es el resultado de la reducción en la permeabilidad de la envoltura bacteriana y de la actividad de las bombas de eflujo, encargadas de eliminar una gran cantidad de compuestos del citoplasma de las bacterias83,84. La secuencia del genoma del M. tuberculosis H37Rv revela la presencia de 13 potenciales proteínas transmembrana y han sido denominadas MmpL (mycobacterial membrane proteins large), que por su naturaleza hidrofóbica y la fuerte asociación de cuatro de sus genes con el metabolismo de los lípidos sugieren que pueden estar envueltos naturalmente en el transporte de ácidos grasos83,84. Se ha observado que la sobreexpresión del gen mmpL7 es la responsable de un alta de resistencia a la isoniazida85. Otro gen envuelto en resistencia a este antifímico, es el iniA, que en estudios de experimentación se ha encontrado esencial para la actividad de bombas de eflujo que le confieren resistencia a la isoniazida y etambutol. Esto sugiere que este gen confiere resistencia a múltiples drogas83. Otros genes involucrados son efpA, pstB y Rv1258c85,86. La resistencia innata a la rifampicina se ha descrito en ausencia de mutación del rpoB, posiblemente como resultado de alteración en la permeabilidad de la barrera celular87-90. Las bombas de eflujo que están involucradas son la Rv1258c, Rv1410c, Rv1819c y Rv2136c90,91.
CONCLUSIONES
Las dificultades para manipular las micobacterias genéticamente, su crecimiento lento y su patogenicidad han hecho de ellas un modelo difícil de caracterizar genéticamente. El desarrollo de herramientas para la manipulación genética han permitido avances en la investigación en este campo, facilitado el entendimiento de la organización del genoma, la expresión de sus genes y la determinación fenotípica, que explican los mecanismos de patogenicidad, estado de latencia y resistencia a fármacos antifímicos. El genoma del Mycobacterium tuberculosis comprende una amplia gama de genes con un alto contenido de G/C que pertenecen a dos familias de proteínas la PE y PPE, que influye en la virulencia y son consideradas fuente de variabilidad genética de gran relevancia inmunológica que son de particular interés para estudios futuros orientados a buscar tratamientos nuevos para el control de esta enfermedad.
CONFLITO DE INTERES
Ninguno por declarar
FINANCIACIÓN
Recursos propios de los autores.
REFERENCIAS BIBLIOGRÁFICAS
1. Wheeler P, Ratledge C. Tuberculosis: Pathogenesis, Protection, and Control. En: Ed. Bloom BR. Washington DC: ASM Press; 1994. p. 353-85. [ Links ]
2. Brennan P, Draper P. Tuberculosis: Pathogenesis, Protection, and Control. En: Ed. Bloom BR. Washington DC: ASM Press; 1994. p. 271-84. [ Links ]
3. Kolattukudy P, Fernandes N, Azad A, Fitzmaurice A, Sirakova T. Biochemistry and molecular genetics of cell-wall lipid biosynthesis in mycobacteria. Mol. Microbiol. 1997;24:263-70. [ Links ]
4. Chan J, Kaufmann S. Tuberculosis: Pathogenesis, Protection, and Control. En: Ed. Bloom BR. Washington DC: ASM Press; 1994. p. 271-84. [ Links ]
5. Cole ST, Brosch R, Parkhill J, Garnier T, Churcher C, Harris D, et al. Deciphering the biology of Mycobacterium tuberculosis from the complete genome sequence. Nature. 1998;393:537-43. [ Links ]
6. Lamichhane G, Zignol M, Blades N, Geiman D, Dougherty A, Grosset J, et al. A postgenomic method for predicting essential genes at subsaturation levels of mutagenesis: application to Mycobacterium tuberculosis. Proc Natl Acad Sci. 2003;100:7213-18. [ Links ]
7. Fleischmann R, Alland D, Eisen J,Carpenter L. Whole Genome comparison of Mycobacterium tuberculosis Clinical and Laboratory strains. Journal of Bacteriology. 2002;184(19):5479-90. [ Links ]
8. Vissa V, Sakamuri R, Li W, Brennan PJ. Defining mycobacteria: Shared and specific genome features for different lifestyles. Indian J Microbiol. 2009;49:11-47. [ Links ]
9. Gordon SV, Heym B, Parkhill J, Barrell B, Cole ST. New insertion sequences and a novel repeated sequence in the genome of Mycobacterium tuberculosis H37Rv. Microbiology. 1999;145(Pt 4):881-92. [ Links ]
10. Cave T, Eisenach K, Crawford J, Bates H, Gicquel G. IS6210, an IS-like element of Mycobacterium tuberculosis complex. Nucleic Acids Res. 1990;18:188. [ Links ]
11. Collins DM, Stephens DM. Identification of an insertion sequence, IS 1081, in Mycobacterium bovis. FEMS Microbiol Lett. 1991;67(1):11-5. [ Links ]
12. Fang Z, Morrison N, Watt B, Doig C, Forbes K. IS 61 10 transposition and evolutionary scenario of the direct repeat locus in a group of closely related Mycobacterium tuberculosis strains. J Bacteriol. 1998;180:2102-9. [ Links ]
13. Mariani F, Piccolella E, Colizzi V, Rappuoli R, Gross R. Characterization of an IS-like element from Mycobacterium tuberculosis. J Gen Microbiol. 1993;139(8):1767-72. [ Links ]
14. Saves I, Lewis LA, Westrelin F, Warren R, Daffé M, Masson JM. Specificities and functions of the recA and pps1 intein genes of Mycobacterium tuberculosis and application for diagnosis of tuberculosis. J Clin Microbiol. 2002;40(3):943-50. [ Links ]
15. Baldeviano C, Luna C, Cáceres T, Calderón R. Detección sensible y específica de Mycobacterium tuberculosis a partir de muestras clínicas, mediante la amplificación de un elemento repetitivo de la familia REP13E12. Rev Peru Med Exp Salud Publica. 2007;24(1):5-12. [ Links ]
16. Bibb LA, Hatfull GF. Integration and excision of the Mycobacterium tuberculosis prophage-like element, phiRv1. Mol Microbiol. 2002;45(6):1515-26. [ Links ]
17. Young D, Fruth U. New Generation Vaccines. In: Levine M, Woodrow G, Kaper J, Cobon GS. Editors. New York: Marcel Dekker; 1997. p. 631-45. [ Links ]
18. Brennan M, Fruth U, Mlstien J, Tiernan R, de Andrade Nishioka S, Chocarro L, et al. Development of new tuberculosis vaccines: a global perspective on regulatory issues. PLoS Med. 2007;4(8):e252. [ Links ]
19. Young D, Dye C. The development and impact of tuberculosis vaccines.Cell. 2006;124:683-7. [ Links ]
20. Brennan MJ. The tuberculosis vaccine challenge. Tuberculosis. 2005;85:7-12. [ Links ]
21. Fruth U, Young D. Prospects for new TB vaccines: Stop TB Working Group on TB vaccine development. Int J Tuberc Lung Dis. 2004;8:151-5. [ Links ]
22. Akhter Y, Ehebauer MT, Mukhopadhyay S, Hasnain SE. The PE/PPE multigene family codes for virulence factors and is a possible source of mycobacterial antigenic variation: perhaps more?. Biochimie. 2012;94(1):110-6. [ Links ]
23. Voskuil MI, Schnappinger D, Rutherford R, Liu Y, Schoolnik GK. Regulations of Mycobacterium tuberculosis PE/PPE genes. Tuberculosis (Edinb). 2004;84(3-4):256-62. [ Links ]
24. Gey van Pittius NC, Sampson SL, Lee H, Kim Y, van Helden PD, Warren RM. Evolution and expansion of the Mycobacterium tuberculosis PE and PPE multigene families and their association with the duplication of the ESAT-6 (esx) gene cluster regions. BMC Evol Biol. 2006;6:95. [ Links ]
25. McEvoy CR, van Helden PD, Warren RM, Gey van Pittius NC. Evidence for a rapid rate of molecular evolution at the hypervariable and immunogenic Mycobacterium tuberculosis PPE38 gene region. BMC Evol Biol. 2009;9:237. [ Links ]
26. McEvoy CR, Cloete R, Müller B, Schürch AC, van Helden PD, Gagneux S, et al. Comparative analysis of Mycobacterium tuberculosis pe and ppe genes reveals high sequence variation and an apparent absence of selective constraints. PLoS One. 2012;7(4):e30593. Epub 4 Abr 2012. [ Links ]
27. Sayes F, Sun L, Di Luca M, Simeone R, Degaiffier N, Fiette L, et al. Strong immunogenicity and cross-reactivity of Mycobacterium tuberculosis ESX-5 type VII secretion: encoded PE-PPE proteins predicts vaccine potential. Cell Host Microbe. 2012;11(4):352-63. [ Links ]
28. Gordon SV, Eiglmeier K, Brosch R, Garnier T, Honoré N, Barrell BG, Cole ST. Genomics of Mycobacterium Tuberculosis and Mycobacterium Leprae. In: Ratledge C, Dale J, editors. Mycobacteria: molecular biology and virulence. Oxford: Blackwell Science;1999. p. 93-109. [ Links ]
29. Arráiz N. Factores sigma y respuesta a estrés en micobacterias. Kasmera. 2002;30(2):112-25. [ Links ]
30. Rodrigue S, Provvedi R, Jacques PE, Gaudreau L, Manganelli R. The sigma factors of Mycobacterium tuberculosis. FEMS Microbiol Rev. 2006;30(6):926-41. [ Links ]
31. Gruber TM, Gross CA. Multiple sigma subunits and the partitioning of bacterial transcription space. Annu Rev Microbiol. 2003;57:441-66. [ Links ]
32. Gruber TM, Markov D, Sharp MM, Young BA, Lu CZ, Zhong HJ, et al. Binding of the initiation factor sigma(70) to core RNA polymerase is a multistep process. Mol Cell. 2001;8(1):21-31. [ Links ]
33. Panaghie G, Aiyar SE, Bobb KL, Hayward RS, de Haseth PL. Aromatic amino acids in region 2.3 of Escherichia coli sigma 70 participate collectively in the formation of an RNA polymerasepromoter open complex. J Mol Biol. 2000;299(5):1217-30. [ Links ]
34. Zuber P, Healy J, Carter HL, Cutting S, Moran CP Jr, Losick R. Mutation changing the specificity of an RNA polymerase sigma factor. J Mol Biol. 1989;206(4):605-14. [ Links ]
35. Wu S, Howard ST, Lakey DL, Kipnis A, Samten B, Safi H, et al. The principal sigma factor sigA mediates enhanced growth of Mycobacterium tuberculosis in vivo. Mol Microbiol. 2004;51(6):1551-62. [ Links ]
36. Smith I. Mycobacterium tuberculosis pathogenesis and molecular determinants of virulence. Clin Microbiol Rev. 2003;16(3):463-96. [ Links ]
37. Graham JE, Clark-Curtiss JE. Identification of Mycobacterium tuberculosis RNAs synthesized in response to phagocytosis by human macrophages by selective capture of transcribed sequences (SCOTS). Proc Natl Acad Sci U S A. 1999;96(20):11554-9. [ Links ]
38. Manganelli R, Dubnau E, Tyagi S, Kramer FR, Smith I. Differential expression of 10 sigma factor genes in Mycobacterium tuberculosis. Mol Microbiol. 1999;31(2):715-24 [ Links ]
39. Chen P, Ruiz RE, Li Q, Silver RF, Bishai WR. Construction and characterization of a Mycobacterium tuberculosis mutant lacking the alternate sigma factor gene, sigF. Infect Immun. 2000;68(10):5575-80. [ Links ]
40. Wayne LG, Hayes LG. An in vitro model for sequential study of shiftdown of Mycobacterium tuberculosis through two stages of nonreplicating persistence. Infect Immun. 1996;64(6):2062-9. [ Links ]
41. Mathews CK, Van Holde KE, Ahern KG. Procesos oxidativos: ciclo del ácido cítrico y ruta de las pentosas fosfato. En: Mathews CK, Van Holde KE, Ahern KGm, editores. Bioquímica. 3a ed. España: Pearson Educación, 2002. p. 568-71. [ Links ]
42. Voskuil MI, Visconti KC, Schoolnik GK. Mycobacterium tuberculosis gene expression during adaptation to stationary phase and low-oxygen dormancy. Tuberculosis (Edinb). 2004;84(3-4):218-27. [ Links ]
43. Aguilar LD, Infante E, Bianco MV, Cataldi A, Bigi F. Immunogenicity and protection induced by Mycobacterium tuberculosis mce-2 and mce-3 mutants in a Balb/c mouse model of progressive pulmonary tuberculosis. Vaccine. 2006;24(13):2333-42. Epub 12 Dic 2005. [ Links ]
44. Boon C, Dick T. How Mycobacterium tuberculosis goes to sleep: the dormancy survival regulator DosR a decade later. Future Microbiol. 2012;7(4):513-8. [ Links ]
45. Yepiz-Plascencia GM, Radebaugh CA, Hallick RB. The Euglena gracilis chloroplast rpoB gene. Novel gene organization and transcription of the RNA polymerase subunit operon. Nucleic Acids Res. 1990;18(7):1869-78. [ Links ]
46. Woychik NA, Young RA. RNA polymerase II: subunit structure and function. Trends Biochem Sci. 1990;15(9):347-51. [ Links ]
47. Gingeras TR, Ghandour G, Wang E, Berno A, Small PM, Drobniewski F, et al. Simultaneous genotyping and species identification using hybridization pattern recognition analysis of generic Mycobacterium DNA arrays. Genome Res. 1998;8(5):435-48. [ Links ]
48. Miller LP, Crawford JT, Shinnick TM. The rpoB gene of Mycobacterium tuberculosis. Antimicrob Agents Chemother. 1994;38(4):805-11. [ Links ]
49. Ebrahimi-Rad M, Bifani P, Martin C, Kremer K, Samper S, Rauzier J, et al. Mutations in putative mutator genes of Mycobacterium tuberculosis strains of the W-Beijing family. Emerg Infect Dis. 2003;9(7):838-45. [ Links ]
50. Agapito J, Neyra V, Baldeviano C, Espínoza JR, Accinelli R. Caracterización de las mutaciones en el gen rpob asociadas a la resistencia a rifampicina y tipificación molecular mediante rflp (IS6110) en cepas de M. Tuberculosis de pacientes con tuberculosis pulmonar. Enfermedades del Tórax. 2003;46(1):9-24. [ Links ]
51. Telenti A, Imboden P, Marchesi F, Lowrie D, Cole S, Colston MJ, et al. Detection of rifampicin-resistance mutations in Mycobacterium tuberculosis. Lancet. 1993;341(8846):647-50. [ Links ]
52. Chakravorty S, Aladegbami B, Motiwala A, Dai Y, Safi H, Brimacombe M, et al. Rifampicin resistance, Beijing-W CladeSingle Nucleotide Polymorphism Cluster group 2 phylogeny, and the Rv2629 191-C-Allele in Mycobacterium tuberculosis strains. J Clin Microbiol. 2008:46(8):2555-60. [ Links ]
53. Almeida Da Silva PE, Palomino JC. Molecular basis and mechanisms of drug resistance in Mycobacterium tuberculosis: classical and new drugs. J Antimicrob Chemother. 2011;66(7):1417-30. Epub 9 May 2011. [ Links ]
54. Caws M, Duy PM, Tho DQ, Lan NT, Hoa DV, Farrar J. Mutations prevalent among rifampin- and isoniazid-resistant Mycobacterium tuberculosis isolates from a hospital in Vietnam. J Clin Microbiol. 2006;44(7):2333-7. [ Links ]
55. De La Iglesia AI, Morbidoni HR. Mecanismos de acción y de resistencia de rifampicina e isoniacida en Mycobacterium tuberculosis: nueva información sobre viejos conocidos. Rev Argent Microbiol. 2006;38(2):97-109. [ Links ]
56. Heym B, Alzari PM, Honoré N, Cole ST. Missense mutations in the catalase-peroxidase gene, katG, are associated with isoniazid resistance in Mycobacterium tuberculosis. Mol Microbiol. 1995;15(2):235-45. [ Links ]
57. Pym AS, Saint-Joanis B, Cole ST. Effect of katG mutations on the virulence of Mycobacterium tuberculosis and the implication for transmission in humans. Infect Immun. 2002;70(9):4955-60. [ Links ]
58. Wengenack N, Rusnak F. Evidence for isoniazid-dependent free radical generation catalyzed by Mycobacterium tuberculosis KatG and the isoniazid-resistant mutant KatG(S315T). Biochemistry. 2001;40(30):8990-6. [ Links ]
59. Ramaswamy SV, Reich R, Dou SJ, Jasperse L, Pan X, Wanger A, et al. Single Nucleotide Polymorphisms in Genes Associated with Isoniazid Resistance in Mycobacterium tuberculosis. Antimicrob Agents Chemother. 2003;47(4):1241-50. [ Links ]
60. Abate G, Hoffner SE, Thomsen VO, Miörner H. Characterization of isoniazid-resistant strains of Mycobacterium tuberculosis on the basis of phenotypic properties and mutations in katG. Eur J Clin Microbiol Infect Dis. 2001;20(5):329- 33. [ Links ]
61. Alland D, Steyn AJ, Weisbrod T, Aldrich K, Jacobs WR Jr. Characterization of the Mycobacterium tuberculosis iniBAC promoter, a promoter that responds to cell wall biosynthesis inhibition. J Bacteriol. 2000;182(7):1802-11. [ Links ]
62. Pagán-Ramos E, Master SS, Pritchett CL, Reimschuessel R, Trucksis M, Timmins GS, et al. Molecular and physiological effects of mycobacterial oxyR Inactivation. J Bacteriol. 2006;188(7):2674-80. [ Links ]
63. Zahrt TC, Song J, Siple J, Deretic V. Mycobacterial FurA is a negative regulator of catalase-peroxidase gene katG. Mol Microbiol. 2001;39(5):1174-85. [ Links ]
64. Timmins GS, Master S, Rusnak F, Deretic V. Requirements for nitric oxide generation from isoniazid activation in vitro and inhibition of mycobacterial respiration in vivo. J Bacteriol. 2004;186(16):5427-31. [ Links ]
65. Hillas PJ, del Alba FS, Oyarzabal J, Wilks A, Ortiz De Montellano PR . The AhpC and AhpD antioxidant defense system of Mycobacterium tuberculosis. J Biol Chem. 2000;275(25):18801-9. [ Links ]
66. Master SS, Springer B, Sander P, Boettger EC, Deretic V, Timmins GS. Oxidative stress response genes in Mycobacterium tuberculosis: role of ahpC in resistance to peroxynitrite and stage-specific survival in macrophages. Microbiology. 2002;148(Pt 10):3139-44. [ Links ]
67. Chauhan R, Mande SC. Characterization of the Mycobacterium tuberculosis H37Rv alkyl hydroperoxidase AhpC points to the importance of ionic interactions in oligomerization and activity. Biochem J. 2001;354(Pt 1):209-15. [ Links ]
68. Zahrt TC, Deretic V. Reactive nitrogen and oxygen intermediates and bacterial defenses: unusual adaptations in Mycobacterium tuberculosis. Antioxid Redox Signal. 2002;4(1):141-59. [ Links ]
69. Dubrac S, Touati D. Fur positive regulation of iron superoxide dismutase in Escherichia coli: functional analysis of the sodB promoter. J Bacteriol. 2000;182(13):3802-8. [ Links ]
70. Ulger M, Aslan G, Emekdaş G, Tezcan S, Serin MS. [Investigation of rpsL and rrs gene region mutations in streptomycin resistant Mycobacterium tuberculosis complex isolates]. Mikrobiyol Bul. 2009;43(1):115-20. [ Links ]
71. Chaoui I, Sabouni R, Kourout M, Jordaan AM, Lahlou O, Elouad R, et al. Analysis of Isoniazid, Streptomycin and Ethambutol resistance in Mycobacterium tuberculosis isolates from Morocco. J Infect Dev Ctries. 2009;3(4):278-84. [ Links ]
72. Ozturk CE, Sanic A, Kaya D, Ceyhan I. Molecular analysis of Isoniazid, Rifampin and streptomycin resistance in Mycobacterium tuberculosis isolates from patients with tuberculosis in Düzce, Turkey. Jpn J Infect Dis. 2005;58(5):309-12. [ Links ]
73. Juréen P, Werngren J, Toro JC, Hoffner S. Pyrazinamide resistance and pncA gene mutations in Mycobacterium tuberculosis. Antimicrob Agents Chemother. 2008;52(5):1852-4. Epub 2008 Mar 3. [ Links ]
74. Belanger AE, Besra GS, Ford ME, Mikusová K, Belisle JT, Brennan PJ, et al. The embAB genes of Mycobacterium avium encode an arabinosyl transferase involved in cell wall arabinan biosynthesis that is the target for the antimycobacterial drug ethambutol. Proc Natl Acad Sci U S A. 1996;93(21):11919-24. [ Links ]
75. Telenti A, Philipp WJ, Sreevatsan S, Bernasconi C, Stockbauer KE, Wieles B, et al. The emb operon, a gene cluster of Mycobacterium tuberculosis involved in resistance to ethambutol. Nat Med. 1997;3(5):567-70. [ Links ]
76. Von Groll A, Martin A, Jureen P, Hoffner S, Vandamme P, Portaels F, et al. Fluoroquinolone Resistance in Mycobacterium tuberculosis and Mutations in gyrA and gyrB. Antimicrob Agents Chemother. 2009;53(10):4498-500. Epub 2009 Aug 17. [ Links ]
77. Coll P. Fármacos con actividad frente a Mycobacterium tuberculosis. Enferm Infecc Microbiol Clin. 2009;27(8):474-80. Epub 2009 Sep 18. [ Links ]
78. Malik S, Willby M, Sikes D, Tsodikov OV, Posey JE. New Insights into Fluoroquinolone Resistance in Mycobacterium tuberculosis: Functional Genetic Analysis of gyrA and gyrB Mutations. PLoS One. 2012;7(6):e39754. Epub 2012 Jun 28. [ Links ]
79. Georghiou SB, Magana M, Garfein RS, Catanzaro DG, Catanzaro A, Rodwell TC. Evaluation of Genetic Mutations Associated with Mycobacterium tuberculosis Resistance to Amikacin, Kanamycin and Capreomycin: A Systematic Review. PLoS One. 2012;7(3):e33275. Epub 2012 Mar 29. [ Links ]
80. Fajardo A, Martinez-Martin N, Mercadillo M, Galán JC, Ghysels B, Matthijs S, et al. The neglected intrinsic resistome of bacterial pathogens. PLoS One. 2008;3(2):e1619. [ Links ]
81. Louw GE, Warren RM, Gey van Pittius NC, McEvoy CR, Van Helden PD, Victor TC. A balancing act: Efflux/ Influx in mycobacterial drug resistance. Antimicrob Agents Chemother. 2009;53(8):3181-9. [ Links ]
82. Nikaido H. Preventing drug access to targets: cell surface permeability barriers and active efflux in bacteria. Semin Cell Dev Biol. 2001;12(3):215-23. [ Links ]
83. Brennan PJ, Nikaido H. The envelope of mycobacteria. Annu Rev Biochem. 1995;64:29-63. [ Links ]
84. Viveiros M, Portugal I, Bettencourt R, Victor TC, Jordaan AM, Leandro C, et al. Isoniazid-induced transient high-level resistance in Mycobacterium tuberculosis. Antimicrob Agents Chemother. 2002;46(9):2804-10. [ Links ]
85. Tekaia F, Gordon SV, Garnier T, Brosch R, Barrell BG, Cole ST. Analysis of the proteome of Mycobacterium tuberculosis in silico. Tuber Lung Dis. 1999;79(6):329-42. [ Links ]
86. Machado D, Couto I, Perdigão J, Rodrigues L, Portugal I, Baptista P, et al. Contribution of Efflux to the emergence of Isoniazid and multidrug resistance in Mycobacterium tuberculosis. PLoS One. 2012;7(4):e34538. Epub 2012 Apr 6. [ Links ]
87. Pasca MR, Guglierame P, De Rossi E, Zara F, Riccardi G. mmpL7 gene of Mycocabterium tuberculosis is responsible for Isoniazid efflux in Mycobacterium smegmatis. Antimicrob Agents Chemother. 2005;49(11):4775-7. [ Links ]
88. Colangeli R, Helb D, Sridharan S, Sun J, Varma-Basil M, Hazbón MH, et al. The Mycobacterium tuberculosis iniA gene is essential for activity of an efflux pump that confers drug tolerance to both isoniazid and ethambutol. Mol Microbiol. 2005;55(6):1829-40. [ Links ]
89. Gupta AK, Chauhan DS, Srivastava K, Das R, Batra S, Mittal M, et al. Estimation of efflux mediated multi-drug resistance and its correlation with expression levels of two major efflux pumps in mycobacteria. J Commun Dis. 2006;38(3):246-54. [ Links ]
90. Jiang X, Zhang W, Zhang Y, Gao F, Lu C, Zhang X, et al. Assessment of efflux pump gene expression in a clinical isolate Mycobacterium tuberculosis by real-time reverse transcription PCR. Microb Drug Resist. 2008;14(1):7-11. [ Links ]
91. Obata S, Zwolska Z, Toyota E, Kudo K, Nakamura A, Sawai T, et al. Association of rpoB mutations with rifampicin resistance in Mycobacterium avium. Int J Antimicrob Agents. 2006;27(1):32- 9. Epub 2005 Dec 20. [ Links ]