Introducción
El cáncer de vesícula biliar es una entidad infrecuente, la cual tiene una incidencia global de entre 1.5-2 casos por 100 000 habitantes y ocupa el quinto lugar en frecuencia de neoplasias malignas del tubo digestivo en Estados Unidos1. Su incidencia tiene una variabilidad geográfica, con una incidencia de 21.5 a 12.9 casos por cada 100 000 habitantes en poblaciones indígenas de Chile, Ecuador, Perú, Pakistan, India y Tailandia2, con una mayor proporción en mujeres que en hombres de 3:1, mientras que en México existen pocos registros. En un reporte de 6954 colecistectomías en un Hospital de la Ciudad de México, se presentó una prevalencia de 0.23 casos por 100 0003.
Su etiología es multifactorial, con algunas mutaciones genéticas como KRAS, TP53 o c-ERB-B2, así como factores ambientales como la obesidad, edad avanzada, sexo femenino, colecistitis crónicas, pólipos, obesidad, factores dietéticos y exposición a metales (arsénico) o químicos (aflatoxinas) e infecciones como salmonelosis, los cuales se consideran algunos de los factores de riesgo más importantes4.
Más del 90% de estas neoplasias son adenocarcinomas y los subtipos histológicos incluyen carcinoma papilar, mucinoso, escamoso o adeno-escamoso. Con una tendencia a una diferenciación de tipo biliar seguido de un patrón intestinal1.
El adenocarcinoma de la vesícula biliar es silencioso en etapas iniciales5, presentando sintomatología ambigua, vaga e inespecífica en etapas avanzadas, fácilmente confundido con diversas entidades (colelitiasis, colecistitis aguda, colangitis, hepatitis aguda, absceso, síndrome de Budd-Chiari, entre otros)5-9.
Más de la mitad de los adenocarcinomas vesiculares son diagnosticados de manera incidental ya sea durante la cirugía (0.28%) o más comúnmente durante el examen histopatológico de las piezas resecadas posterior a una colecistectomía por patología benigna como colecistitis o colelitiasis10. Es por esto que se debe tener una alta sospecha clínica para incrementar el diagnóstico preoperatorio, al respecto se ha demostrado que debe sospecharse una neoplasia vesicular si además de tener factores de riesgo clásicos, existe la elevación preoperatoria de fosfatasa alcalina11. Además, la presencia de sintomatología como dolor abdominal constante en hipocondrio derecho asociado a anorexia y pérdida de peso son signos de enfermedad avanzada, sumados a la presencia de ictérica y síntomas consuntivos implica un peor pronóstico5.
La toma de marcadores tumorales como el antígeno carcinoembrionario o la anhidrasa carbónica 19-9 (CA 19-9) se han asociado a las neoplasias vesiculares pero son pobres herramientas de diagnóstico, el primero se puede elevar en cualquier neoplasia gastrointestinal con baja sensibilidad (50%) mientras que un nivel de Ca 19-9 elevado (mayor a 20U/ml para Estados Unidos y mayor a 37 U/ml en población colombiana) incrementan la sospecha de un tumor pancreato-biliar con sensibilidad del 75%1. Sin embargo, los niveles aumentados del Ca 19-9 pueden estar falsamente elevados si existe obstrucción benigna de la vía biliar, es por estas limitantes que su uso se reserva a la vigilancia1.
El diagnóstico oportuno se inicia con la sospecha clínica y la realización de métodos de imagen como el ultrasonido de abdomen con los hallazgos de sospecha como calcificaciones, masa protruyendo la cavidad, pérdida de interfase entre hígado y vesícula, infiltración hepática directa, pólipos mayores a 10 mm, litos mayores a 15 mm o una pared engrosada de manera irregular2,5-6 Sin embargo, no es posible evaluar adecuadamente estadio local y extensión a distancia5,6,10-14, Por estos motivos se recomienda una tomografía axial toracoabdominal contrastada, ya que permite conocer el grado de invasión de la pared, así como la presencia de invasión linfovascular y de evidenciar enfermedad a distancia y la posibilidad de resección hepática5. La colangioresonancia magnética nuclear (CRMN) es un estudio no invasivo que puede ayudar a diferenciar entre patología benigna y maligna de la vesícula biliar15.
La invasión tumoral es el principal factor determinante en el pronóstico de la enfermedad, para esto fue publicada la clasificación TNM de la AJCC (American Joint Committee on Cancer)16, siendo suficiente una colecistectomía para aquellos casos Tis o T1a (invasión a lámina propia), mientras que todos aquellos con T1b (invasión a capa muscular) o mayor requieren de una intervención extensa 1,7-9,16.
Desafortunadamente, hasta el 40-75% de los pacientes diagnosticados de manera incidental se encuentran en estadios avanzados, presentando metástasis17. Su tratamiento clínico resulta retador, incluso en los casos operables, debido a la rápida diseminación linfática o hematógena y posterior micrometástasis regional de este agresivo cáncer5,6,17, lo que lo convierte en el cáncer del tracto biliar con el menor tiempo medio de supervivencia 1,17-18, resultando imperativa la derivación del paciente para su análisis por parte de un equipo multidisciplinario de oncología5, pudiendo ser beneficiosa la quimioterapia neoadyuvante en pacientes localmente avanzados o con factores de alto riesgo quirúrgico8.
El objetivo de este trabajo es presentar un caso clínico de un paciente latino de 72 años con adenocarcinoma vesicular, el cual fue diagnosticado de manera oportuna y fue tratado mediante colecistectomía extendida laparoscópica con buena evolución postquirúrgica y adecuado control oncológico.
Caso clínico
Paciente masculino, latino, de 72 años de edad, sin antecedentes heredofamiliares de importancia, con antecedente de Hipertensión Arterial Sistémica e Hipotiroidismo, ambas de 10 años de evolución y bajo tratamiento médico, niega ingesta de estatinas, que inicia con un cuadro de un año de evolución con cuadros intermitentes de dolor abdominal, tipo cólico en el hipocondrio derecho, sin irradiación, acompañado de náuseas previamente abordado como un cuadro de colelitiasis en otra institución con tratamiento médico con antiespasmódicos (butilhioscina y AINES). Progresa 6 meses previos agregándose pérdida de peso no intencionada de 10 kg. Se presenta a sala de urgencias tras un nuevo cuadro de dolor abdominal intenso. A la exploración física presentó obesidad grado I (IMC 32 kg/m2), signos vitales sin alteración, y con un abdomen globoso a expensas de panículo adiposo con peristalsis presente, sin irritación peritoneal ni masa palpable y con signo positivo de Murphy inespecífico,. Se decidió tomar laboratorios de biometría hemática, química sanguínea y pruebas de función hepática, las cuales reportaron estar dentro de parámetros normales.
Ante la pérdida no intencionada de peso y los síntomas sugestivos de etiología biliar, se realizó una TAC toracoabdominal, que reportó una vesícula biliar con aspecto distendido de medidas de 9 x 3.4 mm, dilatación de colédoco intrapancreático de 10 mm e imagen sugestiva de lesión nodular en fondo de vesícula biliar, que a la aplicación de contraste IV reportó un engrosamiento de hasta 3.6 mm a nivel del fondo vesicular con realce posterior a la administración de contraste, con invasión de capa muscular, sin comprometer serosa visceral, ni infiltrar hígado, sin evidencia de adenopatías regionales o enfermedad a distancia, clasificándose sugestivo de proceso neoplásico en etapa temprana (T1bN0M0) (Fig. 1). Al tratarse de una neoplasia vesicular en etapa temprana se complementó con un CA 19-9 con valor de 29.16 u/ml.

Fuente:
Figura 1 TAC Toracoabdominal con contraste IV que identifica un engrosamiento de hasta 3.6 mm a nivel del fondo vesicular con realce posterior a la administración de contraste, sugestivo de proceso neoplásico.
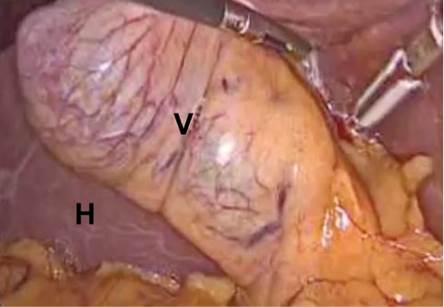
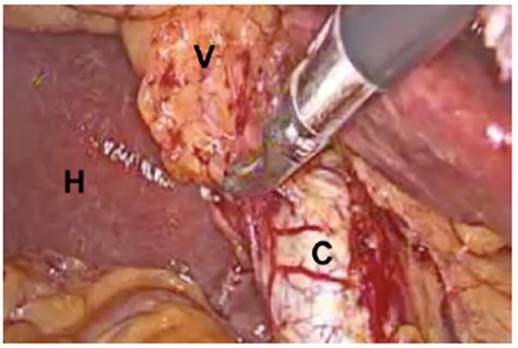
Se desarrolló un abordaje multidisciplinario con oncología médica y quirúrgica, mediante un único procedimiento laparoscópico: una colecistectomía extendida, la cual se llevó a cabo con la colocación de 4 trocares, 2 de 11 mm en región umbilical y subxifoidea y 2 trocares de 5mm en hipocondrio derecho y flanco derecho; se revisó cavidad abdominal en donde no se visualizó presencia de lesiones metastásicas a órganos vecinos. Posterior a esto, se identificó vesícula biliar, la cual se traccionó desde la parte del fondo y bolsa de Hartmann (Fig. 2a), se disecó pedículo hasta localizar conducto y arteria cística, que fueron engrapadas con 2 en extremo proximal y 1 en distal a cada estructura; también se realizó linfadenectomía pericoledociana derecha (Fig. 2b) y se cortaron individualmente la arteria y conducto cístico, a su vez con una delimitación a 2 cm de fosa vesicular sobre parénquima hepático para hepatectomía parcial en cuña con dispositivo de energía bipolar avanzada (Fig. 2c). Se verificó hemostasia y se colocó drenaje sobre lecho hepático, el cual se extrajo por puerto de flanco derecho. Se realizó el cierre por planos y el paciente pasó a recuperación sin eventualidades.
El paciente evolucionó de una manera favorable y satisfactoria, fue egresado al tercer día posoperatorio. El reporte de patología confirmó el hallazgo de un adenocarcinoma vesicular Grado 1, con infiltración a capa muscular, pero respetando la serosa, con bordes libres, 8 ganglios reportados negativos, concluyéndose un T1bN0M0, Estadio Clínico I (Ver tabla 1 y 2). A 6 meses de su cirugía, el paciente continúa asintomático, con TAC demostrando lecho quirúrgico sin actividad tumoral, se continuará bajo el protocolo de vigilancia cada 3 meses durante el primer año y después cada 6 meses por 1 año y posteriormente cada año.
Tabla 1 Clasificación de TNM para estadificar cáncer de vesícula.
| Estadio T | Tumor primario |
|---|---|
| Tx | Tumor primario no puede evaluarse. |
| T0 | Sin evidencia de tumor primario. |
| Tis | Carcinoma in situ. |
| T1 | Tumor invade la lamina propia o capa muscular. |
| T1a | Tumor invade lamina propia. |
| T1b | Tumor invade capa muscular. |
| T2 | Tumor invade el tejido conectivo perimuscular en el lado peritoneal, sin involucrar serosa (peritoneo visceral) o tumor invade el tejido conectivo del lado hepático sin extenderse al hígado. |
| T2a | Tumor invade tejido conectivo perimuscular en el lado peritoneal, sin involucro de serosa. |
| T2b | Tumor invade tejido conectivo perimuscular en el lado hepático, sin extensión directa al hígado. |
| T3 | Tumor penetra la serosa/invade directamente el hígado y/u órganos adyacentes o estructuras como duodeno, colon, páncreas, omento o conductos biliares extrahepáticos. |
| T4 | Tumor invade la vena porta o la arteria hepática o 2 o más órganos extrahepáticos. |
| Estadio N | Ganglios linfáticos regionales. |
| Nx | No pueden evaluarse. |
| N0 | Sin metástasis a ganglios linfáticos regionales. |
| N1 | Metástasis a 1-3 ganglios linfáticos regionales. |
| N2 | Metástasis a 4 o más ganglios linfáticos regionales. |
| Estadio M | Metástasis a distancia. |
| M0 | Sin metastasis a distanica. |
| M1 | Con metástasis a distancia. |
Fuente:
Tabla 2 Estadio clínico por grupos del cáncer de vesícula biliar.
| Estadio | T | N | M | Descripción. |
| 0 | Tis | N0 | M0 | Cáncer in situ. |
| I | T1 | N0 | M0 | Tumor delimitado a vesícula biliar. |
| II | T2 | N0 | M0 | Tumor con extensión a tejido conectivo perimuscular sin extensión a otro sitio. |
| IIIA | T3 | N0 | M0 | Tumor con extensión fuera de la vesícula, pero no invade arterias o venas, sin invasión a ganglios linfáticos u órganos distantes. |
| IIIB | T1-3 | N1 | M0 | Tumor de cualquier tamaño que se extiende a ganglios linfáticos, pero respeta arterias o venas u órganos distantes. |
| IVA | T4 | N0-1 | M0 | Tumor con extensión a arterias, venas o ganglios regionales, pero sin invasión a órganos distantes. |
| IVB | Cualquier T | Cualquier N | M1 | Tumor con extensión a órganos distantes. |
Fuente:
Discusión
El cáncer de vesícula biliar es una patología infrecuente con una incidencia global entre 1.5-2 casos por 100 000 habitantes y con una mortalidad elevada1. Los reportes de series en México parecen indicar que su prevalencia es aún menor, con cifras entre 0.4-0.23 casos por 100 0003,19, como lo documento Aizpuru E, et al. en su estudio retrospectivo, donde analizó 6954 pacientes sometidos a colecistectomías durante un periodo de 13 años encontrando una prevalencia de 0.23% y una incidencia de 2.3 cánceres de vesícula biliar por cada 1000 procedimientos de colecistectomía3. La mayoría de estas neoplasias se detectan de manera incidental tras el análisis histopatológico de piezas de colecistectomía por otras causas5,6-8, esto se ha explicado por la sintomatología ambigua y casi silenciosa en etapas iniciales, que en muchos casos conlleva a presentaciones en etapas avanzadas18, en contraste con nuestro caso, cuyo diagnóstico se realizó de manera temprana.
Existen algunos factores de riesgo que aumentan la sospecha de neoplasia vesicular, entre ellos se ha mencionado: edad mayor a 65 años, obesidad, diabetes, litos vesiculares mayores a 3 cm, pólipos vesiculares mayores a 10 mm, infecciones crónicas por Salmonella o Helicobacter pylori, así como alteraciones congénitas como quistes biliares o uniones pancreatobiliares anómalas1,5,6,9-12; de estos, los principales factores encontrados en nuestro paciente fueron la edad avanzada y la obesidad. Sin embargo, llama la atención que el sexo de nuestro paciente no fue femenino, como ha sido reportado por otros autores como Boyan W et al. (2015) quien, en su reporte de cuatro casos, todos fueron pacientes mujeres; lo anterior se ha inferido debido a la influencia hormonal del estrógeno, que incrementa los niveles de colesterol en la bilis, fomentando el desarrollo de colelitiasis 20. La etiología de estas neoplasias es idiopática, sin embargo, se ha planteado que el principal denominador es una inflamación crónica de la pared vesicular, con la consecuente proliferación celular1. La principal fuente de inflamación es la presencia de litos vesiculares, en especial aquellos mayores de 3 cm o una infección crónica por Salmonella typhi4. Esto es compatible con la historia de nuestro paciente, el cual durante más de 6 meses fue tratado por un cuadro de colelitiasis y no tenía historia de infecciones por Salmonella.
Dentro de los diagnósticos diferenciales de este paciente, cabe mencionar que se pueden dividir en benignos, como la colecistitis crónica litiásica, el síndrome de Mirizzi, colangitis aguda, hepatitis aguda, perihepatitis, absceso, síndrome de Budd- Chiari, trombosis de la vena porta, disfunción del esfínter de Oddi, infecciones por Salmonella o parásitos, y malignos, como el hepatocarcinoma, colangiocarcinoma y tumores pancreáticos principalmente7-12. De acuerdo a Okumura et al., la pérdida de peso, anorexia y dolor abdominal son alertas en las que se debe descartar el diagnóstico de un cáncer vesicular1, factor que se encontró presente en este caso, lo cual orientó a la realización de una tomografía axial computarizada (TAC) con contraste; una de las herramientas diagnósticas másimportantes para identificar un adenocarcinoma, a pesar de no ser la de primera elección, permite establecer la presencia de una masa, el engrosamiento mural irregular de la pared, así como delimitar el grado de invasión de la pared o del componente linfovascular y de evidenciar enfermedad a distancia1,4-5. Esto concuerda con otros reportes de casos, como mencionan Boyan W et al. y Jia Y et al., en los que la realización de TAC en el área de urgencias permitió elevar la sospecha de neoplasia vesicular en la mayoría de los casos reportados5,20.
Como en cualquier otra neoplasia, la estadificación es crucial para decidir su tratamiento y determinar su pronóstico. Al respecto, las guías de la AJCC permiten la clasificación por TNM (ver tabla 1) con estadísticas sobre su pronóstico. La supervivencia a 5 años para los estadios I es del 50%, con un dramático descenso en la sobrevida cuando la enfermedad progresa, siendo del 29% para estadios II, 8% para estadios IIIa, 7% para estadios IIIb y 3% para estadios IV 1,16.
El tratamiento se individualiza con base al estadio TNM. Cuando los tumores son incipientes Tis o T1a, se pueden tratar con una colecistectomía simple. Cualquier paciente con T1b o mayor se beneficia de una colecistectomía extendida con linfadenectomía y resecciones hepáticas de al menos 2 cm, como se realizó en nuestro paciente1,5. La resección del colédoco con reconstrucciones biliodigestivas se reservan para casos con compromiso del conducto cístico, sin embargo, en nuestro caso no fue necesario. Por otro lado, la linfadenectomía, de al menos 6 ganglios en pacientes T1b es necesaria, debido a la tasa de metástasis a ganglios regionales de hasta un 25 % y a un mayor riesgo de recurrencia locorregional del 50%. Se recomienda además iniciar con un abordaje laparoscópico, ya que hasta en el 33% de los casos no se visualizan metástasis regionales en los estudios de imagen18. Para los casos T3-T4 se recomienda un manejo multidisciplinario, con algunos autores proponiendo resecciones multiorgánicas con hepatectomías parciales, colectomías o pancreaticoduodenectomías; sin embargo, no se ha demostrado un beneficio en la supervivencia a 5 años con este tipo de cirugías12-15,21.
Los avances tecnológicos en los últimos años han permitido generalizar el uso de cirugía laparoscópica para la mayoría de los tumores digestivos, incluido colon, estómago, hígado y vesícula biliar. Zhao X et al. comenta en su metaanálisis de 1217 pacientes que al comparar los resultados de la cirugía laparoscópica contra la cirugía abierta, la tasa de sobrevida a 5 años fue mayor en el grupo de laparoscopia (48,4 % vs 38,5 % OR 1.63, p = 0.001), la tasa de recurrencia no tuvo diferencia (44,8 % vs 42,2 %, OR 0.86, p = 0.29); pero la cirugía laparoscópica se asoció a una menor cantidad de sangrado intraoperatorio y menor estancia intrahospitalaria, por lo que recomiendan el uso de esta técnica en centros que cuenten con la capacidad técnica y experiencia21, lo cual apoya la técnica propuesta por nuestro grupo de trabajo para este caso.
Se ha propuesto la administración de quimioterapia para todos aquellos estadios III-IV de manera preoperatoria, utilizando esquemas basados en gemcitabina/cisplatino, gemcitabina/oxaliplatino, capecitabina/oxaliplatino y combinaciones con 5-FU, esto basado en reportes que han demostrado disminuir la carga tumoral evitando resecciones innecesarias 1,14. Lamentablemente, la mayoría de los pacientes con tumores irresecables o metastásicos tienen una mala respuesta, con la única opción de un tratamiento paliativo 1,18, lo cual resalta la importancia de un diagnóstico temprano que permita la resección completa y ofrecer un potencial curativo, como se planea en este caso.
Dentro de las principales limitantes de este trabajo se encuentra un corto periodo de vigilancia postquirúrgica (6 meses); sin embargo, dentro de sus principales fortalezas se encuentra el haber sido detectado de manera preoperatoria mediante la conjunción de factores de riesgo, sintomatología de alarma y la realización de una tomografía contrastada, lo cual permitió realizar en un solo tiempo quirúrgico una resección extendida mínimamente invasiva, a diferencia de la mayoría de los casos reportados, en los que el diagnóstico se hace posterior a la colecistectomía, conllevando retrasos en el diagnóstico y en su mayoría tratamiento complementario con reintervenciones agresivas o en algunos casos tratamientos sistémicos con un poco sobrevida.
Conclusión
El adenocarcinoma vesicular es una patología que, a pesar de ser infrecuente, su pronóstico desfavorable obliga a todo el personal médico a mantener un elevado índice de sospecha basado en los factores de riesgo y sintomatología de los pacientes con la finalidad de realizar una detección temprana que permita impactar con un tratamiento quirúrgico oportuno. Como en el caso presentado, la realización de una tomografía contrastada permite estadificar las lesiones y en conjunto con un manejo multidisciplinario, orienta al tipo de tratamiento, con base al grado invasión tumoral y la presencia o no de invasión locorregional y/o a distancia.
Responsabilidades éticas
Protección de personas y animales: los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos: los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado: los autores declaran que en este artículo no aparecen datos de pacientes.