Introducción
La diabetes mellitus (DM) es un trastorno metabólico crónico que se genera por una alteración en la producción de insulina. La degeneración o disfunción de las células β y la resistencia a la insulina juegan un papel importante en la patogénesis, ya que las células de los tejidos periféricos no responden eficazmente a la insulina y no pueden absorber la glucosa de la sangre1.
La DM se puede dividir en diabetes tipo 1 y tipo 2; donde la hiperglucemia es la consecuencia compartida de ambos tipos de diabetes. En consecuencia, la DM no controlada prolongada da como resultado complicaciones macrovasculares y microvasculares, las primeras comprenden enfermedad arterial coronaria, enfermedad arterial periférica y enfermedad cerebrovascular y las microvasculares incluyen retinopatía diabética, nefropatía y neuropatía2.
En 2021, aproximadamente 537 millones de adultos, entre 20 y 79 años, padecían DM en todo el mundo3. Los reportes de la Cuenta de Alto Costo indican que 3 de cada 100 colombianos tiene DM; siendo esta la quinta causa de muerte en personas entre los 30 y 70 años. Para el año 2021 se reportaron 1'474 567 personas diagnosticadas con DM, siendo Bogotá, Antioquia y Valle del Cauca los principales departamentos con este tipo de población4.
Entre los factores de riesgo para DM, se encuentra el IMC; el cual se asocia con una prevalencia de un 4% mayor por cada unidad de aumento de este, la edad, el sedentarismo y los antecedentes familiares también se encuentran relacionados. Por eso, perder peso y las modificaciones del estilo de vida son recomendables para mantener la salud a largo plazo y evitar cualquier daño permanente en el organismo. Así como un seguimiento estricto de los valores de hemoglobina glicosilada (HbA1c), la cual un nivel elevado de esta se ha asociado con más probabilidad de causar daños5-7.
Los pacientes con DM tienen un mayor riesgo de desarrollar úlceras en los miembros inferiores. La úlcera es el resultado de una rotura de la barrera dérmica, con la subsiguiente erosión del tejido subcutáneo subyacente, que puede estar asociada a infección, ulceración o destrucción de los tejidos del pie asociada a neuropatía y/o arteriopatía periférica. La enfermedad arterial periférica se caracteriza por una disminución del flujo sanguíneo arterial secundaria a un mecanismo obstructivo, intrínseco o extrínseco, generando daño del tejido fibroso entre la capa íntima y muscular de la pared arterial8,9. En casos graves, la úlcera puede presentar exacerbaciones (úlceras superficiales, profundas, gangrenas), extendiéndose al músculo y al hueso, atribuida a una alteración del riego sanguíneo arterial, neuropatía, deformidades musculoesqueléticas o una combinación de estos factores; a su vez pueden presentar complicaciones como infecciones u osteomielitis2.
La ulceración del pie afecta al 15-34 % de los diabéticos en algún momento de su vida. Con la prevalencia de la DM hay un riesgo del 19-34 % y una tasa de recurrencia del 65 % en 5 años10, Las úlceras del pie diabético tienen complicaciones devastadoras, como amputaciones, mala calidad de vida e infecciones potencialmente mortales. Pueden ser prolongadas, tardando mucho tiempo en curarse y recidivar tras la curación. Son costosas y consumen muchos recursos sanitarios; entre ellos el manejo multidisciplinario, ya que estos pacientes requieren manejo por medicina, nutrición y rehabilitación; el costo por consultas médicas frecuentes y hospitalizaciones genera gastos para el sistema de salud y los pacientes2,8. La enfermedad del pie diabético (EPD) es la principal causa de amputaciones a nivel mundial y una de las principales causas de la carga de discapacidad9. La infección por úlcera del pie diabético (IUPD) es una causa frecuente de hospitalización representando alrededor del 25 % de estas9. El diagnóstico de IUPD se realiza principalmente de manera clínica y con el uso de biomarcadores inflamatorios, que incluyen la velocidad de sedimentación de eritrocitos (VSG), la proteína C reactiva (PCR), la procalcitonina (PCT) y el recuento de glóbulos blancos (GB); los cuales permiten diferenciar las úlceras del pie diabético (UPD) no infectadas frente a las UPD infectadas5.
El enfoque de diagnóstico actual recomendado por las pautas para diagnosticar la IUPD incluye una combinación de PCR, VSG, PCT, rayos X simples, imágenes por resonancia magnética, probe-to-bone y la prueba estándar de oro de biopsia ósea con evaluación microbiológica; todas estas ayudas diagnósticas con el fin de objetivar un tratamiento inicial además de definir el riesgo y complicaciones5. En cuanto al control de la infección, se debe realizar una limpieza de la herida y el inicio empírico de antibióticos de amplio especto como cefalosporinas de tercera generación o quinolonas; seguido de la toma de cultivo para un tratamiento dirigido. El desbridamiento para eliminación de tejido muerto o necrótico evitara una sobreinfección o progresión de la misma, con un cuidado de la herida y control de la glucosa.
Debido a esto es útil reconocer la importancia paraclínica del hemoleucograma, la PCR, y la VSG para el diagnóstico y tratamiento temprano de la osteomielitis u otras complicaciones en pacientes con pie diabético; para así realizar un diagnóstico temprano, reduciendo los costes de salud y evitar secuelas como la amputación, incluso la muerte de los pacientes. El objetivo de este estudio caracterizar los pacientes con pie diabético y sus complicaciones asociadas, identificando las diferencias relacionadas con las características sociodemográficas, clínicas y de laboratorio con sus consiguientes exacerbaciones.
Materiales y métodos
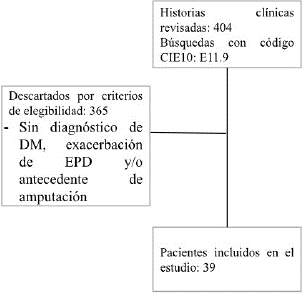
Se realizó un estudio observacional descriptivo transversal, donde se analizaron 404 historias clínicas; pero sé incluyeron 39 (ver Figura 1), donde los sé tuvieron en cuenta como criterios de inclusión, pacientes con DM mayores de edad con diagnóstico clínico y de laboratorio que presentaron úlceras pie diabético entre enero de 2018 y diciembre de 2020 en la Clínica Universitaria Bolivariana, Medellín, Colombia, los cuales fueron atendidos en servicio de urgencias y hospitalización entre el 2018 y 2020. Las variables clínicas fueron: peso (kg), altura (m), índice de masa corporal, perímetro abdominal (cm), tipo de diabetes mellitus (tipo 1, tipo 2, otros tipos), tiempo desde el diagnóstico de la diabetes, tiempo desde el diagnóstico del pie diabético, exacerbaciones de pie diabético (con exacerbación, sin exacerbación), número de exacerbaciones, tipo de exacerbación, recurrencia de la herida, infección en el sitio de la úlcera, osteomielitis y requerimiento de cirugía; mientras que las variables de laboratorio fueron: hemoglobina glicosilada (%), glicemia (mg/dl), PCR (mg/dl), VSG (mm/hr) y hemoleucograma. Aquellos pacientes donde por criterios de exclusión como historias incompletas, en las cuales no se encontraron datos (diagnóstico de DM, exacerbación de EPD o pruebas de laboratorio) para realizar el estudio y con antecedente de amputación por pie diabético fueron excluidos. Se realizó un muestreo no probabilístico por conveniencia.
La fuente de la información fueron las historias clínicas. Para la recolección se elaboró un formulario que contenía las variables del estudio, el cual permitió la consignación de las mismas de manera virtual. Muestra: Según la información brindada por las instituciones donde se realizará el estudio, se tomará la totalidad de pacientes que logren cumplir con los criterios de elegibilidad planteados durante este periodo. Los datos fueron consignados en una base de datos de Microsoft Excel para su análisis univariado por medio de frecuencias absolutas y relativas expresado en porcentajes y proporciones para las variables cualitativas; y promedio, media con desviación estándar y valores mínimo (mín) y máximo (máx) para las cuantitativas.
Este proyecto fue aprobado por el comité de ética de la institución donde se llevó a cabo; según la Resolución número 008430 de 1993 del Ministerio de Salud de la República de Colombia. Esta investigación fue clasificada como sin riesgo.
No se declaran conflictos de interés.
Resultados
Variables sociodemográficas
Se incluyeron 39 pacientes con enfermedad de pie diabético, donde el 38,5% (15) se encontraban entre los 61 a 70 años, el 59% (23) eran de sexo masculino (ver Tabla 1).
Tabla 1 Características sociodemográficas.
ND: no dato.
Área metropolitana: área urbana.
Fuera del área metropolitana: área rural.
Fuente: autores.
Variables clínicas
La mediana de peso en kilogramos (kg) fue de 66 (mín 43 - máx 105); donde el 10,2% (4) de los pacientes tenía un peso de 82 kg, la altura en metros tuvo una mediana de 1,55 (mín 1,39 - máx 1,85); la mediana de Índice de Masa Corporal (IMC) fue 25,86 (ver tabla 2). La DM más prevalente fue la DM tipo 2, con un 92,3% (36).
El tiempo (en años) transcurrido entre el diagnóstico de DM y la EPD tuvo una mediana de 8 años (min 2 -máx 46); mientras que el tiempo entre diagnóstico de EPD y la exacerbación tuvo una mediana de 4,2 años (mín 1 - máx 18).
Tabla 2 Índice de masa corporal en Kg/m2
| Índice de masa corporal (Kg/m2) | n (%) |
|---|---|
| 18 - 24,9 | 30,7 (12) |
| 25 - 29,9 | 23 (9) |
| 30 - 34,9 | 10,3 (4) |
| 35 - 39,9 | 5,3 (2) |
| ND | 30,7 (12) |
Fuente: autores.
Respecto a las exacerbaciones asociadas a la EPD, se encontró que el 85,7 % (18) de los pacientes tuvieron recurrencia de estas, según los reportes encontrados en las historias clínicas (ver Tabla 3).
Tabla 3 Caracterización de las exacerbaciones de la EPD.
| Variable | % (n) | |
|---|---|---|
| Presencia de exacerbación n (39) | sí | 53,8 (21) |
| No | 41,1 (16) | |
| ND | 5,1 (2) | |
| Tipo de exacerbación n (21) | Ulcera superficial | 23,8 (5) |
| Ulcera profunda | 33,3 (7) | |
| Gangrena limitada | 28,6 (6) | |
| ND | 14,3 (3) | |
| Numero de exacerbaciones n (21) | < 3 | 76,2 (16) |
| > 3 | 9,5 (2) | |
| ND | 14,3 (3) | |
| Infección en el sitio de la lesión n (21) | Sí | 76,2 (16) |
| No | 19 (4) | |
| ND | 4,8 (1) | |
| Osteomielitis asociada n (21) | Sí | 57,1 (12) |
| No | 38,1 (8) | |
| ND | 4,8 (1) | |
Fuente: autores.
Variables de laboratorio
Respecto al valor de la hemoglobina glicosilada (HbA1c) al momento del diagnóstico de EPD, el 5,1 % (2) de los participantes tenía un valor < 5,7 % para la HbA1c; en el 12,8 % (5) se encontró un valor entre 5,8 y 6,4 %; el 53,8 % (21) tuvo un valor > a 6,4 % y en el 28,2 % (11) de los participantes no se encontró datos (ver Tabla 4).
Tabla 4 Variables de laboratorio
| Reactante | Mediana (min - máx) | |
|---|---|---|
| Pre | ||
| Velocidad de sedimentación globular (VSG) mm/h | 36, 5 (4 - 83) | 32 (4 - 50) |
| Proteína C reactiva (PCR) mg/dL | 7,4 (0,42 - 139) | 7,3 (0,41 - 37,1) |
| Recuento de neutrófilos células/mm³ | 6.600 (3.150 - 9.950) | 7.475 (1.890 - 16.520) |
Fuente: autores.
Con relación a los pacientes que presentaron exacerbaciones - 53,8 % (21) -, el 19 % (4) tuvieron un valor de HbA1c entre 5,7 a 6,4 al momento de la exacerbación por EPD; el 33,3 (7) tuvieron valores > 6,4 y en el 47,6 % (10) no se encontró este dato. Respecto a los reactantes de fase aguda pre y post exacerbación de la EPD se encontró que la Velocidad de Sedimentación Globular (VSG) tuvo una disminución, presentando una mediana de 36,5 mm/h y de 32 mm/h pre y post exacerbación respectivamente; la Proteína C Reactiva (PCR) tuvo una mediana previa a la exacerbación de 7,4 mg/dL y una posterior de 7,3 mg/dL.
De los pacientes que fueron diagnosticados con osteomielitis, 35,9 (14) recibieron tratamiento antimicrobiano para su infección. Mientras que los pacientes que presentaron exacerbaciones en la EPD, 38,5 % (15) de ellos requirieron cirugía por su exacerbación; la cual fue amputación de la extremidad afectada.
Discusión
La EPD es la principal causa de amputaciones a nivel mundial y uno de los motivos de discapacidad más frecuentes12; a su vez, la infección y la isquemia se consideran las dos amenazas más importantes en este tipo de pacientes13.
Un alto IMC aumenta el riesgo de desarrollar DM, además, en el caso de las UPD, puede aumentar la presión sobre los pies y dificultar la cicatrización, con respecto a estos valores, en el estudio de Wukich et al. de 2022, donde se evaluó la amputación y la infección de los pacientes con complicaciones diabéticas en los pies, determinando el grado de UPD, reportaron una mediana de 33,5 kilogramos/metros cuadrados (kg/m2) mientras que en el presente estudio la mediana de IMC fue 25,86 kg/m2; datos distintos, donde existe una asociación del sobrepeso y obesidad con la presencia de DM y UPD14.
En cuanto a las EPD, la DM está relacionada fuertemente ya que el aumento de la glucemia de manera crónica daña los nervios y vasos sanguíneos en los pies. En este estudio la DM más prevalente fue la DM tipo 2, con un 92,3 % (36), dato similar al observado en el estudio realizado por Choi et al. del año 2022 donde se analizó la amputación y la infección como complicaciones en pacientes con EPD, los cuales tuvieron un seguimiento durante al menos 6 meses tras la cicatrización de la herida en el que reportaron 96,6 % (491) con este mismo tipo de diabetes15.
En el trabajo de 2022 por Pintaudi et al. en el que realizaron un estudio observacional, retrospectivo, de un solo centro, el cual se basó en el seguimiento a pacientes con DM a un año, reportaron una mediana de duración de la DM hasta el diagnóstico de la EPD de 26,6 años,16 mientras que el estudio de Choi et al., reportó un seguimiento desde el inicio de EPD hasta la exacerbación con una mediana de 4,4 años15; estos datos son comparables con este estudio donde se tuvo una mediana de 8 años entre el diagnóstico de DM y EPD; y 4,2 años entre el diagnóstico de EPD y alguna exacerbación. Esto en comparación con el estudio de Andersen et al. donde de evaluó el tratamiento conservador de las UPD no infectadas consiguen una cicatrización fiable de la herida y la recuperación de la extremidad en caso de isquemia leve-moderada, donde todas las heridas cicatrizaron y no hubo recurrencia de EPD con infección para los pacientes en un tiempo medio de seguimiento de 0,9 años16.
Con relación al tipo de lesión, causadas por la pérdida de sensibilidad en los pies, la exacerbación de la EPD en este estudio fue de un 33,3 %, 28,6 % y 23,8 %, donde presentaron úlcera profunda, gangrena limitada y úlcera superficial respectivamente, en comparación con el trabajo realizado por Andersen et al.16 donde se tuvo en cuenta el tratamiento conservador de las úlceras del pie diabético y la recuperación de la extremidad, reportaron un 85,2 %, 9,8 % y 5 % para ulceraciones superficiales, gangrena seca y heridas que no cicatrizan respectivamente.
Limitaciones del estudio
Es importante destacar las limitaciones presentadas en el presente estudio, debido a que no se realizaron medidas de asociación entre las variables estudiadas, lo que limita la capacidad para analizar las mismas. Estas pueden generar cierta discrepancia en los hallazgos y, por lo tanto, deben ser tenidos en cuenta al comparar los resultados con otras poblaciones.
Conclusión
La diabetes no controlada y sin seguimiento puede llegar a resultar en una comorbilidad importante en este tipo de pacientes. Es importante tener en cuenta la relación entre la DM tipo 2 y las complicaciones asociadas a la EPD, así como la evaluación de un enfoque integral en el diagnóstico, prevención y tratamiento. Abordar los factores de riesgo que pueden influir en el mal pronóstico, como el IMC es importante para prevenir daños anatómicos y mejorar procesos de cicatrización. El control de la glucemia y la prevención de infección en pacientes con diagnóstico de EPD es de vital importancia para evitar sobreinfecciones, osteomielitis y el requerimiento de procesos quirúrgicos que pueden terminar en la amputación de la extremidad. El apoyo en las ayudas diagnósticas y seguimiento con los reactantes de fase aguda pueden proporcionar información valiosa en cuanto al estado inflamatorio. Se debe tener en cuenta la necesidad de una atención multidisciplinaria que aborde aspectos clínicos como los factores de riesgo para prevenir complicaciones y discapacidades; todo esto con el fin de promover una mejor calidad de vida en esta población.