Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Vitae
Print version ISSN 0121-4004
Vitae vol.15 no.1 Medellín Jan./June 2008
FARMACOLOGÍA Y TOXICOLOGÍA
BAJA GENOTOXICIDAD DE EXTRACTO ORGÁNICO DE AGUA DE MAR DE COVEÑAS (SUCRE, COLOMBIA)
LOW GENOTOXICITY OF ORGANIC SEA WATER EXTRACTS FROM COVEÑAS (SUCRE, COLOMBIA)
Wilmer SOLER T.1*; Nelly D. VELÁSQUEZ E.2; Juan P. SOLER A.3
1. Facultad de Medicina. Universidad de Antioquia. A.A. 1226, Medellín, Colombia
2. Instituto de Biología. Facultad de Ciencias Exactas, Universidad de Antioquia. A.A. 1226, Medellín, Colombia.
3. Facultad de Química Farmacéutica. Universidad de Atnioquia. A.A. 1226, Medellín Colombia.
RESUMEN
El agua de mar natural se utiliza en algunos países iberoamericanos como elemento nutritivo y terapéutico, y en los países desarrollados se usa como complemento nutricional de forma refinada y comercial. Los estudios de ingesta de agua de mar tratada muestran que no hay toxicidad; sin embargo, el uso de agua cercana a las playas representa un riesgo para la salud debido a la polución de los centros urbanos. En este estudio se emplearon linfocitos humanos y la electroforesis de células individuales (ensayo cometa), para comparar la genotoxicidad de un extracto orgánico de agua de mar tomada de la orilla respecto a muestras obtenidas mar adentro en el pequeño municipio de Coveñas-Sucre, Colombia, que vierte sus aguas domésticas directamente al mar o a pozos sépticos. Se observa genotoxicidad a
37 ºC pero no a 4 ºC, este efecto es dependiente de la concentración del extracto (p<0.0001), del sitio de muestreo (p=0.0026) y de la interacción de estos dos factores (p=0.0001). La muestra orgánica que presenta menor genotoxicidad es la de mar adentro. La citotoxicidad del extracto orgánico de agua de mar es muy baja comparada con la obtenida de muestras del acueducto de Medellín (Colombia).
Palabras clave: agua de mar, extracto orgánico, genotoxicidad, citotoxicidad, ensayo cometa
ABSTRACT
Natural sea water is used as a nutritive and therapeutic element in Ibero-American countries, and commercial, refined sea water as a nutritional complement in developed countries. Although treated sea water has no toxicity, as demonstrated by previous sea water ingestion studies, consumption of near-shore seawater poses a health risk due to pollution of nearby urban centers. In this study, human lymphocytes and single cell gel electrophoresis (comet assay) were used to compare the genotoxicity of an organic sea water extract taken near shore with that of sea water samples taken offshore in the small municipality of Coveñas (Sucre, Colombian), where domestic waters are flushed directly into the sea or into septic tanks. Genotoxicity was observed at 37°C, but not at 4°C. This effect depends on the concentration of extract (p<0.0001), the sampling site (p=0.0026), and the interaction of these two factors (p=0.0001). The lowest genotoxicity was observed in offshore organic samples. The cytotoxicity of sea water organic extracts was very low compared to that of the freshwater samples from the water supply system in Medellín (Colombia).
Keywords: sea water, organic extract, genotoxicity, cytotoxicity, comet assay.
INTRODUCCIÓN
En la cultura occidental, las propiedades terapéuticas del agua de mar (AM) se conocen desde sus inicios (1). Las investigaciones científicas se iniciaron hace cerca de 100 años, con los trabajos del fisiólogo francés Rene Quinton, quien demostró la similitud entre el AM y los líquidos fisiológicos de diversos organismos, incluyendo el ser humano, por el contenido de minerales y oligoelementos. Con sus estudios se iniciaron los dispensarios marinos, como lugares donde se hacían aplicaciones subcutáneas para el control de graves epidemias infecciosas y de desnutrición, que afectaba particularmente a la población infantil (2, 3). En décadas recientes ha renacido el interés por las propiedades terapéuticas y nutricionales del AM, a tal punto que hoy se consigue una amplia variedad de productos comerciales de AM refinada o filtrada, como complemento nutricional, por su alto contenido de minerales como Mg y Ca y cerca de 95 oligoelementos en cantidades traza (4). En el campo médico son interesantes los estudios recientes realizados en humanos sobre el efecto de la ingesta de AM en problemas de piel (5), rinitis alérgica (6); en animales se ha observado prevención de la aterosclerosis e hiperlipidemias (7, 8). Uno de los aspectos que llama la atención del AM es su acción inespecífica en diversas patologías, lo que se atribuye al contenido de minerales y oligoelementos que afectan positivamente todos los sistemas del organismo y podría ayudar a resolver los mayores problemas de salud de los países occidentales, por el estilo de vida, en particular la dieta refinada, pobre en algunos minerales como Mg, Ca y micronutrientes. Por otra parte, se ha mostrado la ausencia de toxicidad en animales que ingirieron AM refinada de profundidad (mayor de 200 m) y de superficie (8, 9). En una de nuestras investigaciones mostramos la ausencia de genotoxicidad del AM natural sobre linfocitos humanos incubados por una hora y la estabilidad de los eritrocitos frente a un periodo de incubación de tres horas (10).
En Colombia y otros países de Iberoamérica se viene utilizando el AM natural como elemento terapéutico y nutricional. Se obtiene de las orillas en lugares limpios y poco habitados, o de mar adentro a varios kilómetros de la playa, ya sea de la superficie ó a 10-20 m de profundidad. En Medellín (Colombia) y municipios cercanos se consume AM obtenida en la isla de Barú y Coveñas, de la costa Caribe colombiana. Sin embargo, existen riesgos de contaminación en Coveñas por las posibles fugas de petróleo, dado que ahí funciona un puerto petrolero, y por las aguas vertidas de las zonas urbanas, que se suman a la falta de alcantarillado (11).
Dada la baja concentración del material orgánico del agua de consumo humano, incluyendo el AM, se ha utilizado la extracción por cromatografía y luego la incubación del material concentrado en las pruebas de toxicidad celular. Esta técnica ha sido empleada en Colombia y otros países para detectar la presencia de sustancias genotóxicas en aguas de río y de mar (12, 13, 14,15, 16). En varios de estos estudios y en el presente trabajo se utilizó la electroforesis de células individuales o Ensayo Cometa como indicador de genotoxicidad, ya que detecta rupturas de cadena sencilla y/o reparación del ADN en cualquier población de células eucarióticas (19). Además, es una metodología rápida y sensible, ampliamente utilizada en el biomonitoreo y pruebas de genotoxicidad de productos naturales, sustancias contaminantes y fármacos (17, 18). Con el fin de determinar in vitro la bioseguridad de la ingesta del AM de Coveñas, el material orgánico contenido en tres muestras de AM se concentró mediante cromatografía de columna y resinas XAD 2/7, y luego se compararon sus respectivas citotoxicidad y genotoxicidad en linfocitos humanos.
MATERIALES Y MÉTODOS
Toma de muestras y procesamiento. Se tomaron tres muestras de AM de 100 L cada una, en la zona de Coveñas, frente al Centro Colombiano de Talasoterapia a distancias de 10 m, 5 y 8 km de la línea costera. Para las dos últimas, a una profundidad de 10 m utilizando una bomba de succión o achique de material plástico especial para esta clase de agua. Dos de las muestras (10 m y 5 km) se colectaron cerca de las 10 a.m. del mismo día en el mes de noviembre, después de un día de lluvia, y a los 15 días se colectó la tercera muestra (8 km) con el fin de evitar algún efecto del agua lluvia. Las muestras se depositaron en recipientes plásticos de polietileno de alta densidad (HDPE) y luego se transportaron toda la noche por vía terrestre a temperatura ambiente hasta el laboratorio de Bioquímica de la Facultad de Medicina de la Universidad de Antioquia, para su procesamiento inmediato. Se les midió el pH, la salinidad y la presencia de coliformes totales y fecales, como indicador de contaminación microbiológica terrestre.
Concentración del extracto orgánico (EO). Se concentró el EO a partir de 100 L de cada una de las tres muestras de AM, dado que los compuestos genotóxicos pueden estar a muy bajas concentraciones. La adsorción del EO no volátil contenido en estas muestras de agua se hizo por el método de adsorción en resinas styrene divinylbenceno amberlita XAD-2 y XAD-7 no polares, de acuerdo con los procedimientos descritos (20, 21), con algunas modificaciones. Cada muestra se pasó por una columna que contenía 100 g de resina XAD-2 y 100 g de XAD-7 a una velocidad aproximada de 15 mL/min. La elución se realizó con 300 mL de acetona. El volumen del eluyente se retiró por rota evaporación a baja presión, hasta eliminar la acetona, y la porción acuosa se liofilizó. Se pesaron los extractos liofilizados, se diluyeron en DMSO al 50% y se guardaron a 4ºC para realizar posteriores pruebas de viabilidad y genotoxicidad.
Prueba de viabilidad (efecto citotóxico): Mediante el método de centrifugación en gradiente de Ficoll, se aislaron linfocitos humanos a partir de sangre total tratada con EDTA de un donante no consumidor de AM (para lo cual se obtuvo el consentimiento informado). Después del aislamiento, se evaluó la viabilidad por el método de exclusión del colorante azul tripano (0.2 %). Luego se incubaron a tres diluciones del EO del AM, a 4ºC y a 37ºC por una hora, después de lo cual, nuevamente se evaluó la viabilidad. Con este procedimiento se encontró la concentración más alta, a la cual no se afectó la viabilidad.
Prueba de genotoxicidad (ensayo cometa): Para determinar el daño en el ADN, se siguió la técnica SCGE o ensayo cometa, según el protocolo descrito (19). Se utilizó H2O2 (150uM) como control positivo y buffer fosfato salino (PBS) como control negativo. Se prepararon tres diluciones del EO, a partir de la más alta, que no presentó alteración en la viabilidad celular, con diluciones sucesivas a la mitad y por duplicado. Después del tratamiento por una hora de los linfocitos con las diluciones del concentrado orgánico de AM, se tomaron 10 µL de esta suspensión y se mezclaron con 75 µL de agarosa de bajo punto de fusión (LMA) a 37ºC y se colocaron en un portaobjetos el cual ha sido previamente recubierto con una capa de agarosa de punto de fusión normal (NMA). Luego las láminas se sumergieron en una solución de lisis (NaCl 2.5 M, Na2EDTA 100mM, Tris 10 mM, triton X-100 1%, DMSO 10%) a 4ºC por una hora, después se llevaron a un buffer de electroforesis a pH 13 (Na2EDTA 1 mM, NaOH 300mM) a 4ºC por 30 minutos, para permitir desenrollamiento del ADN y expresión de sitios lábiles a álcalis. Luego se realizó la electroforesis durante 30 minutos a 25 voltios y 300mA. Después, las láminas se lavaron con buffer neutralizante (tris 0.4 M pH 7.5) por 15 minutos. Finalmente las láminas se colorearon con 50 µL de bromuro de etidio al 2% y se examinaron en un microscopio de fluorescencia equipado con un filtro de excitación de 515-560 nm y un filtro barrera de 590 nm usando una magnificación de 40X. Para cada dilución del concentrado orgánico de AM, se analizaron al menos 50 células, usando un programa de computador de acceso público (22), especial para el ensayo cometa, que permite medir la longitud de la migración y la intensidad de la fluorescencia, como Momento de Olive (MO), que nos da la relación entre la distancia desde el centro de gravedad de la cabeza (CGH) al centro de gravedad de la cola (CGT) y el porcentaje de DNA en la cola % DNAT:

Para el análisis de los datos, se realizó un análisis de varianzas, con dos factores: la concentración y el lugar de muestreo. Se consideró un nivel de significancia p<0.05. Se utilizó el paquete estadístico STATISTICA 7.0 (Stat Soft, Inc. Tulsa, OK, USA).
RESULTADOS
Las características fisicoquímicas de las muestras de AM recogidas a distancias media y adentro son similares respecto al pH y la presencia de coliformes; sin embargo, difieren en salinidad, con menor porcentaje para la muestra de media distancia y muy cercana al valor de la muestra de la orilla (Véase tabla 1).
Tabla 1. Características fisicoquímicas y microbiológicas de tres muestras de agua de mar de Coveñas-Sucre, Colombia.
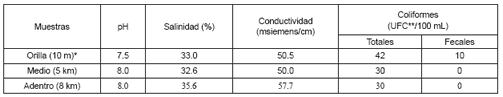
* Distancia de colección desde la línea de playa. A los 5 y 8 km se obtuvo a 10 m. de profundidad.
** UFC: unidades formadoras de colonias
El rendimiento de la obtención del EO de AM por cromatografía de amberlita XAD 2/7, fue 10 veces mayor respecto a lo obtenido a partir de agua del acueducto de la ciudad de Medellín (Véase tabla 2).
Tabla 2. Características físicas del extracto orgánico extraído de tres muestras de agua de mar de Coveñas-Sucre, Colombia.

* Distancia de colección desde la línea de playa, a los 5 y 8 km se obtuvo a 10 m de profundidad
** AM: agua de mar
La viabilidad de las células incubadas en EO de AM bajó del 90% cuando se utilizó una concentración de 5 mg/mL, con similar resultado para las tres muestras de AM, mientras que para el extracto del agua del acueducto, clorada y sin clorar, bajó del 90% cuando se utilizó una concentración de 0.27 mg/mL (Véase tabla 3).
Tabla 3. Viabilidad de los linfocitos humanos expuestos a extracto orgánico de agua de mar (Coveñas-Sucre, Colombia) y agua de acueducto (Medellín).

*EO: extracto orgánico. La viabilidad de los linfocitos tratados con PBS (control negativo) y con H2O2 (control positivo) fue mayor del 95%.
Cuando los linfocitos se trataron con EO de AM a concentraciones de 1.7, 3.3, y 5.0 mg/mL por una hora a 4ºC, no se observó daño genotóxico. Por el contrario, el tratamiento de estas células con el mismo extracto e iguales concentraciones, pero a una temperatura de 37°C sí ocasionó daño genotóxico (Véase figura 1). Este efecto fue dependiente de la concentración del extracto orgánico (p<0.0001), del sitio de recogida (p=0.0026) y con efecto significativo de la interacción de estos dos factores (p= 0.0001), según el análisis de varianzas del MO transformado logarítmicamente.
Figura 1. Electroforesis de linfocitos humanos después de incubación a 37 ºC en extracto orgánico de agua de mar de Coveñas-Sucre, Colombia (ensayo cometa).

A= mitad 5.0 mg/mL, B= adentro 5.0 mg/mL, C= control negativo, D= control positivo
El mayor daño del ADN se presentó a la concentración más alta de EO (5.0 mg/mL). La muestra que presentó el menor daño a esta concentración fue la de mar adentro, que además presentó la menor variación del promedio del MO entre las tres concentraciones de EO utilizadas en la incubación (Véase figura 2).
Figura 2. Análisis de varianzas de medias del Momento de Olive de linfocitos humanos incubados en tres extractos orgánicos de agua de mar de Coveñas-Sucre, Colombia en función de la concentración, a 37 ºC.
Sitio recogida p=0.0026, Concentración p=0.0000, Interacción p=0.0001. Las barras verticales indican el intervalo de confianza del 95 %. El número de células utilizado a las concentraciones de 1.7, 3.3 y 5.0 mg/mL fue respectivamente: orilla: 254, mitad: 212 y adentro: 206
DISCUSIÓN DE RESULTADOS
El alto contenido de EO obtenido del AM, comparado con el agua de acueducto, la califican como un medio orgánico (3, 23). La fracción de este material, separado por cromatografía de resinas XAD, corresponde a moléculas sencillas y macromoléculas derivadas del carbono de carácter hidrofóbico, posiblemente carbohidratos y proteínas no identificadas plenamente que hacen parte del material orgánico disuelto en el AM y son productos metabólicos de los microorganismos marinos (23, 24). Se conoce que buena parte de estas moléculas se encuentran en forma de complejos con elementos traza y minerales tan abundantes como Ca y Mg; por ejemplo, se ha calculado que más del 99% del Cu contenido en el AM está en forma de complejos orgánicos (25). El desarrollo de la química bioinorgánica (26) ha mostrado la presencia de fuertes complejos orgánico-metálicos en los sistemas biológicos, algunos metales como Fe, Cu, Zn, entre otros, ocupan centros activos en enzimas y otras proteínas.
Las concentraciones del EO de AM utilizadas en los experimentos de viabilidad y genotoxicidad fueron muy altas, en particular si se considera que en la prueba de viabilidad de los linfocitos incubados con este extracto se observó daño de membrana a una concentración 20 veces mayor que la obtenida con EO de agua potable del acueducto de Medellín. En los linfocitos humanos incubados a 4ºC con el EO de AM no se observó genotoxicidad significativa, lo que permite sugerir baja toxicidad de este material. Los resultados obtenidos a 37ºC pueden originarse de un proceso de reparación de las modificaciones ocasionadas por el material orgánico, proceso que se inhibe cuando la incubación se realiza a 4ºC (19, 27). También hay que considerar que la fragmentación del ADN observada a 37ºC puede explicarse porque a mayor temperatura habrá mayor transporte y reactividad entre las sustancias genotóxicas y las macromoléculas de las células.
El efecto de dosis para el EO de las muestras de AM no fue lineal. La muestra que presentó el menor MO, a la concentración más alta de 5 mg/mL fue la de mar adentro (8 km), y la mayor fue para la muestra de la mitad (5 km). Se puede explicar este resultado por la presencia de corrientes marinas, que se pudieron observar a simple vista; por el color marrón de las corrientes de aguas lluvias cerca de la playa, color que se atribuye a la presencia de material orgánico disuelto en las corrientes de aguas de procedencia terrestre (28). El color marrón del EO de la muestra de AM obtenida a 5 km indica la presencia de aguas lluvias mezcladas con AM. La presencia de coliformes fecales en la muestra de la orilla, aunque en baja cantidad, se explica por la ausencia de alcantarillado y el uso de pozos sépticos en la población de Coveñas. En consecuencia, es recomendable recoger el AM para consumo humano en otros lugares menos poblados o, en su defecto, aplicar algún tratamiento para desinfectarla.
Con los resultados de este estudio in vitro podemos concluir que este EO del AM ofrece bioseguridad para el consumo humano respecto al efecto genotóxico, de manera particular si es agua obtenida en las condiciones que aseguren su estado natural, libre de mezclas con aguas lluvias y servidas que arrastran sedimentos y microorganismos terrestres. Los efectos de la polución orgánica dependen principalmente de la cantidad de contaminantes introducidos, pero modificados por factores tales como la configuración del fondo, las mareas y las corrientes, que influyen sobre la difusión de los contaminantes, y en especial, por el catabolismo que realizan los microorganismos marinos sobre este componente orgánico (29)
REFERENCIAS BIBLIOGRÁFICAS
1. Diógenes L. Vidas de los más ilustres filósofos griegos. Barcelona: Orbis SA; 1985. [ Links ]
2. Mahé A. El plasma de Quinton. El agua de mar nuestro medio interno. Barcelona: Icaria; 1999. [ Links ]
3. Quinton R. L´eau de mer milieu organique. Constance du milieu marin originel comme milieu vital des cellules, à travers la série animale. 39ª ed. Paris: Encre; 1995 [1904]. [ Links ]
4. Nozaki Y. A fresh look at element distribution in the North Pacific. [Sitio en internet]. Disponible en: http://www.agu.org/eos_elec/97025e.html. Consultado: 17 de septiembre de 2007. [ Links ]
5. Kimata H, Tai H, Nakagawa K, Yokoyama Y, Nakajima H, Ikegami Y. Improvement of skin symptoms and mineral imbalance by drinking deep sea water in patients with atopic eczema/dermatitis syndrome (AEDS). Acta Médica 2002; 45(2):83-84. [ Links ]
6. Kimata H, Tai H, Nakajima H. Reduction of allergic skin responses and serum allergen-specific IgE and IgE-inducing cytokines by drinking deep-sea water in patients with allergic rhinitis. Otorhinolaryngol Nova 2001; 11(6):302-303. [ Links ]
7. Yoshioka S, Hamada A, Cui T, Yokota J, Yamamoto S, Kusunose M, et al. Pharmacological activity of deep-sea water: examination of hyperlipemia prevention and medical treatment effect. Biol Pharm Bull 2003; 26(11):1552-1559. [ Links ]
8. Miyamura M, Yoshioka S, Hamada A, Takuma D, Yokota J, Kusunose M, et al. Difference between deep seawater and surface seawater in the preventive effect of atherosclerosis. Biol Pharm Bull 2004; 27(11):1784-1787. [ Links ]
9. Tsuchiya Y, Watanabe A, Fujisawa N, Kaneko T, Ishizu T, Fujimoto T, et al. Effects of desalated deep seawater on hematologic and blood chemical values in mice. Tohoku J Exp Med 2004; 203(3):175-182. [ Links ]
10. Soler W, Velásquez N del C, Miranda LF, Zuluaga DC. Ausencia de genotoxicidad de agua de mar de Coveñas: estudio in vitro en eritrocitos y leucocitos humanos. Revista Facultad Nacional de Salud Pública 2005; 23 (2):25-30. [ Links ]
11. Ministerio de Salud. Perfiles epidemiológicos. Región costa Atlántica. Bogotá: Ministerio de Salud; 1996. [ Links ]
12. Velásquez N. Mutagenicidad y genotoxicidad de extractos de agua tratada para el consumo humano y de subproductos de la cloración. [Tesis] Medellín: Universidad de Antioquia; 2000. [ Links ]
13. Yuan J, Liu H, Zhou LH, Zou YL, Lu WQ. Oxidative stress and DNA damage induced by a drinking-water chlorination disinfection by product 3-chloro-4-(dichloromethyl)-5-hydroxy-2(5H)-furanone (MX) in mice. Mutat Res 2006; 609(2):129-136. [ Links ]
14. Aleem A, Malik A. Genotoxicity of water extracts from the River Yamuna at Mathura. Environ Toxicol 2003; 18(2):69-77. [ Links ]
15. Wu JY. Assessing surface water quality of the Yangtze Estuary with genotoxicity data. Mar Pollut Bull 2005; 50(12):1661-1667. [ Links ]
16. Zietz BP, Nordholt G, Ketseridis G, Pfeiffer EH. Mutagenicity of Baltic seawater and the relation to certain chemical and microbiological parameters. Mar Pollut Bull 2001; 42(10):845-851. [ Links ]
17. Márquez-Fernández ME, López-Ortiz JB, Correa-Londoño G, Pareja-López A, Giraldo-Solano A. Detección del daño genotóxico agudo y crónico en una población de laboratoristas ocupacionalmente expuestos. Iatreia 2003; 16(4):275-282. [ Links ]
18. Pareja-López A, García-García CP, Abad-MejíaPJ, Márquez-Fernández ME. Estudio in vitro de la citotoxicidad y genotoxicidad de los productos liberados del acero inoxidable 316L con recubrimientos cerámicos bioactivos. Iatreia 2007; 20(1):12-20. [ Links ]
19. Singh NP, McCoy MT, Tice R, Schneider EL. A simple technique for quantitation of low levels of DNA damage in individual cells. Exp Cell Res 1988; 175(1):184-191. [ Links ]
20. Meier JR, Blazak WF, Knohl R. Mutagenic and clastogenic properties of 3-chloro-4-(dichloromethyl)-5-hydroxy-2(5H)-furanone: A potent bacterial mutagen in drinking water. Environ Mol Mutagen 1987; 10(4):411-424. [ Links ]
21. Stahl RG. The genetic toxicity of organic compounds in natural waters and wastewaters. Ecotoxicol Environ Saf 1991; 22 (1):94-125. [ Links ]
22. Comet Score. Version 1.5 Free comet scoring software (TriTek-Corp, USA). [Sitio en internet]. Disponible en: http://autocomet.com Consultado: 17 de septiembre de 2007. [ Links ]
23. Ogawa H, Tanoue E. Dissolved organic matter in oceanic waters. J Oceanography 2003; 59(2):129-147. [ Links ]
24. Aluwihare LI, Repata DJ, Chen RC. A major biopolymeric component to dissolved organic carbon in surface seawater. Nature 1997; 387:166-169. [ Links ]
25. Hirose K. Chemical speciation of trace metals in seawater: a review. Anal Sci 2006; 22(8):1055-1063. [ Links ]
26. Voet D, Voet JG, Pratt Ch W. Fundamentos de Bioquímica. La vida a nivel molecular. 2ª ed. Buenos Aires: Editorial Médica Panamericana; 2006. [ Links ]
27. Meyers CD, Fairbairn DW, O´Neill KL. Measuring the repair of H2O2-induced DNA single strand breaks using cell gel assay. Cytobios 1993; 74(298-299):147-153. [ Links ]
28. Coble P, Hu Ch, Gould RW, Chang G, Word M. Coastal ocean optics and dynamics. Oceanography 2004; 17(2):50-59. [ Links ]
29. Hood DW. Los ciclos químicos del mar. En: Vetter RC. Oceanografía. La última frontera. Buenos Aires: El Ateneo; 1976: 30-40. [ Links ]
AGRADECIMIENTOS
Los autores agradecen al CODI (Universidad de Antioquia) por la financiación de este trabajo, a la Fundación española Aquamaris y al Centro Colombiano de Talasoterapia por el apoyo logístico; al profesor Benjamín Alberto Rojano, de la Universidad Nacional-sede Medellín, por su apoyo técnico, y al profesor Abel Díaz Cadavid del Centro de Investigaciones Médicas de la Universidad de Antioquia por la asesoría estadística.
Recibido: Noviembre 4 de 2007; Aceptado: Abril 8 de 2008
* Autor a quien se debe dirigir la correspondencia: wsoler@udea.edu.co















