Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista MVZ Córdoba
Print version ISSN 0122-0268On-line version ISSN 1909-0544
Rev.MVZ Cordoba vol.13 no.3 Córdoba Sept./Dec. 2008
ORIGINAL
PARTIAL CHARACTERIZATION OF ANTILISTERIAL COMPOUNDS PRODUCED BY NATIVE LACTIC ACID BACTERIA
Blanca Botina A,1 M.Sc, Barbara H. Zimmermann,2 Ph.D, *María Vanegas L,1 M.Sc.
1 Universidad de los Andes, Laboratorio de Ecología Microbiana de Alimentos (LEMA), Cr 1 N° 18 A - 10. Edificio J, Laboratorio 209. Bogotá, Colombia.
2 Universidad de los Andes, Bioquímica y Biología Molecular de Parásitos (BBMP), Cr 1 N° 18 A - 10. Edificio M, Laboratorio 302.Bogotá, Colombia. *Correspondencia: mvanegas@uniandes.edu.co
Recibido: Julio 8 de 2008; Aceptado: Diciembre 10 de 2008
RESUMEN
Objetivo. Caracterizar los metabolitos producidos por bacterias ácido lácticas nativas con capacidad antilisterial. Materiales y métodos. Se analizaron 42 muestras tomadas de alimentos y equipos procesadores de alimentos, de donde se aislaron bacterias ácido lácticas, las cuales se identificaron por medio de pruebas bioquímicas. Se evaluó la actividad antagónica de las cepas aisladas frente a 17 cepas de L. monocytogenes pertenecientes a los serotipos 4b, 4e, y 3b utilizando la técnica de la gota y doble capa. Se obtuvieron extractos crudos para la caracterización de los metabolitos inhibitorios del crecimiento de las cepas de L. monocytogenes, los cuales fueron tratados con catalasa, ácido clorhídrico, proteinasa K y temperaturas de 95°C y 121°C. El peso molecular de las proteínas se aproximó utilizando la técnica de electroforesis SDS-PAGE y bioensayos. Resultados. De un total de 250 aislamientos se lograron identificar 75 cepas de bacterias ácido lácticas. La evaluación de la actividad antagónica indicó que los metabolitos inhibitorios producidos por las bacterias ácido lácticas no actuaban de igual manera frente a las diferentes cepas de L. monocytogenes. Sin embargo, se encontró que tres de los aislamientos nativos identificados como Lactobacillus spp., Leuconostoc spp. y Enterococcus spp. presentaban una mejor actividad antilisterial debido a que sintetizan proteínas o metabolitos de peso molecular menor a 7600 Da. Conclusiones. En los alimentos distribuidos en Colombia existen cepas de bacterias ácido lácticas con potencial bioprotector.
Palabras clave: Bacterias ácido lácticas, L. monocytogenes, antagonismo, bacteriocinas.
ABSTRACT
Objective. Characterization of antilisterial compounds produced by native lactic acid bacteria. Materials and methods. Lactic acid bacteria (LAB) were isolated from 42 samples collected from foods and food processing equipment. Identification of LAB species was assessed by biochemical reactions. The antilisterial activities of the isolates were tested against 17 L. monocytogenes strains belonging to 4b, 4e and 3b serotypes, by the agar differed spot on the lawn technique. Crude extracts were subjected to catalase, proteinase K, hydrochloric acid and high temperature (95°C and 121°C) treatments in order to characterize the antilisterial compounds. The molecular weights were estimated by SDS-PAGE and bioassays were performed. Results. Seventy five strains were identified out of 250 lactic acid bacteria isolates. The inhibitory compounds produced by LAB displayed dissimilar activities against the different L. monocytogenes strains. Furthermore, three native isolates identified as Lactobacillus spp., Leuconostoc spp. and Enterococcus spp. showed improved antilisterial effect due to the production of compounds with molecular weight below 7600 Da. Conclusions. We demonstrated the presence of native lactic acid bacteria with potential as biocontrolers in foods distributed in Colombia.
Key words: Lactic acid bacteria, L. monocytogenes, antagonistic, bacteriocins.
INTRODUCCIÓN
Las bacterias ácido lácticas (BAL) consideradas por la FDA (Food and Drug Administration, USA) como bacterias GRAS (Generally Recognised As Safe) (1,2) han sido utilizadas en la elaboración de alimentos fermentados, con el objetivo de proporcionar sabor, color y aroma característicos durante la fermentación (3,4). Sin embargo, la capacidad de producir biocompuestos que pueden inhibir el crecimiento de microorganismos como ácidos orgánicos, peróxido de hidrógeno, sustancias de bajo peso molecular y las bacteriocinas, hacen que estas bacterias o sus metabolitos sean utilizados como biopreservantes en la industria de alimentos, frente a microorganismos deteriorantes y/o patógenos, como alternativas a los métodos de conservación químicos tradicionales, debido a la capacidad de competencia y/o acción de sus productos metabólicos (5).
Informes epidemiológicos han indicado desde 1981 hasta el 2003 una incidencia de L. monocytogenes con una alta tasa de mortalidad la cual ha oscilado entre el 15 y el 40% debido al consumo de alimentos contaminados en países como Canadá, Estados Unidos, Dinamarca, Francia e Inglaterra (6). En Colombia se determinó la presencia de L. monocytogenes en una gran variedad de productos cárnicos como carne bovina fresca, pollo procesado, jamón y derivados cárnicos, productos lácteos como leche cruda, leche pasteurizada, queso fresco, queso madurado, yogurt casero y vegetales (7). La habilidad de sobrevivir en un amplio rango de condiciones adversas como altos niveles de pH, bajas temperaturas, altos niveles de sal entre otras (8,9), hace que este microorganismo sea de difícil control en la industria de alimentos.
A nivel mundial las BAL y las bacteriocinas purificadas con marca registrada son comercializados por empresas productoras ubicadas en países industrializados como Dinamarca, Italia, Estados Unidos y algunos países latinoamericanos como Argentina, los cuales utilizan la bioconservación como un mecanismos de control de bacterias en la elaboración de sus productos (10). En países en desarrollo como Colombia, la falta de experiencia e insuficiente control en la aplicación de cultivos biocontroladores en microempresas hace que se presenten grandes obstáculos, por esta razón no se ha implementado esta tecnología en las industrias productoras de alimentos. Sin embargo para nuestro país es muy importante desarrollar programas adaptados a las condiciones culturales y tecnológicas para contrarrestar la presencia de patógenos como L. monocytogenes.
Estudios previos indican que en Colombia circulan BAL que cumplen funciones antagónicas frente a microorganismos patógenos y frente a otras BAL no productoras de bacteriocinas (11-14). Esto indica, que aunque en Colombia no se esté utilizando las BAL con fines bioprotectores, se tiene una gran diversidad de microorganismos nativos de los cuales se pueden obtener grandes beneficios. El objetivo del presente trabajo fue seleccionar cepas de BAL nativas con capacidad antilisterial por medio de la caracterización de los metabolitos inhibitorios del crecimiento de cepas de L. monocytogenes.
MATERIALES Y MÉTODOS
Cepas control. Se utilizaron las cepas control LAC 01 Lactobacillus plantarum (cepa donada por el Dr. Siegfried Scherer del Zentralinstitut für Ernährungs- und Lebensmittelforschung (ZIEL) de la universidad Technische Universität München de Alemania). LAC 03 Pediococcus acidilactici y LAC 04 Leuconostoc mesenteroides (cepas donadas por el Dr. Jean Marc Berjeaud de la Université de Poitiers, Francia) productoras de las bacteriocinas Pediocina A, Pediocina PA-1 y Mesenteronicina Y 105 respectivamente.
La actividad antagónica de las BAL se evaluó frente a 17 cepas de L. monocytogenes de serotipos 3b, 4b y 4e, aisladas de diferentes fuentes (Tabla 1) pertenecientes al Laboratorio de Ecología Microbiana y de Alimentos (LEMA), las cuales fueron cultivadas en agar sangre a 37°C y mantenidas en refrigeración a 4°C.

Aislamiento e identificación de BAL. Se tomaron 42 muestras en las que se incluyeron 33 quesos artesanales, 3 muestras de jamón de cerdo empacadas al vacio, 5 muestras de jamón de cerdo con deterioro del empaque y una muestra de una tajadora de cárnicos. Las muestras fueron procesadas y sembradas en agar De Man Rogosa Sharpe (MRS) (Scharlau Chemie, Barcelona España) e incubadas a 30°C/72 h. Las cepas que presentaron reacciones bioquímicas y crecimiento característico de BAL se mantuvieron en agar MRS a temperatura ambiente y en caldo MRS con 10% de glicerol a -20°C y -70°C (2).
Actividad antagónica de las BAL frente a Listeria monocytogenes. El efecto de la actividad antagónica de las BAL aisladas de alimentos se evaluó con la técnica de la gota y doble capa (15). Se inocularon las cajas de Petri con BAL previamente incubadas en caldo MRS a 30°C/24 h. Posteriormente, se adicionó una segunda capa de agar MRS fundido e inoculado con la cepa de L. monocytogenes incubada en caldo BHI a 37°C/24 h. Las cajas de agar MRS inoculadas con los dos microorganismos se incubaron a 37°C/24 h. Se observó la formación de zonas de inhibición alrededor de las BAL, lo cual se consideró como prueba positiva de la actividad antagónica y a su vez se obtuvo el diámetro corregido de los halos formados, para lo cual se realizó la sustracción del diámetro de la colonia y el diámetro del halo de inhibición. Este procedimiento se realizó por triplicado.
Caracterización de compuestos inhibitorios. Los cultivos de BAL que mejor actividad antagónica presentaron fueron centrifugados (4800 x g/4°C/15 min) y filtrados en membranas de celulosa de 0.45 µm (Millipore). Los extractos crudos, libres de células, fueron ajustados a pH 6.5 con HCL 10%, de donde se tomaron 4 alícuotas a las que se les realizó diferentes tratamientos. Una de las alicuotas fue tratada con catalasa (Sigma) (300 UI/ ml) y otra con proteinasa K (1 mg/ml), estas dos alícuotas se incubaron a 37°C/1 h, las dos alícuotas restantes fueron tratadas con temperaturas de 95°C/30 min y 121°C/15 min. Se utilizó la técnica de la gota y doble capa para evaluar la actividad antagónica de cada una de las alícuotas tratadas frente a las 15 cepas de L. monocytogenes serotipo 4b, la cepas LMO 49 serotipo 4e y LMO 52 serotipo 3b (15).
Electroforesis de proteínas SDS - PAGE. El peso molecular de la bacteriocina en el extracto crudo de las cepas BAL, fue estimado por medio de una electroforesis de proteínas en poliacrilamida dodecil sulfato de sodio (Sodium Dodecyl Sulfate- Polyacrylamide Gel Electrophoresis, SDS - PAGE) (16) y la técnica de la doble capa descrita previamente. Para la separación de proteínas se utilizó un sistema de gel que estaba constituido por un gel de concentración del 4% y un gel de separación en gradiente del 16 - 20%. El marcador de peso molecular polipéptido SDS - PAGE (Ref. 161- 0326. Bio-Rad) fue cargado con Loading buffer 5X (1M Tris HClpH 6.8. 2-mercaptoetanol, glicerol 100%, azul de bromofenol 0.01%, y SDS al 20%) y corrido en el gel a 100 v/15 min y luego a 150 v/ 1h. El gel se fijó durante 30 min con solución de fijado de péptidos, se tiño con azul de Coomassie G-250 (Sigma) por 1 h y por último se destiñó con solución decolorante.
La muestra de extracto crudo de BAL fue cargada con buffer 5X sin 2-mercaptoetanol.
Luego de correr la electroforesis bajo las condiciones previamente descritas, se lavó el gel con agua destilada estéril y se colocó sobre una capa de agar MRS sólido inoculado con L. monocytogenes. Sobre el gel se adicionó una segunda capa de agar MRS fundido e inoculado con L. monocytogenes, éste fue incubado a 37°C/24 h y se observó la zona de inhibición directamente en el gel (17).
Análisis estadístico. Se realizó un análisis de varianza (ANOVA) y la prueba de Tukey como prueba de comparación múltiple, utilizando el sofware Statistix 8 (2005, USA), para evaluar la actividad antilisterial de las cepas de BAL, extractos crudos y extractos tratados frente a las diferentes cepas de L. monocytogenes.
RESULTADOS
Aislamiento e identificación de bacterias ácido lácticas. De un total de 250 aislamientos realizados se lograron identificar 75 cepas BAL pertenecientes a los géneros de Lactobacillus spp., Pediococcus spp., Streptococcus spp., Leuconostoc spp., Enterococcus spp., Tetragenococcus spp. y Lactococcus spp.
Selección de cepas con actividad antagónica frente a L. monocytogenes. Se determinó la capacidad antagónica de las 75 cepas de BAL aisladas y las tres cepas control de BAL, frente a las cepas de L. monocytogenes con códigos LMO 49 serotipo 4e, LMO 53 serotipo 3b, LMO 6, LMO 7, LMO 77 y LMO 79 serotipo 4b, utilizando la técnica de la doble capa. Esta técnica permitió ver los halos de inhibición (Figura 1) de donde se obtuvo el promedio de las tres replicas de la medida de los diámetros para cada una de las cepas BAL aisladas (datos no mostrados), los cuales se interpretaron de forma cualitativa como se observa en la tabla 2. Esta tabla indica el comportamiento de las 14 cepas BAL seleccionadas que presentaron una mejor actividad antagónica frente a las cepas de L. monocytogenes. Las cepas de L. monocytogenes que presentaron una mayor sensibilidad al efecto antagónico de las BAL fueron LMO 07 serotipo 4b, LMO 49 serotipo 4e y LMO 53 serotipo 3b.


Extracción y caracterización de las sustancias inhibitorias producidas por BAL. Para la caracterización de sustancias inhibitorias producidas por las BAL nativas se seleccionaron las 14 cepas de la tabla 2. Estas cepas se escogieron debido a que durante las tres replicas realizadas siempre presentaron halos de inhibición frente a más de 5 cepas de L. monocytogenes. Como cepa control se escogió la cepa LAC 03 P. acidilactici productora de la bacteriocina Pediocina A. Para evaluar la actividad antagónica se seleccionaron las cepas de L. monocytogenes con código LMO 07 serotipo 4b, LMO 49 serotipo 4e y LMO 53 serotipo 3b.
Únicamente los extractos crudos libres de células de las cepas LAC 11, LAC 92 y LAC 86 identificadas como Lactobacillus spp., Enterococcus spp. y Leuconostoc spp. (Tabla 3), presentaron halos inhibición como mínimo frente a dos cepas de L. monocytogenes el resto de extractos crudos obtenidos después de la centrifugación y filtración de las 11 cepas de BAL restantes no presentaron halos de inhibición. La figura 2 indica los halos de inhibición de los extractos crudos con y sin tratamientos de la cepa control LAC 03.
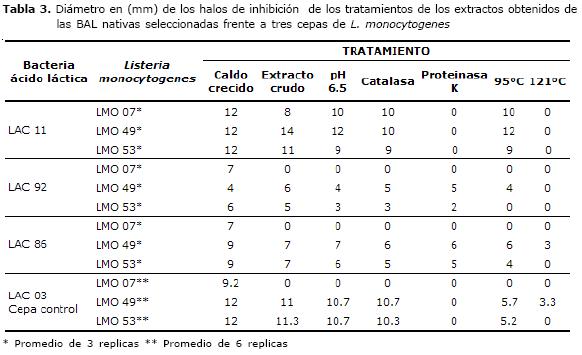

La tabla 3 indica la medida de los diámetros de los halos de inhibición de los diferentes tratamientos realizados a los extractos obtenidos de las BAL nativas seleccionadas frente a tres cepas de L. monocytogenes. La presencia de los halos de inhibición en los extractos libres de células y los sometidos bajo los diferentes tratamientos térmicos y enzimáticos, con excepción de la proteinasa K, hace pensar que la cepa nativa LAC 11 identificada como Lactobacillus spp., tiene una alta probabilidad de sintetizar metabolitos proteínicos con potencial bactericida, debido a su efecto antagónico frente a las tres cepas de L. monocytogenes. Los extractos crudos de las cepas LAC 92 y LAC 86, mostraron una actividad antilisterial únicamente frente a las cepas LMO 49 y LMO 53. Sin embargo, la presencia de halo en el extracto tratado con proteinasa K, indica que los metabolitos sintetizados por estas bacterias no son sensibles al efecto proteolítico de esta enzima.
Debido a que las cepas de serotipo 4b presentaron una mayor resistencia ante la presencia de los extractos generados por las BAL nativas se evaluó el efecto antagónico de las cepas control LAC 01 Lb. plantarum, LAC 03 P. acidilactici y las cepas nativas LAC 11, LAC 92 y LAC 86, frente a 15 cepas de L. monocytogenes serotipo 4b. Como resultados se observó que los extractos crudos, es decir libres de células, presentaban comportamientos diferentes ante las cepas de L. monocytogenes serotipo 4b aisladas de distintos orígenes.
Electroforesis de proteínas SDS-PAGE. Las bandas del marcador de peso molecular utilizado en el presente estudio para estimar el peso molecular de los péptidos sintetizados por las cepas nativas, se observan en la figura 3a. En la figura 3b, el halo de inhibición presente al final del gel del extracto de la cepa LAC 11 Lactobacillus spp., se encontro por encima del frente de corrido. Esto demostró que el péptido que genera la actividad antilisterial tiene un peso molecular por debajo del marcador de peso molecular de 6510 Da, el cual es un valor esperado teniendo en cuenta las características del tamaño de las bacteriocinas. De la misma manera se logró estimar el peso molecular de los péptidos sintetizados por las cepas LAC 86 Leuconostoc spp., y LAC 92 Enterococcus spp., los cuales se encuentran por debajo de 6477 Da y 3970 Da respectivamente para cada cepa.

Análisis estadístico. El análisis de varianza realizado para evaluar la actividad antagónica de las BAL y las diferentes alícuotas de los extractos frente a las cepas de L. monocytogenes, con un 95% de confianza indicó que hay diferencias significativas entre el comportamiento de las BAL con capacidad inhibitoria y los tratamientos realizados a los extractos libres de células frente a las diferentes cepas de L. monocytogenes. El análisis de comparación múltiple demostró que la cepa nativa LAC 11 identificada como Lactobacillus spp., la cual fue aislada de un jamón en deterioro, presentó un mejor potencial antilisterial, además, demostró que la bacteria productora de los metabolitos inhibitorios de BAL fue la de mejor actividad antagónica frente a las cepas de L. monocytogenes.
DISCUSIÓN
Los productos derivados de materias primas como carne y leche son medios de cultivo ideales para el desarrollo de diversos microorganismos como las BAL debido a que tienen altas cantidades de nutrientes como agua, proteínas y compuestos orgánicos e inorgánicos solubles, lo cual permite el desarrollo de estas bacterias en esta clase de matrices naturales (18, 19). Lo anterior se ve reflejado en el presente estudio al identificar las 75 cepas de BAL en los aislamientos de fuentes naturales realizados en el agar MRS.
Durante la selección de cepas de BAL con actividad antagónica frente a las diferentes cepas de L. monocytogenes, se observó que la ausencia del halo de inhibición y la variación del tamaño de los diámetros indicados en algunos casos en los resultados de la tabla 2, demuestran que las cepas de BAL nativas no siempre logran inhibir el crecimiento de las cepas de L. monocytogenes. Estos resultados concuerdan con investigaciones previas (17,20) en las que se ha presentado un comportamiento variable de resistencia o sensibilidad de diferentes cepas de L. monocytogenes frente al uso de BAL o de las bacteriocinas. Hasta el momento, no se ha encontrado ninguna correlación entre la actividad antagónica de las BAL y el origen o el serogrupo de una variedad de cepas de L. monocytogenes (20). Sin embargo, se han establecido diferentes proposiciones que permiten explicar el comportamiento de resistencia por parte de las cepas de L. monocytogenes. Una de estas indica que puede haber una expresión de clones individuales o una mezcla de los mismos presentes en el microorganismo que eviten el efecto antagónico, como la síntesis de enzimas que degradan la bacteriocina (21), como respuesta a los diferentes factores ambientales por los cuales un alimento es sometido (20).
Por otra parte, es necesario considerar que las condiciones del medio de cultivo en el cual se desarrollan las cepas BAL, como pH y temperatura, no siempre son las óptimas para la producción y acción de las bacteriocinas. Por lo tanto, la baja concentración de las mismas hace que no se presente un efecto antagónico sobre una bacteria (3,22).
Los niveles de pH de los extractos purificados oscilaron entre 3.8 y 5.9, lo que indica que durante el tiempo de incubación en el cual se mantuvieron los caldos de cultivo MRS, las BAL lograron liberar los ácidos orgánicos al medio permitiendo el descenso del mismo. El ácido láctico es uno de los principales metabolitos sintetizados por las BAL que inhiben el crecimiento de otros microorganismos (23,24). Sin embargo, teniendo en cuenta los resultados obtenidos en los extractos crudos de las BAL LAC 03, LAC 11, LAC 92 y LAC 86 (Tabla 3) se observó que estos niveles no afectaron el crecimiento de ninguna de las cepas de L. monocytogenes utilizadas en esta investigación, lo que indica que son resistentes a bajos niveles de pH, por lo tanto no se ven afectadas por la formación del gradiente de protones al interior de la célula (10,25). Por otro lado, la presencia del halo de inhibición en la alícuota tratada con catalasa, indica que el peróxido sintetizado por las BAL, no era el que causaba la actividad antagónica frente a L. monocytogenes. Sin embargo, estudios previos han demostrado que determinadas concentraciones de peróxido sintetizado por las BAL han logrado inhibir especies pertenecientes a los géneros Proteus, Pseudomonas y Bacillus (24).
El peso molecular estimado por la electroforesis SDS-PAGE y el bioensayo, permiten sugerir que los metabolitos sintetizados por las cepas LAC 11, LAC 92 y LAC 86 podrían ser bacteriocinas de clase IIa debido a que presentan las características relevantes de este grupo como por ejemplo, ser péptidos de bajo peso molecular, activos frente a cepas de Listeria spp. y termoestables (26). Sin embargo, teniendo en cuenta que estos resultados son preliminares, se sugiere enfatizar en la caracterización bioquímica de los metabolitos sintetizados por las cepas nativas con el fin de poder realizar una comparación con las bacteriocinas hasta el momento reportadas en la literatura.
En conclusión, las cepas nativas LAC 11 Lactobacillus spp., LAC 86 Leuconostoc spp. y LAC 92 Enterococcus spp. aisladas de alimentos distribuidos en Colombia tienen potencial antilisterial, debido a que producen proteínas o metabolitos de peso molecular alrededor de 6510 y 3970 Da, que generan una actividad antagónica frente a diferentes cepas y serotipos de L. monocytogenes.
Agradecimientos
A los laboratorios LEMA (Laboratorio de Ecología Microbiana de Alimentos) y BBMP (Bioquímica y Biología Molecular de Parásitos) de la Universidad de los Andes por su apoyo en la realización de este proyecto.
REFERENCIAS
1. Cleveland J, Montville TJ, Nes IF, Chikindas ML. Bacteriocins: safe, natural antimicrobials for food preservation. Int J Food Microbiol 2001; 71: 1-20. [ Links ]
2. Ammor MS, Mayo B. Selection criteria for lactic acid bacteria to be used as functional starter cultures in dry sausage production: An update. Meat Sci 2007; 76: 138-146. [ Links ]
3. Messens W, De Vuyst L. Inhibitory substances produced by Lactobacilli isolated from sourdoughs-a review. Int J Food Microbiol 2002; 72:31- 43. [ Links ]
4. Schneider R, Fernández FJ, Aguilar MB, Guerrero-Legarreta I, Alpuche-Solís A, Ponce-Alquicira E. Partial characterization of a class IIa pediocin produced by Pediococcus parvulus 133 strain isolated from meat (Mexican "chorizo"). Food Control 2006; 17:909-915. [ Links ]
5. Russel NJ, Gould GW. Food Preservation. Starter and protective cultures. Segunda edición. New York, Estados Unidos: Kluwer academic/ Plenum Publishers; 2003. [ Links ]
6. Swaminathan B, Gerner P. The epidemiology of human listeriosis. Microbes Infect 2007; 9:1236- 1243. [ Links ]
7. Torres KJ, Sierra SC, Poutou RA, Vera H, Carrascal AK, Mercado M. Incidencia y diagnóstico de Listeria monocytogenes microorganismo zoonótico emergente en la industria de alimentos. UDCA 2004; 7(1):27-57. [ Links ]
8. Alves VF, Martínez RCR, Lavrador MAS, De Martinis ECP. Antilisterial activity of lactic acid bacteria inoculated on cooked ham. Meat Sci 2006; 74: 623-627. [ Links ]
9. Naghmouchi K, Kheadr E, Lacroix C, Fliss I, Class I/Class IIa bacteriocin cross-resistance phenomenon in Listeria monocytogenes. J Food Microbiol 2007; 24: 718-727. [ Links ]
10. Naidu AS. Natural food antimicrobial systems. 2000, Estados Unidos: CRC Press; 431-689. [ Links ]
11. Romero PA. Efecto antagónico de bacterias ácido lácticas tolimenses sobre Salmonella enteritidis aviar. [Trabajo de grado]. Bogotá, Colombia: Pontificia Universidad Javeriana; 1999. [ Links ]
12. León CF. Efecto antagónico de bacterias ácido lácticas aisladas a partir de productos lácteos artesanales obtenidos del departamento del Tolima sobre Salmonella enteritidis aviar.[Trabajo de grado no publicada]. Bogotá, Colombia: Pontificia Universidad Javeriana; 1998. [ Links ]
13. Hernández CG, Pantoja LK, Turriago SC. Evaluación de la presencia de bacteriocinas en cultivos de bacterias ácido lácticas. [Trabajo de grado]. Chía-Cundinamarca, Colombia: Universidad de la Sabana; 2002. [ Links ]
14. Vásquez PM, Efecto antagónico de Lactobacillus casei y Lactobacillus acidophilus frente a Escherichia coli y Shigella spp. aislados de materia fecal obtenida de un grupo de niños entre 1 y 7 años. [Trabajo de grado]. Bogotá, Colombia: Pontificia Universidad Javeriana; 1995. [ Links ]
15. Teixeira de Carvalhoa AA, Aparecida de Paula R, Mantovania HC, Alencar de MC. Inhibition of Listeria monocytogenes by a lactic acid bacterium isolated from Italian salami. J Food Microbiol 2006; 26:213-219. [ Links ]
16. Laemmli U. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature 1970; 227 (5259):680-685. [ Links ]
17. Millete M, Dupont C, Archambault D, Lacroix M. Partial characterization of bacteriocins produced by human Lactococcus lactis and Pediococcus acidilactici isolates. J Appl Microbiol 2007; 102: 274-282. [ Links ]
18. ICMSF. Microorganismos de los alimentos 6. Ecología microbiana de los productos alimentarios. España: Acribia S.A; 1998. [ Links ]
19. León V, Totosaus A, Guerrero I, Pérez M. Efecto de bacterias ácido lácticas termorresistentes en salchichas cocidas. Cienc Tecnol Aliment 2006; 5(2):135-141. [ Links ]
20. Buncic S, Avery S, Rocourt J, Dimitrijevic M. Can food-related environmental factors induce different behaviour in two key serovars, 4b and 1/2a, of Listeria monocytogenes? Int J Food Microbiol 2001; 65:201-212. [ Links ]
21. Abee T, Krockel L, Hill C. Bacteriocins: modes of action and potentials in food preservation and control of food poisoning. Int J Food Microbiol 1995; 28: 169-185. [ Links ]
22. González L, Sandoval H, Sacristán N, Castro, JM, Fresno JM, Tornadijo ME. Identication of lactic acid bacteria isolated from Genestoso cheese throughout ripening and study of their antimicrobial activity. Food Control 2007; 18(6):716-722. [ Links ]
23. Stiles EM, Holzapfel WH. Lactic acid bacteria of foods and their current taxonomy. Int J Food Microbiol 1997; 36:1-29. [ Links ]
24. Gilliland SE. Bacterial Starter cultures for foods. Estados Unidos: CRC PRESS; 1985. [ Links ]
25. Tome E, Teixeira P, Gibbs PA. Antilisterial inhibitory lactic acid bacteria isolated from commercial cold smoked salmon. Food Microbiol 2006; 23:399-405. [ Links ]
26. Salminen S, Wright A, Ouwehand A. Lactic Acid Bacteria Microbiologycal and functional Aspects Edición 3. New York: Marcel Dekker; 2004. [ Links ]














