INTRODUCCIÓN
Los insectos son considerados como plagas en la agricultura moderna, sin embargo desde hace siglos forma parte de la gastronomía de los seres humanos 1. Varios estudios reportan su composición nutrimental y en la actualidad toma gran interés la presencia de sustancias funcionales como algunos lípidos bioactivos 2. Independientemente del reconocimiento que tienen los insectos en los aspectos ambiental y sanitario, también se valora el papel alimentario en animales y humanos 3, sin que ello quiera decir que se generalice y acepte a través del mundo, sobre todo en países europeos y Norteamérica 1,3. La incorporación de harina de insectos en concentrados para animales no altera el índice de conversión alimenticia, inclusive en algunos estudios se incrementa, esto se debe al contenido de aminoácidos indispensables como lisina, metiotina y leucina 3,4.
Existen más de 1600 especies de insectos utilizados en la alimentación humana, son apreciados por el valor nutritivo al ser fuente de vitaminas, minerales y proteína, sin embargo, el cultivo es aun escasamente promovido 5.
El estudio nutricional de insectos es de interés en países de los continentes americano, africano y europeo; algunos de ellos son Brasil, Colombia, Ecuador, México, Angola, España y Portugal 3,5,6,7,8,9,10.
En investigaciones recientes, un aspecto prioritario es conocer los contenidos de ácidos grasos (AG), particularmente de aquellos con propiedades funcionales. Por ejemplo, el oleico (C18:1, c9), principal AG del grupo de los monoinsaturados, los cuales se vinculan con actividad anticancerígena, disminución de colesterol plasmático, mejoras en el sistema inmune y reducción de riesgo de enfermedad cardiovascular e inflamatoria 5.
En Colombia, se tienen diversos insectos comestibles, uno de ellos del género Cotinis Burmeister (1842) con 28 especies, cuya distribución va del norte de Sudamérica a la parte central de Estados Unidos 11. México cuenta con 18 especies, de las cuales 14 son endémicas en diversos hábitats, Estados Unidos posee cinco especies y Colombia registra tres, una de ellas es el escarabajo C. columbica Burmeister, que pertenece a la subfamilia cetoniinae; no obstante, sobre este existen pocas investigaciones 11. El escarabajo C. columbica Burmeister se distribuye por toda la cordillera colombiana (oriental, central y occidental) en ecosistemas de bosque seco y bosque húmedo. Las larvas se encuentran en troncos podridos, entre las raíces de epífitas, hoyos de los árboles, estiércol, detritus, hormigueros o materia en descomposición de madrigueras de roedores abandonadas 9. Los pobladores autóctonos de los municipios de la cordillera colectan las larvas para consumirlas como parte de su alimentación 12.
Dada la importancia del tema, la escasez de información de composición nutrimental y en particular, sobre el contenido de ácidos grasos en la larva del escarabajo C. columbica Burmeister, el objetivo del presente estudio fue determinar la composición química proximal y perfil de ácidos grasos en la larva C. columbica Burmeister provenientes de los municipios Mogotes (Santander) y Garzón (Huila), Colombia.
MATERIALES Y MÉTODOS
Origen de las muestras. Se obtuvieron muestras de larvas C. columbica Burmeister de los municipios Mogotes (Santander) y Garzón (Huila), Colombia.
Mogotes se localiza en el Departamento de Santander, tiene una superficie de 484 km2, altitud 1700 msnm, latitud 6° 28'59" norte, longitud 72°58'1" oeste. Limita al noroeste con el municipio de Curití, al este y sur con san Joaquín. Húmedo y lluvia durante todo el año con temperatura de 15 a 22°C, octubre y noviembre son los meses más húmedos del año. Distancia de Mogotes a Bogotá 242 km 13.
Garzón se localiza en el Departamento de Huila, entre las montañas Central y Oriental, limita por el norte con el municipio de Gigante, por el sur con el municipio de Guadalupe, al sur-oeste con Altamira; por el oriente con el Departamento del Caquetá y por el occidente con el municipio Agrado. Posee una extensión de 580 km2 que equivalen al 29% de la superficie total del Departamento del Huila. La altitud de la cabecera municipal es de 828 msnm y se ubica a 2°11'57" de latitud norte y 75°38'59" de longitud oeste. La temperatura media es de 24°C con humedad de 57%. Distancia de Garzón a Bogotá 424 km 14.
Obtención de muestras. Las muestras de larva se obtuvieron durante mayo, junio y julio del 2021, en intervalos de 30 días. Se colectaron 500 g de larva C. columbica Burmeister que se cultivan en Mogotes y Garzón, haciendo un total de 2 muestras por mes durante tres meses (6 muestras en total de 500 g cada una). Las muestras se pesaron en balanza digital (Pocket Scale, China).
La obtención de larvas de Mogotes y Garzón se realizó de manera manual, una a una fueron colectadas de las palmas morete (Mauritia flexuosa L.) y chonta (Acrocomia aculeata). Las larvas del municipio de Garzón se depositaron en terrarios (lugar de cultivo), de acuerdo a información técnica para el cultivo de larvas y métodos utilizados por campesinos del municipio 15, se mantuvieron en harina de trigo y alimentaron con humus orgánico (cáscaras de plátano, café y frutas) durante 72 horas, esto debido a la distancia (430 km) que se tuvo que recorrer para su colecta. Las larvas colectadas se encontraban en su tercer estadío antes de convertirse en pupas, se lavaron con agua potable y se blanquearon en agua a 85°C durante 3 minutos, se secaron a temperatura ambiente al sol (25°C). Todas las muestras se molieron (molino Universal Landers, L14200, Colombia) y la harina resultante se empacó en bolsas de plástico, debidamente etiquetadas, posteriormente fueron trasladadas en hielera (~4°C) al laboratorio de análisis.
Análisis químico proximal (AQP) y perfil de ácidos grasos. Se tomaron 150 g de las muestras molidas de larvas para AQP y perfil de ácidos grasos. En la Tabla 1 se registran los métodos analíticos utilizados en la determinación de cada variable composicional y perfil de ácidos grasos, en todos los casos se hicieron tres repeticiones y se siguieron los protocolos de los métodos de referencia de la Asociación de Químicos Analistas Oficiales; empleados en diferentes investigaciones 16,17,18,19,20,21.
Tabla 1. Métodos empleados en el análisis químico proximal y perfil de ácidos grasos de larvas C. columbica Burmeister.
| Variable | Método (Referencia) |
|---|---|
| Hidratos de carbono | Matemático por diferencia |
| Cenizas | Calcinación |
| Fibra cruda | Digestión ácida/alcalina y calcinación |
| Grasa | Hidrólisis ácida |
| Humedad | Secado en estufa |
| Proteína | Kjeldahl |
| Sólidos totales | Matemático por diferencia |
| Perfil de ácidos grasos | Determinación de ésteres metílicos de ácidos grasos por cromatografía de gases con detector de ionización de flama y columna capilar |
Análisis de ácidos grasos por cromatografía de gases con detector de ionización de flama. La determinación de AG se realizó mediante sus ésteres metílicos, previamente metilados con hidróxido de potasio en metanol 2N e inyectados, por duplicado, al cromatógrafo de gases con detector de ionización de flama 21.
Condiciones cromatográficas. Se empleó un cromatógrafo de gases Thermo Scientific TRACE Serie 1300 (Italia) con columna capilar de sílica fundida de 105 m de longitud, 0.25 mm de diámetro interno y 0.2 um de espesor de película (RTX-2330, No. Cat. 10729, USA). Temperaturas: 95 a 240, 245 y 230°C del horno, detector e inyector respectivamente. Rampa de temperaturas: T1=95°C durante 5 min, con incremento de 2.65°C x min hasta llegar a T2=240°C y se mantuvo por 30 min. El tiempo total de corrida fue de 81.17 min. Se utilizó nitrógeno como gas de arrastre a flujo de 2 mL/min; la inyección fue tipo split. La identificación y cuantificación de las señales cromatográficas (picos) se llevó a cabo por el método del estándar externo y mediante el software Chromeleon™ Chromatography Data System (CDS) Software Thermo Scientific Versión 7.2 (Italia). El estándar que se utilizó fue mezcla de 37 ácidos grasos (Food Industry FAME Mix, 37 components, RESTEK No. Cat 35108 USA). El volumen de inyección de la muestra y el estándar fue de 2 μL.
Análisis estadístico. Se empleó el programa estadístico IBM® SPSS® versión 24.0 para Windows (Armonk NY, USA). Las variables medidas fueron las obtenidas del análisis químico proximal y perfil de ácidos grasos.
El estudio fue descriptivo durante tres meses, con observación mensual. Con los datos obtenidos se construyó una base de datos que fue sometida a análisis exploratorio para observar el comportamiento de distribución, y en su caso, valores atípicos. Se obtuvieron las medidas descriptivas y se aplicó la prueba t de Student para comparación de medias de variables de AQP y ácidos grasos de larvas C. columbica Burmeister provenientes de dos municipios. Se consideró una significancia p<0.05, 95%.
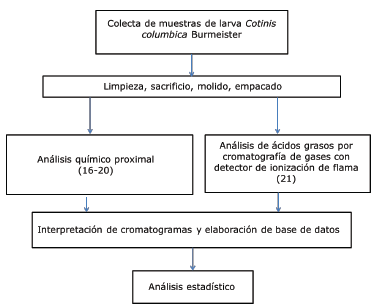
Esquema general del trabajo. En la figura 1 se presenta el esquema general del trabajo.
RESULTADOS
Análisis químico proximal. Los análisis bromatológicos de las larvas C. columbica Burmeister provenientes de Mogotes y Garzón arrojaron valores para hidratos de carbono, cenizas, fibra cruda, grasa, humedad, proteína y solidos totales (Tabla 2). Se evidencian los porcentajes considerables de proteína y grasa, siendo mayores en larvas de Garzón (25.9 vs 23.3% y 31.1 vs 21.2% respectivamente). Los análisis estadísticos no arrojaron diferencia significativa (p>0.05) en las medias de todas las variables analizadas. La dispersión de los datos fue mayor en Mogotes, particularmente en grasa, humedad y solidos totales.
Tabla 2 Composición químico proximal (base seca) de larva C. columbica Burmeister de los municipios de Mogotes y Garzón, Colombia.
| Variable (%) | Mogotes X±DE | Garzón X±DE | Promedio |
|---|---|---|---|
| Carbohidratos | 5.6a±6.9 | 6.2a±1.9 | 5.9 |
| Cenizas | 3.0a±1.0 | 3.6a±0.5 | 3.3 |
| Fibra cruda | 7.0a±2.6 | 9.6a±2.3 | 8.3 |
| Grasa | 21.2a±10.8 | 31.1a±1.9 | 26.1 |
| Humedad | 39.8a±20.6 | 23.4a±5.6 | 31.6 |
| Proteína | 23.3a±2.1 | 25.9a±1.4 | 24.6 |
| Sólidos totales | 60.2a±20.6 | 76.6a±5.6 | 68.4 |
x̅: media aritmética, DE: desviación estándar. Letras diferentes en medias de la misma fila indican diferencia estadística al 95%.
El análisis de correlación bivariada de Pearson encontró correlaciones positivas en grasa con carbohidratos y cenizas (a mayor contenido de grasa, mayores contenidos de carbohidratos y cenizas), proteína con cenizas (a mayor contenido de proteína, mayor contenido de cenizas) y, correlaciones negativas en humedad con carbohidratos, cenizas y grasa (a mayor contenido de humedad, menores contenidos de carbohidratos, cenizas y grasa) (Tabla 3). No se observó correlación en fibra cruda.
Tabla 3 Correlaciones de variables químico proximal de larva C. columbica Burmeister de los Municipios de Mogotes y Garzón, Colombia.
| CHOS | CE | FC | Grasa | HU | Proteína | ST | |
|---|---|---|---|---|---|---|---|
| CHOS | 1 | ||||||
| Cenizas | 0.76 | 1 | |||||
| FC | 0.21 | 0.23 | 1 | ||||
| Grasa | 0.82* | 0.92* | 0.46 | 1 | |||
| Humedad | -0.86* | -0.92** | -0.50 | -0.99** | 1 | ||
| Proteína | 0.42 | 0.91* | 0.13 | 0.73 | -0.71 | 1 | |
| ST | 0.86* | 0.92* | 0.50 | 0.99** | -1.0** | 0.71 | 1 |
CHOS: carbohidratos, CE: Cenizas; FC: fibra cruda, HU: Humedad; ST: sólidos totales.
*: correlación significativa con p<0.05, 95% (bilateral); **: correlación significativa con p<0.01, 99% (bilateral).
La distribución de grasa a través del tiempo presentó una tendencia mayor en larvas de Garzón, excepto en el mes de junio, donde se presentó un valor mayor para Mogotes (Figura 2). No hubo diferencia significativa (p≥0.05).
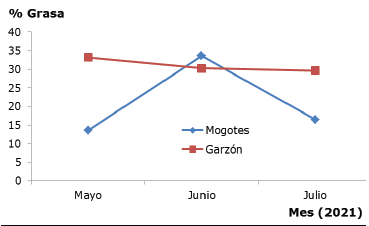
Figura 2 Contenido de grasa (%) en larvas C. columbica Burmeister de los municipios de Mogotes y Garzón, Colombia, 2021.
Ácidos grasos. El análisis cromatográfico detectó y cuantificó 18 ácidos grasos (% p/p), saturados e insaturados, en la materia grasa de las larvas (Tabla 4) de ambos municipios. Se identificaron como AG mayoritarios a C16:0, C18:1 c9 y C18: c9,12, con valores en Mogotes de 24.11, 31.59 y 30.0 (% p/p) respectivamente y en Garzón 20.26, 32.35 y 29.86 (% p/p). El resto de AG obtuvo valores menores a 4.14 (% p/p). La prueba t de Student para muestras independientes arrojó significancia (p<0.05) en C10:0, con valor mayor en Garzón (2.56 vs 035 % p/p), los demás AG no presentaron significancia estadística (p≥0.05). Los contenidos de grupos de ÁG saturados, monoinsaturados y poliinsaturados oscilaron entre 30.20 y 36.92 (% p/p), sin alcanzar la diferencia estadística.
Tabla 4 Composición media de ácidos grasos (% p/p) en larvas C. columbica Burmeister de los municipios de Mogotes y Garzón, Colombia.
| Ácido graso | Mogotes x̅±DE | Garzón x̅ ±DE |
|---|---|---|
| C4:0 | 0.09a±0.13 | 0.15a±0.21 |
| C6:0 | 0.57a±0.59 | 1.18a±1.03 |
| C8:0 | 0.67a±1.11 | 1.15a±2.00 |
| C10:0 | 0.35a±0.32 | 2.56b±1.18 |
| C11:0 | 0.37a±0.13 | 0.76a±0.30 |
| C12:0 | 0.02a±0.03 | 0.03a±0.03 |
| C13:0 | 2.01a±1.41 | 1.49a±0.82 |
| C14:0 | 0.87a±0.71 | 0.95a±0.41 |
| C16:0 | 24.11a±4.37 | 20.26a±4.99 |
| C16:1, c9 | 1.26a±1.62 | 1.77a±2.17 |
| C18:0 | 0.12a±0.10 | 0.22a±0.34 |
| C18:1, c9 | 31.59a±3.72 | 32.35a±5.26 |
| C18.2, c9,12 | 30.00a±1.12 | 29.86a±1.09 |
| C18:3, c9,12,15 | 4.14a±0.78 | 3.62a±1.41 |
| C20:2, c11,14 | 0.33a±0.33 | 0.44a±0.14 |
| C20:3, c11,14,17 | 0.89a±0.69 | 0.57a±0.25 |
| C22:0 | 1.05a±0.61 | 1.44a±0.77 |
| C22:2, c13,16 | 1.57a±1.27 | 1.19a±1.20 |
| Saturados | 30.23a±1.93 | 30.20a±2.01 |
| Monoinsaturados | 32.85a±2.50 | 34.12a±3.61 |
| Poliinsaturados | 36.92a±0.57 | 35.68a±1.70 |
x̅: media aritmética, DE: desviación estándar.
Letras diferentes en medias de la misma fila indica diferencia al 95%.
En los grupos de ácidos grasos la correlación fue negativa en ácidos grasos monoinsaturados (AGS) con ácidos grasos saturados y en ácidos grasos poliinsaturados (AGPI) con AGMI (Tabla 5). No se observó correlación entre AGPI y AGS.
Tabla 5 Correlaciones de grupos de ácidos grasos de larva C. columbica Burmeister de los Municipios de Mogotes y Garzón, Colombia.
| AGS | AGMI | AGPI | |
|---|---|---|---|
| AGS | 1 | ||
| AGMI | -0.95** | 1 | |
| AGPI | 0.71 | -0.90* | 1 |
AGS: ácidos grasos saturados, AGMI: ácidos grasos monoinsaturados, AGPI: ácidos grasos poliinsaturados. *: correlación significativa con p<0.05, 95% (bilateral); **: correlación significativa con p<0.01, 99% (bilateral).
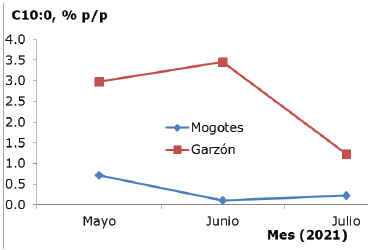
En la figura 3 se muestran los contenidos de C10:0 a través del tiempo. Las larvas de Mogotes registraron valores menores a 1 (% p/p) y las de Garzón estuvieron entre 1.2 y 3.5. En ambos municipios la tendencia fue decreciente, con máximos en mayo; Garzón arrojó niveles mayores durante el estudio (mayo, junio y julio).
DISCUSIÓN
El análisis químico proximal evidenció contenidos similares en los porcentajes de carbohidratos, cenizas, fibra cruda, grasa, humedad, proteína y sólidos totales, de larvas C. columbica Burmeister colectadas en los municipios Mogotes y Garzón (Tabla 1).
En la revisión bibliográfica no se encontraron referencias sobre la composición nutrimental de la larva C. columbica Burmeister, por lo que los valores obtenidos en este trabajo se contrastaron con pupas y larvas de otras especies. Los niveles de proteína fueron menores a los encontrados en pupas de gusano de seda (Bombyx morí L.) provenientes del Departamento del Cauca, Colombia (24.6 vs 50.9 % base seca) 3, diferencias que pueden atribuirse a la humedad en larvas de este estudio, que mostraron un promedio de 31.6%, mientras que para las pupas fue 5%. En otra investigación realizada en larvas y pupas de Bombyx morí L. en Hidalgo, México, se encontraron valores de 13.0 y 60.1% base húmeda, respectivamente 5. Los valores en base seca fueron 62.6 y 64.3%, respectivamente. Estos datos evidencian la concentración mayor de proteína conforme avanza el ciclo de vida del insecto y deja al descubierto que el contenido de humedad es mayor en larva (79.2%) que en pupa (6.5%) 5. Sin embargo, cuando se observan los valores de proteína en base seca (larva vs pupa), los valores son muy cercanos (62.6 vs 64.3%). En otro estudio sobre larvas de Pachymerus nucleorum se informó 33.1% de proteína con humedad 54.2% 6. Los contenidos de proteína informados dan cuenta de la variabilidad que existe en las especies de insectos y ciclo de vida.
La grasa contenida en larvas de este estudio estuvo entre 21 y 31% para Mogotes y Garzón respectivamente, con un promedio de 26%, 13.5 puntos porcentuales inferior al hallazgo en pupas de gusano de seda (39.5%) en Cauca, Colombia 3. Se puede considerar bajo el promedio de grasa en este trabajo respecto el estudio colombiano, pero esta consideración es relativa, ya que el contenido de humedad de las larvas fue 36.1% y 5% en pupas, lo que hace que la concentración de grasa sea mayor a menor humedad. En México, se reportaron valores para larvas de Bombyx morí L. de 3.4 y 16.4% con 79.1 y 0% de humedad respectivamente 5, valores muy por debajo de lo encontrado en esta investigación. En un trabajo brasileño, larvas de Pachymerus nucleorum tuvieron un valor de 37.9% de grasa con 54.2% de humedad 6. Esta información y la correlación negativa entre humedad y grasa (Tabla 2), explican el mayor porcentaje de humedad con menor porcentaje de grasa.
En los valores de grasa a través del tiempo, las muestras de Mogotes presentaron porcentajes menores respecto a Garzón (Figura 2) en mayo y julio, con niveles muy próximos en junio, sin llegar a presentar significancia estadística (p≥0.05). Esto se debe a que la alimentación de las larvas en Garzón (Huila) se hizo durante el proceso de cuarentena con harina de trigo, residuos biodegradables y humus orgánico 15.
Los hallazgos en la composición proximal en esta investigación y en diferentes países sobre larvas de insectos diversos, demuestran que la variabilidad es amplia, no sólo en el contenido graso, si no en la mayoría de las variables analizadas 3,5,6,10 (Tabla 6).
Tabla 6 Composición proximal (% base seca o húmeda) de larvas, pupas e insectos en varios países.
| Especie | CHOS | CE | FC | GR | HU | P |
|---|---|---|---|---|---|---|
| Cotinis columbica Burmeister, L1 | 5.9 | 3.3 | 8.3 | 26.1 | 31.6 | 24.6 |
| Bombyx morí L., P2 | 2.2 | 3.4 | - | 39.5 | 5.2 | 50.9 |
| Bombyx mori L., L3 | 2.7 | 1.0 | 0.6 | 3.4 | 79.2 | 13.0 |
| Tenebrio molitor, L3 | 4.2 | 2.8 | 6.9 | 38.3 | 0 | 45.8 |
| Liometopum apiculatum, L3 | 18.2 | 3.3 | 1.7 | 34.3 | 0 | 49.1 |
| Pachymerus nucleorum, L4 | - | 3.1 | 15.4 | 37.9 | - | 33.1 |
| Triboleum castaneum, L5 | 18.9 | 1.1 | 1.9 | 6.4 | 56.3 | 15.3 |
CHOS: carbohidratos; CE: Cenizas; FC: Fibra cruda; GR: Grasa; HU: Humedad; P: Proteína; 1: este estudio; 2: (3) (Colombia); 3: (5) (México); 4: (6) (Brasil); 5: (10) (Portugal).
La caracterización bromatológica de larvas C. columbica Burmeister no se aleja de datos informados para 14 especies de larvas de coleópteros comestibles en África, en donde los valores de cenizas oscilaron entre 1.5 y 7.8%, fibra cruda 1.5 y 28.1%, grasa 11.8 y 66.6%, humedad 1.0 y 59.4% y proteína 18.8 y 50.6% 22. Estos datos revelan la dispersión que existe en cada variable, la cual depende, primordialmente, de factores como la especie, alimentación y clima 22.
Ácidos grasos. Los métodos de cromatografía de gases con columnas capilares se utilizan en la caracterización de grasas alimenticias, se emplean en la determinación de fracciones lipídicas como esteroles, triacilglicéridos y ácidos grasos 23. En la presente investigación se determinaron los contenidos (% p/p) de ácidos grasos (AG) en larvas C. columbica Burmeister colectadas en los municipios Mogotes y Garzón, Colombia. En la Tabla 4 se observa que los valores de AG (% p/p) en las larvas de los dos municipios estudiados no presentaron diferencia estadística, excepto para el C10:0. Al realizar una inspección visual, se detecta que los valores de C10:0 durante el periodo de estudio fueron menores en Mogotes respecto a Garzón, teniendo valores por abajo de 1 (% p/p), mientras que en Garzón estuvieron en el intervalo de 1.2 a 3.5 (% p/p) (Figura 3). Esto probablemente se deba a que las larvas de Mogotes se alimentaron de manera natural con los residuos de las palmas en descomposición durante el mes de mayo, temporada de lluvia (invierno), y temperatura de 15°C a 20°C; y en Garzón, el cultivo fue en terrario y su proceso de alimentación se basó en residuos biodegradables, humus orgánico y harina de trigo, temporada de lluvia (invierno), y temperaturas entre 20°C y 24°C. En general, el perfil de AG respecto a otras investigaciones realizadas en insectos alrededor del mundo es variable, el número de AG oscila entre 8 y 18, por supuesto el perfil se informa en diferentes especies y fases del ciclo de vida de insectos por lo que es difícil contrastar estos valores, pero sin duda ofrece información que debe valorarse, sobre todo al estudiar el efecto de la zona geográfica y alimentación. Sin embargo, los altos contenidos son característicos para algunos AG, lo cual permite tipificar los grupos de AG mayoritarios en la grasa de los insectos (Tabla 7). En este estudio son notables los niveles de palmítico (C16:0, 22.18 % p/p) y oleico (C18:1, 31.97 % p/p) en larvas de C. columbica Burmeinster, los cuales coinciden con lo encontrado en otros países como Brasil (Specíomerus ruficornís), Ecuador (Rhynchophoruspalmarum L.), España (Hermetia illucens), Perú (Rhynchophorus palmarum L.) y Corea (Protaetia brevitarsis seulensis) con intervalos de 17.67 a 43.91 (% p/p), 32.19 y 62.17 (% p/p), respectivamente (Tabla 7). Las proporciones de AGS, AGMI y AGPI también presentan diferencias notables entre las naciones, pero existe similitud con los valores de España.
Tabla 7 Contenido de ácidos grasos (% p/p) en insectos de varios países.
| Acido graso | Este estudio | Brasil1 | Ecuador2 | España3 | Perú4 | Corea5 |
|---|---|---|---|---|---|---|
| C4:0 | 0.12 | - | - | - | 0.26 | - |
| C6:0 | 0.87 | - | - | - | 0.29 | - |
| C8:0 | 1.82 | - | - | 1.1 | 0.28 | - |
| C10:0 | 1.45 | 0.14 | - | 0.6 | - | - |
| C11:0 | 0.56 | - | - | - | - | - |
| C12:0 | 0.02 | 21.34 | 0.1 | 0.4 | - | - |
| C13:0 | 1.75 | - | - | - | - | - |
| C14:0 | 0.91 | 19.01 | 2.8 | 0.7 | 2.56 | 1.86 |
| C15:0 | - | - | - | 1.6 | - | 0.60 |
| C16:0 | 22.18 | 17.67 | 28.0 | 19.6 | 43.91 | 17.05 |
| C16:1, c9 | 1.51 | 0.45 | 1.2 | 0.7 | 1.72 | 1.17 |
| C16:3 | - | - | - | - | - | 0.31 |
| C17:0 | - | - | - | - | - | 0.10 |
| C18:0 | 0.17 | 4.16 | 5.9 | 6.5 | 5.16 | 1.69 |
| C18:1, c9 | 31.97 | 32.19 | 59.2 | 36.1 | 43.01 | 62.17 |
| C18.2, c9,12 | 29.93 | 4.81 | 1.1 | 26.0 | 0.76 | 4.92 |
| C18:3, c9,12,15 | 3.88 | - | 0.3 | 1.4 | 0.29 | 0.19 |
| C20:0 | - | - | - | 0.8 | 0.58 | 0.50 |
| C20:1 | - | - | - | 0.3 | - | - |
| C20:2, c11,14 | 0.38 | - | - | - | - | - |
| C20:3, c11,14,17 | 0.73 | - | - | - | - | - |
| C20:4 | 0.16 | 0.3 | ||||
| C22:0 | 1.24 | - | 1.1 | - | 0.31 | |
| C22:2, c13,16 | 1.38 | - | - | - | - | |
| C22:5 | - | - | 0.6 | - | - | |
| Saturados | 30.22 | 62.39 | 36.8 | 32.5 | 53.03 | 21.80 |
| Monoinsaturados | 33.48 | 32.64 | 60.4 | 37.1 | 44.73 | 71.7 |
| Poliinsaturados | 36.30 | 4.97 | 1.5 | 28.2 | 1.05 | 5.73 |
1(24), 2(7), 3(9), 4(25), 5(26).
Las correlaciones arrojaron que a mayor contenido de AGPI y AGMI menor es el contenido de AGS (Tabla 5). Lo cual es apreciable ya que hay evidencia científica sobre los efectos benéficos de algunos AG insaturados sobre el organismo humano; en los ácidos grasos insaturados se distinguen dos grupos, los AG omega 3 y 6 y, dependiendo de la posición de los átomos de hidrógeno en los dobles enlaces se identifican como cis (hidrógeno en el mismo lado) o trans (hidrógeno en lados opuestos). Las propiedades funcionales de los AG dependen, en general, del tamaño de la cadena hidrocarbonada, número de dobles enlaces y configuración cis o trans 27,28. Los AGPI son las más benéficos para el cuerpo humano, algunos de ellos no pueden ser sintetizados por el organismo y se requiere sean proporcionados a través de la dieta (como el linoleico, C18:2 y linolénico, C18:3), por lo que se les considera AG esenciales 27,28. Se reporta que los AG esenciales protegen al corazón porqué tienen actividad antiarterioesclerosis, antiinflamatoria y antiarritmica, a través de la modificación de activación de la vía de señalización de TLR4, al suprimir la dimerización en membranas celulares, lo que conduce a la inhibición de la expresión de TLR4 y una mayor mitigación de metainflamación, enfermedad cardiovascular y riesgos de diabetes mellitus tipo 2 en humanos obesos 27,28. Asimismo, el grupo de AG monoinsaturados, compuesto en su mayoría por C18:1, se asocia a actividad anticancerígena, reducción del colesterol plasmático, fortalecimiento del sistema inmune y disminución del riesgo de enfermedad cardiovascular e inflamatoria 29. En monocitos humanos cultivados (THP-1), se descubrió que el ácido oleico (C18:1), es responsable de la inducción de hipometilación y mejoras en los patrones de inflamación 27. Además, de acuerdo a estudios científicos 23,29 se reconocen beneficios del consumo de AG de cadena corta y media, como al C4:0 que tiene efecto antitumoral en próstata, mama y colón; a C6:0, C8:0 y C10:0 se les asocia en inhibición de crecimiento microbiano y viral y disolución de depósitos del colesterol en pruebas in vitro y en animales de ensayo. Por esto, los valores encontrados en las larvas C. columbica Burmeister son base para considerarse como fuente natural e importante de AG de cadena corta, media, C81:1 (31.97 % p/p) y C18:2 (29.93 % p/p).
En conclusión, se caracterizó la composición proximal y perfil de ácidos grasos de larvas Cotinis columbica Burmeister provenientes de los municipios Mogotes (Santander) y Garzón (Huila), Colombia. Los valores de composición y ácidos grasos fueron similares, excepto para C10:0. Las larvas Cotinis columbica Burmeister resultan atractivas, en términos nutricionales, debido a sus concentraciones de proteína (24.6%), grasa (26.1%) y ácidos grasos esenciales C18:1 (31.97 % p/p) y C18:2 (29.93% p/p).