Introducción
Los psicofármacos son medicamentos que tienen su diana de acción en el sistema nervioso central, pueden atravesar la placenta y la barrera hematoencefálica del feto, llegando a alterar las funciones cerebrales perinatales, impactar en el desarrollo neurológico a largo plazo, causar malformaciones cardíacas y otras condiciones como la abstinencia neonatal 3.
Para las mujeres, la incidencia máxima de diversos trastornos psiquiátricos, como la esquizofrenia, se produce durante su edad fértil. Entre los trastornos más comunes en este período se encuentran el trastorno depresivo mayor y el trastorno afectivo bipolar. La depresión unipolar prenatal es una de las condiciones más frecuentes, cuyos síntomas no difieren mucho de los observados en la población no gestante. Se ha demostrado que su prevalencia se asocia con un mayor riesgo de múltiples resultados obstétricos deficientes, como aborto espontáneo, sangrado obstétrico, cesáreas y parto prematuro 1.
Los trastornos psiquiátricos maternos tratados inadecuadamente tienden a resultar en comportamientos poco saludables durante el embarazo, atención prenatal deficiente, vínculos infantiles insuficientes y entornos familiares estresantes 4. La detección temprana de estos trastornos y su abordaje adecuado tienen un impacto en el pronóstico y en la prevención de complicaciones 2.
Se han descrito diversos factores maternos, fetales, farmacológicos y sociales que influyen en el resultado del uso de psicofármacos, lo cual afecta la elección del enfoque terapéutico con el objetivo de minimizar el impacto en la madre, el feto, el recién nacido y el niño en desarrollo. El riesgo potencial de no tratar las enfermedades psiquiátricas durante el embarazo, ha aumentado la conciencia sobre la importancia de su tratamiento 4.
Farmacocinética durante el embarazo
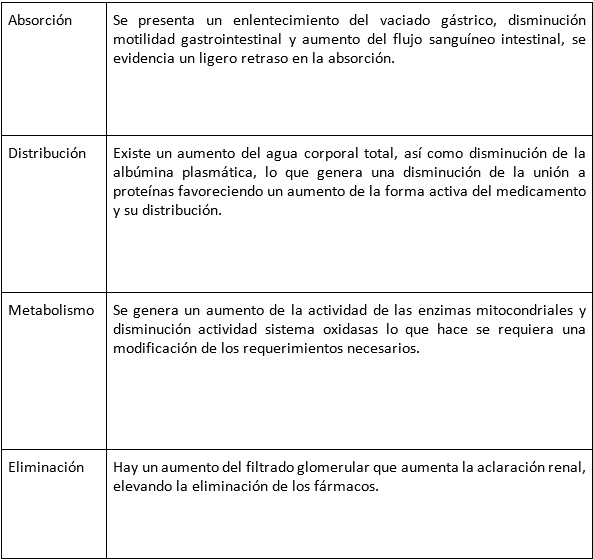
Durante la etapa gestacional se producen varios cambios fisiológicos adaptativos importantes que interfieren en la absorción, distribución, metabolismo y eliminación de la medicación, llegando a afectar la efectividad y seguridad (aumento del volumen plasmático, disminución de con anterioridad a la gestación por padecer algún tipo de unión a proteínas, aumento del filtrado glomerular, etc.) 5. Los cambios más importantes se encuentran en la tabla 1:
El efecto que un fármaco causa en el feto y la madre depende del momento de su administración, se han descrito tres períodos, el primero de implantación, seguido de organogénesis y por último de desarrollo, cada etapa presenta sus riesgos particulares para el feto (ver tabla 2)
La clasificación de riesgo más conocida es la de la FDA, la cual se originó posterior a los daños ocasionados por el uso de la talidomida en las gestantes:
Categoría:
1. Estudios controlados no han demostrado riesgo. Bajo riesgo de daño fetal.
2. No hay descritos riesgos en humanos, hay estudios en animales donde no se reporta riesgos, se acepta su uso durante el embarazo.
3. No puede descartarse riesgo fetal. Hay estudios en animales que demuestran efectos adversos, pero no existe estudios en gestantes. Se debe evaluar beneficio/riesgo.
4. Existen indicios de riesgo fetal. Hay estudios en embarazadas donde se muestra riesgo de efectos adversos, por lo que solo debe usarse en casos de inexistencia de alternativas.
5. Contraindicados en el embarazo, existen estudios en embarazadas y en animales que han demostrado que los riesgos potenciales superan claramente a los posibles beneficios
Metodología
Se realizó una búsqueda en Pubmed usando MESH como “psychotropic drugs”, “pregnant”, “antidepressants agents”, “Antipsychotic Agents”, “ lithium”, “valprote”, “lamotrigine”, se utilizó varias combinaciones con el MESH “pregnant”, usando “AND” como conector. Para esta revisión se emplearon principalmente ensayos clínicos publicados en los últimos 10 años, escritos tanto en idioma español como en inglés.
Psicofármacos utilizados en el embarazo
1.Antidepresivos
Existen varios estudios que han estudiado las concentraciones de los diferentes antidepresivos en la placenta y en el feto; al analizar la venlafaxina y el citalopram, estos han mostrado más penetración en el líquido amniótico, mientras que las más bajas fueron para fluvoxamina y fluoxetina, respecto al plasma del cordón umbilical, la nortriptilina tuvo las concentraciones más altas seguidas por bupropión; en la leche materna, la venlafaxina y el escitalopram tenían mayor concentración (6).
1.1 Antidepresivos tricíclicos
Este grupo de antidepresivos fue el primero en ser desarrollado y su uso se inició en 1950. Aunque en sus inicios tuvieron un amplio uso, en la actualidad se reservan sólo para casos específicos 7. Estos medicamentos se consideran como último recurso debido a su baja tolerancia y al riesgo de ser letales en caso de sobredosis. Sin embargo, no se ha asociado su uso con riesgo de teratogenicidad. En un estudio publicado en 2017 que incluyó una población gestante de 18,487 mujeres y que comparó diferentes tipos de antidepresivos (inhibidores selectivos de la recaptación de serotonina (ISRS), inhibidores de la recaptación de serotonina y norepinefrina (IRSN), antidepresivos tricíclicos (TCA) y otros antidepresivos), se encontró que el uso de amitriptilina en el primer trimestre se asoció con un aumento en malformaciones oculares, auditivas, defectos faciales y del cuello (OR 2.45, IC 95% 1.05-5.72), así como defectos digestivos. Sin embargo, estas asociaciones no fueron mayores que las observadas en la población que no utilizó este medicamento 7.
A pesar de que la mayoría de ATC no ha sido relacionada con teratogénesis, fármacos como la clomipramina se han relacionado con aumento de riesgo de defectos cardíacos 8. No se ha establecido una relación entre los antidepresivos tricíclicos (ATC) y el parto prematuro. Sin embargo, se ha observado una asociación entre los ATC y la preeclampsia en un estudio realizado en Columbia Británica, donde se evidenció que el 10% de la población de más de 100 mujeres que recibieron ATC desarrollaron preeclampsia, en comparación con el 2% que no los recibieron 9.
Además, se ha encontrado una asociación entre la exposición a los ATC cerca del momento del parto y la hemorragia posparto, con un aumento en el riesgo de hemorragia posparto de 1.4 a 1.9 veces 10. También se ha relacionado el uso de ATC con la aparición de síntomas de abstinencia neonatal, como hipoglucemia, alteraciones respiratorias, síntomas del sistema nervioso central e ictericia 8. Entre los efectos adversos en mujeres embarazadas se encuentran el estreñimiento, la presión arterial baja, el aumento de peso, la sedación excesiva y la taquicardia.
1.2 Inhibidores de recaptación de serotonina (ISRS)
Los inhibidores selectivos de la recaptación de serotonina (ISRS) son los medicamentos más utilizados en trastornos del ánimo. Actualmente, son el grupo de primera línea en el tratamiento del trastorno depresivo debido a su seguridad y mejor tolerancia. También se utilizan en el tratamiento del trastorno de pánico, los trastornos obsesivo-compulsivos, la ansiedad social y la bulimia nerviosa 12.
Se reconoce que la fluoxetina y el citalopram tienen la capacidad de atravesar la placenta. El aumento de serotonina que se produce con el uso de estos medicamentos puede afectar diversos tejidos, incluida la placenta, lo que se sospecha que puede afectar la vasoconstricción y la coagulación y provocar hematomas. Se sospecha que la exposición a estos medicamentos durante el período de organogénesis puede estar relacionada con alteraciones en el desarrollo del sistema nervioso central y el desarrollo craneofacial 12.
Sin embargo, los estudios realizados en este grupo de medicamentos no han demostrado asociación significativa con un mayor riesgo de teratogenicidad. Un estudio realizado en 2016 en Gales, Noruega y Dinamarca no encontró un riesgo absoluto adicional significativo de teratogenicidad asociado con los ISRS 11. El riesgo se superpone con el riesgo general de la población (2-4%).
Se han encontrado múltiples estudios que han informado que los ISRS están asociados a aumento del riesgo de defectos cardiovasculares, se ha encontrado que el uso de paroxetina aumenta hasta el doble de riesgo de enfermedades cardíacas, especialmente defectos del tracto de salida del ventrículo derecho 1 % de los expuestos vs 0.5% de los no expuestos. Otros estudios han informado un aumento del riesgo de atresia anal hasta de 4 veces mayor con el uso de antidepresivos (0.06 % en la población general vs un 0.2% en los expuestos a sertralina) 13.
Los recién nacidos expuestos a sertralina durante el primer trimestre del embarazo tenían un riesgo relativo de atresia anal 4 veces mayor que los recién nacidos expuestos a otros antidepresivos, Sin embargo, la atresia anal es una malformación congénita muy rara (5 de 10.000 neonatos, 0,06%), mientras que el riesgo para un lactante expuesto a sertralina es del 0,2% 14.
No se ha encontrado una asociación entre los ISRS y el aborto espontáneo, se ha evidenciado que los trastornos del estado del ánimo pueden aumentar el riesgo de aborto espontáneo, así como ciertos estilos de vida como fumar o beber; un estudio realizado en Quebec mostró que la incidencia del aborto espontáneo fue comparable con el grupo de control (13 vs 14%) 15. Los ISRS no se han asociado a aumento del riesgo de síndrome de abstinencia, trabajo de parto pretérmino, diabetes gestacional, depresión respiratoria posparto o bajo peso al nacer, además de mortalidad neonatal 12.
Se ha encontrado una asociación entre los ISRS y un mayor riesgo de trastorno hipertensivo en el embarazo. Un metaanálisis que incluyó a más de un millón de mujeres embarazadas encontró esta asociación, aunque se identificaron factores de confusión como la edad materna, la diabetes mellitus y el tabaquismo que podrían influir en los resultados 16. En cuanto a la diabetes mellitus gestacional, se ha sugerido que la asociación con los ISRS puede haber sido sobreestimada, aunque la evidencia disponible es insuficiente para confirmarlo 19.
Se ha estudiado la posibilidad de una asociación entre el uso de ISRS en el tercer trimestre y un mayor riesgo de hemorragia posparto. Sin embargo, se ha observado que estos resultados pueden verse influenciados por las indicaciones de uso de los ISRS. Se ha demostrado que es seguro suspender su uso 30 días antes del parto para minimizar este riesgo 17.
En cuanto a los posibles cambios en el comportamiento del feto, se ha asociado el uso de ISRS con una mayor actividad y comportamiento de exploración. Sin embargo, no se encontraron diferencias significativas en la ansiedad, el comportamiento social, el aprendizaje y la memoria, el comportamiento ingestivo y de recompensa, el comportamiento motor, los reflejos o la sensibilidad al dolor 20.
No hay un ISRS más seguro que otro para su uso durante el embarazo, excepto la paroxetina, que se ha asociado a malformaciones cardiovasculares congénitas. Sin embargo, esta asociación es controvertida, ya que existen estudios que no han encontrado dicho riesgo. Actualmente, aunque se han llevado a cabo numerosos estudios con ISRS, no hay suficiente evidencia para evaluar los riesgos de manera definitiva. Además, los nuevos ISRS como el escitalopram, así como los menos utilizados como la fluvoxamina, han sido menos estudiados en este contexto 20)(21.
Guías como el consenso de la Asociación Británica de Psicofarmacología recomiendan los ISRS como tratamiento farmacológico de primera línea para la depresión en etapa pregestacional, prenatal y posnatal debido a su seguridad reproductiva. Por lo tanto, se considera una buena opción como antidepresivo en pacientes que no han utilizado medicamentos para la depresión previamente 20)(21.
En pacientes que están recibiendo tratamiento antes del embarazo, no se debe suspender de manera repentina al descubrir la gestación debido al riesgo de recurrencia y síndrome de abstinencia. Siempre se debe evaluar la relación beneficio/riesgo para tomar decisiones informadas. Según un metaanálisis publicado en 2020, no se observó un mayor riesgo de recaída de la depresión durante el embarazo en mujeres que suspendieron los antidepresivos en comparación con aquellas que continuaron tomándose (riesgo relativo [RR] = 1,74; IC del 95 %, 0,97 a 3,10; P = 0,06). Sin embargo, en el subanálisis, se encontró un riesgo significativamente mayor de recaída en casos de depresión grave o recurrente (RR = 2,30; IC del 95 %, 1,58 a 3,35). 21.
No hay consenso sobre la reducción/discontinuación o mantenimiento de los antidepresivos en el período cerca del embarazo, ya que puede representar riesgo de mala adaptación neonatal. 18.
1.3 Antidepresivos duales (IRSN):
Hay pocos estudios publicados sobre la duloxetina y venlafaxina en comparación con los ISRS. En los estudios realizados con duloxetina, no se ha encontrado una asociación causal entre malformaciones mayores.
En un estudio de cohorte publicado en 2020 que incluyó entre 2500 y 3000 gestantes expuestas a duloxetina al principio del embarazo y entre 900 y 950 expuestas al final del embarazo, no se encontró evidencia suficiente para considerar la duloxetina como teratógeno (el porcentaje de malformaciones fue similar al de la población general, alrededor del 2-3%). Sin embargo, se detectó un pequeño aumento del riesgo de malformaciones cardíacas. Además, se ha relacionado con un mayor riesgo de hemorragia posparto, por lo que su uso debe individualizarse, sopesando los potenciales riesgos frente al riesgo de depresión y síndrome doloroso en gestantes. 22.
Ni la duloxetina ni la venlafaxina se han asociado con aborto espontáneo. En un estudio de cohorte comparativo observacional prospectivo publicado en 2019, que recopiló datos del Servicio de Información de Teratología del Reino Unido (UKTIS) entre 1995 y 2018 e incluyó 281 embarazos, se concluyó que no había diferencias estadísticamente significativas en el riesgo de aborto espontáneo después del uso gestacional de venlafaxina en comparación con cualquier otro antidepresivo sin exposición. 23.
La duloxetina y la venlafaxina pueden estar asociadas con un mayor riesgo de trastornos hipertensivos del embarazo, pero los estudios han tenido una muestra limitada para ser concluyentes. 24. Los estudios sobre los IRSN no han podido establecer conclusiones firmes respecto a los efectos en el recién nacido, como la sedación y las alteraciones de la succión 25.
En conclusión, los datos acumulados no son concluyentes, aunque han mostrado seguridad en los estudios realizados. Siempre es importante individualizar el tratamiento en las gestantes.
1.4 Antidepresivos atípicos
Bupropion: su uso se ha considerado seguro durante la gestación, convirtiéndose en una buena opción para el manejo del hábito tabáquico, el cual se ha asociado fuertemente con desenlaces desfavorables durante la gestación 26. El riesgo de teratogenicidad se considera bajo, y no parece haberse asociado con trastornos hipertensivos del embarazo, hemorragia posparto ni complicaciones en el recién nacido, como el bajo peso al nacer. Sin embargo, se ha encontrado una baja relación con abortos espontáneos 27.
Mirtazapina: los estudios son muy limitados, pero no parece haber asociación con efectos teratogénicos. No hay claridad respecto a la relación con aborto espontáneo y parto prematuro. Además, no se ha asociado con trastornos hipertensivos del embarazo ni hemorragia post natal 28.
2. Antipsicóticos
2.1 Antipsicóticos típicos o de primera generación
El mecanismo de acción de este grupo de fármacos consiste en bloquear los receptores dopaminérgicos D2. Sin embargo, debido a sus múltiples efectos adversos, se han sintetizado diversos fármacos con el objetivo de lograr acciones más selectivas y mejor toleradas por los pacientes 29)(30)(31.
Durante décadas, su seguridad durante el embarazo ha sido cuestionada, principalmente debido a trastornos del neurodesarrollo, aunque también podría deberse a otros factores como predisposición genética o ambiental, e incluso al uso concomitante de otros fármacos 32.
En las últimas tres décadas, el uso de estos agentes ha aumentado en la población gestante debido a la necesidad de tratar a una población vulnerable. Sin embargo, los datos sobre su seguridad y los mejores medicamentos siguen siendo muy limitados. La práctica actual sugiere considerar los posibles riesgos y complicaciones al iniciar, suspender o ajustar las dosis de antipsicóticos.
Según el consenso realizado en 2021 por las asociaciones de pediatría, obstetricia y psiquiatría (Federatie Medisch Specialisten), el antipsicótico de primera generación con mayor evidencia es el haloperidol. A pesar de existir riesgo de diabetes gestacional y teratogenicidad, se ha demostrado que logra controlar los trastornos psicóticos y el trastorno afectivo bipolar. En cuanto al neurodesarrollo, no hay evidencia que sugiera un aumento en la incidencia de TDAH y trastorno del espectro autista 33.
2.2. Antipsicóticos atípicos o de segunda generación
Durante los últimos años, se ha demostrado que los antipsicóticos de segunda generación son una alternativa principal e incluso se han presentado como la primera línea de tratamiento debido a su menor riesgo de efectos adversos en comparación con los antipsicóticos de primera generación, así como a su mayor espectro de tratamiento de trastornos afectivos 31.
Estos medicamentos son lipofílicos y atraviesan la barrera materno-placentaria con facilidad, lo que los hace potencialmente teratogénicos o con la capacidad de causar serias consecuencias en el neurodesarrollo 32, aunque los datos al respecto son limitados. Los trastornos del espectro autista y el trastorno por déficit de atención e hiperactividad (TDAH) son los más comúnmente asociados a su uso. Sin embargo, los modelos animales suelen ser heterogéneos, ya que los receptores en el cerebro y los hallazgos durante las diferentes etapas gestacionales no suelen ser los mismos.
No obstante, en un estudio de cohortes realizado por Wang, se concluye que no existe una relación directa entre el uso de antipsicóticos de segunda generación y los trastornos del neurodesarrollo, aunque el riesgo puede ser hasta 2 veces mayor en comparación con la población general 32.
Una desventaja adicional está relacionada con el síndrome metabólico, por lo que es natural asociar este grupo farmacológico con una mayor incidencia de diabetes gestacional, una patología que conlleva serias consecuencias tanto para la madre como para el feto. Un cambio notable está relacionado con el índice de masa corporal (IMC), en el cual la quetiapina, la clozapina y la olanzapina tienen un efecto importante. Es importante tener en cuenta que los trastornos psicóticos son un factor de riesgo para el sobrepeso y la obesidad 31.
Un desenlace que podría estar asociado al uso de antipsicóticos atípicos durante el embarazo son las cardiopatías congénitas, los defectos del tracto gastrointestinal y el paladar hendido. Aunque podría existir un riesgo más alto 34, las poblaciones estudiadas suelen presentar comorbilidades importantes como la obesidad y el consumo de sustancias lícitas e ilícitas, además del uso concomitante de otros psicofármacos 35, por lo que no se puede considerar concluyente 36.
A pesar de los posibles riesgos, la prescripción de estos fármacos ha aumentado principalmente en el período pregestacional y en el primer trimestre, pero aún existen limitaciones en los trimestres posteriores. Sin embargo, el criterio clínico sigue siendo fundamental para equilibrar los beneficios y riesgos en cada caso individual. Si bien los antipsicóticos pueden ser seguros durante el embarazo, los diversos estudios sugieren que deben administrarse en la dosis mínima posible para reducir el riesgo de secuelas importantes tanto para la madre como para el feto.
3. Estabilizadores del ánimo
3.1 Litio: Parece que el litio se equilibra completamente a través de la placenta ya que se ha encontrado una relación de 1:1 entre los niveles en sangre del cordón umbilical y la sangre materna. Sin embargo, los niveles de litio pueden disminuir a medida que avanza el embarazo, por lo que es necesario ajustar la dosis 37.
Se ha asociado el litio con efectos teratogénicos, especialmente con malformaciones cardíacas como la anomalía de Ebstein, defectos de obstrucción del tracto de salida del ventrículo derecho, coartación de la aorta y atresia mitral. Se ha encontrado que la dosis está relacionada con el riesgo, siendo mayor con dosis superiores a 900 mg al día en comparación con dosis inferiores a 600 mg 38.
En un metaanálisis colaborativo internacional de seis estudios de cohortes que incluyeron 22,124 embarazos, de los cuales 727 estuvieron expuestos al litio, no se encontró asociación entre la exposición al litio y complicaciones predefinidas del embarazo. Sin embargo, se observó un mayor riesgo de readmisión neonatal después de los primeros 28 días de vida en aquellos cuyas madres recibieron litio durante el embarazo (prevalencia combinada del 27.5% frente al 14.3%). También se observó una mayor asociación con malformaciones mayores (prevalencia agrupada del 7.4% frente al 4.3%) en este estudio 39.
En otro estudio posterior, se encontró una asociación entre el litio y el parto prematuro espontáneo, así como con un mayor peso para la edad gestacional, hipoglucemia neonatal y malformaciones cardiovasculares (40). Por lo tanto, el uso de litio debe individualizarse, sopesando los riesgos del trastorno afectivo bipolar con el riesgo del uso de litio.
3.2 Valproato: El ácido valproico puede atravesar la placenta y se ha relacionado con más de 8 malformaciones congénitas mayores importantes, como defectos del tubo neural, espina bífida, cataratas congénitas, defectos craneofaciales (como hendiduras orales y craneosinostosis), malformaciones cardiovasculares, hipospadias y malformaciones de las extremidades (como pie zambo y polidactilia) 41.
Además, entre otros efectos no relacionados con malformaciones mayores, se ha encontrado una disminución en el coeficiente intelectual y trastornos del desarrollo como el trastorno del espectro autista y el trastorno por déficit de atención/hiperactividad, así como pérdida o deterioro de la audición después de la exposición en el útero 42. El uso de este medicamento no se recomienda en gestantes con epilepsia, para la prevención de migrañas y en el trastorno afectivo bipolar.
3.4 Lamotrigina: Este medicamento es capaz de atravesar la placenta humana, se puede medir sus niveles en la sangre de recién nacidos vivos. No se ha asociado a un aumento en la incidencia de malformaciones congénitas mayores, por lo que lo convierte en una excelente opción en paciente con trastorno afectivo bipolar. 43.
4. Benzodiacepinas
Todavía no hay consenso respecto la existencia de malformaciones congénitas, sin embargo, parece indicar que no hay asociación causal, los estudios sugieren que hay relación con el aborto espontaneo y parto prematuro. 44. Adicionalmente se ha mostrado que el uso crónico de las benzodiacepinas puede provocar toxicidad neonatal y abstinencia provocando Apgar bajo, apnea, hipotermia, hiperreflexia, hipertonía o hipotonía, letargo, temblor, vómito e inquietud motora. 45.
Conclusión
El manejo de la enfermedad mental en la gestante reviste de importantes desafíos para el médico, ya que la seguridad de los psicofármacos durante el embarazo requiere una evaluación individualizada de los beneficios y riesgos, se debe sopesar en todos los casos los riesgos que conlleva la descompensación de la patología mental comparado con los riesgos de la medicación, ofreciendo el manejo más seguro. Aunque algunos grupos de psicofármacos se consideran relativamente seguros, es necesario tener precaución y considerar las posibles complicaciones asociadas con su uso durante el embarazo.