Introducción
Dentro de los residuos generados durante el beneficio del grano de cacao se encuentra la cáscara o cacota, que representa cerca del 75 % p/p del fruto. Esta no es aprovechada completamente debido a las grandes cantidades que se producen durante épocas de cosecha (10 ton cáscara húmeda / ton grano seco) 1, convirtiéndose en focos de contaminación para el cultivo debido a su acumulación, promoviendo el desarrollo de agentes patógenos como Phytophoraspp Moniliophthoraroreri y Crinipellis perniciosa en los cultivos 2.
Dentro de las alternativas de valorización se encuentra la extracción de polifenoles presentes en este residuo vegetal 3. Dentro de los grupos de polifenoles se destacan los flavonoides, puesto que son los más abundantes; estos a su vez se clasifican en flavonoles, flavonas, isoflavonas, antocianinas y flavanoles 4. Los flavanoles son los polifenoles con mayor presencia en la cáscara de cacao, principalmente catequinas, epicatequinas y proantocianidinas 5. Estos polifenoles son de gran beneficio para la salud gracias a sus propiedades antioxidantes y la capacidad que tienen para atrapar radicales libres 6. Los polifenoles en el mercado tienen un alto valor y ha ido en aumento cada año, según Market Analysis Report7, para el 2018 el mercado global de polifenoles estuvo en 1.28 mil millones USD y aumentará en un 7.2 % desde el 2019 hasta el 2025.
Uno de los métodos más utilizados para extraer polifenoles a partir de vegetales y residuos sólidos agroindustriales es la extracción con solventes 8, conocida también como extracción sólido-líquido. Los solventes más utilizados han sido agua acidificada, etanol, metanol y acetona 9.
Numerosos trabajos de investigación han estudiado la extracción de compuestos bioactivos (entre ellos los polifenoles) como alternativa de valorización de residuos vegetales 10. También, se han realizado estudios de simulación de procesos a escala industrial para la obtención de polifenoles a partir de la cáscara de cacao 3. Sin embargo, el común denominador de los trabajos desarrollados ha sido la extracción de los compuestos a partir de material agroindustrial secado; justificado por una mayor estabilidad en el tiempo, al inhibir el crecimiento microbiano y las reacciones enzimáticas 11. No obstante, desde el punto de vista industrial, incluir una etapa de secado para procesar este material resulta considerablemente costoso. Según Villamizar-Jaimes y López-Giraldo 3, el costo energético asociado a esta etapa representa el 47 % del consumo total de energía del proceso, por lo tanto, para el pretratamiento de esta materia prima, recomiendan buscar alternativas que permitan reducir este gasto tanto energético como de inversión.
Dentro de las principales variables a tener en cuenta a la hora de extraer polifenoles de matrices vegetales se encuentran: temperatura, pH de solución, tipo de solvente y relación soluto:solvente 12. Para el caso de la temperatura de extracción, un calentamiento durante el proceso puede favorecer el arrastre de estos compuestos debido al ablandamiento del material vegetal 13; sin embargo, la temperatura no debe exceder los 60 °C debido a la degradación térmica 14. Con respecto al pH de la solución, este puede afectar la solubilidad de los compuestos, y con ello, su extracción 15. En cuanto al solvente, debe ser de naturaleza y polaridad similar a la de los polifenoles para favorecer su extracción; algunos autores recomiendan trabajar con mezclas de solventes como etanol y agua, para mejorar los rendimientos de extracción 16. Por último, la relación soluto:solvente (p:v), la cual funciona como fuerza impulsora en la transferencia de masa 17.
Además de analizar las condiciones de extracción algunos estudios han evaluado la cinética de extracción en distintas matrices (cáscara de patata 18; cáscara de pitahaya 19; cáscara de granada 20, entre otros. La cinética de extracción permite conocer el tiempo requerido para extraer la mayor cantidad de compuestos fenólicos, y el ajuste de parámetros cinéticos permite obtener información del proceso, por ejemplo, la velocidad de extracción. Dentro de los modelos cinéticos más utilizados en este tipo de extracciones y con mejor ajuste han sido los modelos de Peleg y Peleg Modificado 20.
Como se mencionó anteriormente, se ha evaluado la extracción de polifenoles en cáscara de cacao previamente secada. A pesar de ello, a la fecha se desconocen reportes en donde se informe el efecto que pueden tener estas mismas variables en el rendimiento de extracción utilizando este material húmedo. Teniendo en cuenta lo anterior, el objetivo de este trabajo fue determinar la influencia de procesar cáscara de cacao húmeda y las condiciones de proceso sobre el rendimiento de extracción, y el contenido de polifenoles y capacidad antioxidante de los extractos.
Metodología
Condiciones ambientales y localización geográfica del proyecto
El proyecto se desarrolló en el municipio de Piedecuesta/Santander, ubicado geográficamente a 6° 59′ 15″ Norte, 73° 2′ 58″ Oeste y a 1005 m sobre el nivel del mar, considerado como zona de clima tropical según la clasificación de Köppen.
Adecuación de materia prima (inactivación polifenol oxidasa)
La cáscara de cacao fresca fue suministrada por Fedecacao (clon CCN-51), esta fue picada (trozos de 1 cm3 aproximadamente), sumergida en baño de agua caliente a 96 °C, 5 min, y posteriormente, en agua fría (~5 °C), 20 min, con el fin de inactivar la enzima polifenol-oxidasa y evitar pérdida de antioxidantes durante el almacenamiento. Parte de esta cáscara fue secada a 50 °C, 26 h, y molida, con el objetivo de obtener el material de referencia (cáscara secada) 1; y la otra parte, fue llevada a molienda directamente antes de la extracción de polifenoles. Es importante aclarar que, el término “cáscara de cacao húmeda” hace referencia a la cáscara fresca que no fue llevada a secado.
Extracción de polifenoles a escala laboratorio
Para las extracciones con cáscara de cacao secada (que para este estudio se toma como referencia) se trabajó con una relación soluto:solvente 1:60(p:v; es decir g:mL), etanol:agua 50:50(v:v; es decir mL:mL), 60 °C y pH de solución que naturalmente se encontró en todos los ensayos entre 6.1 - 6.5; condiciones de extracción similares a las óptimas reportadas por Villamizar-Jaimes and López-Giraldo (3). Para la cáscara húmeda, se determinó su humedad para establecer la cantidad de solvente a utilizar, y mantener la relación soluto:solvente equivalente a la empleada con la matriz secada.
Para la determinación de las condiciones óptimas de extracción usando cáscara de cacao húmeda se planteó un diseño experimental de superficie de respuesta 23 con puntos centrados en las caras, por duplicado, y análisis ANOVA con significancia del 95 %, a través de TIBCO Statistica® 13.5.0 y Statgraphics Centurion XVI.I versión de prueba. Los niveles fueron los mismos trabajados por el Grupo de investigación en Ciencia y Tecnología de Alimentos de la Universidad Industrial de Santander - CICTA/UIS para cáscara de cacao secada, a excepción del pH, el cual se trabajó con el dado por la mezcla soluto- solvente (valores entre 6.1 y 6.5). En la Tabla 1 se muestran las variables, los niveles y la variable de respuesta evaluada en cada una de las corridas experimentales las cuales fueron en total 32.
Tabla 1 Niveles evaluados en el diseño de experimentos.
| Factor | Temperatura (°C) | Etanol:Agua (v:v) | Soluto:Solvente (p:v) | Variable de respuesta | |||
|---|---|---|---|---|---|---|---|
| Nivel | Mínimo | Máximo | Mínimo | Máximo | Mínimo | Máximo | Polifenoles totales (mgEAG/gMS) |
| Valor | 20 | 60 | 0:100 | 100:0 | 1:120 | 1:24 | |
Fuente: Autores.
Todas las extracciones, tanto en cáscara secada como en cáscara húmeda, se realizaron en balones de vidrio fondo plano de 50 - 250 mL de capacidad, en plancha de calentamiento con agitación magnética y termómetro para el seguimiento de la temperatura.
Validación del punto óptimo de extracción
Se realizó la extracción bajo condiciones óptimas encontradas por el modelo y se comparó con el valor predicho por este. Para determinar la capacidad de predicción del modelo se utilizó la ecuación para la desviación relativa absoluta promedio, AARD (Ec. 1).
Donde, n: número de datos, Ve: valor experimental de polifenoles (mgEAG/gMS), Vc: el valor calculado predicho por el modelo (mgEAG/gMS).
Ajuste de parámetros cinéticos
Se realizó el seguimiento de la cinética de extracción de polifenoles (usando cáscara húmeda) durante 4 h, tomando alícuotas de 1mL cada 10 min durante las primeras 2 h, y cada 30 min después de esta. Se hizo el ajuste de parámetros cinéticos evaluando modelos reportados en literatura 21 mostrados en la Tabla 2 utilizando el método Quasi-Newton del paquete TIBCO Statistica® 13.5.0.
Tabla 2 Modelos matemáticos sugeridos para la descripción de la cinética de extracción.
| Modelo | Ecuación | Parámetros |
|---|---|---|
| Peleg |
|
k1, n: constantes de Peleg. |
| Peleg Modificado |
|
k2: inverso de la velocidad de extracción. |
| k3: inverso de concentración máxima. | ||
| Logarítmico |
|
A, B: constantes del modelo logarítmico. |
| Rakotondramasy |
|
k4: constante de velocidad global (1/min). |
Fuente: Bucic'-Kojic' et al.21.
Caracterización de los extractos
Los polifenoles totales (PT) se cuantificaron a partir de la reducción del reactivo Folin-Ciocalteu, la absorbancia fue medida a 765 nm mediante un espectrofotómetro UV-vis (Multiskan GO ThermoScientific) 26. Se utilizó la técnica de cromatografía líquida HPLC para identificar y cuantificar las familias de polifenoles presentes en los extractos, para esto utilizó un HPLC Thermo Scientific UltiMate 3000, equipado con un sistema de autoinyección y detector UV-VIS (Thermo Scientific VWD-3100). Se utilizó una columna analítica de fase inversa (Zorbax Eclipse XDB C18 150 mm x 2.1 mm x 5 µm) y una columna semipreparativa (Mediterránea Sea 150 mm x 4,6 mm x 5 µm). La columna se calentó a 40 °C utilizando un horno (Thermo Scientific TCC-3000 SD). Todos los compuestos se detectaron a 204 nm 26. La capacidad antioxidante se determinó por el método ORAC mediante espectrofluorímetro de microplacas (ThermoScientific®), fluoresceína como solución de trabajo y AAPH como radical libre, usando longitudes de onda de emisión y excitación de 485 y 528 nm, respectivamente 26. Para el método de radical libre DPPH, se preparó el reactivo 1,1-difenil-2picrilhidrazil (DPPH) en metanol, se mezcló con la muestra, y luego de 30 min, se leyó el resultado por espectrofotometría UV-vis (Multiskan GO ThermoScientific), con a una absorbancia de 515 nm 22. Todas las mediciones se realizaron por duplicado.
Resultados y discusión
Extracción de polifenoles en cáscara de cacao secada
El contenido de polifenoles totales obtenidos de la cáscara de cacao secada fue de 54.75±1.49 mgEAG/gMS y la capacidad antioxidante fue de 1002.59±110.21 µmolET/gMS (ORAC) y 417.12±11.35 µmolET/gMS (DPPH) a pH de solución 6.3. Los valores obtenidos en este estudio fueron ligeramente inferiores a los encontrados por Toro-Uribe et al.23 y Villamizar-Jaimes y López-Giraldo 3, para cáscara secada, los cuales fueron de 61±1.8 y 60.01±2.8 mgEAG/gMS, respectivamente. A pesar de que el pH de extracción (6.1 - 6.5) en el presente trabajo fue diferente al pH reportado por los autores mencionados anteriormente, entre 4 y 5 3,23, no se evidenció cambios considerables causados por esta variable en el proceso de extracción. Lo anterior permitiría suponer que no es necesario acidificar el medio de extracción para recuperar la mayor cantidad de compuestos fenólicos; además, desde un punto de vista productivo, el costo disminuiría debido a la reducción de insumos.
Es importante mencionar que a pesar de que las extracciones y mediciones realizadas por los diferentes autores involucraron diferentes épocas de cosecha, el contenido de polifenoles extraídos permaneció en valores similares. Este resultado, abre la posibilidad a este tipo de materia prima, puesto que la variación entre los productos obtenidos de cosecha a cosecha puede considerarse menor. Estudios más detallados sobre este tema permitirán profundizar más sobre el mismo.
Con respecto a la capacidad antioxidante-ORAC del extracto obtenido, esta fue inferior a la capacidad antioxidante del grano de cacao reportada por Zapata et al. 24 para este clon, la cual fue de 1473.22±65.15 µmolET/gMS (ORAC); sin embargo, se encuentra en el mismo orden de magnitud (1002.59±110.21 µmolET/gMS), por lo tanto, la cáscara de cacao también puede considerarse como una buena fuente antioxidante. En cuanto a la capacidad antirradicalaria (DPPH), el valor encontrado fue superior al reportado por Zapata et al.25 para grano de cacao CCN-51 (251.59±10.62 µmolET/gMS). Estas diferencias en la capacidad antioxidante (por ORAC) y antirradicalaria (por DPPH) pueden deberse a que los extractos obtenidos por los diferentes autores tienen distintos perfiles de concentración de compuestos polifenólicos. En efecto, Pico-Hernández et al.26 mostraron que la capacidad antioxidante de un extracto polifenólico de granos de cacao depende de la proporción de cada una de las familias presentes en el extracto; de acuerdo con sus resultados, los extractos con mayor capacidad antioxidante-ORAC son aquellos ricos en dímeros de epicatequina; además, ellos evidenciaron que conforme aumentan las proporciones de monómeros y oligómeros de epicatequina la capacidad antioxidante-ORAC disminuye.
Extracción de polifenoles en cáscara de cacao húmeda
La humedad del material fresco utilizado en el presente estudio fue de 89.01±0.07 % p/p, similar a datos históricos encontrados por el Grupo de investigación en Ciencia y Tecnología de Alimentos de la Universidad Industrial de Santander - CICTA/UIS para la cáscara del mismo clon (90 % p/p). Para cáscara de cacao secada el %humedad fue de 5.63±0.30 % p/p, esto demuestra que la cantidad de agua que debe remover la etapa de secado es alta, por esta razón, implementar un proceso de secado a gran escala puede implicar un costo energético alto 3.
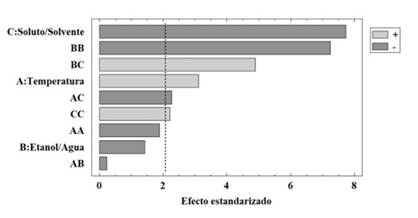
En la Figura 1 se puede observar el diagrama de Pareto obtenido de las pruebas de extracción realizadas. De acuerdo con dicha figura, la relación soluto:solvente y la temperatura tienen una influencia significativa dentro del proceso. Aunque la relación etanol:agua no tiene un efecto significativo, la interacción de esta con otras variables y su valor cuadrático sí, por lo tanto, se podría inferir que la extracción de polifenoles se ve influenciada por todas las variables evaluadas. De manera similar, para cáscara secada se encontró una influencia similar de estas mismas variables sobre la extracción de polifenoles.
En la Figura 2 se muestra los efectos principales que tienen las variables evaluadas sobre los polifenoles totales extraídos. En esta figura se observa que para la temperatura y la relación etanol:agua existen máximos dentro del rango de valores evaluados. En el caso de la temperatura, el máximo se encuentra en 55 °C; esto puede deberse al ablandamiento del tejido vegetal, lo que facilita la extracción de polifenoles 13. Por encima de esta temperatura la extracción disminuye, debido a la sensibilidad térmica de estos compuestos bioactivos; por encima de 60 °C comienzan a degradarse 14. Para el caso del etanol:agua, se observa un máximo en una relación de 40:60, favoreciendo la solubilidad de los compuestos fenólicos debido a las polaridades presentes en estos extractos polifenólicos. Otros estudios han reportado este mismo comportamiento, el cual es favorecido al utilizarse etanol como solvente 27. En cuanto a la relación soluto:solvente, se puede observar que hay un aumento de la extracción con la relación 1:120. Esto puede deberse a la lenta saturación del solvente, que se encuentra para esta relación en mayor cantidad, alejándose del punto de equilibrio 28. Por otro lado, los cambios en la estructura vegetal que experimenta la cáscara durante el secado favorecen el proceso de extracción. Esto se puede corroborar al comparar el resultado con el obtenido en cáscara secada donde la relación soluto:solvente óptima fue de 1:60 (p:v).
A partir de los resultados obtenidos se realizó el ajuste matemático mediante el Software TIBCO Statistica®13.5.0., obteniendo un polinomio de segundo orden (Ec. 2). En la Tabla 3 se pueden observar los valores para cada constante del polinomio.
Tabla 3 Valor de las constantes del polinomio.
| 𝛽0 | 𝛽1 | 𝛽2 | 𝛽3 | 𝛽4 | 𝛽5 | 𝛽6 | 𝛽7 | 𝛽8 | 𝛽9 | |
|---|---|---|---|---|---|---|---|---|---|---|
| Valor | 19.331 | 0.787 | 0.275 | -910.46 | -6.604*10-3 | -1.904*10-4 | -5.478 | -4.057*10-3 | 4.722 | 11202.4 |
Donde, PT: Polifenoles totales en mgEAG/gMS; T: Temperatura en °C; EA: relación etanol:agua (v:v); SS: relación soluto:solvente (p:v).
En la Figura 3 se muestran las gráficas de superficie de respuesta obtenidas de la Ec. 2. En esta figura se evidencia la influencia de cada una de las variables sobre el contenido de polifenoles totales, en donde se observan máximos en el contenido de polifenoles en los extractos, para una relación soluto:solvente de 1:120 (p:v), relaciones intermedias de etanol:agua y temperaturas superiores a 45 °C.
Condiciones óptimas de extracción para cáscara de cacao húmeda
Las condiciones óptimas de extracción fueron determinadas a partir del modelo matemático ajustado usando el software Statgraphics (Ec. 2). El cálculo se realizó teniendo en cuenta los resultados obtenidos en todas las corridas experimentales; bajo estas consideraciones, las condiciones encontradas fueron: relación etanol:agua(v:v) de 40:60, soluto:solvente(p:v) de 1:120 y temperatura de extracción 55 °C. El contenido de polifenoles recuperado experimentalmente bajo estas condiciones óptimas de extracción fue de 46.43±0.07 mgEAG/gMS. Con las mismas condiciones de extracción, el valor estimado con la Ec. 2 completa fue 38.82 mgEAG/gMS y el obtenido con la Ec. 2 sin las variables que no fueron significativas según el ANOVA (EA, T2, y T*EA) fue 52.06 mgEAG/gMS.
Para la validación del modelo se calculó la desviación relativa absoluta promedio-AARD (Ec. 1). De lo anterior, se encontró que %AARD para la ecuación simplificada fue de 12.13 % y para la ecuación completa fue 16.39 %. Pico et al. 1, para la cáscara de cacao secada mediante extracción con fluido supercrítico, reportaron errores relativos absolutos de hasta un 12.20 % aproximadamente, mostrando así, el buen grado de ajuste que tiene el modelo aquí presentado.
Comparación de los polifenoles extraídos de la cáscara de cacao secada y húmeda
En la Figura 4 se presenta el cromatograma del extracto obtenido con cáscara secada y con cáscara húmeda, a las respectivas condiciones óptimas de extracción. Allí se puede evidenciar que la intensidad de los picos fue mayor para el extracto de cáscara secada, esto debido a la mayor concentración de polifenoles presentes en los extractos obtenidos, favorecido por los cambios que sufre la estructura vegetal durante el proceso de secado. Contreras 29 afirma que el proceso de secado en matrices vegetales provoca cambios físicos y químicos debido al estrés térmico e hídrico que sufre la estructura vegetal, como encogimiento y daño celular, solubilización de pectinas, desnaturalización de proteínas, cambios en los sólidos solubles, entre otros. Estos daños irreversibles, vuelven el material vegetal permeable a los solutos, favoreciendo su extracción.

Figura 4 Cromatograma para los extractos de polifenoles. Donde, Pico 1: Procianidinas B-2, Pico 2: Epicatequinas y Pico 3: Oligómeros.
Los picos representados en la figura 4 están relacionados con epicatequinas (monómeros), procianidinas B2 (dímeros) y otros oligómeros presentes en los extractos. Los análisis mostraron un contenido de (-)-epicatequina de 0.38±0.01 mg/gMS para la cáscara secada, y de 0.28±0.03 mg/gMS para la cáscara húmeda, en coherencia con la intensidad de los picos mostrados en la anterior figura. Estos valores fueron similares a los reportados por Sotelo et al. 30 para cáscara de cacao secada (alrededor de 0.31 mg/gMS, clon TSH - 565). Igualmente, Toro-Uribe et al. 23) destaca la presencia de estos compuestos en extractos de cáscara del mismo clon de cacao.
El contenido de polifenoles totales obtenidos a partir de cáscara secada (valor referencia) fue levemente mayor que el obtenido en cáscara húmeda (18% más, aproximadamente). La capacidad antioxidante determinada para los extractos obtenidos a partir de la cáscara húmeda fue de 909.26±89.32 µmolET/gMS (ensayo ORAC) y 399.09±17.24 µmolET/gMS (ensayo DPPH); valores inferiores en un 10 % con respecto a los realizados en cáscara secada. Por lo tanto, este resultado es favorable teniendo en cuenta que el costo energético del secado a grandes escalas es elevado y la adquisición de este tipo de equipos puede llegar a representar más de la mitad de la inversión inicial 3. Es por esto que, las condiciones óptimas encontradas para la extracción de polifenoles, usando la cáscara de cacao húmeda, son prometedoras si se desea llevar a cabo un escalado del proceso.
Actualmente en el mercado los extractos polifenólicos han tomado gran fuerza en el sector cosmético, como es el caso de productos de belleza enriquecidos con extractos de semilla de uva. Ahora bien, en la literatura se ha encontrado que el contenido de polifenoles en la semilla de uva ronda los 65 mgEAG/gMS 21, valor no muy superior al obtenido para cáscara húmeda (46 mgEAG/gMS), indicando así, la oportunidad que tiene en el mercado los extractos obtenidos a partir de cáscara de cacao.
Ajuste de parámetros cinéticos
En la Tabla 4 se muestran los parámetros y coeficientes de correlación (R2) determinados para cada modelo evaluado. El modelo con el mayor coeficiente de correlación (R2) fue el Peleg modificado (R2=0.9598). Una ventaja sobre los modelos de Peleg y el Logarítmico, los cuales arrojaron coeficientes de correlación cercanos, está en que Peleg modificado arroja información relacionada con la velocidad de extracción; los parámetros cinéticos obtenidos con este modelo fueron similares a los encontrados para cáscara de cacao CCN-51 secada (k2=6*10-3 y k3=2.22*102). En el modelo Peleg modificado la constante k2 está relacionada con el inverso de la velocidad de extracción y su valor es cercano al obtenido para el proceso en seco (6*10-3 min*gMS/mgEAG). En términos de velocidad de extracción, para el proceso en seco fue de 167 mgEAG/gMS*min y para el proceso en húmedo fue de 88 mgEAG/gMS*min, indicando que el proceso de extracción es más rápido en seco que en húmedo. Como se mencionó anteriormente, los cambios en la estructura vegetal del material secado pueden favorecer la extracción de estos compuestos, llegando al equilibrio más rápidamente.
Tabla 4 Parámetros cinéticos para cada modelo matemático evaluado.
| Modelo cinético | Constantes | Parámetros cinéticos cáscara húmeda | Parámetros cinéticos cáscara secada |
|---|---|---|---|
| Peleg | k1 | 3.563 | 1.623 |
| N | 1.429*10-2 | 0.950*10-2 | |
| R2 | 0.9465 | 0.9824 | |
| Peleg modificado | k2 | 1.134*10-2 | 0.6*10-2 |
| k3 | 2.251*10-2 | 2.22*10-2 | |
| R2 | 0.9598 | 0.9900 | |
| Logarítmico | A | 2.227 | 3.479 |
| B | 34.740 | 40.105 | |
| R2 | 0.9562 | 0.9370 | |
| Rakotondramasy | k4 | 0.7653 | 1.1890 |
| R2 | 0.7897 | 0.7916 |
La Figura 5 muestra la cinética de extracción del proceso en seco y en húmedo, ambas simuladas con el modelo Peleg Modificado. En ella se puede observar que el tiempo de extracción no excede los 60 min en ambos casos, tiempo considerado corto en comparación a otras matrices como la soja y semilla de uva (120 y 240 min, respectivamente) 21,31.

Figura 5 Cinética de extracción de polifenoles descrita por el modelo Peleg modificado para cáscara de cacao seca y cáscara de cacao húmeda
Lo mencionado anteriormente es un aspecto positivo desde el punto de vista industrial por los tiempos cortos de operación, reduciendo así, costos energéticos y costos asociados al consumo de reactivos e insumos, debido a las pérdidas por evaporación de solvente (mezcla etanol: agua).
Conclusiones
Se realizó la extracción de polifenoles usando como materia prima la cáscara de cacao del clon CCN-51 tanto en seco como en húmedo, y se pudo observar que a condiciones óptimas de extracción encontradas en húmedo (relación etanol:agua=40:60 v:v; soluto:solvente=1:120 p:v; T=55 °C), el contenido de polifenoles totales extraídos fue cercano al valor obtenido con la matriz secada (85 % de lo extraído en seco). Igualmente, se hizo seguimiento a la cinética de extracción y el ajuste de parámetros cinéticos, donde se pudo observar que el proceso en términos de velocidad de extracción no difiere considerablemente del proceso en seco, mostrando así, la rapidez de la extracción de los polifenoles a partir de cáscara húmeda, a pesar de las posibles diferencias en las características físicas del material. El modelo Peleg modificado sigue describiendo convenientemente la cinética de extracción de polifenoles. Estos resultados son interesantes al momento de considerar el escalamiento de proceso, puesto que a pesar de que la extracción puede verse limitada por la estructura del material en húmedo, el contenido de polifenoles extraídos sigue siendo considerable, permitiendo suponer que no sería necesaria una etapa de secado para el proceso a una mayor escala, disminuyendo los costos asociados con la inversión y funcionamiento.