Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Biotecnología
Print version ISSN 0123-3475
Rev. colomb. biotecnol vol.14 no.2 Bogotá jul./Dec. 2012
ARTÍCULO CORTO
Cuantificación de bacterias cultivables mediante el método de "Goteo en Placa por Sellado (o estampado) Masivo"
Quantification of cultivable bacteria by the "Massive Stamping Drop Plate" method
Andrés Corral-Lugo1 , Yolanda Elizabeth Morales-García1 , Laura Abisaí Pazos-Rojas1 , Araceli Ramírez-Valverde2 , Rebeca Débora Martínez-Contreras1 , Jesús Muñoz-Rojas1.
1 Laboratorio Ecología Molecular Microbiana, Centro de Investigaciones en Ciencias Microbiológicas, Instituto de Ciencias, Benemérita Universidad Autónoma de Puebla, México.
Autor correspondencia: PhD. Jesús Muñoz-Rojas, Edificio 103 J, Ciudad Universitaria, San Manuel, México, C. P. 72570. joymerre@yahoo.com.mx
2 Laboratorio clínico del ISSSTEP, Av. San Baltazar Campeche, Puebla, México.
Recibido: febrero 17 de 2011 Aprobado: noviembre 29 de 2012
Resumen
Cuando se desea cuantificar el número de bacterias presentes en múltiples muestras, los procedimientos de rutina suelen consumir mucho tiempo. En ese periodo las muestras podrían sufrir modificaciones en su población. En el presente trabajo se evaluó una metodología alternativa para cuantificar bacterias cultivables de forma masiva, rápida y económica en la que se implica el sellado, estampado o impresión de diluciones seriadas de muestras de diversa procedencia. El tiempo requerido para preparar 22 muestras para su sellado en placa es de 15 minutos. El método se basó en realizar diluciones seriadas (base 10) de las muestras líquidas originales contenidas en una placa multipozos con la ayuda de una pipeta multicanal. Después, con un replicador se tomó un volumen (aproximadamente 1,65 µl) de muestra de cada pozo, que se inoculó por sellado en un medio de crecimiento gelificado de interés. Las placas se incubaron el tiempo necesario, se contó el número de colonias presentes en la dilución contable y se calculó el número de Unidades Formadoras de Colonia por mililitro (UFC/ml) para cada muestra. La metodología se denominó "Goteo por Sellado en Placa Masivo" (GSPM) y ha sido aplicada para cuantificar exitosamente bacterias provenientes de diferentes muestras de laboratorio, por ejemplo, de cultivos líquidos, muestras clínicas (como exudados y secreciones) y bacterias presentes en la rizósfera de plantas de maíz. Sin embargo, la metodología GSPM podría aplicarse para contabilizar masivamente a bacterias de cualquier otra procedencia.
Palabras clave: UFC, goteo en placa, plaqueo, vaciado en placa, GSPM.
Abstract
In an attempt to quantify the number of bacteria present in a high number of samples, routine procedures are usually very time-consuming. During this period of time, bacterial population could be modified. In this work, an alternative for a massive, quick and economic method was evaluated in order to count viable bacteria, consisting in the sealing or stamping of serial dilutions performed in samples from different origins. The time required to prepare 22 samples for plate stamping is only 15 minutes. The quantification was based in performing serial dilutions (10-fold) of the original liquid samples contained in a multiwell plate using a multichannel micropipette. Afterwards, using a replicator, the same volume of each sample (approximately 1,65 µl) was recovered from each well, and then it was inoculated and sealed in a solid growth media of interest. Plates were incubated as needed, colonies were counted in the quantifiable dilution and Colony Forming Units per milliliter (CFU/ml) was calculated for each sample. We called this method "Massive Stamping Drop Plate" (MSDP) and it has been successfully applied to count bacteria from different lab samples, including liquid cultures, clinical samples (exudates and secretions) and bacteria recovered from the rhizosphere of corn plants. However, MSDP could also be applied to massively count bacteria from any other source.
Key words: CFU, drop plate, plating, spread plate, MSDP.
Introducción
La cuantificación de microorganismos es un elemento crítico en los estudios de ecología microbiana y microbiología clínica. No solo es importante conocer al responsable de un efecto benéfico o identificar al microorganismo potencial de causar alguna infección severa, sino también es importante saber el número de microorganismos implicados, para establecer si éstos serán capaces de desarrollar una función benéfica o perjudicial.
Distintas han sido las estrategias para contabilizar a los microorganismos cultivables en muestras ambientales y de laboratorio; las cuales presentan ventajas y desventajas. El conteo de bacterias podría realizarse mediante el método del Número Más Probable (NPM), éste es útil para contabilizar bacterias que son difíciles de aislar de una muestra, pero que pueden ser detectadas por la actividad de alguna característica metabólica. Por ejemplo el conteo de las especies bacterianas que son capaces de captar nitrógeno atmosférico, bajo condiciones microaerofílicas (Cavalcante y Döbereiner, 1988) se ha realizado mediante el método NPM usando medios semigelificados carentes de nitrógeno; las tablas de Mac Grady son útiles en estos casos.
La metodología de recuento en placa por plaqueo es una metodología ampliamente utilizada (Hoben y Somasegaran, 1982), que consiste en realizar diluciones seriadas 1:10 y extender 100µl de cada dilución en una placa; las placas se incuban hasta que las colonias son apreciables para su recuento. Esta metodología tiene la ventaja de tener un buen límite de detección, sin embargo consume mucho tiempo durante los plaqueos; en el caso de realizar el recuento de bacterias a partir de muestras cuya población se desconoce se requiere realizar el extendido de 7 diluciones y la muestra original (para cada conteo) lo que significa consumir 8 placas de cultivo y alrededor de 25 minutos para los plaqueos, sin tomar en consideración repeticiones. Para disminuir el tiempo de procesamiento de muestra, la metodología ha sufrido modificaciones al paso del tiempo y en la actualidad se usan bolitas de acrílico en lugar de un asa de vidrio para extender las muestras. Otra técnica recuento de bacterias utilizada es la de vaciado en placa, que consiste en colocar 1 ml de muestra de cada una de las diluciones seriadas en las placas, donde se vacía posteriormente el medio de cultivo a punto de gelificar (agar aproximadamente a 45°C); ésta se usa ampliamente para determinar el número de coliformes presentes en muestras de agua y alimentos, sin embargo el método podría ocasionar la muerte selectiva de algunas cepas sensibles a calor (Clarck, 1967), en este método se evita el plaqueo de las diluciones pero el número de placas y medio de cultivo requerido es equivalente. Una de las técnicas cuyo uso se ha intensificado para el recuento bacteriano, es la técnica de goteo en placa (Herigstad et al., 2001; Hoben y Somasegaran, 1982), debido a que ésta es fácil, rápida y económica. El goteo en placa consiste en colocar gotas de 20 µl de cada una de las diluciones seriadas, en placas de medio; después de su crecimiento se cuenta el número de colonias presentes y se realizan los cálculos requeridos. La metodología de goteo en placa requiere de 1 a 2 pacas de cultivo para monitorear todas las diluciones seriadas de cada muestra, lo que facilita elevar el número de repeticiones experimentales y aumentar el tamaño de muestra para comparaciones estadísticas. La eficiencia del método ha resultado muy similar a las técnicas de recuento por plaqueo (Hoben and Somesagarán, 1982).
Cuando se desea cuantificar el número de bacterias presentes en múltiples muestras, los procedimientos de rutina suelen consumir mucho tiempo. En ese periodo las muestras podrían sufrir modificaciones en su población. Una metodología más económica que el recuento por goteo en placa y que puede manejar mayor cantidad de muestras es la metodología de goteo en placa 6X6 (Chen et al., 2003). En este método se realizan diluciones seriadas (base 10) de las muestras líquidas originales contenidas en una placa multipozos con la ayuda de una pipeta multicanal, por lo que se trabajan 6 muestras a la vez. Las diluciones realizadas son dispensadas con la misma pipeta multicanal en una misma placa; razón por la que se ha designado a esta metodología como cuantificación simultánea. La única desventaja es que hay que tener un buen manejo de la pipeta multicanal a la hora de dispensar en el medio de cultivo pues de otra forma el goteo podría mezclarse con diluciones vecinas. La dispensación de cada una de las diluciones implica la toma de puntas con la pipeta multicanal, la absorción de muestra y su colocación en el medio de cultivo.
En el presente trabajo se evaluó la eficiencia de una metodología alternativa para cuantificar bacterias cultivables de forma masiva, rápida y económica en la que se implica el sellado o estampado de diluciones seriadas de muestras de diversa procedencia. En este método se realizaron diluciones seriadas (base 10) de las muestras líquidas originales contenidas en una placa multipozos con la ayuda de una pipeta multicanal, similar al método de goteo en placa 6X6. Después, con un replicador se tomó un volumen (aproximadamente 1,65 µl) de muestra de cada pozo, que se inoculó por sellado en un medio de crecimiento gelificado de interés. Las placas se incubaron el tiempo necesario en acuerdo con el tipo de bacterias en cuestión, se contó el número de colonias presentes en la dilución contable y se calculó el número de UFC/ml para cada muestra. La metodología propuesta se ha denominado "Goteo por Sellado en Placa Masivo" (GSPM) y ha sido aplicada para cuantificar exitosamente bacterias provenientes de diferentes muestras de laboratorio, por ejemplo, de cultivos líquidos, muestras clínicas (como exudados y secreciones) y bacterias presentes en la rizósfera de plantas de maíz. Sin embargo, la metodología GSPM podría aplicarse para contabilizar bacterias de cualquier otra procedencia. El tiempo requerido para preparar 22 muestras para su sellado en placa fue de 15 minutos y resultó menor al tiempo requerido por otras metodologías debido a que solo se colocó un solo sello para dispensar las gotas de las diluciones de las 6 cepas que se cuantificaron en una misma placa. El método permite el ahorro de recursos como puntas que son requeridas por la pipeta multicanal en el método de goteo en placa 6X6 y otros métodos.
Materiales y métodos
En esta sección primero se describe en detalle el método GSPM, después se muestra la reproducibilidad del método GSPM y su comparación frente a otros métodos de conteo de bacterias (experimento 1); usando como modelo el crecimiento hasta fase estacionaria de Pseudomonas putida KT2440 en medio líquido. En un experimento posterior se muestra la eficiencia y rapidez del método para determinar la adhesión a semillas y colonización de rizósfera de maíz de distintas bacterias beneficiosas en un número de replicas elevado (experimento 2). Un último experimento (experimento 3) muestra que la metodología puede servir para cuantificar bacterias de otras muestras; en este caso muestras de exudados faríngeos y secreciones corporales.
Descripción del método de cuantificación de bacterias GSPM
Mediante el método GSPM se cuantificaron bacterias presentes en diversos tipos de muestra en forma de suspensión. Para ello, se colocaron 100µl de suspensión bacteriana de cada una de las muestras exploradas en este trabajo, en la parte superior de una placa multipozos (fila A) (figura 1). Después se depositaron 180µl de agua destilada estéril en el resto de los pozos (fila B-H), con la ayuda de una pipeta multicanal.
Una vez lista la placa, se realizaron las diluciones seriadas en factor 1:10. Este paso se realizó con la ayuda de la pipeta multicanal. Con puntas estériles se tomaron 20 µl de las muestras (fila A) y se transfirieron a la siguiente fila (B), diluyendo y homogenizando las muestras en el agua contenida en los pozos; por medio de una resuspensión que consistió en subir y bajar, durante 8 segundos, la suspensión a través de las puntas de la pipeta. Las muestras de la fila B resultaron en una dilución 1/10. Se cambiaron las puntas de la pipeta multicanal y se toman 20 µl de la dilución 1/10 de la fila B y se transfirieron a la fila C volviendo a diluir y homogenizar la muestra durante 8 segundos. Ahora las muestras de la fila C se encuentran en dilución 1/100. Este procedimiento se continuó realizando hasta diluir la muestra 1/10000000 en la fila H.
Cada una de las diluciones (incluyendo las suspensiones iniciales de las muestras) fue inoculada en los medios de selección o de crecimiento gelificado en acuerdo con el experimento. Para esto se utilizó un replicador estéril, el cual permitió tomar un volumen similar de cada una de las muestras de la placa multipozos y depositarlas en medio (contenido en placas Petri de 90X15 cm) de crecimiento en forma de gota. El volumen de las gotas que tomó cada prolongación del replicador fue de 1,65 µl (SD=0,26), por lo que este valor se usó para los cálculos de UFC/ml. El volumen de gota que tomó el replicador fue previamente medido en experimentos independientes. Una vez que las muestras fueron inoculadas en el medio gelificado respectivo, las placas se incubaron en condiciones óptimas para el crecimiento bacteriano. En este trabajo las bacterias asociadas a plantas crecieron a 30 °C y las bacterias de muestras clínicas a 37 ºC.
Para calcular el número de UFC/ml en cada una de las muestras, se tomó el número de colonias de la dilución contable (ejemplo 4 colonias); asumiendo que una colonia es igual a una UFC/ml, el valor equivale al número de UFC/ml que existe en el volumen de la gota que dejó el replicador. Después mediante una "regla de tres", se determinó el número de colonias que hay en 100 µl y después en 1 ml.
Una vez determinado el número de colonias en 1 ml, el resultado se multiplicó por el factor de dilución en la cual se contaron las colonias y así se obtuvo el número de UFC/ml de la bacteria de interés contenida en la muestra, como se muestra en el siguiente ejemplo: Si las 4 colonias antes mencionadas crecieron en la dilución 6, las UFC en 1 ml (2424,24 UFC), se multiplicaron por 1000000, obteniendo que para esa muestra hay 2,42 X 109 UFC/ml. Para el caso de bacterias adheridas a maíz germinado, adicionalmente se multiplica por el volumen inicial de dilución (3 ml) para obtener el número de UFC/semilla.
Experimento 1. Cuantificación de bacterias a partir de cultivos en fase estacionaria mediante plaqueo, goteo en placa, goteo en placa 6X6 y GSPM
Pseudomonas putida KT2440 fue cultivada en 5 ml de medio LB, crecida toda la noche y a partir de este cultivo se inocularon 30 µl en 50 ml de medio de cultivo LB- con cloranfenicol 50µg/ml (Cm50) (Molina et al., 2000) a una densidad óptica inicial de 0,05. Los cultivos se dejaron crecer durante 24 horas a una densidad óptica máxima (aproximadmente 5,0); la cual corresponde a la fase estacionaria para esta bacteria (Muñoz-Rojas et al., 2006). Una vez en esta fase de crecimiento las muestras fueron cuantificadas mediante plaqueo, goteo en placa, goteo en placa 6X6 y GSPM; en medios LB-Cm80. Para ello, se tomaron 12 muestras de 1 ml para cada método en tubos eppendorf, 12 muestras se cuantificaron de forma independiente mediante plaqueo, 12 mediante goteo en placa y 12 mediante GSPM. Una vez que las muestras fueron procesadas y colocadas en sus medios de cultivo, estas fueron incubadas a 30°C durante 24 horas, el número de colonias fue contado y su respectivo cálculo de bacterias fue realizado. Los resultados de conteo de las 12 replicas fueron registrados y comparados mediante el método estadístico de t-student usando el programa SigmaPlot (Handel Scientific Software). El material y tiempo requerido para el desarrollo de las cuatro metodologías fue registrado. Burkholderia unamae MTl-641 también fue crecida hasta fase estacionaria en medio BAc líquido y su conteo fue realizado mediante los 4 métodos planteados en medio BAc gelificado (Estrada de los Santos et al., 2001).
Para explorar la rapidez de la metodología GSPM se realizaron los siguientes dos experimentos:
Experimento 2. Cuantificación de bacterias asociadas a plantas de maíz
En este ensayo, se empleó el método de GSPM para determinar la efectividad de la colonización de diferentes cepas bacterianas. Para ello se cuantificó el inóculo, la adhesión y finalmente la colonización. Se utilizaron varias cepas para evaluar su capacidad para asociarse a plantas de maíz. Las bacterias exploradas en este ensayo y su medio donde crecen para su selección en placa fueron: P. putida KT2440 en LB-Cm80, Bradyrhizobium sp. en LB-Gm50 (Trujeque-Montiel, 2009), Sphingomonas sp. en LB5%-lindano (Böltner et al., 2008), B. unamae> MTl-641 en BAc, Azospirillum brasilense en Rojo Congo (Rodríguez-Cáseres, 1982) y Gluconacetobacter diazotrophicus UAP 5560 en LGI (Caballero-Mellado et al., 1998). Cada una de las cepas fueron crecidas en 20 ml de medio MESMA (Fuentes-Ramírez et al., 1999) hasta fase estacionaria, las células fueron lavadas por centrifugación y resuspendidas en el mismo volumen de agua destilada estéril y la suspensión de cada cepa se cuantificó por los método GSPM y goteo en placa, usando los medios de selección; los resultados de los dos métodos fueron comparados mediante la prueba t student en cada caso.
La suspensión de cada bacteria se usó para inocular durante 1 h a 25 germinados, por tratamiento, de maíz axénico obtenidos por el método de Morales-García et al. (2010b). En este trabajo se utilizó una variedad de maíz rosa autóctona del estado de Tlaxcala-México. Durante la inoculación, los germinados se mantuvieron sumergidos en la suspensión bacteriana para permitir la adhesión de bacterias (Morales-García et al., 2011). Los germinados inoculados fueron posteriormente colocados en tubos Falcon (50 ml) conteniendo 5 g de vermiculita estéril y se regaron con 25 ml de solución MSJ3 (Morales-García et al., 2010b). Un control con semillas germinadas sumergidas en agua destilada estéril (1 h) fue incluido. A las 12 horas, cinco semillas, germinadas e inoculadas, de cada tratamiento fueron extraídas y colocadas en tubos falcon (15 ml de capacidad) con 3 ml de agua destilada estéril. Se agitaron vigorosamente con ayuda de un vortex durante 40 segundos y la suspensión generada fue usada para realizar diluciones seriadas en factor 1:10 para cuantificar el número de bacterias adheridas mediante el método GSPM. Los germinados sembrados restantes fueron colocados en una cámara de crecimiento de plantas durante 10 días y se regaron a los 5 días con 10 ml de agua destilada estéril. La temperatura de crecimiento de las plantas estuvo en un rango de 20-28°C (noche-día), con un fotoperiodo de luz/obscuridad 16/8 y a 80% de humedad relativa. Para cuantificar el número de bacterias presentes en la rizósfera de las plantas, se extrajeron de los sistemas, dieciséis plantas de cada tratamiento a los 10 días de su crecimiento, las raíces de las plantas fueron sacudidas y colocadas en tubos Falcon conteniendo 20 ml de agua destilada estéril. Se agitó vigorosamente con ayuda de un vortex y la suspensión generada se sometió a cuantificación mediante GSPM. Los medios utilizados para cuantificar las células bacterianas fueron específicos en cada caso como se mencionó previamente.
Experimento 3. Cuantificación de bacterias de muestras clínicas
Se procesaron 22 muestras provenientes del hospital ISSSTEP de Puebla, México. Dichas muestras fueron recolectadas en tubos de ensayos estériles y provenían de pacientes con posible infección. Veinte de las muestras eran exudados faríngeos y dos secreciones corporales. La toma de muestra fue en acuerdo a protocolos establecidos (Norma Oficial Mexicana NOM-007-SSA3-2011, Para la organización y funcionamiento de los laboratorios clínicos) y se colocaron inicialmente en solución salina isotónica que fue resuspendida hasta homogeneidad. Esta suspensión fue utilizada para realizar las diluciones y contabilizar mediante GSPM en medios gelificados Sal y Manitol, Mac Conkey y Agar Sangre.
Resultados
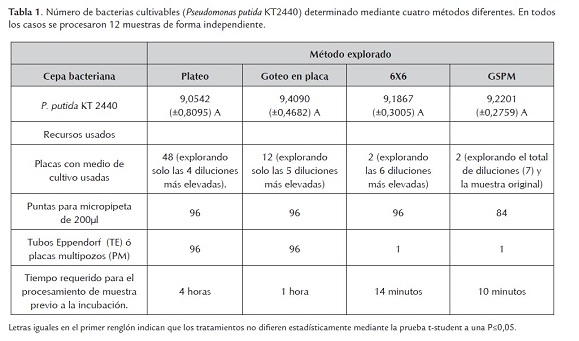
Experimento 1. Los resultados muestran que independientemente del método utilizado (plateo, goteo en placa, goteo en placa 6X6 o GSPM) el número de bacterias obtenido fue estadísticamente igual para el conteo de bacterias de P. putida KT2440 (tabla 1), lo mismo ocurrió para B. unamae> MTl-641 (datos no mostrados). Sin embargo, la desviación estándar observada para el método de plaqueo es mayor a la observada para el método de goteo en placa y a su vez esta es mayor al método de 6X6 y el método GSPM; lo que implica los métodos GSPM y 6X6 son más exactos y reproducibles. En este experimento se comparó el número de placas y tiempo experimental requerido para llevar a cabo las diversas metodologías (tabla 1), observando que la metodología GSPM es mucho mas ahorradora en tiempo y recursos.
Experimento 2. El número de bacterias presentes en la suspensión fue determinado en cinco repeticiones por tratamiento (30 muestras) y se muestra en la tabla 2. El número de bacterias presente en la suspensión bacteriana se observó en el rango de 108 UFC/ml y es comparable estadísticamente al número de bacterias determinado por goteo en placa. El número de bacterias que se adhieren a las semillas germinadas de maíz también fue determinado, en cinco semillas de cada tratamiento (30 muestras) (tabla 2). Todas las bacterias exploradas se adhieren correctamente a maíz en números requeridos para una buena interacción planta-bacteria. En los germinados sin inocular no se detectaron bacterias. La colonización de las bacterias en la rizósfera se evaluó en 16 plantas por tratamiento (96 muestras) y estuvo en el rango de 106 a 107, excepto para P. putida KT2440 que colonizó en el orden de 105 UFC/ml a la variedad de maíz explorada. El tiempo requerido para llevar a cabo el proceso de contabilización de las muestras de la suspensión y la adhesión, mediante GSPM, fue de 40 minutos en ambos casos y el tiempo para realizar el conteo de bacterias presentes en rizósfera (GSPM) fue de 2 horas (tabla 4).
Experimento 3. Mediante el método GSPM fue posible contabilizar las bacterias cultivables presentes en las 22 muestras clínicas en aproximadamente 15 minutos en los 3 medios de cultivo utilizados. Con lo que se determinó la carga bacteriana que tenían dichas muestras (tabla 3). Las bacterias más abundantes fueron posteriormente identificadas por métodos automatizados estandarizados (no mostrado). No hubo crecimiento en medio Sal y Manitol y la abundancia de bacterias cultivables capaces de crecer en el medio Mac Conkey fue mayor a la detectada en Agar Sangre; las morfologías encontradas de las bacterias más abundantes en cada medio fueron distintas.
Discusión
El número y la biomasa de los microorganismos, así como la descripción y monitoreo de las comunidades microbianas, es un requisito básico para entender los procesos microbiológicos en el ambiente (Kepner y Pratt, 1994). La cuantificación de bacterias cultivables es importante para laboratorios clínicos, ambientales e industriales y puede realizarse con métodos directos e indirectos. Los métodos directos comprenden a la microscopía; que en muchas ocasiones se acopla a marcadores para la detección de bacterias por microscopía de fluorescencia o bien mediante citometría de flujo (Bölter et al., 2002; Falcioni et al., 2006). Sin embargo, estos no se encuentran al alcance de laboratorios con poco recurso o poco equipados. Los métodos indirectos incluyen: la medición del peso celular (biomasa) y la turbidimetría; en ocasiones se puede acoplar la expresión de un gen reportero que de un color específico que se detecte en el espectrofotómetro (Dalgaard et al., 1994). Sin embargo algunas metodologías moleculares también han sido utilizadas, como la metodología de reacción de polimerasa en cadena (PCR por sus siglas en inglés) en tiempo real (Couillerot et al., 2012) para la detección de A. brasilense y micorrizas.
Una alternativa para contar bacterias está representado por los métodos de cultivo (Josephson et al., 1999) que incluyen: los métodos de plaqueo, la metodología de vaciado en placa, la metodología NMP y la metodología de goteo en placa (Herigstad et al., 2001). La metodología de plaqueo es utilizada frecuentemente en los laboratorios debido a que permite procesar una gran diversidad de muestras con un resultado confiable. Sin embargo, esta metodología fue superada mediante el uso del método de "goteo en placa" (Hoben and Somasegaran, 1982) y el método de goteo en placa 6X6; que son más rápidos, económicos e igual de confiables que el plaqueo (Herigstad et al., 2001; Chen et al., 2003). En el presente trabajo se planteó una metodología denominada GSPM que es más económica, rápida y eficiente (tabla 1 y 4) en comparación con la metodología de goteo en placa e incluso comparada a la metodología goteo en placa 6X6 (Chen et al., 2003). El número de bacterias obtenido mediante GSPM es muy reproducible, similar al método 6X6 y mayor al método de plaqueo. Debido a que se ahorra tiempo y material, la metodología GSPM permite que una sola persona procese para su sellado, hasta 96 muestras en un tiempo aproximado de 2 horas, lo que podría facilitar las repeticiones de un experimento o bien evitar que las poblaciones bacterianas de las muestras no se modifiquen en el transcurso de su procesamiento. La metodología GSPM permite cuantificar de 6 a 8 muestras en una misma placa de cultivo de 90 X 15 cm, en función de las diluciones realizadas; lo que resulta ser muy económico para un laboratorio y es compatible con el medio ambiente al no usar tanto material.
En este trabajo la metodología GSPM permitió procesar para su estampado y posterior cuantificación a 22 muestras clínicas en tan solo 15 minutos y 96 muestras de rizósfera en 2 horas, lo cual resulta bastante práctico y con un número de repeticiones que son requeridos para realizar análisis estadísticos futuros. La cuantificación de bacterias para 96 muestras requeriría más de 16 h si dicho trabajo se efectuará por una sola persona por metodología de "Plaqueo" y 8 h por la metodología de "Goteo en Placa" (tabla 4). GSPM ahorra puntas para micropipeta en comparación con la metodología goteo en placa 6X6, con la ventaja adicional de poder colocar todas las diluciones exploradas dentro de una misma placa; lo cual no ocurre para el método 6X6. Debido a que GSPM permite trabajar en serie, todas las muestras se procesaron en un tiempo parecido obteniéndose un resultado homogéneo (desviación estándar disminuida en referencia a otros métodos). Algunos microorganismos tienen un tiempo de generación muy bajo por lo que es recomendable procesar a las muestras de una forma rápida. Experimentos de mutagénesis al azar para la búsqueda de mutantes defectivas en el crecimiento después de un estrés extremo (Morales-García et al., 2010a), se han acoplado con la metodología GSPM (dato no mostrado). En este trabajo la metodología GSPM se usó para cuantificar el número de bacterias presentes en muestras clínicas y de la rizósfera de plantas, no obstante esta metodología podría funcionar para cuantificar microorganismos en otro tipo de muestras como aquellas que provienen de ambientes endófitos (Cavalcante y Döbereiner, 1988), de aguas residuales (Falcioni et al., 2006) o de suelos (Munguía-Pérez et al., 2011).
Los resultados de adhesión y colonización en rizósfera de maíz de P. putida KT2440, A. brasilense Sp7, Sphingomonas sp. y G. diazotrophicus están en acuerdo con lo reportado anteriormente (Molina et al. 2000; Fallik et al., 1988; Böltner et al., 2008; Caballero-Mellado et al., 1998), lo que corrobora que el método GSPM tiene una detección similar a otros métodos usados para la cuantificación de bacterias de este ambiente. Además, la cuantificación de bacterias de las muestras se pueden explorar rápidamente en diferentes medios, debido a la ventaja de usar el replicador como sello, como se mostró para las muestras clínicas de este trabajo, lo que podría incrementar el rango de cepas aisladas del ambiente que se esté explorando, aumentando la posibilidad de aislar nuevas especies o aquellas designadas como "no cultivables" hasta la fecha (Baker et al., 2003).
Conclusiones
GSPM es una metodología para cuantificar bacterias cultivables de forma masiva, tanto para muestras ambientales como de fluidos humanos, no requiere equipo costoso y es una metodología rápida, reproducible y económica. El método GSPM es 1.4 veces más rápido para el procesamiento de muestras que el método de cuantificación de goteo en placa 6X6, 6 veces más rápido que el método de goteo en placa y más de 10 veces superior en comparación con el método de plaqueo. Además GSPM presenta un ahorro de placas con medio de cultivo de 24 veces en comparación al plaqueo y 6 veces en comparación al goteo en placa. El ahorro de material hace que GSPM contribuya con una menor contaminación para el planeta en referencia a las otras metodologías. La rapidez de la metodología GSPM puede incrementarse dependiendo del tipo y número de replicadores usados, así como del tipo de pipeta multicanal utilizada. GSPM podría acoplarse a sistemas de detección automatizados, junto con metodologías moleculares como la PCR y otras como el método NMP.
Agradecimientos
El presente trabajo fue realizado con financiamiento VIEP-BUAP 2012 y CONACYT (000000000156576). Andrés Corral-Lugo y Abisaí Pazos-Rojas fueron becarios CONACYT y Yolanda Elizabeth Morales-García fue becaria VIEP-BUAP y PROMEP (BUAP-PTC-116), por lo que agradecemos el apoyo de dichas instituciones.
Referencias bibliográficas
1 Baker G. C., Smith J. J., Cowan D. A. 2003. Review and re-analysis of domain-specific 16S primers. Journal of Microbiological Methods 55 (3): 541-555. [ Links ]
2 Bölter M., Bloem J., Meiners K., Möller R. 2002. Enumeration and biovolume determination of microbial cells - a methodological review and recommendations for applications in ecological research. Biology and Fertility Soils. 36 (4): 249-25. [ Links ]
3 Böltner D., Godoy P., Muñoz-Rojas J., Duque E., Moreno-Morillas S., Sánchez L., Ramos J. L. 2008. Rhizoremediation of lindane by root-colonizing Sphingomonas. Microbial Biotechnology. 1 (1): 87-93. [ Links ]
4 Caballero-Mellado J., Martínez-Romero E., Estrada de los Santos P., Fuentes-Ramírez L. E. 1998. Maize colonization by Acetobacter diazotrophicus. Kluwer Academic Publishers, Paris: Biological Nitrogen Fixation for the 21st Century. Elmerich C., Kondorosi A., Newton W. E. (Eds). p. 381-382. [ Links ]
5 Cavalcante V. A., Döbereiner J. 1988. A new acid-tolerant nitrogen fixing bacterium associated with sugarcane. Plant and Soil. 108 (1): 23-31. [ Links ]
6 Chen C.-Y., Nace G. W., Irwin P. L. 2003. A 6X6 drop plate method for simultaneous colony counting and MPN enumeration of Campylobacter jejuni, Listeria monocytogenes, and Escherichia coli. Journal of Microbiological Methods. 55 (2): 475-479. [ Links ]
7 Clark D. S. 1967. Comparison of pour and surface plate methods for determination of bacterial counts. Canadian Journal of Microbiology. 13 (11): 1409-1412. [ Links ]
8 Couillerot O., Ramírez-Trujillo A., Walker V., von Felten A., Jansa J., Maurhofer M., Défago G., Prigent-Combaret C., Comte G., Caballero-Mellado G., Moenne-Loccoz Y. 2012. Comparison of prominent Azospirillum strains in Azospirillum-Pseudomonas-Glomus consortia for promotion of maize growth. Applied Microbiology and Biotechnology. DOI: 10.1007/s00253-012-4249-z. [ Links ]
9 Dalgaard P., Ross T., Kamperman L., Neumeyer K., McMeekin T. A. 1994. Estimation of bacterial growth rates from turbidimetric and viable count data. International Journal of Food Microbiology. 23 (3-4): 391-404. [ Links ]
10 Estrada de los Santos P., Bustillos-Cristales R., Caballero-Mellado J. 2001. Burkholderia, a genus rich in plant-associated nitrogen fixers with wide environmental and geographic distribution. Applied and Environmental Microbiology. 67 (6): 2790-2798. [ Links ]
11 Falcioni T., Manti A., Boi P., Canonico B., Balsamo M., Papa S. 2006. Comparison of disruption of activated sludge floc bacteria by flow cytometry. Cytometry Part B: Clinical Cytometry. 70B (3): 149-153. [ Links ]
12 Fallik E., Okon Y., Fischer M. 1988. Growth response of maize roots to Azospirillum inoculation: effect of soil organic matter content, number of rhizosphere bacteria and timing of inoculation. Soil Biology and Biochemistry. 20 (1): 45-49. [ Links ]
13 Fuentes-Ramírez L. E., Caballero-Mellado J., Sepúlveda J., Martínez-Romero E. 1999. Colonization of sugarcane by Acetobacter diazotrophicus is inhibited by high N-fertilization. FEMS Microbiology Ecology. 29 (2): 117-128. [ Links ]
14 Herigstad B., Hamilton M., Heersink J. 2001. How optimize the drop plate method for enumerating bacteria. Journal of Microbiological Methods. 44 (2): 121-129. [ Links ]
15 Hoben H. J., Somasegaran P. 1982. Comparison of the pour, spread, and drop plate methods for enumeration of Rhizobium spp. In inoculants made from presterilized peatt. Applied and Environmental Microbiology. 44 (5): 1246-1247. [ Links ]
16 Josephson K. L., Gerba C. P., Pepper I. L. 1999. Cultural methods: Environmental Microbiology, Maier R. M., Pepper I. L. and Gerba C. P. (eds.). Academic Press, San Diego, California USA. p. 213-233. [ Links ]
17 Kepner R. L., Pratt J. R. 1994. Use of fluorochromes for direct enumeration of total bacteria in environmental samples. Past and present. Microbiology and Molecular Biology Reviews. 58 (4):603-615. [ Links ]
18 Molina L., Ramos C., Duque E., Ronchel M. C., García J. M., Wyke L., Ramos J. L. 2000. Survival of Pseudomonas putida KT2440 in soil and in the rhizosphere of plants under greenhouse and environmental conditions. Soil Biology and Biochemistry. 32 (3): 315-321. [ Links ]
19 Morales-García Y. E., Duque E., Rodríguez-Andrade O., de la Torre J., Martínez-Contreras R. D., Pérez-y-Terrón R., Muñoz-Rojas J. 2010a. Bacterias preservadas, una fuente importante de recursos biotecnológicos. BioTecnología. 14 (2): 11-29. [ Links ]
20 Morales-García Y. E., Juárez-Hernández D., Aragón-Hernández C., Mascarua-Esparza M. A., Bustillos-Cristales M. R., Fuentes-Ramírez L. E., Martínez-Contreras R. D. Muñoz-Rojas J. 2011. Growth response of maize plantlets inoculated with Enterobacter spp., as a model for alternative agriculture. Revista Argentina de Microbiología. 43 (1): 287-293. [ Links ]
21 Morales-García Y. E., Pazos-Rojas L. A., Bustillos-Cristales M. R., Krell T., Muñoz-Rojas J. 2010b. Método rápido para la obtención de maíz axénico a partir de semillas. Elementos. 80 (17): 35-38. [ Links ]
22 Munguía-Pérez R., Díaz-Cabrera E., Martínez-Montiel N., Muñoz-Rojas J., Martínez-Contreras R. 2011. Fungal diversity in soil samples from a Mexican region with endemic dermatomycoses. Micologia Aplicada International. 23 (1): 11-19. [ Links ]
23 Muñoz-Rojas J., Bernal P., Duque E., Godoy P., Segura A., Ramos J. L. 2006. Involvement of cyclopropane fatty acids in the response of Pseudomonas putida KT2440 to freeze-drying. Applied and Environmental Microbiology. 72 (1): 472-477. [ Links ]
24 Rodríguez-Cáseres, E. A. 1982. Improved medium for aisolation of Azospirillum spp. Applied and Environmental Microbiology. 44 (4): 990-991. [ Links ]
25 Trujeque-Montiel C. V. 2009. Diversidad de bacterias fijadoras de nitrógeno, simbiontes de ambientes forestales de leguminosas, de la sierra norte del estado de Puebla. Puebla, México: Benemérita Universidad Autónoma de Puebla. p. 49. [ Links ]