1. Introducción
Polímeros electrolíticos basados en una matriz polimérica han sido ampliamente estudiados debido a su importancia en el desarrollo de celdas de combustible (Steele y Heinzel, 2001). Dentro de los polímeros que han llamado la atención para desarrollar membranas poliméricas que reúnan buenas propiedades eléctricas, térmicas, estructurales y mecánicas son el polivinil alcohol (PVA) el cual es biodegradable, biocompatible, con buena estabilidad térmica y bajo costo de manufactura (Yuan et al., 2011), el cual al ser dopado por ejemplo con H3PO2 muestra conductividades iónicas consideradas altas para los electrolíticos poliméricos (Vargas et al., 1998; González y Vargas, 2011). El quitosano (CS) derivado de la quitina también presenta biocompatibilidad, biodegravilidad y toxicidad nula (Ma et al., 2014). Estudios realizados por la combinación de estos dos polímeros PVA/CS han demostrado que a distintas concentraciones estos muestran cambios en sus propiedades eléctricas y térmicas (Mena, 2014).
Por otro lado, también se han sintetizado compositas a base de membranas poliméricas y micro o nanopartículas (TiO2, Al2O3, ZrO2, SiO2) con el propósito de controlar sus propiedades físicas y químicas, encontrándose en algunos casos que la dispersión de estas micro o nanopartículas mejoran la conductividad protónica y las propiedades mecánicas para algunas concentraciones del dispersor (Wang et al., 2008; Ahn et al., 2003; Casciola et al., 2005). En este trabajo se prepararon membranas en una combinación PVA/CS 80:20 + 40%H3PO2 + xNb2O5 con concentraciones de x = 0.02 hasta x = 0.10 donde para la caracterización de las muestras se utilizaron las técnicas de calorimetría diferencial de barrido (DSC), termogravimetría (TGA).
2. Métodos experimentales
Se prepararon las muestras a base de poli vinil alcohol (PVA) 98-99% hidrolizado con peso molecular Mw31000-5000 de la compañía SIGMA-ALDRICH, quitosano (CS) clasificación mediano, ácido hipofosforoso (H3PO2) y micro partículas nanoporosas de óxido niobio (Nb2O5). Se preparó una solución a base de ácido acético a 2% en volumen, luego se definieron las cantidades necesarias para preparar las soluciones al 7.5% en peso de PVA, 2% en peso de CS teniendo en cuenta la solución de ácido acético como solvente y la mezcla de CS y PVA como soluto, se le adicionó un porcentaje de ácido hipofosforoso 0.4H3PO2 el cual mostró una mejor conductividad y concentraciones de óxido de niobio Nb2O5 de 2% al 10%. Las concentraciones de los solutos fueron de acuerdo con la ecuación (20%CS + 80%PVA) + 0.4H3PO2 + 10%Nb2O5.
La caracterización térmica se realizó usando un calorímetro diferencial de barrido DSC de TA Instrument modelo Q100 a una tasa de calentamiento de 10 °C/min bajo una atmosfera controlada de Ni en un rango de temperatura de -75 °C a 350 °C. Las medidas de termogravimetría se llevaron a cabo en una microbalanza de TA Instrument modelo TGA 2050 a una velocidad de calentamiento de 10 °C/min, con flujo de Ni controlado desde temperatura ambiente hasta 480 °C.
3. Resultados y discusión
Las curvas de cambios térmicos, debidos bien sea a transiciones de fases o reacciones de descomposición, obtenidas a partir del análisis térmico de las membranas y de los polímeros precursores PVA, CS, ácido hipofosfórico y el cerámico Nb2O5, mediante la técnica de calorimetría diferencial de barrido se observan en la Figura 1a.
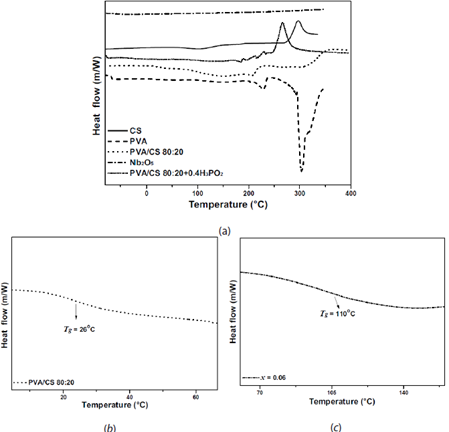
Figura 1 a) Diagramas DSC para el PVA (línea a trazo), CS (línea sólida), PVA/CS 80-20 (línea punteada), Nb2O5 (línea a trazo-punteada) y PVA/CS 80:20 + 0.4H3PO2 (línea punteada acortada). Temperaturas vítreas (Tg) de los sistemas b) PVA/CS 80-20 y c) PVA/CS 80:20 + 0.4H3PO2 + xNb2O5 con x = 0.06 (línea a trazo punteada acortada)
Para el CS (línea sólida) se observa un pico alrededor de los 115 °C con una temperatura de arranque de 75 °C y una entalpia de 30.2 J/g atribuible al proceso de deshidratación de la membrana, similar al PVA. Al final del barrido se observa un proceso exotérmico alrededor de 307 °C con una temperatura de arranque de 290 °C y una entalpia de -144.8 J/g atribuible al rompimiento espontáneo de las cadenas poliméricas. Para el Nb2O5 (línea a trazo-punteada) no se observan eventos térmicos indicando la presencia de una sola fase en todo el rango de barrido de temperatura.
Para el PVA (línea a trazo), se presenta una pequeña caída en la línea de base alrededor de los 115 °C debido al proceso de deshidratación de la muestra o evaporación del agua absorbida en la superficie de la membrana o atrapadas dentro de las cadenas de la matriz del polímero. Seguidamente, alrededor de 218 °C, se observa un segundo pico endotérmico cuyo punto de arranque es 204 °C con una entalpia de 46.2 J/g y atribuido al punto de fusión del polímero. Al final del barrido se observa un tercer pico endotérmico a los 292 °C cuyo punto de arranque es 285 °C con una entalpia de 522.2 J/g y atribuido a la descomposición del polímero.
Para la combinación de PVA/CS 80:20 (línea punteada), la temperatura vítrea (T g ) se observa alrededor de 26 °C (ver Figura 1b), luego se observa una caída en la línea de base hasta los 195 °C debido a la deshidratación de la muestra, seguido de un pico endotérmico alrededor de 207 °C antes del punto de fusión del PVA que ocurre alrededor 218 °C con una temperatura de arranque a los 197 °C y una entalpia de 2.1 J/g. Al final del barrido y por arriba de los 300 °C se observa el inicio del proceso de descomposición de esta combinación polimérica. Nótese que no aparece el pico endotérmico de la descomposición del PVA en la descomposición de este que ocurrió a 292 °C. Este resultado nos permite colegir que los polímeros PVA/CS al combinarse se forma una nueva estructura polimérica.
Para PVA/CS 80:20 + 0.4H3PO2 (línea punteada-acortada), la T g se observa alrededor de 95 °C, luego se observa una caída en la línea de base hasta los 190 °C debido a la deshidratación de la muestra, seguido de un pico exotérmico en 267 °C con una temperatura de arranque en 253 °C y una entalpia de -156.1 J/g relacionado con el rompimiento de las cadenas del polímero y la descomposición de la membrana.
Los termogramas de la Figura 2 corresponden a las membranas de PVA/CS 80:20 + 0.4 H3P02 + xNb2O5 con x = 0.02 hasta x = 0.1. Para todas las concentraciones se observa la T g alrededor de los 110 °C la cual está por arriba que la de los precursores, ver por ejemplo para x = 0.06 en la Figura 1c. Luego se observa un pico alrededor de los 180 °C debido a una anomalía endotérmica con una temperatura de arranque 171 °C y una entalpia de 19.3 J/g el cual corresponde al punto de fusión. Finalmente se observa otro pico exotérmico alrededor de 256 °C con temperatura de arranque de 245 °C y una entalpia de -187.2 J/g debido al rompimiento de las cadenas del polímero y a su descomposición, similar a lo observado para el quitosano.

Figura 2 Diagramas DSC para PVA/CS 80:20 + 0.4H3P02 + xNb2O5 con concentraciones x = 0.02 (línea a trazo), 0.04 (línea punteada), 0.06 (línea a trazo punteada acortada), 0.08 (línea a trazo doble punteada) y 0.10 (línea continua).
Al comparar las curvas DSC de las membranas con composición PVA/CS 80:20 + 0.4H3P02 + xNb2O5 con x = 0.02 hasta x = 0.10 y las de los precursores (Figura 1) se observa que el pico endotérmico de descomposición de PVA ocurre alrededor de 292 °C y no se presentan en ninguna de las combinaciones. Por otro lado, el pico de fusión de la parte cristalina del PVA que ocurre alrededor de 218 °C, si ocurre en todas las combinaciones, pero con una entalpia de transición mucho menor y temperaturas más bajas (alrededor de 180 °C). Sin embargo, el pico exotérmico del CS que ocurre alrededor 307 °C, aparece en las combinaciones alrededor de 250 °C con ligeras variaciones en la entalpia y en la temperatura que dependen de la concentración del óxido de niobio, indicando que hay coordinación entre los polímeros y el Nb2O5. También se puede evidenciar que al agregar el Nb2O5 el punto de fusión cambia comparado con los precursores y en la membrana dopada con ácido hipofosforoso se observa una disminución de este, por ejemplo para PVA/CS80:20 es de 218 °C y para PVA/CS80:20 + 0.4H3PO2 es de 215 °C mientras que para las dopadas con óxido de niobio el punto de fusión de estas disminuye en un rango entre los 171 °C y 183 °C dando lugar a picos endotérmico los cuales disminuyen al agregar el Nb2O5 a los precursores.
La Figura 3 muestra los resultados de TGA para todas las muestras. Para el PVA (línea a trazo) se observa una primera pérdida de peso desde 30 °C hasta 229 °C del orden de 6.7% atribuible al proceso de deshidratación de la muestra, inicialmente la evaporación del agua absorbida en la superficie de la membrana y luego al agua atrapada dentro de las cadenas de la matriz del polímero. Finalmente, una pérdida abrupta de peso alrededor de 229 °C a 285 °C del orden de 64.3% debido a la descomposición de la muestra. Para el CS (línea sólida) se observa una pérdida inicial del peso de 14.4% desde 30 °C hasta aproximadamente 100 °C, atribuible a la evaporación del agua superficial, para permanecer su peso constante hasta aproximadamente 255 °C, donde experimenta una pérdida rápida de peso hasta el 38.2% de su peso inicial a los 332 °C. Para el Nb2O5 (línea a trazo punteada), se observa que su peso permanece constante en todo el rango de temperatura, desde 0 °C hasta 350 °C.

Figura 3 Curvas de termogravimetría (peso porcentual contra temperatura) para: PVA (línea a trazo), CS (línea sólida), CS/PVA 80-20 (línea punteada), N2bO5 (línea a trazopunteada), PVA/CS 80:20 + 0.4H3PO2 (línea punteada acortada) y PVA/CS 80:20 + 0.40H3P02 con concentraciones desde x = 0.02 (línea punteada 1), 0.04 (línea punteada 2), 0.06 (línea punteada 3), 0.08 (línea punteada 4) y 0.10 (línea punteada 5).
Para el PVA/CS 80:20 (línea punteada), se observa un comportamiento diferente a la de sus precursores, indicando un polímero diferente (copolímero) con una salida de agua permanente al aumentar la temperatura hasta aproximadamente 136 °C, donde ha perdido un peso total de 5.7%. Luego se observa otra pérdida más rápida de masa de alrededor de 8.6% desde 136 °C hasta los 254 °C, hasta lograr una pérdida total de masa de 23.0% a los 334.6 °C, que podría deberse a su descomposición.
Para las otras curvas de TGA correspondientes a PVA/CS 80:20 + 40%H3PO2 (línea punteada acortada) y PVA/CS 80:20 + 40%H3PO2 + x%Nb2O5 con concentraciones de x = 0.02 (línea punteada 1), 0.04 (línea punteada 2), 0.06 (línea punteada 3), 0.08 (línea punteada 4) y 0.10 (línea punteada 5), la complejidad de la pérdida de masa es similar. Asa, tenemos una pérdida de peso desde 25 °C hasta alrededor de 170 °C del orden de 14% debido al proceso de deshidratación de la membrana, luego se observa otra caída abrupta de peso desde 170 °C hasta alrededor de 270 °C del orden de 26%, seguida de una caída lenta de peso de los 270 °C hasta los 400 °C y finalmente por arriba de 400 °C otra caída abrupta que corresponde a un peso del orden del 30%.
Relacionando los resultados de TGA con los de DSC, observamos correlaciones entre los picos asociados a la descomposición de las diferentes muestras. Para el PVA la descomposición ocurre alrededor de 280 °C lo cual concuerda aproximadamente con el pico de DSC que ocurre alrededor 290 °C. Para el CS se observa una pérdida de masa fuerte alrededor de 300 °C, lo cual coincide con el pico exotérmico del DSC alrededor de esta misma temperatura. Sin embargo, para la combinación de PVA con CS, no aparece la fuerte pérdida de masa del PVA, que concuerda con la ausencia del correspondiente pico endotérmico del PVA en la curva de DSC. Al agregarle el ácido a la combinación de PVA/CS, resulta más compleja la curva de pérdida de masa lo que atribuimos a diferentes etapas de descomposición del polímero (pirolisis). Esta tendencia continúa en las muestras en las que se han dispersado las micropartículas nanoporosas de Nb2O5, con ligeras variaciones en la rapidez con la que se pierde masa. Sin embargo, es de notarse que el ácido y el Nb2O5 permiten mayores temperaturas de estabilidad de las muestras (valores más altos en la descomposición final de las muestras) comparado con el PVA o el CS.
4. Conclusiones
Al comparar las curvas DSC de las membranas con composición PVA/CS80:20 + 40%H3P02 + xNb2O5 concentraciones x = 0.02 hasta x = 0.10 con las de los precursores (Figuras 1 y 2) se observa que el pico endotérmico de descomposición de PVA que ocurre alrededor de 292.7 °C no se presentan en ninguna de las combinaciones. Por otro lado, el pico de fusión de la parte cristalina del PVA que ocurre alrededor de 218 °C, si ocurre en todas las combinaciones, pero con una entalpia de transición mucho menor y temperaturas más bajas (alrededor de 185 °C). Sin embargo, el pico exotérmico del CS que ocurre alrededor 307 °C, aparece en las combinaciones alrededor de 250 °C con ligeras variaciones en la entalpia y en la temperatura que dependen de la concentración del óxido de niobio, indicando la coordinación química del PVA con el CS para formar un copolimero y entre éstos con el ácido proveedor de protones conductores y las micropartículas nanoporosas de Nb2O5 dispersadas.
Relacionando los resultados de TGA con los de DSC, observamos correlaciones entre los picos asociados a la descomposición de las diferentes muestras. Para el PVA la descomposición ocurre alrededor de 280 °C lo cual concuerda aproximadamente con el pico de DSC que ocurre alrededor 290 °C. Para el CS se observa una pérdida de masa fuerte alrededor de 300 °C, lo cual coincide con el pico exotérmico del DSC alrededor de esta misma temperatura. Sin embargo, para la combinación de PVA con CS, no aparece la fuerte pérdida de masa del PVA, que concuerda con la ausencia del correspondiente pico endotérmico del PVA en la curva de DSC. Al agregarle el ácido a la combinación de PVA: CS, resulta más compleja la curva de pérdida de masa lo que se atribuye a diferentes etapas de descomposición del polimero (pirolisis). Esta tendencia continúa en las muestras en las que se han dispersado las micropartículas nanoporosas de Nb2O5, con ligeras variaciones en la rapidez con la que se pierde masa. Es de notarse que el ácido y el Nb2O5 permiten mayores temperaturas de estabilidad de las muestras (valores más altos en la descomposición final de las muestras) comparado con el PVA o el CS.














