Introducción
El hueso es un tejido especializado compuesto por células (osteocitos) y componentes extracelulares calcificados, con capacidad para regenerarse tras un trauma o por una injuria controlada. En cualquiera de estos dos casos es común el uso de injertos óseos para la regeneración y formación de hueso nuevo, que llega a ser similar al prexistente 1. Dentro de las alternativas terapéuticas en ciru gía oral y maxilofacial en pacientes afectados por lesiones incapacitantes como lo son los procesos infecciosos, osteonecrosis, fracturas patológicas, malformaciones congénitas, secuelas oncológicas, trauma facial, dentoalveolar y reabsorción ósea, se encuentra la utilización de constructos artificiales capaces de inducir la formación de tejido óseo con las mismas características macro y micro morfoló gicas de cada individuo 2,3,4.
Teniendo como referente clínico que cada defecto óseo tiene un abordaje diferente para cada pacien te, es pertinente conocer los materiales de relleno desde el punto de análisis morfológico (forma y ta maño de las partículas), topográfico (características de superficie) y composición porcentual (análisis de compuestos), elementos primordiales para ser considerados como injertos óseos con fines tera péuticos5,6.
Los injertos óseos cumplen una doble función me cánica y biológica. Inicialmente se debe determinar Gallón et al. Caracterización morfológica y Evaluación clínica de sustitutos óseos de origen porcino de la casa 3Biomat para su aplicación en lesiones óseas bimaxilares cuál es la función del injerto a utilizar para ejecutar una correcta cirugía ósea regenerativa que pretende regenerar el hueso alveolar perdido por diferentes tipos de secuelas traumáticas. Las interacciones que se presentan entre el injerto óseo y el huésped son de alta complejidad empezando con la adecua da incorporación del injerto y la vascularización de la zona de implantación e inmunogenética en tre donante y huésped, pasando por las técnicas y conservación, uso de medicamentos, los factores locales y sistémicos y las enfermedades crónicas de generativas y terminando en las propiedades me cánicas que dependen de la morfología, topografía y composición del tipo de injerto utilizado, bajo estos principios se han desarrollado diferentes téc nicas encaminadas a rellenar los defectos óseos con materiales que induzcan: osteogénesis, osteoinducción y osteoconductividad 7,8,9.
Los injertos óseos se clasifican según la naturaleza del material y a la afinidad entre el ser donante y el ser receptor, de la siguiente manera: autoinjerto (del mismo individuo), aloinjerto (diferente indivi duo pero misma especie) y xenoinjerto (de especies diferentes). Idealmente un injerto óseo debe tener estas propiedades, además de ser biocompatible y proporcionar estabilidad biomecánica.
El proceso de incorporación de un injerto óseo es un mecanismo complejo que varía dependiendo del sitio de colocación y el tipo de injerto utilizado; está delimitado por:
1. Fase temprana (1 a 3 semanas): osificación membranosa en la zona adyacente a la cortical ósea y conversión del hematoma postoperatorio en estroma fibroblástico alrededor del injerto.
2. Fase intermedia (4 a 5 semanas): incorpora ción y remodelación del injerto con una zona central cartilaginosa y osificación endocondral alrededor de la misma.
3. Fase tardía (6 a 10 semanas): mayor cantidad de médula ósea en la formación de hueso corti cal alrededor de la zona central y remodelación ósea 9.
Materiales y Métodos
Caracterización morfológica productos BiottMc Cx y Biomod
Para la caracterización morfológica se tomaron sustitutos óseos de origen porcino de la casa 3Biomat, para un total de 12 muestras distribuidas en 6 de matriz ósea desmineralizada y liofilizada Biomod, con un tamaño de partícula de 300-600|im, Referencia BMD03061, y 6 Membranas de colágeno multilaminar Biomsc Cx con una dimensión de 15x22mm barrera media referencia BCX015022BM.
Se realizó un primer análisis de la muestra por medio de estereomicroscopía (HM-LUX 3) con diferentes tipos de aumentos (4x, 10x, 40x) y fil tros (azul, verde y rojo para longitud de 450nm, 550nm, 700nm). El análisis morfológico se realizó bajo histología básica, las muestras se fijaron en for mol al 10%. Posteriormente, las muestras se embe bieron en parafina, se seccionaron a un espesor de 5mm para su posterior coloración con Hematoxilina-Eosina y tricrómico de Masson, se evaluaron bajo microscopia óptica con diferentes aumentos (4x, 40x, 100x, 400x) Nikon 80-I.
El campo óptico de análisis de cada sección in cluyo partículas completas de hueso y segmentos iniciales y finales de membranas de colágeno en un área de 1mm para 25x, 40x, 1000x y 5000x. Las imágenes fueron digitalizadas y trazadas utili zando el sistema Motic Imagen Plis 2.0 software. Para crear regiones de interés individual.
El análisis estructural se determinó por medio de microscopía de barrido electrónico con aumentos de (400x, 1000x y 5000x) JOEL, modelo JSM 6490-LV, para lo cual las muestras fueron some tidas a técnicas de alto vacío y posterior metali zación con partículas de oro, las imágenes captu radas se analizaron por el sistema Motic Imagen Plis 2.0.
Los análisis químicos de las muestras (composición porcentual) se llevaron a cabo por medio de microanálisis cualitativo y cuantitativo EDS (Detector de Espectroscopía de Disipación de Energía)
La microscopía de barrido electrónico SEM es una técnica de obtención de imágenes con alta resolu ción y capacidad de analizar características morfo lógicas, estructurales y químicas de diferentes tipos de muestras.
Evaluación Clínica
Se realizaron documentos de consentimiento infor mado para exodoncia dental, sustitutos óseos de ori gen porcino de la casa 3Biomat, implantes dentales, rehabilitación oral y manejo de material biológico (biopsias).
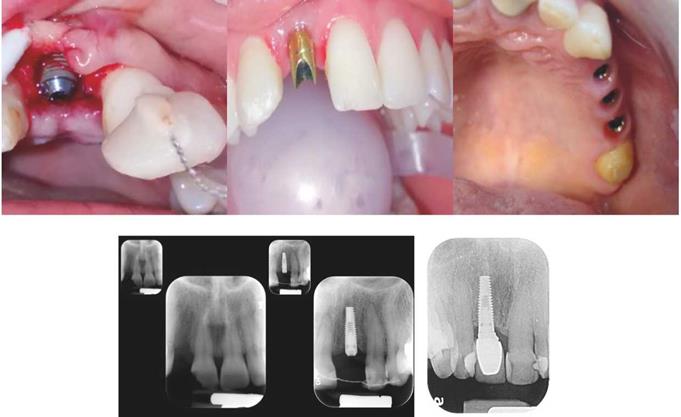
La actividad clínica se llevó a cabo por medio de un estudio de tipo comparativo y prospectivo con una muestra intencional de 31 pacientes con un to tal de 83 implantes, con previo requisito de injerto óseo de fémur porcino. Se tuvo en cuenta para las Exodoncia previa dosis antibiótica de 2 gramos de amoxicilina un día antes y durante 4 días más para conseguir dosis plasmáticas adecuadas en el coágulo primario. Previa asepsia y antisepsia del campo ope ratorio, se realizaron procedimientos quirúrgicos ta les como implante pos-exodoncia más injerto óseo, implante dental y en el mismo tiempo quirúrgi co, injerto óseo; y por último, injerto óseo con un tiempo de 4 meses de integración para la coloca ción de implantes dentales. Se hidrata el sustituto óseo con solución salina fisiológica, compactando el material en medianos incrementos dejando fluir el coágulo medular. No se sobre-corrige el defecto para permitir confrontar los tejidos a los cuales se posicionan membranas de colágeno de capa media, con el objetivo de confrontar los tejidos con menos fuerza tensil de las suturas y obtener un mejor selle primario.
Se tomaron biopsias de tejido óseo en la región operatoria por medio de una fresa trefina de 2,3 mm. La muestra biológica se preservó en formol al 10% para su posterior fijación en parafina; los cor tes histológicos fueron teñidos con tinción de hematoxilina-eosina, tinción tricrómica de Masson. Las muestras para microscopía de barrido electrónico fueron metalizadas en oro en alto vacío y analizadas en 400x, 1000x, 5000x para su posterior análisis de EDS (mapping). El detector de espectroscopía por dispersión de energía (EDS) permite además la rea lización de microanálisis cualitativos y cuantitativos.
La interpretación de los datos fue realizada por medio del programa de digitalización de imágenes Ba210 Motic images Plis 2,0 software. Área de análi sis 1mm para 25x, lecturas realizadas 25x, 40x,100x, 1000x, 5000x.
Se realizaron controles clínicos y radiográficos ini ciales a los 2 y 4 meses. Se evaluó al primer y segun do mes la integridad del injerto. Posteriormente, en los controles clínicos se tiene en cuenta, como crite rio mayor, el no presentar dehiscencias ni signos de infección pos-quirúrgica.
El método de evaluación se realizó con radiografías periapicales con películas de fósforo marca Soderex Imagin Plates, con técnica de paralelismo por me dio de aditamentos de la casa Dentsplay. La dosis estimada por placa fue de 7,4μSv donde se evaluó el comportamiento posicional de la cresta ósea marginal mesial y distal teniendo como referencia la plataforma del implante. Las mediciones fue ron tomadas con un calibrador Vernier digital serie 799 con una capacidad de 0-150mm y una reso lución de 0.01mm; se realizaron calibraciones cada 10 mediciones. Los datos se confinan en tablas que relacionan longitud del implante, altura de la cresta mesial y distal, tipo de maxilar y datos demográficos de sexo y edad. Se relacionan con criterios de éxito, supervivencia, mal pronóstico y fracaso.
Resultados
Análisis estadístico. Se utilizó el programa R versión 3.2.0 de 2015 de la Universidad de Zurich, Suiza. El nivel de significancia se fijó en p< 0,01.
Para comparar los cambios en la altura ósea en mm, a diferentes tiempos (Inicial, 2 ,4 meses) se utilizó la prueba t pareada y para comparar los tres grupos de tratamiento a los dos maxilares se utilizó análisis de varianza (ANOVA).
Los análisis de microscopía muestran caracterís ticas morfológicas y estructurales de partículas córtico-medulares con un tamaño de partícula de 300-600μm. Las partículas con morfología cor tical aparecen como una masa sólida y continua con cortes regulares bien definidos. Su matriz ósea mineralizada está depositada en laminillas, Figuras 1 y 3.

Figura 1 Partículas óseas con técnica de metalización, estereomicroscopía aumento 40x (foto 1 y 2). En las foto 3 y 4 se aprecian las diferencias entre superficie esponjosa y cortical respectivamente
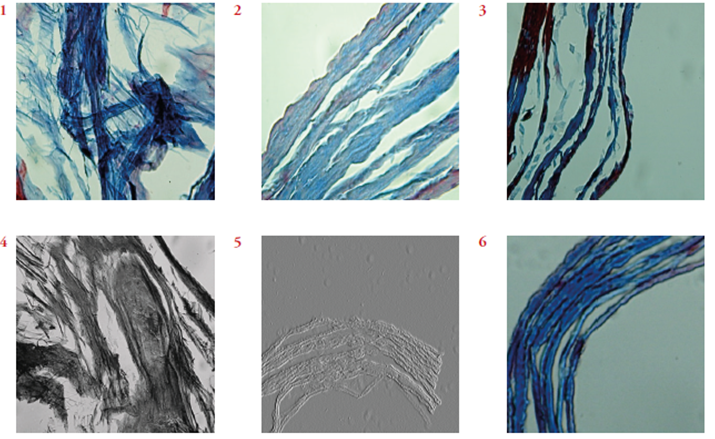
Figura 2 Fibras colágenas, microscopía óptica 40x-100x. Tinción tricrómica de Mansson. Fibras de colágeno que forman enlaces cruzados. Las moléculas de tropocolágeno se polimerizan en sentido longitudinal y lateral, para formar fibrillas reforzadas por numerosos puentes intermoleculares.

Figura 3 Osteoblastos activos y osteoide H-E corte sin descalcificar tejido humano. Aumento 40x -100x. Estas microfotografías muestran osteoblastos que están depositando en forma activa osteoide sobre una superficie ósea. En las fotos 1 y 6 se observa hueso mineralizado intensamente tenido y osteoide en menor intensidad, producido por la hilera de osteoblastos cuboides.
En las partículas con morfología medular (reticu lado, trabeculado), las láminas intersticiales están distribuidas de forma irregular formando placas y trabéculas.
Al examen histomorfométrico todas las áreas de análisis demostraron homogeneidad de las partí culas. Las muestras no presentaron ningún tipo de interferencia de materiales. Los análisis se estima ron para 1mm en 25x, 40x, 1000x, 5000x.
Las fibras colágenas presentan una estructura se cundaria en forma de cadena bien definida. Bajo el análisis de microscopía de barrido electrónico, pre senta zonas electrodensas en sus bandas trasversa les. Estas regiones contienen más tinción y crean el aspecto bandeado de las fibrillas colágenas.
Todas las muestras son acelulares, no presentan interferencias con otros tipos de materiales, los datos analizados por medio del microanálisis EDS (detector de espectroscopia de disipación de ener gía) demostró que la composición porcentual de los elementos encontrados en las partículas (calcio, fósforo, oxígeno, carbono) son constituyentes del tejido óseo.
Los datos analizados en las biopsias demostraron que la concentración de calcio es mayor en hueso maxilar superior que en el inferior. Lo mismo es cierto para oxígeno y fosforo pero la concentración de calcio es 7 veces mayor en el maxilar inferior. Para los injertos hay menos calcio y fósforo, pero más oxígeno en el maxilar inferior que en el maxi lar superior.
Las fibras colágenas no presentan ningún tipo de partícula interferente, son completamente acelulares y presentan morfología típica de fibras coláge nas.
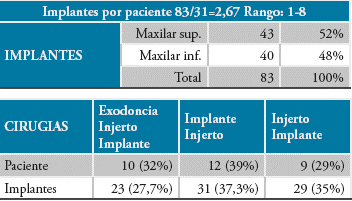
Los datos clínicos demuestran que la cantidad de implantes por paciente es en promedio 2,67, con un rango 1 a 8 implantes, presentando un porcen taje de éxito del 98% para un total de 83 implan tes distribuidos en el maxilar superior (52%) y 40 implantes en el maxilar inferior (48%). De los 83 implantes, 1 se catalogó como fracaso.
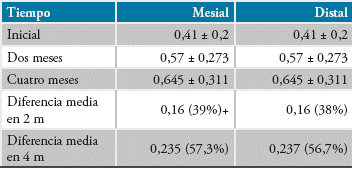
La Tabla 2 presenta los resultados de altura del hueso crestal. Cada periodo de tiempo está rela cionado de mesial a distal, donde al primer mes la cresta mesial presenta un promedio de 0,41±0,2 (promedio ± desviación estándar), a los 2 meses de 0.57± 0,273 y los 4 meses de 0,645± 0,311. Los resultados de la cresta distal presentaron al primer mes un promedio de 0,418± 0,22, a los 2 meses de 0,577±0,27 y a los 4 meses de 0,655± 0,311.
La Tabla 3 presenta los resultados del análisis esta dístico expresando la probabilidad de la prueba t pareada, que indica que todas las diferencias fue ron significativas para un nivel de significación p< 0,01. Se muestra también la diferencia entre cada periodo tanto en mm como en porcentaje de cam bio respecto al periodo de tiempo anterior.
En la Tabla 4 se relacionan los datos con criterios de éxito, supervivencia, mal pronóstico y fracaso, estimándose como criterios mayores.
Conclusiones estadísticas. Todas las diferencias (me sial y distal) de los meses evaluados son estadísti camente significativas de acuerdo con la prueba t pareada, p< 0,01.
El aumento promedio en dos meses fue 0,16mm que representa 39% por mesial y 38% por distal. El aumento promedio en 4 meses fue 0,235mm por mesial (57,3%) y 0,237mm por distal (56,7%) para el total de datos.
El ANOVA para comparar los tres grupos de trata miento también muestra diferencias significativas.
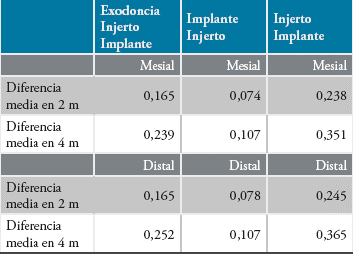
El grupo con exodoncias tuvo la mayor ganancia para 2 y 4 meses. En la comparación de implantes en maxilar superior no hay diferencias, como tam poco hay diferencias entre mesial y distal, tendien do a ser mayor la ganancia por distal.
Para comparar los cambios en la altura ósea en mm, a diferentes tiempos (inicial, 2 y 4 meses) se utilizó la prueba t pareada y para comparar los tres grupos de tratamiento a los dos maxilares se utilizó análisis de varianza (ANOVA).
Resultados
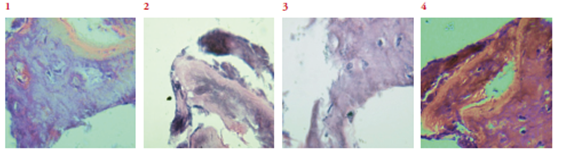
Figura 4 Osteoblastos activos y osteoide H-E corte tejido humano, aumento 40x, 100x. Los osteoblastos activos son células grandes, anchas, de forma fusiforme o cuboides, con abundante citoplasma basófilo que contiene gran cantidad de retículo endoplásmico rugoso. Estas características reflejan la alta tasa de síntesis de proteínas (colágeno Tipo 1).
Tabla 5 Comparación de la composición quimica tisular.
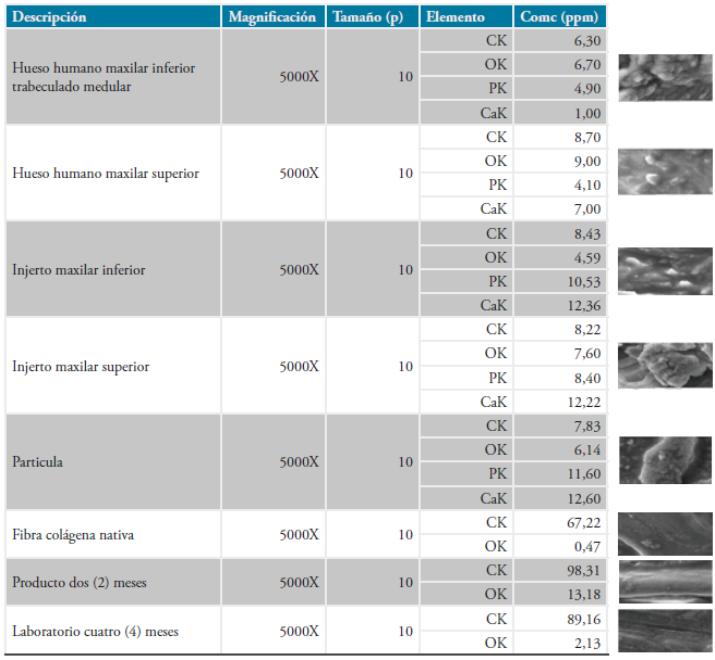
Comparación de la composición química tisular entre humano de maxilar superior e inferior Vs. sustitutos óseos Biomec CX y Biomod. Se comprobó que son materiales aptos para su uso en procesos regenerativos en los que se presenten lesiones óseas bimaxilares.
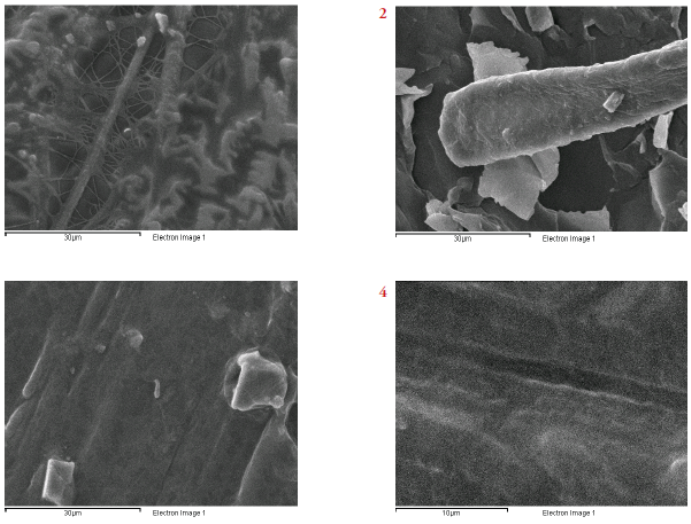
Figura 5 Micrografías electrónicas. Aumento 3000x, coloración tricrómica de Mansson. Las moléculas de colágeno se agregan para formar las fibrillas con sus bandas transversales. Las lagunas o agujeros contienen más tinción y crean el aspecto bandeado de las fibrillas colágeno. Se puede observar variabilidad en los patrones de orientación, tamaño y densidad. Las fibras de colágeno son grandes, se disponen densamente agrupadas y orientándose en una dirección para conseguir la máxima resistencia a la tracción.

Figura 6 Micrografías de barrido electrónico aumento 3000x para las fotos 1 y 3 y 5000x para la foto 2. Se observan características morfológicas de partículas de origen medular (foto 1) y cortical (foto 3).
Discusión
La regeneración de defectos óseos causados por traumas faciales, dento-alveolares, enfermedades periodontales, iatrogenias, secuelas oncológicas, malformaciones congénitas o simplemente la pér dida de la altura ósea por mecanismos de reabsor ción, durante décadas ha sido un reto para los in vestigadores que buscan la rehabilitación estética y funcional de estos defectos en el paciente.
Los sustitutos óseos estudiados demostraron cum plir con características que son importantes a la hora de escoger un material para procesos regene rativos. Entre estas encontramos que al ser disposi tivos de origen xenogénico, estos deben presentar una baja o nula celularidad, lo que permite que no se generen reacciones inmunogénicas no deseadas en el organismo receptor. Por otro lado, el pro ducto Biomec CX que se caracteriza por ser un dis positivo compuesto en su mayoría por colágeno, presentó una estructura bien definida, de aspecto bandeado típico de fibras colágenas. Esto facilita que se dé una adecuada migración de células como los fibroblastos que son importantes en los proce sos de regeneración ya que se encargan de la libe ración de factores de crecimientos importantes en los procesos de osteoinducción y osteogénesis. El producto Biomod que está compuesto por partícu las de hueso córtico-esponjoso de fémur porcino mostró una adecuada distribución de las partículas que van de 300 a 600 micras, y una morfología continua. Esto es importante ya que es necesario que los procesos de reabsorción de los injertos sean eficientes, para que los tejidos en neoformación co rrespondan a lo deseado.
Una vez se conocen las propiedades de los materia les que se desean utilizar en procesos de regenera ción es importante que el especialista en su práctica clínica realice un adecuado control y monitoreo del paciente teniendo en cuenta un apropiado diag nóstico inicial, antecedentes sistémicos del paciente, aplicación adecuada de protocolos quirúrgicos, compatibilidad de materiales, microambiente ce lular, tiempos adecuados de integración biológica, condiciones de asepsia y antisepsia, y seguimiento pos-operatorio; ya que todas esta variables pueden representar el éxito o fracaso de una adecuada rege neración tisular 10-16.
Luego de realizar el procedimiento de injertar un material de regeneración, varios autores han pro puesto un límite de 1,5mm de pérdida ósea alre dedor de implantes osteointegrados exitosamente durante el primer ano de carga y un límite para los siguientes años de 0,2mm 10,11,2,17,18,19. Recientemente el consenso del Congreso In ternacional de Implantólogos orales 20, aprobó cuatro categorías clínicas que definen las condicio nes de éxito, supervivencia y fracaso de los implan tes dentales. Allí se estableció que un implante se clasifica en grupo de éxito cuando cumple las si guientes condiciones: ausencia de dolor a la palpa ción, percusión o función, sin movilidad clínica en cualquier dirección, ausencia de exudado y pérdida ósea marginal radiográfica menor de 2mm.
Los implantes evaluados en este estudio y su direc ta relación con la cresta ósea se puede catalogar en el grupo de éxito a los 4 meses. Estos datos deter minan el éxito de la futura carga funcional mos trando una marcada estabilización de la anatomía peri-implantar. Arismendi JA en su estudio com parativo de implantes de superficie lisa y rugosa, resultado a 36 meses, determinó que los implantes de superficie lisa con carga funcional presentaron una pérdida ósea de 0,4mm, mientras que a los 24 y 36 meses la pérdida ósea fue de 1,5mm. Igual mente los implantes de superficie rugosa con car ga funcional a los 12 meses, demostraron pérdida ósea promedio de 0,6mm. A los 24 meses dicha pérdida incrementó en promedio 1,4 mm, y a los 36 meses se aumentó ligeramente a 1,5 mm en promedio.
Chang y Wennstrom 21, estudiaron 18 pacientes con un total de 43 implantes sin ningún tipo de in jerto, evaluando las alteraciones del hueso crestal y su relación con tejidos blandos durante 3 años. En los 6 meses después de la cirugía de colocación de implantes de una etapa, el margen del tejido blando retrocedió aproximadamente 0,6mm y 1,1mm sin reportes significativos. Durante los meses siguientes estos mismos autores reportan un estudio evaluado en 5 años con controles radiográficos analizando la topografía del hueso proximal en unidades de dien te/implante con un n=36 comparados con implan te/implante con un n=67 y un p<0,052. Los resul tados reportados muestran que en las unidades de diente/implante la pérdida de hueso proximal era de 0,4mm y en las unidades de implante/implante es de 0,5mm, demostrando una mayor pérdida ósea en el espacio de interimplantación. En el presen te estudio se evaluaron 83 implantes, se realizaron procedimientos quirúrgicos tales como implante pos-exodoncia más injerto óseo, implante dental y en el mismo tiempo quirúrgico, injerto óseo, y por último, injerto óseo con un tiempo de 4 meses de integración para la colocación de implantes den tales Todas las diferencias (mesial y distal) de los meses evaluados son estadísticamente significativas según la prueba t pareada, p< 0,001 y ANOVA. El aumento promedio en 4 meses fue 0,235mm por mesial (57,3%) y 0,237mm por distal (56,7%).
Lars Schropp 15 realizó un estudio comparando los cambios del hueso crestal después de implantes pos-exodoncia contra implantes de 3 meses des pués de la exodoncia, en 46 pacientes relacionados en dos grupos, n=23, realizando controles clínicos y radiográficos. Los resultados demuestran una supervivencia del 91% en la implantación inme diata con una pérdida ósea de 2mm, un 96% en el grupo de 3 meses y una pérdida ósea de 1,5 mm en promedio. En el presente estudio se presentó éxito del 90% con una altura promedio de la cresta ósea de 1mm con varianzas homogéneas y pequeñas en tre 0,18mm y 0,22mm demostrado como injertos previos no solamente son rellenos de cavidades, sino elementos osteoconductivos que asociados a implantes colocados infracrestalmente promueven una nueva formación de hueso crestal.
Los resultados sobre pérdida ósea ocurrida en estu dios 2,6 que evalúan el comportamiento de im plantes del sistema Branemark después del primer año de carga funcional, muestran que la dismi nución ósea se encuentra entre 0,4 y 1,6mm con promedio de 0,93mm. Los resultados obtenidos en esta investigación se encuentran en un prome dio de 0,18mm con un aumento de la altura ósea en segundo mes de 0,16 mm que representa 39% por mesial y 38% por distal. El aumento prome dio en 4 meses fue 0,235mm por mesial (57,3%) y 0,237mm por distal (56,7%) para el total de datos.
La composición de hueso y membrana de origen porcino de la casa 3Biomat es morfológicamente si milar a la del hueso humano en el maxilar superior/ maxilar inferior. Los resultados clínicos demostra ron tener una ganancia alrededor de la cresta ósea. Es importante resaltar que este material no presentó reacción a cuerpo extraño, poca reacción inflama toria, no se presentó dehiscencia de la herida qui rúrgica en ninguno de los casos clínicos; elementos importantes de biocompatibilidad 22-24.
La capacidad osteoconductiva, se demostró desde el inicio de la caracterización de los materiales es timada por su morfología y estructura regular, ta maño de partícula, su superficie de contacto córtico-medular y la interconexión entre poros los cuales determinan una respuesta biológica de crecimiento y aposición celular, elementos importantes en la formación de tejido óseo neoformado 25-27.
Conclusiones
A partir de los resultados obtenidos tanto en las características morfológicas como en la evaluación clínica de los sustitutos óseos Biomec Cx y Biomod, se comprobó que son materiales aptos para su uso en procesos regenerativos en los que se pre senten lesiones óseas bimaxilares.
Los sustitutos óseos Biomec Cx y Biomod son materiales biocompatibles con mínima respuesta inflamatoria. En ninguno de los tiempos evaluados se presentó reacción a cuerpo extraño.
Los sustitutos óseos Biomec Cx y Biomod favo recen el proceso normal de regeneración ósea com portándose como un material osteoconductivo que permite el crecimiento óseo en sentido horizontal y vertical.
El tiempo de reabsorción está ubicado en 4 me ses, periodo analizado en este estudio.