Abreviaturas
Dosis de referencia crónica (cRfD).
Dosis ajustada poblacional crónica (cPAD).
Agencia de Protección Ambiental (EPA).
Puntaje de ubicuidad de aguas subterráneas (GUS).
Potencial de adsorción (Koc).
Dosis letal media (DL50).
Concentración letal media (LC50).
Nivel más bajo de efectos adversos observados (LOAEL).
Concentraciones de efectos adversos más bajas observadas (LOAEC).
Concentración tóxica máxima aceptable (MATC).
Concentración sin efecto observado (NOEC).
Cociente de riesgo (RQ).
Introducción
El conocimiento del destino ambiental y de transporte de los plaguicidas es una parte integral de la caracterización de sus exposiciones ambientales. Agencias como la Environmental Protection Agency (EPA) 27 integran caracterizaciones de exposición con efectos ecológicos para determinar los riesgos del uso de pesticidas, en otras palabras, la probabilidad de que se presenten efectos adversos en animales y plantas acuáticos y terrestres para los escenarios típicos de uso de pesticidas. Con respecto al destino ambiental de los plaguicidas, estos dependen de las propiedades físicas y químicas del plaguicida, así como de las condiciones ambientales. Las propiedades fisicoquímicas de los plaguicidas pueden ayudar a predecir su movimiento a través del suelo, el agua y el aire. Las principales propiedades que se discuten a continuación incluyen: la puntuación de ubicuidad en aguas subterránea (Groundwater Ubiquitous Score - GUS), el coeficiente de adsorción de carbono (Koc), la solubilidad en agua, la presión de vapor, y la vida media.
El índice GUS es una herramienta ampliamente empleada para clasificar a los pesticidas en función de su riesgo de lixiviación hacia el agua subterránea. Este índice relaciona la persistencia (vida media en suelos) y el coeficiente de adsorción de carbono (Koc) del compuesto al suelo. Esto se usa a menudo para clasificar el potencial de un pesticida para moverse hacia el agua subterránea, en otras palabras, da una indicación de si es probable que un químico salga de los 1,5 metros superiores del suelo. Es un componente importante en las bases de datos de propiedades de los plaguicidas. La tabla 1 muestra la interpretación de los valores de GUS según el National Pesticide Information Center 17.
Tabla 1 Rangos de interpretación del Groundwater Ubiquity Scores (GUS*).

*GUS = log 10 (half life) x [4 - log 10 (Koc)] Fuente: National Pesticide Information center (NPIC, http://npic.orst.edu/HPT/)17
El potencial del pesticida para adherirse al suelo es importante, ya que generalmente está relacionado con su potencial para descender hacia las aguas subterráneas y también con el tiempo que pueden persistir en el medio ambiente. En general, los suelos que tienen menor contenido de arcilla o materia orgánica no son muy atractivos para los pesticidas. Cuanta más arena y limo tiene un suelo, menos atractivo es para un pesticida orgánico (a base de carbón). Por ejemplo, el compost tiene un alto contenido de materia orgánica y, por lo tanto, los pesticidas tienden a adherirse al suelo rico en materia orgánica. Los valores de Koc se calculan típicamente para los principales tipos de suelo: arcilla, limo y arena. En la tabla 2 se muestra la clasificación de Koc según el NPIC 17.
Tabla 2 Coeficiente de adsorción (Koc) e interpretación para suelos.

Fuente: National Pesticide Information center (NPIC, http://npic.orst.edu/HPT/)17
La solubilidad en agua se mide en mg/l. Algunos pesticidas son muy solubles en agua y otros no. Los pesticidas altamente solubles pueden viajar con el agua a medida que se mueven en el medio ambiente, aumentando su probabilidad de llegar a aguas subterráneas. Además, es más probable que sean absorbidos por las raíces de las plantas y es menos probable que se adhieran a las partículas del suelo, pero hay excepciones como el glifosato. La tabla 3 muestra la interpretación de la solubilidad en agua según el NPIC 17.
Tabla 3 Interpretación de la solubilidad en agua.

Fuente: National Pesticide Information center (NPIC, http://npic.orst.edu/HPT/)17
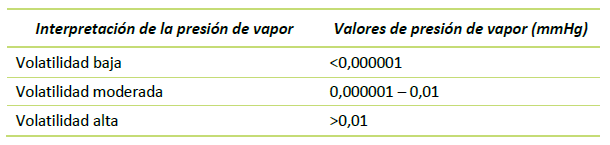
La presión de vapor es la tendencia de un pesticida a evaporarse. En general, es menos probable que los pesticidas con una presión de vapor baja, se conviertan en vapor y lleguen al aire, mientras que aquellos con una presión de vapor alta tienden a moverse al aire más rápido y más fácilmente. De manera similar, los pesticidas que se disuelven bien en agua o se adhieren al suelo tienen menos probabilidades de volatilizarse. La presión de vapor se mide típicamente en torr o milímetros de mercurio (mmHg) a 25 °C. La tabla 4 muestra la interpretación de la presión de vapor según el NPIC 17.
La vida media (T1/2) puede ayudar a estimar si un pesticida tiende a acumularse en el medio ambiente. Para el propósito de interpretar la persistencia, los plaguicidas pueden agruparse en 3 grupos: bajo (( 16 días T1/2), moderado (16 a 59 días T1/2) y alto (˃60 días T1/2). Obviamente, aquellos con vidas medias más largas tienen más probabilidades de acumularse después de aplicaciones repetidas y pueden aumentar el riesgo de contaminar las aguas superficiales, subterráneas, plantas y animales cercanos. Es importante tener en cuenta que cualquier plaguicida puede tener muchas vidas medias dependiendo de las condiciones del medio ambiente y de si se mide en el suelo, el agua y las superficies de las plantas. Las condiciones ambientales que influirán en la vida media de un plaguicida incluyen la luz solar, la temperatura, la presencia de oxígeno (condiciones aeróbicas versus anaeróbicas), el tipo de suelo y su acidez, la actividad microbiana y los ingredientes del producto. Por estas razones, es imposible describir una vida media única y consistente para un pesticida. También es importante tener en cuenta que cuando un pesticida se descompone, no desaparece, sino que forma nuevos químicos que pueden ser más o menos tóxicos que el químico original. En general, los pesticidas orgánicos se degradan en estructuras más pequeñas hasta que solo quedan dióxido de carbono, agua y minerales.
En estudios de toxicología tradicionales, los sujetos son expuestos a un rango de concentraciones durante 1 a 4 días en condiciones de laboratorio. Siempre que la mortalidad en el control (es decir, sin pesticida) sea inferior al 10%, se pueden usar estos experimentos para determinar la concentración letal que matará al 50% de la población (es decir, el valor de CL50). Utilizando la clasificación de la EPA 27 de Estados Unidos, la toxicidad de un pesticida se clasifica como se muestra en la tabla 5.
Tabla 5 Categorías de toxicidad aguda para organismos acuáticos (CL50) y terrestres (LC50-dieta y DL50).
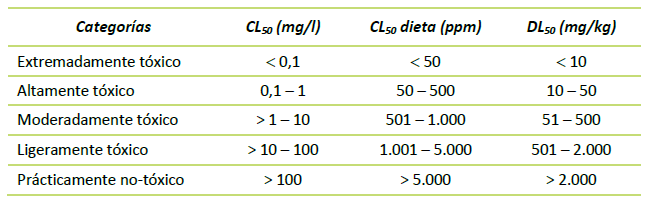
Fuente: U.S. Environmental Protection Agency, 2004.27 DL50: dosis letal media. CL50: concentración letal media.
Al evaluar el riesgo, la CL50 se compara con las concentraciones de la sustancia química que se encuentra en la naturaleza. Para establecer un límite superior seguro para las concentraciones de una sustancia química en la naturaleza, la EPA utiliza un índice conocido como "cociente de riesgo" (Risk Quotient - RQ). El RQ se calcula dividiendo la concentración esperada de la sustancia química en la naturaleza por el valor de CL50 para las especies más sensibles de un grupo. Para no dañar la vida silvestre, esta relación no debe exceder 0,05, es decir, la concentración que esperamos ver en la naturaleza no debe exceder el 5% de la CL50 para las especies más sensibles. La lógica es que, si la concentración de CL50 mata al 50% de los animales, el 5% de este número debería proporcionar una concentración que mata a pocos o ninguno de los animales.
Desafortunadamente, el enfoque basado en RQ no proporciona una estimación cuantitativa de la probabilidad o magnitud de un efecto adverso. Una advertencia para interpretar los estudios de toxicidad aguda es que, por lo general, se realizan en entornos de laboratorio que no son realistas en condiciones de campo, como en tanques de vidrio estáticos sin renovación (acuarios) y sin ligandos ambientales como sedimentos, partículas en suspensión, plantas acuáticas, materia orgánica, y actividad microbial; lo que podría reducir potencialmente la exposición a la fauna acuática. Además, las características físicas del agua, como el flujo, las temperaturas frías y el pH neutro, pueden reducir la toxicidad aguda de los plaguicidas. En consecuencia, los datos toxicológicos derivados de muchas pruebas de laboratorio pueden tergiversar el entorno físico y químico en condiciones de campo.
Se han investigado exhaustivamente numerosos herbicidas por su potencial para producir efectos adversos en organismos no diana. Muchos usos requieren que se realicen evaluaciones de riesgo ecológico basadas en los posibles efectos agudos y crónicos. Este documento tiene como objetivo brindar una visión general de lo que se conoce actualmente sobre el destino ambiental y los efectos ecológicos asociados con tres de los principales herbicidas utilizados en Colombia.
Materiales y métodos
Los datos se recopilaron utilizando fuentes primarias que incluyeron las publicaciones de agencias reguladoras como la EPA [(EPA Registration Eligibility Decision (RED) y la base de datos ECOTOX de la EPA] 22-25, la base de datos del National Pesticide Information Center (NPIC) 17, y además revistas indexadas en la Biblioteca Nacional de Medicina y los Institutos Nacionales de la Salud de los Estados Unidos (PubMed). La base de datos del NPIC 17 se utilizó para obtener información para la interpretación de las propiedades fisicoquímicas de los herbicidas, como se muestra en las tablas 1-4. El EPA RED 28-30 se utilizó para obtener información sobre la toxicidad aguda de los herbicidas. Por lo general, los datos son recopilados de estudios sobre especies sustitutas no diana, que pretenden ser representativas de amplios grupos taxonómicos y, por lo tanto, se utilizan para extrapolar los efectos potenciales sobre una gran variedad de especies acuáticas y terrestres no diana.
El criterio principal de valoración de la toxicidad aguda de los plaguicidas es la CL50 (mg/l) para los organismos acuáticos, la DL50 (mg/kg de peso corporal) y CL50-dieta (ppm) para los organismos terrestres. Las categorías de toxicidad aguda de la EPA (2004) 27 se utilizaron como se muestra en la tabla 5. Aunque la estimación de la CL50 o las dosis en las pruebas de toxicidad aguda es el método convencional para evaluar las consecuencias probables de la aplicación de pesticidas en organismos no diana, también se incluyen la valoración de estudios de exposición crónica que miden otros efectos adversos a concentraciones subletales y que pueden afectar la supervivencia de la especie. De hecho, estas alternativas pueden ser más relevantes del punto de vista medioambiental porque se exponen los sujetos a concentraciones que son más probables en condiciones naturales. Los datos sobre las ventas de plaguicidas en Colombia para el año 2019 se obtuvieron de la base de datos del ICA (Instituto Colombiano Agropecuario) 11. El número de hectáreas sembradas con cultivos de coca se obtuvo del Observatorio de Drogas de Colombia 18. La página web de la Unión Internacional para la Conservación de la Naturaleza (UICN) 9,26 se empleó para identificar el número de especies catalogadas en peligro para el país y localizadas en los principales departamentos productores de coca.
Resultados y discusión
El volumen total de plaguicidas vendidos en 2019 en Colombia fue de 133.484.661 kg, de los cuales los herbicidas fue la categoría principal con 71.982.509 (kg). La segunda y tercera categoría de plaguicidas vendidos fueron insecticidas con 31.944.593 kg y fungicidas con 26.919.141 (kg). La tabla 6 muestra las ventas de los 10 herbicidas más utilizados en Colombia en 2019. El glifosato representó aproximadamente la mitad del volumen total de herbicidas vendidos en 2019 con 38.271.506 kg (Tabla 6). Desde 1997, los campos de coca ilegal en Colombia se han rociado con una formulación de glifosato llamada Glyphos-Cosmo-Flux, que contiene el surfactante “amina de sebo etoxiladas” (polyethoxylated tallow amines - POAE) (Solomon et al., 2009) 24. La tabla 7 muestra las propiedades físico-químicas para cada uno de los tres herbicidas seleccionados 17.
Tabla 6 Ventas de herbicidas en Colombia para el 2019.
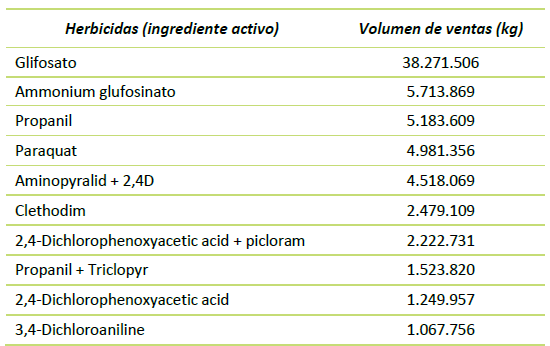
Fuente: Instituto Colombiano Agropecuario. Boletín de Estadísticas de comercialización de Plaguicidas - 2019 11
Tabla 7 Propiedades fisicoquímicas de los tres herbicidas más usados en Colombia.
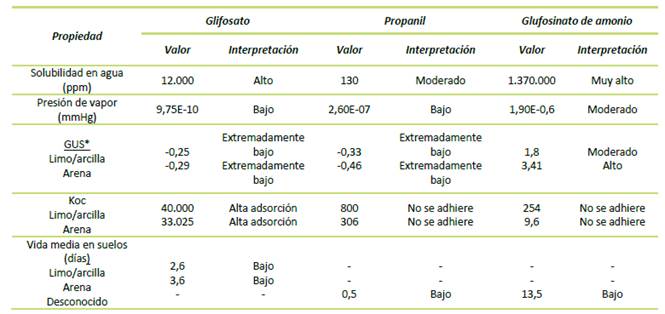
*Groundwater Ubiquity Score (GUS).
Fuente: National Pesticide Information center (NPIC, http://npic.orst.edu/HPT/)17
Glifosato: destino ambiental
El glifosato [N-(fosfonometil) glicina] es un herbicida sistémico no selectivo que se usa ampliamente para controlar las malezas en cultivos agrícolas y sitios no agrícolas. Es el ingrediente activo en cientos de productos diferentes que se venden en todo el mundo y generalmente está presente como sal de isopropilamina. Sin embargo, debido a su naturaleza aniónica, el glifosato por sí solo no penetra fácilmente en las cutículas de las plantas. Por eso se combina con surfactantes que facilitan la penetración a través de las ceras cuticulares de las plantas diana. Basado en las propiedades físico-químicas del glifosato, aunque es altamente soluble en agua, no es probable que se filtre al agua subterránea ni se transfiera del suelo a aguas superficiales a través de la lluvia porque se adhiere fuertemente al suelo (US EPA, 2009 - RED para glifosato) 28. Debido a esta propiedad de adherirse fuertemente a las partículas del suelo, debe aplicarse directamente a las superficies de las plantas para que sea eficaz.
Esta cualidad explica por qué las áreas tratadas con glifosato se pueden plantar con cultivos poco después de la aplicación. Sin embargo, siempre existe la posibilidad de contaminar aguas superficiales si se aplica directamente a un medio acuáticos. Además, el glifosato tiene un bajo potencial de volatilización del suelo o del agua debido a su baja presión de vapor. Según el NPIC 17, su vida media en suelos con condiciones aeróbicas es baja, de 1,8 a 5,4 días, y en sistemas aeróbicos de agua y sedimentos es de 7 días. Esto requiere degradación microbiana porque no se descompone en condiciones anaeróbicas y por procesos abióticos como la fotólisis en agua. Sin embargo, estudios que utilizaron técnicas isotópicas en condiciones de laboratorio mostraron una tasa de mineralización mucho menor para diferentes tipos de suelo en Colombia (Figura 1, Cuervo y Fuentes, 2014) 3.
La tasa de mineralización en muestras de suelo de cultivos de arroz con una larga historia de uso de plaguicidas, entre ellas el glifosato, fue la más baja, mientras que la tasa de degradación en suelos forestales sin uso de plaguicidas fue la más alta. Específicamente, después de 106 días, el valor máximo de mineralización acumulada para las muestras de bosque fue de 53% en promedio, 38% para el suelo de pastizales y solo el 23% de la molécula intacta del herbicida se degradó en las muestras de suelo de cultivo de arroz (Figura 1). En general, estos resultados indican que se requieren varios meses para degradar el glifosato en los suelos tropicales de Colombia 3.
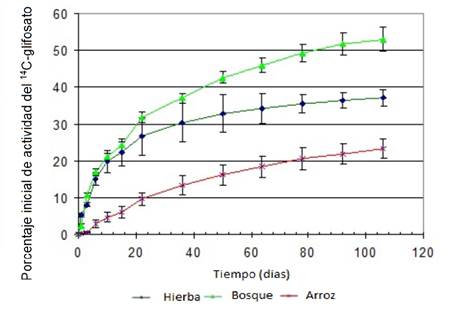
Fuente: Cuervo y Fuentes (2014) 3.
Figura 1 Mineralización acumulada de 14C-glifosato medida mediante la evolución de CO2, durante 106 días en condiciones de microcosmos.
Glifosato: ensayos de toxicidad aguda
El glifosato puro es prácticamente no tóxico para los mamíferos terrestres y las aves de forma aguda, pero es moderadamente tóxico (1-10 mg/l; clasificación de la EPA de los EE. UU., 2004) 27 para los organismos acuáticos (es decir, ranas, truchas, pulgas de agua). Sin embargo, para algunas especies de anfibios, se ha demostrado que las formulaciones de glifosato son altamente tóxicas con valores de CL50 por debajo de 1 mg/l (Figura 2) 20. Por ejemplo, algunas de las especies de anfibios más sensibles son de las ranas toro (Lithobates catesbeianus) y rana mirona primaveral (Pseudacris crucifer), ambas tienen valores de CL54-d de 0,8 mg/l. Si seguimos el protocolo de evaluación de riesgos de la EPA y dividimos este valor por 20, el límite superior que protegería a las larvas de anfibios sería de 0,04 mg/l. Se podría esperar fácilmente un valor tan bajo en el agua basado solo en la deriva de una aplicación aérea, sin mencionar una sobre-aspersión inadvertida que puede ocurrir durante las aplicaciones forestales o de campos de coca. Desafortunadamente, la EPA ha utilizado típicamente estudios de mojarras de oreja azules (Lepomis macrochirus), con una CL50 de 3,17 mg/l, como especies sustitutas de anfibios en sus procesos de decisión de elegibilidad de registros (US EPA, 2009 - RED para glifosato) 28. Luego utilizaron una concentración ambiental esperada en el agua basada solo en contaminación por deriva de 0,095 mg/l para estimar el RQ (0,095/3,17 = 0,03). Si hubieran utilizado estudios en anfibios, está claro que el cociente de riesgo superaría el nivel de preocupación de 0,05. Estos estudios apoyan la noción de que las agencias reguladoras deberían exigir datos de toxicidad en anfibios como parte de sus requisitos de registro 28.
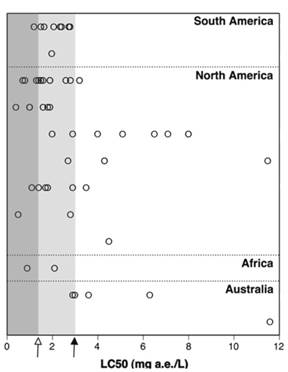
(Fuente: Relyea, 2011) 20.
Figura 2 Estudios de CL50 en larvas de anfibios expuestos a formulaciones de glifosato que contienen el surfactante POEA. Cada círculo representa una prueba individual de una especie de anfibios bajo un conjunto de condiciones determinadas (pH, señales de depredadores, etc.). La flecha negra indica una concentración en el peor escenario de aplicaciones de 3 mg/l. La flecha blanca indica el peor escenario del gobierno canadiense en aplicaciones forestales de 1,43 mg/l.
No se puede subestimar la importancia de los cuerpos de agua de los humedales para la reproducción y desarrollo de etapas tempranas de vida para muchos de los anfibios del mundo. La aplicación directa de formulaciones que contienen aminas de sebo polietoxiladas (POEA), como el producto original Roundup(, está expresamente prohibida en cuerpos de agua. Las concentraciones ambientales esperadas en usos acuáticos se obtienen típicamente con cálculos simples de dilución basados en la masa del plaguicida aplicado y el volumen del cuerpo de agua. Suponiendo el escenario más desfavorable de un exceso de aspersión inadvertida en un sistema acuático poco profundo, la concentración ambiental prevista para la formulación original de Roundup( basada en la tasa de aplicación media de la etiqueta de 4,7 l/hectárea y calculada para una profundidad en un humedal de 15,24 cm sería 1,1 mg/l (Fuentes et al, 2011) 7. Esta tasa de aplicación de Roundup( es similar a la utilizada por Glyphos-Cosmo-Flux (3,7 kg/ha) para controlar los cultivos ilícitos de coca (Solomon et al., 2009) 24.
El estudio de Fuentes et al., (2001) 7 calculó el margen potencial de seguridad (MOS) dividiendo la NOEC para seis especies de anuros larvarios de América del Norte por la concentración ambiental prevista de 1,1 mg/L (derivada de la tasa de aplicación media de 4,7 L/ha). Todos los valores de MOS, menos uno, estaban por encima de 1, por lo que concluyeron que no se esperarían efectos tóxicos en las larvas de anfibios. Dicho esto, encontraron un margen muy estrecho entre la NOEC y el 100% de mortalidad. En consecuencia, se esperaría que mayores tasas de aplicación en condiciones de agua menos profundas y estáticas resulten en concentraciones potencialmente letales. En línea con un margen estrecho de concentraciones entre NOEC y niveles letales, los estudios que también han determinado concentraciones letales en 8 especies de ranas encontraron pendientes de la curva-respuesta altas, con CL1 que estaban solo 1,5-2 veces por debajo de los valores de CL50 (Bernal et al., 2009a) 1. Por lo tanto, la evaluación de riesgos de la EPA que usa concentraciones 20 veces por debajo de la LC50 puede no corresponder con valores realistas para la toxicidad aguda en anfibios de las formulaciones de glifosato que contienen POAE.
Glifosato: toxicidad de los surfactantes en formulaciones de glifosato
Curiosamente, la toxicidad aguda de Roundup( es similar al surfactante más comúnmente utilizado, las aminas de sebo polietoxiladas (POEA), que es un orden de magnitud más tóxico para la fauna acuática (trucha arco iris, bagres, pez de agallas azules) que el glifosato puro (Folmar et al., 1979 6; Mann et al., 2003 14; Mitchell et al., 1987 15). Por ejemplo, cuando se estudió la toxicidad de los surfactantes en diferentes especies de ranas de América del Norte, la exposición única al POEA mostró una toxicidad similar a la de la formulación original de Roundup( cuando se comparaban los datos sobre la base de concentraciones de ácido equivalente del glifosato (Howe et al., 2004) 10. En consecuencia, los surfactantes contribuyen con la mayor parte, si no con la totalidad, de la toxicidad aguda de Roundup(. Se desconoce si las concentraciones del surfactante POEA pueden alcanzar niveles tóxicos en sitios de agua poco profundos, lénticos o efímeros porque hay pocos datos medidos disponibles para la disipación de los POEA. Las estimaciones conservadoras han establecido una vida media de 21 a 42 días en aguas naturales y de 7 a 14 días en el suelo (Giesy et al., 2000) 8.
Glifosato: estudios de exposición crónica
Los experimentos de exposición crónica (exposición total de 42 días) a concentraciones de 0,6 mg/l, que son más bajas que las que se utilizan normalmente para estudios agudos, revelaron que la formulación original de Roundup® y los POEA tenían efectos similares sobre la mortalidad, daños en las colas de renacuajo y retrasos en el desarrollo de metamorfosis (Howe et al., 2004) 10. Los resultados mostraron que el valor promedio de días hasta la metamorfosis se prolongó significativamente, y el número de renacuajos supervivientes para alcanzar el estadio 42 de Gosner también se redujo significativamente. Otros efectos reportados fueron la reducción de la longitud de la cola y la presencia de gónadas anormales de los renacuajos (es decir, intersexualidad en la fase crítica de la metamorfosis), lo que sugiere una alteración las hormonas tiroideas. Los autores concluyeron: "Los resultados actuales indican que las formulaciones del pesticida glifosato que incluyen el surfactante POEA en concentraciones ambientales que se podrían encontrar en humedales después de una aplicación de campo pueden ser tóxicas para las fases tempranas de los anfibios comunes de América del Norte" (Howe et al 2004, p. 1933) 10. Además, otros estudios han demostrado que la exposición a Roundup( a concentraciones subletales de 0,5 mg/l, más posibles en el medio ambiente, tiene efectos dramáticos sobre el comportamiento y las respuestas anti-depredadores de los renacuajos de la rana de bosque (Moore et al., 2015) 16.
Básicamente, su capacidad para responder a señales de congéneres lesionados, que es una fuente importante de información con respecto al riesgo de depredación, se vio afectada. Llegaron a la conclusión de que una desactivación total o parcial de las señales de alarma por Roundup( podría tener consecuencias negativas para supervivencia de las ranas en su medio natural. Además, para el glifosato y otros pesticidas, se ha demostrado que agregar señales ambientales como el olor de los depredadores en el agua hace que los pesticidas sean más letales para los renacuajos (Relyea, 2011) 20. Otro estudio de exposición crónica en una rana endémica colombiana, la rana de sabana (Dendropsophus molitor), a concentraciones subletales (325 y 750 ppb) de Roundup Active( durante 30 días encontró alteraciones histopatológicas en el hígado (p ej., acumulación de vesículas lipídicas, dilatación sinusoidal, desorganización del retículo endoplásmico rugoso) que dependían de la concentración y podían afectar las funciones hepáticas (Riaño et al., 2020) 22.
Glifosato: estudios colombianos
Un estudio colombiano que simuló el hábitat de las ranas en mesocosmos al aire libre (es decir, fondos con capas de suelo y 15 cm de agua) encontró que la mortalidad (CL50 4-d = 9-11 mg/l) para renacuajos, juveniles y adultos de 4 especies colombianas de ranas solo se observaban a tasas de aplicación de 3 a 4 veces por encima de una aplicación normal de ( 4 kg/ha (Bernal et al., 2009a) 1. Sin embargo, las concentraciones de glifosato no se midieron en ese estudio y se estimaron en base a concentraciones nominales para una aplicación de 8,9 y 10,9 kg de glifosato/ha de Glyphos-Cosmo-Flux, una formulación de glifostato que contiene POAE y es utilizada en plantaciones ilegales de coca. Es importante destacar que en dichos experimentos de mesocosmos el agua tenía un pH más bajo (pH(7) que en los estudios de laboratorio (pH = 8,2) donde se vio que la CL50 4-d para Glyphos-Cosmo-Flux en las mismas especies variaba de 1,2 a 2,8 mg/l (Bernal et al., 2009b) 2. Está claro que ambos estudios no son comparables porque se sabe que el herbicida es menos letal a un pH más bajo. Estos estudios fueron realizados por investigadores colombianos para imitar concentraciones iguales o mayores que la tasa de aplicación normal utilizada en los programas de erradicación de campos de coca ilegal. Lo sorprendente es que los investigadores atribuyeron las tasas de mortalidad más bajas en los experimentos de mesocosmos no al pH más bajo, sino a la presencia de suelo, que se ha demostrado que no altera el efecto sobre la letalidad de Roundup( (Relyea, 2005) 21.
Contrario a estos resultados, otros valores de CL50 publicados para muchas especies de renacuajos son considerablemente más bajos que 2,5 mg a.e./l (Figura 2). Por ejemplo, un estudio que utilizó concentraciones más bajas de Roundup( de 1 mg/l en mesocosmos de estanques al aire libre, causó un 29% de mortalidad en la rana leopardo y un 71% de mortalidad en sapos americanos (revisión de Relyea, 2011) 20. Los estudios de Relyae (20, 21) sugieren que el suelo juega un papel menor de lo anticipado anteriormente y el factor crítico es el medio que el Roundup( contacta primero, si el agua o el suelo. Si llega al agua primero, como sucedería durante una aspersión directa sobre el agua, es probable que el herbicida permanezca disuelto en el agua debido a su alta solubilidad, y no se adhiera al sedimento de un humedal que podría hacer que el agua fuese segura para los anfibios. Sobre la base de los estudios anteriores, se puede concluir que la aspersión inadvertida de humedales en los programas de erradicación de coca en Colombia podría tener efectos devastadores para las poblaciones de anfibios.
La Unión Internacional para la Conservación de la Naturaleza (UICN) 26 es la fuente de información más completa del mundo sobre el estado de conservación global de especies de animales, hongos y plantas. Su Lista Roja es un indicador crítico de la salud de los seres vivos del mundo. Clasifican las especies en riesgo en 9 categorías, de las cuales “en peligro” (EN) y “en peligro crítico” (CR) están diseñadas para reflejar un riesgo muy alto o extremadamente alto de extinción en la naturaleza, respectivamente. Casi 300 de las más de 700 especies de anfibios en Colombia, la gran mayoría de las cuales son ranas, están clasificadas como vulnerables, casi amenazadas, en peligro o en peligro crítico según la Lista Roja de la UICN para 2019 (Figura 3) 9. El número de especies que encontramos para cada una de las categorías amenazadas fueron: vulnerable (85), casi amenazado (44), en peligro (78) y en peligro crítico (54) 26.
Los Departamentos del Pacífico Sur y Sur del país más productores de coca concentraron el mayor número de anfibios EN y CR de la siguiente manera: Nariño (n = 20), Valle del Cauca (n = 17), Cauca (n = 12) (Tabla 8). Existen 132 especies de anfibios colombianos catalogados como en peligro (EN = 78) o peligro crítico (CR = 54) en la Lista Roja de la IUCN. En 2008, con base en datos de ubicación de anfibios recolectados en Colombia, se obtuvieron registros para 193 especies (28% de la diversidad nacional) de ranas y sapos encontradas en localidades dentro de los 10 Km de áreas donde se cultiva coca (Lynch y Arroyo, 2009) 13.
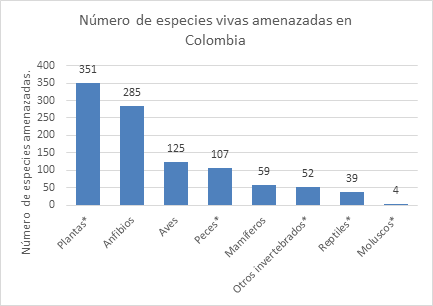
Fuente: Lista Roja de la UICN versión 2019-3: Tabla 8 9,26
Figura 3 Número de especies vivas amenazadas en Colombia en la Lista Roja de la UICN a diciembre de 2019, por tipo taxonómico. La Figura debe interpretarse como el número de especies que se sabe que están amenazadas dentro de las especies que se han evaluado hasta la fecha, y no como el número total de especies amenazadas para cada grupo. Según la fuente, las especies vivas amenazadas incluyen especies que están en peligro crítico (CR), en peligro (EN) o vulnerables (VU).
Tabla 8 Principales Departamentos productores de coca en Colombia y áreas (hectáreas) de tierra sembrada en 2015-2019. Número de especies de anfibios en peligro de extinción para cada Departamento.
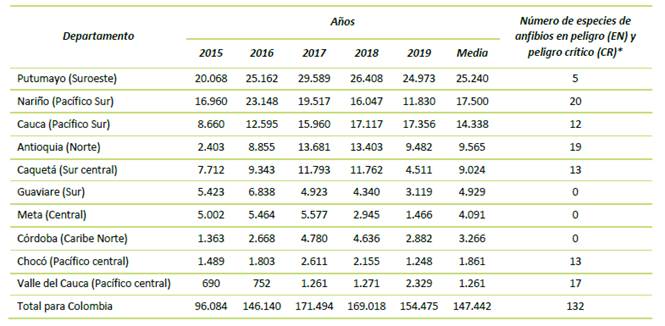
Fuente: Observatorio de Drogas de Colombia 18 (http://www.odc.gov.co/sidco/oferta/cultivos-ilicitos/departamento-municipio).
Glifosato: ejemplo de medidas de protección
Un ejemplo interesante para proteger a los anfibios de los impactos de los pesticidas es la rana de patas rojas de California (Rana draytonii; antes, Rana aurora draytonii). Fueron catalogadas como amenazadas bajo la lista de especies en peligro de extinción en 1996 porque su número había disminuido más del 90% y la especie ya no se encontraba en el 70% de su área de distribución anterior (U.S.A. Fish and Wildlife Service, 2002) 31. El 20 de octubre de 2006, el tribunal del distrito de los EE. UU. para el Norte de California impuso zonas de prohibición de “no uso” de pesticidas alrededor de los hábitats acuáticos y zonas donde habita la rana de patas rojas de California. Bajo la orden judicial, las zonas de “no uso” eran de 60 pies ((20 metros) para aplicaciones terrestres y de 200 pies ((66 metros) para aplicaciones aéreas alrededor de los hábitats de la rana.
Propanil: destino ambiental
El propanil (N-(3,4-diclorofenil) propanamida) es un herbicida post-emergente selectivo que se utiliza para controlar las malezas de hoja ancha y gramíneas, particularmente en los arrozales en los que hay poco riesgo de dañar el cultivo de arroz. Se metaboliza rápidamente en condiciones aeróbicas metabólicamente activas tanto en el agua como en el suelo, con una vida media de 0.5 días en suelo aeróbico (U.S. EPA, 2003 - RED para propanil) 29. Como tal, los estudios en arrozales mostraron que generalmente es indetectable después de no más de un día en el agua. Sin embargo, es estable a los procesos de degradación química como la hidrólisis y fotodegradación acuosa. No se absorbe al suelo (Koc bajo) y, como tal, tiene una movilidad media, especialmente en suelos arenosos. Debido a que tiene una solubilidad moderada en agua y no se absorbe al suelo, tiene el potencial de alcanzar el agua subterránea, pero debido a su corta vida media, no es probable que persista durante el tiempo suficiente para lixiviarse en cantidades significativas. No obstante, puede contaminar el agua a través de la escorrentía después de eventos de lluvia o por filtración; en consecuencia, la EPA solicita un signo advertencia que indique el potencial de contaminar las aguas superficiales.
Propanil: ensayos de toxicidad aguda
El propanil es ligeramente tóxico para los mamíferos con una DL50 (oral, rata) de 1.080 mg/kg. El principal efecto tóxico del propanil es la metahemoglobinemia y la anemia hemolítica, que se considera el criterio de valoración más sensible que se presenta en diferentes especies mamíferas con exposiciones a plazo intermedio (U.S. EPA, 2003 - RED para propanil) 29. Curiosamente, después del paraquat, es el herbicida que más muertes causa en los países asiáticos por autoenvenenamiento (Roberts et al., 2009) 23. La muerte se atribuye en gran medida a la metahemoglobinemia severa. En estudios de toxicidad crónica en ratas, la LOAEL para metahemoglobinemia se estableció en 9 mg/kg/día después de 13 semanas de exposición 29. Cuando se calculó un riesgo dietético crónico utilizando el valor de consumo promedio de alimentos y los valores promedio de residuos (estimados a partir de datos de ensayos de campo) en esos alimentos, ni la dosis crónica de referencia (cRfD), ni la dosis crónica ajustada para la población (cPAD) de 0,009 mg/kg/día se excedieron para ser motivo de preocupación. Al modelar el riesgo dietético del agua potable, los datos también mostraron que las concentraciones ambientales estimadas en el agua no excedían el riesgo permitido en los alimentos, que se determina como el "nivel de comparación del agua potable".
El propanil se clasifica como moderadamente tóxico para las aves en exposiciones agudas ya que los valores de DL50 se encuentran entre 51 y 500 mg/kg (U.S. EPA, 2003 - RED para propanil) 29. Los valores de CL50 se encuentran dentro del rango de 2.861 y ˃5.000 ppm, lo que lo clasifica como leve o prácticamente no tóxico para las aves en la dieta. Desafortunadamente, no existen estudios sobre los efectos crónicos en las aves como existen en mamíferos. Con respecto a los peces e invertebrados de agua dulce, es de leve a moderadamente tóxico según los valores de CL50 96h: trucha arco iris (12,8 ppm), mojarras de oreja azules (14,0 ppm), bagres (6 ppm), pulga de agua (11,4 ppm). Curiosamente, parece ser un poco más tóxico para los peces estuarinos/marinos y los moluscos según las CL50 96h: bolín (Cyprinodon variegatus - 4,6 ppm), ostión de Virginia (Crassostrea virginica - 4,96 ppm). La especie más sensible parece ser el camarón (Americamysis bahía) con una CL50 96h de 0,4 ppm. Debido al peligro ecológico para los camarones, la EPA solicita un aviso en la etiqueta que indique "este pesticida es tóxico para los camarones" 29.
Sin embargo, y lo que es más importante, pueden producirse efectos indirectos por muerte o reducción del fitoplancton, que reduciría el suministro de oxígeno y la eliminación de desechos nitrogenados tóxicos, así como la producción del zooplancton. Se ha demostrado que el propanil es un potente inhibidor de la producción de oxígeno fotosintético (Tucker, 1987) 25. Un estudio que evaluó el impacto de diferentes herbicidas, incluido el propanil, en mesocosmos experimentales, mostró que el propanil a las tasas de aplicación proyectadas (4,5 kg de ingrediente activo/ha) redujo el oxígeno disuelto a niveles críticamente importantes para la supervivencia de los peces en las siguientes 48 horas después aplicación (Perschbacher et al., 1997) 19.
El efecto se correlacionó con una menor producción de fitoplancton en lugar de una mayor respiración comunitaria. Una curva típica de dosis-respuesta mostró que concentraciones de pocas ppb reducían la producción neta de oxígeno durante un período de incubación de 3 horas en muestras de agua recolectadas de estanques de cultivos de bagre (Figura 4, de Tucker, 1987) 25. Los valores de concentración efectiva 50 (CE50) a las 3 horas variaron de 51 a 109 ppb y las concentraciones sin efecto observado fueron de 10 ppb. La conclusión de estos estudios fue que, durante los primeros 2 días después de la contaminación, concentraciones bajas de propanil (50 ppb o menos) podrían tener grandes efectos adversos sobre la dinámica del oxígeno disuelto en estanques de bagres (Tucker, 1987) 25.
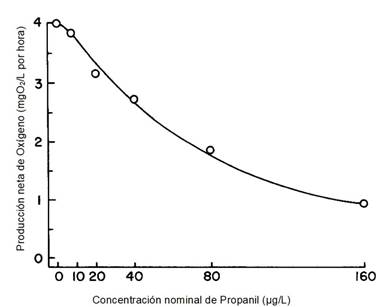
Fuente: Tucker, 1987 25
Figura 4 Curva típica de dosis-respuesta que describe el efecto del propanil sobre la producción neta de oxígeno. La comunidad de fitoplancton consistió predominantemente en Lyngbya y Closterium spp.
Propanil: ensayos de toxicidad crónica
A pesar de tener una toxicidad relativamente baja en exposiciones agudas, los datos crónicos muestran que el crecimiento y desarrollo de peces e invertebrados se afecta a concentraciones de más de 9 ppb (U.S. EPA, 2003 - RED para propanil) 29. Las concentraciones de efecto adverso más bajas observadas (LOAEC) y que afectaron la supervivencia y la desarrollo en la carpita cabezona (Pimephales promelas) fue de 19,0 ppb. Un estudio que evaluó los efectos crónicos y subletales del propanil en pulgas de agua (Daphnia magna) mostró que los parámetros reproductivos también eran muy sensibles al efecto del propanil (Villarroel et al., 2003) 32. Calcularon la concentración máxima aceptable de tóxico (MATC) utilizando como parámetro de evaluación la tasa intrínseca de aumento natural (r), que es, muy simplemente, la tasa de reproducción menos la tasa de muerte para cada generación. La interpolación de estos resultados dio valores de MATC de 80 ppb de propanil 32. Estos estudios revelan que es probable que se produzcan efectos tóxicos directos sobre los organismos acuáticos cuando el propanil se aplica directamente en los estanques o por la deriva aérea de los arrozales pulverizados.
Propanil: regulación
Debido a que el agua de los cultivos arrozales se libera a los hábitats acuáticos adyacentes, la EPA determinó las concentraciones preocupantes para las especies de peces e invertebrados no diana basándose en los efectos adversos más sensibles y los períodos mínimos de retención de agua en los campos de arroz para reducir la exposición prevista a estos organismos (U.S. EPA, 2003 - RED para propanil) 29. La intención de los períodos de retención de agua en el arroz es permitir que el propanil se degrade en el arrozal a concentraciones que minimicen el riesgo para los peces acuáticos e invertebrados que habitan los medios acuáticos adyacentes. Basado en diferentes modelos, recomiendan un período de retención de agua (descarga) de 7 días para todas las áreas de producción de arroz, asumiendo las tasas típicas de aplicación de 2 kg/acre 29. Esta recomendación también abordó la protección de plantas acuáticas no diana. Finalmente, los productores de bagres y aplicadores aéreos cerca de los campos de arroz deben ser conscientes de la posibilidad de que una contaminación inadvertida podría causar mortalidad de los peces a través de los efectos indirectos del químico sobre el estado del oxígeno disuelto de los estanques.
Glufosinato de amonio: destino ambiental
El glufosinato [amonio-(3-amino-3-carboxipropil)-metilfosfinato] está registrado para su uso en el control de hierbas y malezas de hoja ancha en cultivos de árboles frutales, maíz, patatas, soja, canola, remolacha azucarera, uvas y frutos secos. Debido a sus propiedades físico-químicas de alta solubilidad en agua y alta permeabilidad en el suelo (bajo Koc), puede lixiviarse al agua subterránea y llegar al agua superficial a través de escorrentías (U.S. EPA, 1999 - RED para el glufosinolato) 30. Debido a su potencial para contaminar las aguas superficiales y subterráneas, las etiquetas deben indicar que no se deben aplicar directamente al agua, o áreas donde hay aguas de escorrentía o en zonas intermareales que estén debajo de la marca de agua máxima promedio. Es estable a los procesos de degradación abiótica como la hidrólisis y la fotólisis, y requiere para degradarse de la acción microbiana. Las vidas medias estimadas en suelos aeróbicos y sistemas acuáticos son de 23 y 64 días, respectivamente. Las estimaciones del límite superior de las concentraciones que se pueden encontrar en las aguas superficiales y subterráneas a las tasas de aplicación máximas (1.5 kg/ha) para la remolacha son de 54,2 y 1,2 ppb, respectivamente 30.
Glufosinato de amonio: Efectos ecológicos
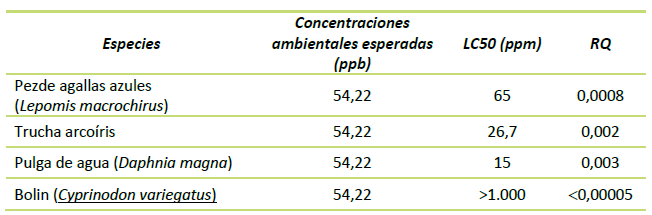
Según los datos de toxicidad aguda, se clasifica como prácticamente no tóxico (DL50 ( 2.000 mg/kg; CL50 ( 5.000 ppm) para especies de aves y mamíferos (U.S. EPA, 1999 - RED para el glufosinato) 30. Los RQ de una sola y múltiples aplicaciones del herbicida en aves y mamíferos en peligro y no amenazados oscilaron entre 0,03 y 0,6, que están por debajo de los niveles preocupantes, por lo que la EPA calculó que no existe un riesgo crónico inaceptable para los organismos terrestres. Es ligeramente tóxico (CL50 = 10-100 ppm) para peces de agua dulce e invertebrados acuáticos. El nivel de preocupación por el riesgo agudo para los peces y los invertebrados acuáticos es de 0,05 para las especies más sensibles. Sin embargo, debido a que el RQ agudo para algunos peces e invertebrados acuáticos está por debajo de ese nivel de preocupación, la EPA calculó que prácticamente no hay riesgo agudo por el uso del herbicida (Tabla 9). Desafortunadamente, no hay datos de toxicidad crónica disponibles para peces de agua dulce o invertebrados acuáticos. La caracterización del riesgo ambiental que llevó a cabo la EPA identificó que el mayor riesgo ambiental ocurre en las especies de plantas terrestres no diana, que ocupan áreas semiacuáticas y pueden estar sujetas a la escorrentía de los campos tratados. Las áreas semiacuáticas son aquellas áreas húmedas bajas que pueden estar secas en ciertas épocas del año. El RQ para plantas terrestres en áreas semiacuáticas, expuestas a escorrentía, varían de 1.2 a 1.9, y excedían el nivel de preocupación propuesto para dosis de una aplicación única 30.
Conclusiones
Para realizar evaluaciones de riesgo del uso de plaguicidas, las agencias reguladoras típicamente integran caracterizaciones de exposición con efectos ecológicos. Para los organismos acuáticos, los ensayos más tradicionales han sido exposiciones agudas a un rango de concentraciones durante 1-4 días en condiciones de laboratorio. Siempre que la mortalidad en el control (es decir, sin pesticida) sea inferior al 10%, se pueden usar estos experimentos para determinar la concentración letal que matará al 50% de la población (es decir, el valor de CL50). Al evaluar el riesgo, la CL50 se compara con las concentraciones de la sustancia química que se encuentra en la naturaleza. Luego, para establecer un límite superior seguro para las concentraciones de una sustancia química en la naturaleza, la EPA utiliza un índice conocido como "Cociente de riesgo" (RQ). Desafortunadamente, el enfoque basado en RQ no proporciona una estimación cuantitativa de la probabilidad o magnitud de un efecto adverso y tampoco proporciona información sobre exposiciones crónicas a concentraciones subletales. Tradicionalmente, las agencias reguladoras han utilizado especies sustitutas no diana (p ej. peces) como representativas de grupos taxonómicos amplios en la decisión de elegibilidad de registro (RED); sin embargo, esas especies pueden no representar la sensibilidad de los anfibios. Aunque las formulaciones de glifosato se consideran típicamente de toxicidad moderada (LC50 = 1-10 ppm) para la mayoría de las especies acuáticas, para numerosas especies de anfibios son altamente tóxicas (LC50 ˂ 1 ppm).
Idealmente, las evaluaciones de riesgo ecológico también deberían realizarse basándose en los efectos potenciales a exposiciones crónicas, particularmente en grupos taxonómicos no diana, como los anfibios. Las exposiciones crónicas a concentraciones subletales pueden tener una aproximación más realista para concentraciones que se suelen alcanzar en el medio ambiente. Para las formulaciones de glifosato, en particular las que contienen POEA, se ha demostrado que los anfibios expuestos a concentraciones subletales que se asemejan más a las de la alcanzadas después de las aplicaciones aéreas, provocan una disminución de la supervivencia, intersexualidad gonadal, daño en la cola, prolongación del tiempo en que alcanzan la metamorfosis, y lipidosis hepática. Los estudios de comportamiento también han mostrado una desactivación total o parcial de las señales de alarma. Todos esos efectos podrían tener consecuencias negativas para la supervivencia de las poblaciones de anfibios.
A partir de 2019, la Lista Roja de la UICN tenía 285 especies de anfibios en Colombia consideradas amenazadas. Encontramos que 132 especies con categorías EN y CR estaban presentes en 10 de los 32 estados colombianos donde las plantaciones ilegales de coca son fumigadas con una formulación de glifosato que contiene POEA. Con base en los datos de ubicación de anfibios recolectados en Colombia, se obtuvieron registros para 193 especies (28% de la diversidad nacional) de ranas y sapos que se encuentran en localidades dentro de los 10 km de áreas donde se cultiva coca. Sobre la base de los estudios revisados, se puede concluir que la aspersión inadvertida de humedales en los programas de erradicación de coca en Colombia podría tener efectos devastadores para las poblaciones de anfibios. Siguiendo el ejemplo de la rana de patas rojas de California, se debería implementar en Colombia la imposición de zonas de prohibición o buffer de “no uso” alrededor de los hábitats de los anfibios.
Con respecto al propanil, si bien se metaboliza rápidamente en pocas horas bajo condiciones aeróbicas metabólicamente activas, al igual que el glifosato es muy tóxico para anfibios, el propanil lo es en exposiciones agudas para camarones. Además, puede ser indirectamente muy tóxico a todos los organismos acuáticos por disminución rápida del oxígeno disuelto en agua. Los estudios de exposiciones crónicas también muestran que el crecimiento y desarrollo de peces e invertebrados se afecta a concentraciones de tan solo 9 ppb, que se alcanzarían fácilmente si se aplica directamente en estanques o por la deriva aérea de los arrozales pulverizados.