Introducción
La cirugía de control de daños se ha establecido como tratamiento para los pacientes críticamente enfermos con lesiones traumáticas del abdomen y otras cavidades 1-4. Las estrategias de este tipo de cirugía incluyen una laparotomía abreviada seguida del traslado inmediato a la unidad de cuidados intensivos para la reanimación fisiológica y un reparo quirúrgico definitivo diferido a un segundo tiempo en sala de operaciones 5,6. La base fisiológica para recurrir a la cirugía de control de daños es la necesidad de interrumpir el círculo vicioso de acidosis, hipotermia y coagulopatía, presente en pacientes de trauma, el cual implica el agotamiento de la reserva fisiológica y conlleva la muerte 7,8. La introducción de dicha cirugía fue un cambio del paradigma en el manejo del trauma grave y ha representado un aumento significativo en la supervivencia de los pacientes críticamente enfermos. Actualmente, es el tratamiento estándar en los centros especializados en trauma a nivel mundial 9.
Como los pacientes de cirugía general y de cirugía de urgencia que sufren infección intraperitoneal grave o sangrado están expuestos a experimentar los efectos de la acidosis, la hipotermia y la coagulopatía, los cirujanos tratantes han usado gradualmente los principios de la cirugía de control de daños en aquellos con enfermedades de origen no traumático que presentan grave compromiso fisiológico y anatómico 10,11. Recientemente, ha aumentado el número de publicaciones que muestran resultados prometedores en casos de isquemia mesentérica aguda, peritonitis secundaria a perforación de viscera hueca, peritonitis posquirúrgica, pancreatitis aguda, enterocolitis necrosante, hemorragia o síndrome de compartimiento abdominal 12-16. En la mayoría de ellas, se reportan series heterogéneas con muestras pequeñas de pacientes con un rango variado de condiciones; algunas veces, incluyen pacientes tratados con abdomen abierto y laparotomía diferida para reparo quirúrgico definitivo, en ausencia de criterios para cirugía de control de daños 8. La combinación de todos estos factores dificulta el análisis y la interpretación de los resultados.
Por lo anterior, es importante evaluar las indicaciones, las técnicas quirúrgicas y los resultados clínicos en pacientes con enfermedad intraabdominal de origen no traumático sometidos a laparotomía de control de daños, agrupándolos en varias categorías según el diagnóstico clínico e intraoperatorio (perforación, isquemia mesentérica) y condición fisiopatológica (hemorragia, sepsis), para contribuir a mejorar y hacer más eficientes los criterios que caracterizan los que podrían obtener mejores resultados con dicha cirugía.
El objetivo de este estudio fue evaluar si la laparotomía de control de daños con ligadura y reconstrucción intestinal diferida, reduce el número de ostomías en pacientes con peritonitis secundaria a compromiso de víscera hueca.
Métodos
Diseño de estudio
Este fue un estudio retrospectivo de cohorte, aprobado por el Comité de Ética de la Fundación Valle del Lili, un centro de trauma de nivel I con gran volumen de pacientes, ubicado en el suroccidente colombiano, que cuenta con un equipo multidisciplinario conformado por el Servicio de Cirugía General, el de Cirugía de Trauma y el de Cirugía de Emergencias.
Población
Se consideraron todos los pacientes adultos, mayores de 18 años de edad, que ingresaron a la institución entre enero del 2003 y diciembre del 2018, y fueron sometidos a laparotomía de urgencia con diagnóstico de peritonitis.
Los criterios de inclusión fueron:
diagnóstico de peritonitis secundaria a compromiso de víscera hueca y
uso de alguna técnica de reparo intestinal (anastomosis manual o mecánica, sutura primaria), ostomía (ileostomía o colostomía) o ligadura intestinal con reconstrucción definitiva diferida, durante la laparotomía índice o inicial.
Los criterios de exclusión fueron:
peritonitis secundaria a trauma,
peritonitis de origen biliar,
peritonitis secundaria a pancreatitis,
laparotomía por sangrado (aneurisma de aorta abdominal roto, hemorragia de vías digestivas),
isquemia mesentérica,
peritonitis manejadas con lavado y abdomen abierto, sin técnica de reparo intestinal,
muerte antes de la reconstrucción intestinal, y
ausencia de información sobre la estrategia de reconstrucción intestinal.
Estrategias de manejo quirúrgico
Los 306 pacientes se dividieron en tres grupos, según la estrategia de manejo usada durante la laparotomía inicial:
reparo definitivo, es decir, reparo primario o resección y anastomosis intestinal,
ostomía y reparo diferido, o
ligadura intestinal y reconstrucción definitiva diferida.
En el Departamento de Cirugía se encuentran estandarizadas las siguientes consideraciones para seleccionar los pacientes que se consideran de alto riesgo y que, por lo tanto, requieren reparo diferido: signos de hipoperfusión intestinal, puntaje de 15 o más en la escala APACHE II, y comorbilidades como diabetes, enfermedad cardiaca o cáncer; además, uno o más de los siguientes parámetros: respiratorio (PO2/FiO2 <200), renal (creatinina sérica: 3,5-4,9 mg/dl) o hepático (bilirrubina: 6-11,9 mg/dl), presión arterial media menor de 70 mm Hg durante la cirugía, necesidad de vasopresor, y compromiso neurológico (Glasgow <9), trombocitopenia (plaquetas <50.000 mm3) o ambos.
En el grupo 1, el de reparo definitivo, después del drenaje o lavado de la cavidad peritoneal y del desbridamiento o la resección del tejido necrótico o infectado, la peritonitis se controló mediante resección del segmento intestinal comprometido y restauración de la función gastrointestinal durante la laparotomía índice con anastomosis primaria u ostomía primaria (grupo 2). Para el manejo de la pared abdominal, se utilizó el cierre definitivo o un sistema temporal de abdomen abierto según el criterio del cirujano tratante. Según consenso de los cirujanos institucionales, las indicaciones de abdomen abierto son la infección intraabdominal persistente y como prevención del síndrome de compartimiento abdominal.
En el grupo 3, el de ligadura intestinal y reconstrucción definitiva diferida, después del control inicial de la infección con lavado o drenaje de la cavidad peritoneal y con desbridamiento o resección del tejido necrótico o infectado, se practicó la resección intestinal y se ligaron los extremos proximal y distal. Una vez se lograba la estabilidad hemodinámica del paciente y se consideraba factible la reconstrucción intestinal, se llevaba a cabo la reconstrucción definitiva diferida, fuera mediante anastomosis u ostomía.
Análisis estadístico
Se describieron las características demográficas, el estado basal de ingreso, la gravedad anatómica o fisiológica y los resultados clínicos. Se utilizaron la mediana y el rango intercuartílico (RIC) para las variables continuas con distribución no normal y, la media y la desviación estándar, para las variables continuas con distribución normal. Las variables continuas se compararon utilizando pruebas no paramétricas (Kruskal-Wallis) o pruebas paramétricas (Anova), dependiendo de su distribución. Las variables categóricas se resumieron utilizando frecuencias absolutas y porcentajes, y se compararon usando la prueba de ji al cuadrado o la exacta de Fisher, cuando las frecuencias esperadas de las celdas estuvieron por debajo de 5. Los valores de p menores de 0,05 se consideraron estadísticamente significativos. Todos los análisis se llevaron a cabo en el software Stata/MP™, versión 14.0 (StataCorp, College Station, TX).
Resultados
Se identificaron 708 pacientes con diagnóstico de abdomen agudo sometidos a laparotomía de urgencia. De estos, se excluyeron 8 a quienes, después de la laparotomía, se les diagnosticó isquemia mesentérica incompatible con la vida y, por lo tanto, no requirieron una estrategia de manejo adicional. Otros excluidos fueron: 299 pacientes en quienes, después de la laparotomía, la peritonitis solo se manejó con lavado de la cavidad peritoneal y abdomen abierto; 11 con ligadura durante la laparotomía índice pero que murieron antes de poder hacer la reconstrucción, y 84 cuyos datos sobre la técnica de reconstrucción intestinal estaban incompletos.
Los 306 pacientes restantes se incluyeron en el análisis. Se agruparon según el manejo recibido durante la laparotomía inicial, en: grupo 1 (120; 39,2 %), con reparo definitivo, es decir, reparo primario o resección y anastomosis intestinal; grupo 2 (87; 28,4 %), con ostomía y reparo diferido, y grupo 3 (99; 32,3 %), con ligadura intestinal y reconstrucción definitiva diferida (figura 1).

Figura 1 Distribución de los pacientes con diagnóstico de abdomen agudo sometidos a laparotomía de urgencia.
La mayoría (177; 57,8 %) de los pacientes incluidos eran hombres y se encontraban en la séptima década de la vida (64 años; RIC=48-73). La comorbilidad que presentaron con mayor frecuencia estos pacientes fue el cáncer, con una proporción mayor entre los sometidos a ostomía durante la laparotomía índice: 43 (35,8 %) del grupo 1, 46 (52,9 %) del grupo 2 y 24 (24,2%) del grupo 3 (p<0.001); le siguieron la enfermedad cardiaca (70; 22,8 %), la diabetes (44; 14,4 %) y enfermedad renal crónica (30; 9,8 %), sin diferencias estadísticamente significativas entre los grupos para estas últimas (tabla 1).
Tabla 1 Variables sociodemográficas, escalas de severidad, componentes de reanimación y comorbilidades de los pacientes incluidos en el estudio.

* RIQ: rango intercuartílico, UCI: Unidad de Cuidados Intensivos, SOFA: Sequential Organ Failure Assessment, UGR: unidades de glóbulos rojos, UPFC: unidades de plasma fresco congelado.
Los pacientes a quienes se les practicó ligadura intestinal tuvieron mayor puntaje en el Apache II al ingreso a la unidad de cuidado intensivo: grupo 1: 14 (RIC: 10-18); grupo 2: 13 (RIC: 11-18); grupo 3: 18 (RIC: 14-24); (p<0,001). Sin embargo, aquellos con reparo primario o resección y anastomosis durante la laparotomía índice, requirieron de manera significativa mayor volumen de transfusión de glóbulos rojos [grupo 1: 4 (RIC: 2-7); grupo 2: 3 (RIC: 2-7); grupo 3: 4 (RIC: 2-6); p=0,001] durante las primeras 24 horas.
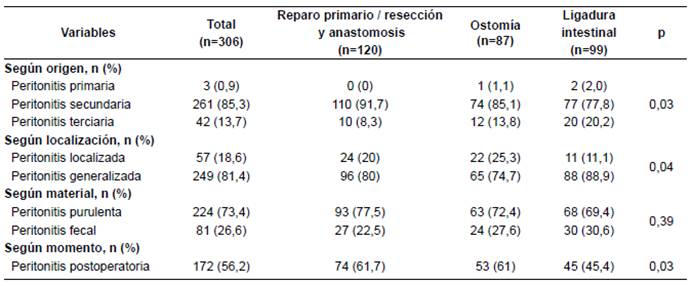
La peritonitis secundaria fue la condición patológica con mayor representación (261, 85,3 %) entre los pacientes incluidos. En la mayoría de los casos, la peritonitis fue: generalizada, en 96 (80 %) del grupo 1, en 65 (74,7 %) del grupo 2 y en 88 (88,9 %) del grupo 3 (p=0,04); purulenta, en 93 (77,5 %) del grupo 1, en 63 (72,4 %) del grupo 2, y en 68 (69,4 %) del grupo 3 (p=0,39); y posquirúrgica, en 74 (61,7 %) del grupo 1, en 53 (61,0 %) del grupo 2 y en 45 (45,4 %) del grupo 3 (p=0,03) (tabla 2).
La proporción de reintervenciones con laparotomía fue significativamente mayor entre los pacientes a quienes se les practicó ligadura intestinal: grupo 1: 1 (RIC: 0-2); grupo 2: 1 (RIC: 0-3); grupo 3: 3 (RIC: 1-4); (p<0,001). Sin embargo, a menos de dos tercios de los pacientes se les hizo un cierre definitivo de la fascia al final de la hospitalización: a 62 (51,7 %) del grupo 1, a 36 (41,4 %) del grupo 2 y a 61 (61,6 %) del grupo 3 (p=0,02). Además, los pacientes con ligadura requirieron más días de asistencia respiratoria mecánica, de estancia en la unidad de cuidados intensivos y de estancia hospitalaria, con diferencias estadísticamente significativas con respecto a los demás subgrupos (tabla 3).
Tabla 3 Desenlaces clínicos de los pacientes con peritonitis sometidos a laparotomía de control de daños

* RIQ: rango intercuartílico, UCI: Unidad de Cuidados Intensivos.
Respecto a la técnica de la reconstrucción intestinal después de la laparotomía índice, en menos de la mitad (34/99; 34,3 %) de los pacientes se utilizó la ostomía, en 49 (49,5 %), la anastomosis manual y, en 34 (34,3 %), la anastomosis mecánica. Murieron 54 (17,6 %) pacientes, sin diferencias estadísticamente significativas según los grupos: 19 (15,8 %) del grupo 1, 16 (18,4 %) del grupo 2, y 19 (19,2 %) del grupo 3 (p=0,79).
Discusión
La hipótesis de este estudio era que la laparotomía de control de daños en pacientes con peritonitis de origen no traumático y secundaria a compromiso de víscera hueca, podría reducir el número de ostomías.
Los hallazgos sugieren que, en pacientes con múltiples comorbilidades, peritonitis purulenta o fecal, de tipo generalizada y, con grave compromiso fisiológico, es factible utilizar la ligadura intestinal con reconstrucción diferida. Aunque este grupo requirió mayor número de reintervenciones con laparotomía, de días de asistencia respiratoria mecánica, de estancia en la unidad de cuidados intensivos y de días de estancia hospitalaria, dicha técnica evitó la ostomía en más de la mitad de los pacientes, los cuales terminaron con reconstrucción definitiva del tubo gastrointestinal antes del alta hospitalaria: 49/99 (49,5 %) con anastomosis manual diferida y 16/99 (16,1%) con anastomosis mecánica diferida.
En estudios previos se ha establecido que la laparotomía de control de daños es una estrategia eficaz para el manejo de pacientes con infección intraabdominal. Sin embargo, la falta de un grupo de control no ha permitido concluir si hay superioridad de este abordaje y, aunque se han propuesto varias técnicas de manejo quirúrgico, todavía falta 'evidencia' que soporte el efecto de esta en los resultados clínicos cuando se realizan procedimientos de reparo definitivo durante la laparotomía índice, en comparación con la reconstrucción definitiva después de la laparotomía abreviada 17,18.
Los resultados de este estudio sustentan la evidencia existente, la cual sugiere que los pacientes con grandes probabilidades de muerte según escalas como la Apache II y la SOFA, con una cantidad heterogénea de comorbilidades como cáncer, enfermedad cardiaca, diabetes o enfermedad renal, podrían beneficiarse de un principio usado en la cirugía de control de daños, que es expectante. Es decir, después de un diagnóstico oportuno de la alteración intraabdominal, una laparotomía abreviada para controlar la fuente de infección, el traslado inmediato a la unidad de cuidados intensivos para la reanimación y el tratamiento complementario con antibióticos, se hace una segunda evaluación de los pacientes que ya se encuentran mejor reanimados, hidratados, con mayor estabilidad según los parámetros hemodinámicos y con control parcial de la fuente de infección.
Khan, et al,19, publicaron una serie de 42 pacientes con condiciones variadas como peritonitis, absceso intraabdominal, isquemia intestinal y sangrado, en quienes la utilización de los principios de la laparotomía de control de daños permitió el cierre temprano de la pared abdominal, lo cual se asoció con menos complicaciones adicionales.
La elección del diseño de este tipo de estudio se basó en el registro de una gran proporción de pacientes sometidos a ligadura intestinal durante la laparotomía índice. A pesar de que los estudios de tipo retrospectivo tienen limitaciones ya conocidas, cabe resaltar que, en esta cohorte de pacientes, se pudieron determinar y describir las técnicas de reconstrucción intestinal y los resultados clínicamente relevantes.
Los hallazgos de este estudio tienen solamente validez interna por las limitaciones inherentes a su diseño. Sin embargo, se ha demostrado que el uso de estas técnicas en enfermedades de naturaleza similar o en otras condiciones, como hemorragia de origen no traumático, peritonitis de origen biliar, pancreatitis necrosante sobreinfectada o tumores con perforación de víscera hueca, entre otras, es posible y tiene efectos benéficos sobre resultados clínicos como la mortalidad 20.
Con base en estos resultados y considerando los potenciales beneficios de estas estrategias quirúrgicas en alteraciones de origen no traumático, se puede afirmar que es necesario continuar ampliando la evidencia disponible e implementar diseños de tipo prospectivo y estudios aleatorizados 21, para determinar cuáles indicaciones podrían ser más sensibles y cuáles más específicas, en los pacientes que podrían manejarse con reconstrucción diferida; además, para establecer cuál es el efecto real de diferir la reconstrucción intestinal en la supervivencia de los pacientes.
Por último, es posible el reparo primario para el control definitivo de la infección en casos de peritonitis grave, siempre y cuando, la condición clínica y la perfusión de la víscera comprometida sean adecuadas. En otros casos, cuando la condición del paciente reviste mayor gravedad, el practicar una laparotomía abreviada y diferir el reparo podría reducir la necesidad de una ostomía como tratamiento definitivo.
En conclusión, en el presente estudio, se logró evitar la ostomía como técnica de reconstrucción definitiva en más de la mitad de los pacientes con peritonitis que se sometieron a laparotomía de control de daños con ligadura intestinal. La implementación de esta técnica en el campo de la cirugía de cuidado agudo es factible. No obstante, se requieren estudios prospectivos que establezcan las variables para predecir tempranamente cuáles pacientes se beneficiarían más con este tipo de intervención.