Introducción
En el mundo el cáncer gástrico produce el 5,6 % de los casos nuevos de cáncer (1.089.103) y el 7,7 % de las muertes (768.793). En 2020, la OMS estimó que el cáncer gástrico en Colombia fue la principal causa de mortalidad por cáncer 1. En Colombia, la principal indicación para realizar gastrectomías es la enfermedad maligna, puesto que el cáncer gástrico es la segunda neoplasia más común en hombres y la cuarta en mujeres 2.
Desde 1926 existen dos indicaciones claras para la realización de gastrectomía: el cáncer y el tratamiento de la úlcera péptica y sus complicaciones. En ese entonces, ya era común la técnica de Devine y las reconstrucciones del tracto gastrointestinal tipo Billroth I y Billroth II 3. Previo a la llegada de la cirugía mínimamente invasiva, las complicaciones de la gastrectomía alcanzaban un 24 %, por lo tanto, se tenía como último recurso cuando otros procedimientos no eran suficientes 4.
La gastrectomía por laparoscopia se describió por primera vez en 1994, en Japón, en un caso de cáncer gástrico temprano 5, aunque otros datos sugieren que la primera gastrectomía por laparoscopia fue realizada en 1992 por Peter Goh, en Singapur, con reconstrucción tipo Billroth II para un paciente con enfermedad acidopéptica 6. Desde entonces los desenlaces quirúrgicos han mejorado sustancialmente. Zia MK, et al., evaluaron 61 pacientes llevados a gastrectomía por laparoscopia en enfermedad benigna y maligna durante 4 años, encontrando una mortalidad global de 1,7 % con seguimiento de 48 meses y una morbilidad de 3,5 % asociada al procedimiento 7.
Una experiencia de 50 años, publicada en 1991, con 2633 individuos permitió reconocer que, a pesar de la alta morbilidad del procedimiento, la sobrevida posterior al mismo cumplía el estándar de expectativa de vida 8. En las últimas dos décadas del siglo XX, se publicaron reportes de experiencias clínicas, como la de hospital de Ulm en Alemania, quienes describieron una población de 484 pacientes en un término de 15 años con una mortalidad perioperatoria de 13,4 % y una sobrevida global a 5 años de 15,9 %. La conclusión de Bittner fue que la mejoría en los desenlaces es consecuencia de estandarizar una técnica quirúrgica 9.
Entre 1993 y 2013 en EE.UU. se realizaron 318.788 gastrectomías, el 58 % (184.805) por patología maligna, mientras que el 42 % (133.983) fueron por enfermedad benigna. Fueron más frecuentes las gastrectomías subtotales, con un total de 232.670, en comparación con las totales, que alcanzaron 67.342 10.
El estudio MAGIC en 2006 mostró que la quimioterapia perioperatoria mejoró los resultados oncológicos en pacientes con cáncer gástrico, en términos de sobrevida, sin que represente una mayor significancia en morbilidad quirúrgica 11. En la actualidad este concepto persiste para los estadíos localmente avanzados, utilizando más frecuentemente del esquema propuesto en el estudio FLOT4 (fluorouracil, leucovorin, oxaliplatin y docetaxel), que demostró aún mejores sobrevidas y tiempos libres de enfermedad 12,13.
Así mismo, se ha demostrado que la linfadenectomía es un estándar quirúrgico y el recuento ganglionar es un predictor de la calidad quirúrgica. La obtención de al menos 12 ganglios es requisito en términos de gastrectomía oncológica. Se han descrito al menos 3 niveles ganglionares resecables, D1 (niveles ganglionares 1 al 6), D2 (niveles 1-12) o D3 (niveles 1-16); la linfadenectomía D2 originalmente incluía una pancreatectomía distal y esplenectomía, pero en un estudio holandés se demostró una mayor morbilidad asociada, sin cambios en la mortalidad. Esto ha llevado a modificar la linfadenectomía para prescindir de estos dos procedimientos (nivel 10) y únicamente resecar los ganglios proximales de la arteria esplénica (nivel 11p) 14.
Con relación al manejo quimioterapéutico de la patología gástrica oncológica, el estudio CLASSIC (Capecitabine and Oxaliplatin Adjuvant Study in Stomach Cancer) evaluó los beneficios de la quimioterapia adyuvante tras una cirugía radical con vaciamiento D2 en el escenario de cáncer gástrico estadio II/III, y documentó un claro beneficio de esta intervención, logrando impactar en la supervivencia, en comparación con la cirugía D2 por sí sola, con una supervivencia a 5 años del 68 % y 53 % respectivamente 15.
En los últimos años se han publicado múltiples estudios comparando los resultados de las gastrectomías por vía abierta y laparoscópica 16,17, aun así, los datos en Colombia son muy limitados 18. Por lo anterior, se consideró que era fundamental identificar las características poblacionales y los resultados quirúrgicos de los individuos que son llevados a gastrectomía por vía laparoscópica, en un área en la que la literatura local es aún escasa.
Métodos
Pacientes y variables
Se realizó un estudio observacional de cohorte retrospectiva de los pacientes sometidos a gastrectomía por laparoscopia en un centro de alta experiencia en un periodo comprendido entre 2013 y 2023. Los procedimientos fueron realizados por cirujanos con más de 5 años de experiencia en gastrectomías. Se incluyeron pacientes mayores de edad, con patologías benignas y malignas, sometidos a cirugía con abordaje laparoscópico, realizada de manera urgente o programada. Se excluyeron pacientes en estado de embarazo, con pérdida del seguimiento en los primeros 30 días, o sin información completa de las variables estudiadas.
La revisión de historias clínicas se realizó de forma individualizada por los investigadores en los sistemas de gestión de historias clínicas SOPHIA versión 7.0.4 para datos de hospitalización y AVICENA versión 7.11.10 para la historia de consulta externa, con auditoría de un segundo investigador. Los datos se registraron de forma anónima en el sistema de recolección de datos REDcap.
Técnica quirúrgica
El grupo de cirujanos gastrointestinales de nuestro centro estandarizó la técnica quirúrgica empleada desde el 2015. Los cinco cirujanos del grupo realizan los mismos pasos de forma sistemática en todos los casos. Las particularidades de nuestra técnica quirúrgica incluyen:
- Uso de tres trócares de 12 mm, supraumbilical, paramedianos derecho e izquierdo; uso de dos trocares de 5 mm, subxifoideo y en flanco izquierdo.
- Uso de sistemas de energía avanzada bipolar o ultrasónico.
- Se realiza de rutina omentectomía total.
- La linfadenectomía incluye los ganglios de la arteria hepática, arteria esplénica, tronco celíaco y ligamento hepatoduodenal.
- El asa alimentaria se secciona a 50 cm del ligamento de Treitz y se asciende antecólica.
- En la gastrectomía total se realiza una esofago-yeyunostomia L-L en Pi (π) descrita por Xing J, et al. 19. En la subtotal el bastón del asa alimentaria se posiciona hacia la curvatura menor (antiperistáltico) para prevenir la estenosis de la anastomosis por el cierre de la enterotomía en este asa. Ambas anastomosis se realizan con sutura mecánica de 60 mm.
- En la gastrectomía total se realiza prueba de azul de metileno en ambas anastomosis.
Análisis estadístico
Para el análisis estadístico se utilizó el programa IBM® SPSS (IBM Corp., Armonk, EE.UU.). En las variables continuas se calcularon medidas descriptivas como media y desviación estándar; estas medidas proporcionan una comprensión general de la tendencia central y la dispersión de los valores observados en el conjunto de datos. En cuanto a las variables discretas, se analizaron individualmente mediante la determinación de frecuencias y porcentajes. Además, se utilizaron tablas y gráficos de frecuencias para presentar de manera clara y concisa la distribución de estas variables. Por último, se realizó una prueba de muestras independientes para evaluar posibles asociaciones estadísticas.
Resultados
Durante el periodo de observación se realizaron aproximadamente 38 gastrectomías por año, con un rango entre 6 y 61. Se evidenció una tendencia acumulada positiva a través de los años (Figura 1).
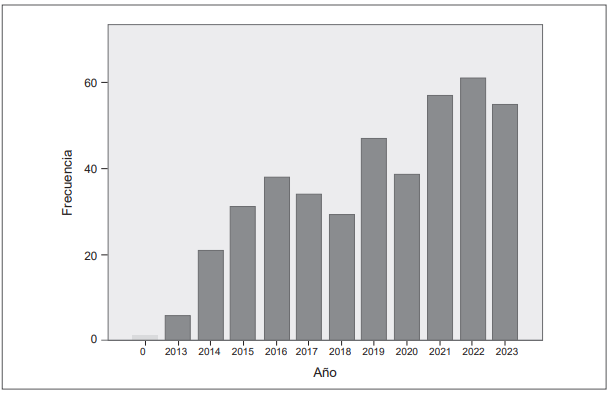
Figura 1. Distribución de gastrectomías durante periodo de observación. Clínica Universitaria Colombia, Bogotá, D.C., Colombia.
Posterior a la revisión de historias clínicas, se incluyeron 418 pacientes, muestra representada en un 58,9 % por hombres y 41, 2% mujeres. La edad promedio fue de 60,88 ± 14,1 años. De estos pacientes, el 52,2 % presentaba un estado nutricional normal por índice de masa corporal (IMC) y solo el 6,0 % fueron catalogados como bajo peso (Tabla 1).
Tabla 1. Características generales de los pacientes estudiados
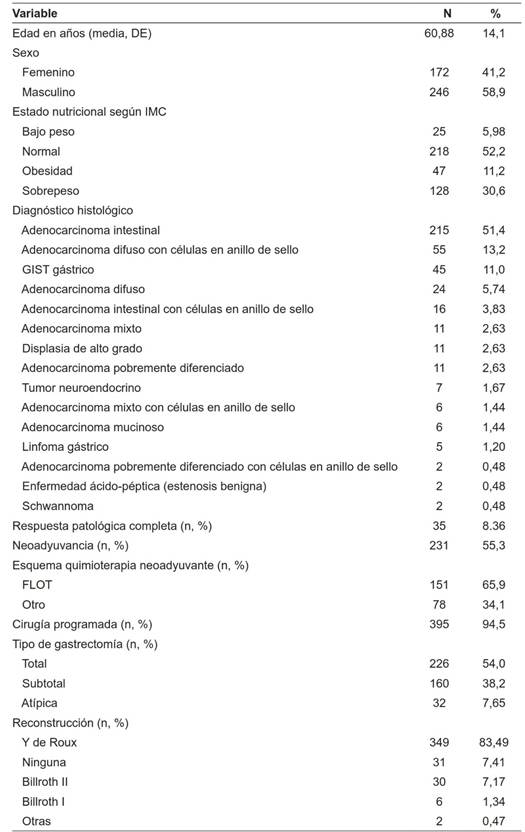
DE: Desviación estándar, IMC: Índice de masa corporal, GIST: Tumor del estroma gastrointestinal.
El principal diagnóstico por el que los pacientes fueron llevados a gastrectomía fue el adenocarcinoma gástrico, con diferenciación histológica intestinal en un 51,4 %, seguido del adenocarcinoma difuso con células en anillo de sello en un 13,2 %. En total, las gastrectomías laparoscópicas fueron por adenocarcinoma en 346 pacientes (82,8 %). Entre el 13,1 % restante con otros tumores, hubo 45 casos (11%) de tumores estromales (GIST), 7 tumores neuroendocrinos gástricos (1,7 %) y 2 schwannomas (0,5 %). Para los pacientes con linfoma o estenosis por enfermedad acido péptica, la indicación quirúrgica estaba dada por la sintomatología del paciente y la respuesta a las primeras líneas de manejo. Por otro lado, 12 de los sujetos requirieron de una conversión a cirugía abierta.
En total, 231 sujetos recibieron neoadyuvancia, y de estos, un 65,9 % estuvieron bajo esquema FLOT, siendo este el esquema actual de quimioterapia perioperatoria en nuestros pacientes, instaurado desde 2017. Previamente el más utilizado, según las características de los pacientes, era el esquema MAGIC.
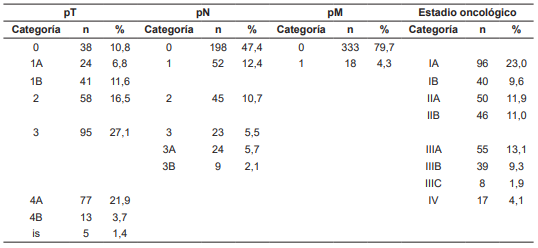
Según la clasificación del American Joint Committee on Cancer (AJCC) edición 8, el 23,0 % de los sujetos se localizaban en un estadio oncológico IA, seguido de 13,1 % en estadio oncológico IIIA (Tabla 2).
Se documentó un tiempo quirúrgico promedio de 228,7 minutos, con un sangrado de 150 ml y un rango intercuartílico de 195 ml. Al realizar un análisis estratificado de los subgrupos, se cuantificó un tiempo quirúrgico mayor en las gastrectomías totales y subtotales en comparación con las gastrectomías atípicas, al igual que en la variable sangrado quirúrgico.
Sin duda, uno de los indicadores de adecuada técnica en cirugía oncológica es el vaciamiento ganglionar, específicamente el recuento ganglionar en la pieza quirúrgica. Al ser analizado durante los 10 años del grupo, se observa que en los primeros años la mediana era inferior a la actual, con un crecimiento exponencial en el número final de ganglios en los casos de vaciamiento D2. Finalmente, la media de resección de ganglios linfáticos fue de 26,1 ± 11,4 (Tabla 3), con casos aislados de vaciamiento subóptimo en los pacientes llevados a cirugía paliativa o no oncológica.
Tabla 3. Desenlaces según el tipo de gastrectomía
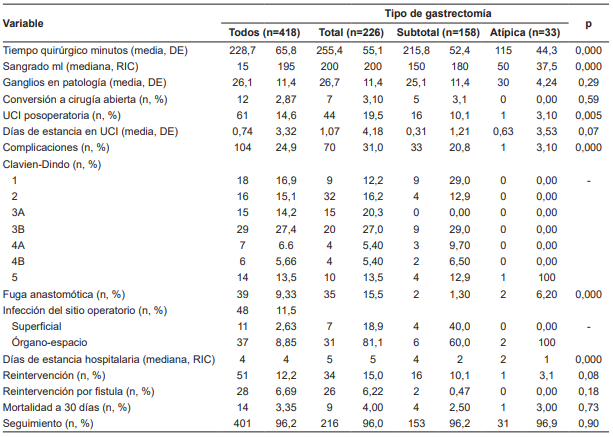
DE: Desviación estándar, RIC: rango intercuartílico, UCI: Unidad de cuidado intensivo.
Sesenta y un pacientes (16,4 %) requirieron traslado posoperatorio a la unidad de cuidados intensivos (UCI), con una estancia media para todas las gastrectomías de 0,4 ± 3,32 días. El impacto directo sobre la estancia en UCI se encuentra en las estrategias de recuperación rápida implementadas desde 2015-2016. Además de esto, los pacientes con fuga anastomótica, comorbilidades importantes e infecciones severas requirieron manejo en UCI. La estancia hospitalaria en promedio fue de 4 ± 4 días, siendo mayor en pacientes con gastrectomía total (promedio de 5 días) frente a la subtotal (4 en promedio) y las atípicas (promedio de 1 día).
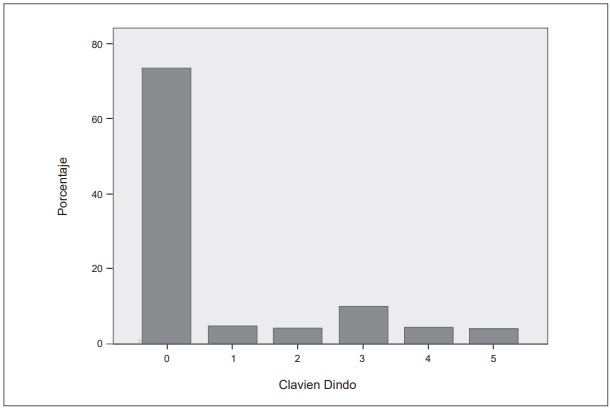
Se registraron complicaciones en 104 sujetos, con una tasa promedio de 24 %, de los cuales 70 (31 %) corresponden al grupo de gastrectomía total y 33 (20,8 %) al grupo de gastrectomía subtotal. Se utilizó la escala Clavien-Dindo para medir la severidad de las complicaciones, de las cuales 29 (27,4 %) obtuvieron una clasificación Clavien-Dindo IIIB (Figura 2). Las complicaciones Clavien-Dindo III fueron principalmente dadas por fuga anastomótica, además de derrame pleural aislado con requerimiento de toracentesis. Las reintervenciones tempranas tuvieron una frecuencia 12,2 %, de las cuales, la mitad fueron secundarias a fuga. Se identificó también hemoperitoneo en 3 pacientes y acodamiento de asa u obstrucción distal a anastomosis en 3 casos más.
En total, se documentaron 39 (9,3 %) casos de fuga de anastomosis, 35 (15,5 %) en el grupo de gastrectomía total, con una asociación estadísticamente significativa (p=0,000). También, se presentaron 48 episodios de infección de sitio operatorio (ISO), de los cuales 11 (2,6 %) correspondieron a una ISO incisional superficial y 37 (8,8 %) de tipo órgano-espacio.
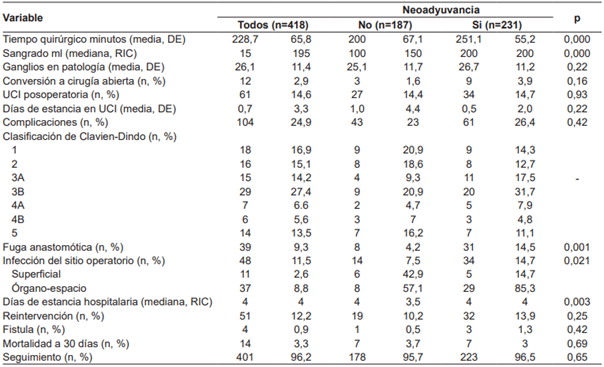
Se encontró que la neoadyuvancia tenía una asociación estadísticamente significativa (p<0,05) con mayor tiempo quirúrgico, mayor sangrado quirúrgico y fuga de la anastomosis (Tabla 4).
Discusión
La Clínica Universitaria Colombia, en Bogotá, D.C., Colombia, donde se desarrolló el estudio, es un centro de alto volumen en patología gastrointestinal superior, en el que se realizan en la actualidad, cada año, entre 60 y 70 gastrectomías. Como grupo quirúrgico, el entrenamiento en cirugía laparoscópica ha tenido un crecimiento exponencial, con cambios importantes en los últimos 10 años frente al manejo perioperatorio del paciente, lo que sin duda impacta directamente en los resultados oncológicos y quirúrgicos.
El grupo de cirugía gastroesofágica ha logrado formar un equipo multidisciplinario, donde patología, terapia física, respiratoria, nutrición y psicología juegan un papel fundamental en la recuperación. Hacia el año 2015 se implementaron las estrategias de soporte nutricional, fast track, prehabilitación y rehabilitación integral, impactando directamente en el tiempo de estancia hospitalaria y la recuperación posoperatoria, tal y como se ha descrito en literatura mundial.
Los resultados de este estudio respecto a la caracterización de la población de pacientes llevados a cirugía son similares a los informados recientemente por Hoyos en el caribe colombiano y Jurado en Medellín, en cuanto a la distribución por sexo y edad 20,21.
En el departamento de cirugía del Royal College of Surgeons en Dublín, Irlanda, desarrollaron una revisión sistemática en la que incluyeron estudios con diseño prospectivo y aleatorizado en pacientes con tumor primario gástrico, sumando un total 6890 pacientes, 46,6 % llevados a cirugía por vía abierta, 49,6 % por laparoscopia y 3,7 % asistida por robot. El análisis no demostró inferioridad de los resultados quirúrgicos y oncológicos en el escenario de pacientes con cáncer gástrico temprano llevados a procedimientos mínimamente invasivos 22.
Así mismo, en Latinoamérica, para el año 2014, Malet MV, et al., reportaron en un hospital de Uruguay una serie de casos de gastrectomía laparoscópica, mostrando que es posible garantizar resultados oncológicos comparables con la cirugía abierta convencional en términos de linfadenectomía y resección R0 23.
Tanto en estudios retrospectivos como en aleatorizados se ha mostrado que el recuento ganglionar y el período libre de enfermedad no cambian al comparar abordajes por vía abierta y laparoscópica 24,25. La estancia hospitalaria promedio reportada en la literatura para pacientes con cáncer fue de 12,6 a 18,2 días, mientras que en enfermedad benigna fue mayor, con un rango de 15,5 a 19,2 días, y la mortalidad intrahospitalaria se encontraba entre 11,9 y 5,9 % 26. En nuestros pacientes, la estancia hospitalaria en promedio fue de 4 ± 4 días, con un promedio de estancia en UCI menor de un día, inferior a lo reportado en otros estudios colombianos 20,21.
Lou S, et al., realizaron un metaanálisis de ensayos clínicos aleatorizados en el escenario de cáncer gástrico, en el que obtuvieron un total de 7.643 pacientes, entre los cuales el abordaje por laparoscopia se asoció a menor tasa de sangrado, menor tasa de complicaciones y recuperación temprana. Sin embargo, en ese estudio este abordaje se relacionó con un mayor tiempo quirúrgico y menor número de ganglios obtenidos 27.
El estudio de Choi YY, et al., que cuenta con una cohorte de alrededor de 10.000 gastrectomías por cáncer gástrico intervenidas por un mismo cirujano, el 69,8 % de los pacientes fueron llevados a gastrectomía subtotal, con un promedio de ganglios obtenidos de 42,3 26. En nuestro estudio, la media de resección de ganglios linfáticos fue de 26,1 ± 11,4, resultado de la estandarización de nuestra técnica, así como el reporte completo de la patología final, como consecuencia de la integración con el servicio de patología en los últimos 5 años, logrando tener comunicación cercana y un grupo selecto de patólogos para los tumores gastrointestinales.
Entre los pacientes publicados por Choi YY, et al. 26, el estadío tumoral más frecuente fue el I (50,1 %) y el menos frecuente fue el IV (4,5 %), similar a lo publicado por el grupo del instituto Nacional de Cancerología de Bogotá, D.C., Colombia 28, mientras en nuestro estudio, sólo el 23,0 % de los sujetos se localizaban en un estadio oncológico IA.
La omentectomía total es un tema controversial en el manejo del cáncer gástrico. En los últimos años, los resultados de 3 metaanálisis han evidenciado no inferioridad de la omentectomía parcial versus total en cáncer gástrico. No obstante, en su mayoría los estudios incluidos dentro de estos metaanálisis son cohortes retrospectivas y se cuenta con muy pocos estudios aleatorizados 29-31. Nuestro grupo realiza omentectomía de rutina, con un sangrado promedio de 213 ml, lo cual está en línea con la literatura mundial 32.
Un metaanálisis de 2015, elaborado por la colaboración Cochrane, recogió 2794 pacientes con cáncer gástrico en 13 ensayos clínicos y comparó gastrectomía abierta con gastrectomía laparoscópica, encontrando que no hay diferencias estadísticamente significativas en mortalidad a 30 días ni eventos adversos a corto o largo plazo 33. No obstante, otro metaanálisis más reciente de Hakkenbrak NAG, et al., basado en 22 ensayos clínicos aleatorizados, demostró resultados a favor del abordaje laparoscópico en términos de menor pérdida sanguínea intraoperatoria y una subsecuente recuperación más rápida del paciente, sin inferioridad en el número de ganglios recogidos en linfadenectomía 34.
El estudio multicéntrico aleatorizado CLASS02, en 2020 mostró que no existe inferioridad en términos de mortalidad entre el abordaje laparoscópico y el abierto, con un tiempo quirúrgico sin diferencias estadísticamente significativas y complicaciones cercanas al 20 %, considerando la cirugía laparoscópica segura 35. El tiempo operatorio suele ser mayor en el abordaje por laparoscopia, y en nuestro estudio fue de 229 minutos. Aun así, el estudio de Etoh T, et al., reportó una menor tasa de complicaciones en este grupo de pacientes 36.
En el abordaje laparoscópico se ha descrito una tasa de conversión a cirugía abierta de 14,5 %, complicaciones intraoperatorias de 1,4 %, incidencia de fístula duodenal del 3,6 % y reintervenciones en el 7,3 %. En nuestro estudio estimamos un 26,7% de complicaciones, lo que se encuentra por encima de la literatura mundial, pero puede corresponder al entorno regional, esto teniendo en cuenta que el reporte de cualquier evento que alterara el curso de la evolución postoperatoria esperada fue para nosotros considerado una complicación. Por esa razón, no fue despreciable el número de pacientes con clasificación Clavien-Dindo I y II, entre los que se identificó principalmente, náuseas y emesis, así como cualquier factor que alterara el curso de la evolución y recuperación postoperatoria. Al ser revisado de esta manera y comparado con instituciones de alto volumen con grupos de excelencia, el reporte completo de las complicaciones fue adecuado y permitió impactar en estrategias de manejo médico o identificación temprana de complicaciones que requieran manejo adicional temprano.
La fuga de la anastomosis es una de las complicaciones más grave de la gastrectomía, más aún en la gastrectomía total. Encontramos una asociación entre el estadio clínico avanzado y el uso de quimioterapia perioperatoria como factores de riesgo para la presencia de esta. Consideramos que esto es debido a que los pacientes con estadios avanzados son llevados a quimioterapia perioperatoria y ambos factores aumentan el riesgo de fuga anastomótica.
Entre nuestros pacientes con complicaciones, hubo dos laparoscopias sin hallazgos positivos, lo cual nos indica que uno de los puntos de mejora continua y trabajo estricto del grupo, incluye la detección temprana de complicaciones y evaluación imagenológica o laparoscópica de las mismas, con el fin de impactar en la disminución de mortalidad, tiempo de estancia hospitalaria y mejorar la recuperación posoperatoria de nuestros pacientes.
La gastrectomía por laparoscopia se había validado en múltiples estudios de diferente poder estadístico en estadios tempranos de cáncer gástrico. Desde el 2013 se cuenta con evidencia del continente asiático sobre la gastrectomía por laparoscopia en estadios avanzados 37 y en los últimos años se han publicado estudios sobre este tema provenientes de occidente 38,39. Así mismo, se ha demostrado que en pacientes con estadío localmente avanzado no hay diferencias respecto al tiempo libre de enfermedad cuando se compara el abordaje abierto y laparoscópico a 3 años, con una tasa de 76,5 y 77,8 % respectivamente, estableciéndose como no inferior 40.
En mayo de 2023, el estudio japonés de Etoh T, et al., con 502 pacientes en estadios avanzados de cáncer gástrico, aleatorizados en dos grupos de gastrectomía por laparoscopia y vía abierta, demostró una no inferioridad del grupo de laparoscopia, con hallazgos similares en complicaciones mayores, mortalidad, supervivencia global (Hazard Ratio 0,83; IC95% 0,57 - 1,21) y libre de enfermedad a 5 años (73,9 %; IC95% 68,7 % - 79,5 %) 36.
Para el año 2022, el ensayo clínico de Huang C, et al., que tomó un total de 1016 pacientes llevados a gastrectomía subtotal en 14 centros de China, aleatorizados 1:1 en cirugía por vía abierta y laparoscópica, mostró que la tasa de sobrevida a 5 años fue similar entre los dos grupos de pacientes con cáncer gástrico localmente avanzado. Sin embargo, ninguno de los pacientes fue llevado a neoadyuvancia previa, lo que limita el análisis de los resultados 16. Esto se corresponde con otros resultados, como el estudio KLASS-01 realizado en Korea, que estimó un tiempo de sobrevida de hasta 90 % para el abordaje abierto, sin inferioridad en el abordaje laparoscópico 41.
Con el pasar de los años, la gastrectomía por laparoscopia se ha convertido en el procedimiento estándar en algunas situaciones específicas. En los GIST la gastrectomía por laparoscopia se ha establecido como el tratamiento estándar, teniendo un impacto significativo en la reducción del tamaño de las incisiones, la mitigación del dolor postoperatorio, la minimización de las adherencias postoperatorias y la disminución de la estancia hospitalaria 42. El abordaje de elección para la resección de dichas lesiones es la gastrectomía en cuña o las resecciones no anatómicas, que se realizan con intención curativa. Teniendo en cuenta que la radicalidad quirúrgica para estos casos solo debe garantizar un margen de sección negativo, técnicamente se puede realizar la resección tumoral limitada, lo que no quiere decir, que una gastrectomía anatómica no sea en muchos casos la elección, por la consideración técnica y funcional en el contexto de cada paciente 42.
En un estudio realizado entre los años 2016 y 2020, que incluyó un total de 126 individuos con GIST aleatorizados en dos grupos de gastrectomía convencional y gastrectomía por laparoscopia, demostró que en el segundo grupo el tiempo operatorio fue menor, el sangrado intraoperatorio reducido y la estancia hospitalaria más corta, en comparación con el grupo de gastrectomía convencional 43.
Conclusiones
Este es un estudio retrospectivo, por lo que la fuerza de asociación de las variables estudiadas es baja, sin embargo, permite dar cabida a la caracterización de los pacientes en nuestra sociedad y su comportamiento, así como la identificación de las diferentes estrategias que han impactado en los desenlaces oncológicos, quirúrgicos y de recuperación postoperatoria. Las características de nuestro estudio no tienen las suficientes herramientas para dar una recomendación al respecto de la relación observada entre el estadio patológico y la neoadyuvancia con la fuga en la anastomosis, ni tampoco es el objetivo del presente estudio demostrar resultados oncológicos.
Consideramos que los desenlaces perioperatorios de los últimos 5 años probablemente tengan mejor impacto al estudiarse de forma individual, una vez que el grupo de cirugía gastrointestinal ha alcanzado la curva de aprendizaje necesaria y se estandarizó una técnica de forma institucional. Es posible afirmar que los desenlaces presentados son comparables con otros estudios internacionales de gastrectomía por vía abierta, sin inferioridad en el vaciamiento ganglionar y los días de estancia hospitalaria. Es necesario conocer abiertamente la experiencia clínica local, regional y nacional para establecer la influencia de nuestros estándares quirúrgicos en el perioperatorio del paciente, con la posibilidad de construir cada vez más recomendaciones basadas en la evidencia.
La creación de un grupo de excelencia requiere de un trabajo en equipo, multidisciplinario, por lo cual no se puede negar que cuando el objetivo común es la recuperación, el bienestar y la conservación de principios oncológicos en los pacientes con cáncer gástrico, los cirujanos debemos apoyarnos en servicios que juegan un papel fundamental para alcanzar dichos objetivos, como enfermería, nutrición, psicología, terapia física y respiratoria, anestesiología y cuidados intensivos, entre otros.